|
|
У своєму виступі Наталія Гудзь докладно зупинилася на аналізі розвитку законодавчої бази фармацевтичного ринку за останнє десятиріччя, розповіла про еволюцію органів контролю ЛЗ у новітній історії України, їх роль на сучасному етапі, навела дані про кількість субстандартних та фальсифікованих ЛЗ, яка постійно зростає. Наприклад, у 2000 р. було виявлено 17 серій фальсифікованих ЛЗ, у 2001 р. — 40, у 2002 р. — 62, а протягом першого півріччя 2003 р. — 21 серію.
Олексій Вікторов зазначив, що загальна кількість повідомлень про ПР ЛЗ неухильно збільшується, але на відміну від даних ВООЗ перше місце за кількістю випадків ПР ЛЗ в Україні займають серцево-судинні препарати. Результати аналізу банку даних підтвердили, що найчастіше ПР ЛЗ спостерігається в осіб віком від 42 до 60 років. О. Вікторов наголосив, що належного рівня національної системи фармаконагляду можна досягти лише завдяки систематичному та своєчасному поданню повідомлень про ПР ЛЗ до ДФЦ МОЗ.
У доповіді Ждани Хоменко йшлося про систему спонтанних повідомлень про ПР ЛЗ в Україні та шляхи вдосконалення якості інформації. За даними ВООЗ, у разі дотримання належних вимог на 1 млн населення реєструється приблизно 200 повідомлень або 10% від загальної кількості лікарів. Серед них не менше 10% припадає на серйозні ПР. Основним джерелом інформації про випадки ПР ЛЗ є лікар, який, використовуючи форму статистичної звітності № 137/о, передає інформацію про будь-які (очікувані, неочікувані; серйозні, несерйозні) ПР ЛЗ до відділу фармацевтичного нагляду ДФЦ.
Основна функція служби фармаконагляду — просвітницька робота та контроль за якістю інформаційних карт на місцях. У рамках діяльності відділу фармакологічного нагляду ДФЦ МОЗ налагоджено роботу з регіонами щодо якості заповнення та своєчасного подання інформаційних карт.
У своїй доповіді «Якість та безпека ліків — пріоритети лікарського забезпечення, спрямованого на захист інтересів пацієнта» Надія Шульга зазначила, що побічна дія чи ПР ЛЗ, відсутність належного терапевтичного ефекту можуть бути пов’язані з відсутністю або неадекватним вмістом активних речовин, неоднорідністю ЛЗ, невідповідною біодоступністю внаслідок недосконалої технології виготовлення, з наявністю токсичних домішок. Тому функції територіальної інспекції як регіонального представника ДІКЯ МОЗ України щодо виявлення, дослідження та результативних дій з захисту споживача (хворого) від застосування субстандартних, фальсифікованих та незареєстрованих в Україні ЛЗ — невід’ємний напрямок у викритті різноманітних ПР, які спричиняють «проблемні» ліки.
Останнім часом виникли нові обставини, які впливають на безпеку ЛЗ. Це розширення виробництва та продажу фальсифікованих і субстандартних ліків, збільшення випадків самолікування, застосування ЛЗ, виготовлених з рослинної сировини, в комбінації з іншими ЛЗ і за існуючої можливості розвитку побічних ефектів при їх взаємодії. Тому одним із ключових завдань ДІКЯ МОЗ стало впровадження таких механізмів контролю якості ЛЗ під час їх оптової, роздрібної реалізації, медичного застосування, які б враховували реалії сучасного українського фармацевтичного ринку.
Якість ЛЗ — сукупність властивостей, які надають ЛЗ здатність задовольняти споживачів відповідно до свого призначення і відповідають вимогам, установленим чинним законодавством (Наказ МОЗ України від 12.12.2001 р. № 497, розділ 2.16).
Для забезпечення якості ЛЗ необхідно досягти відповідних вимог та гарантувати якість ЛЗ на стадії виробництва, транспортування, оптової та роздрібної реалізації, зберігання і медичного застосування. Крім того, має чітко функціонувати самоконтроль (аудит) уповноваженими особами суб’єктів господарської діяльності.
Державний контроль якості ЛЗ здійснюють органи державної виконавчої влади в межах повноважень, визначених законодавством України (ст.13 Закону України «Про лікарські засоби»).
Вхідний контроль якості ЛЗ під час оптової та роздрібної реалізації здійснюють уповноважені особи суб’єктів господарської діяльності за допомогою візуальних методів, які мають ліцензії на право оптової та роздрібної реалізації ЛЗ (п. 1.3 Наказу МОЗ України № 436).
Процедура взаємодії ДІКЯ в Черкаській області та підвідомчої мережі (аптечних закладів та ЛПЗ) щодо виявлення та вилучення з обігу незареєстрованих, фальсифікованих і субстандартних ЛЗ така. У разі надходження з ДІКЯ інформативних приписів та розпоряджень щодо контролю якості ЛЗ, у територіальній ДІКЯ проводять їх реєстрацію та узагальнення. Опрацьовану інформацію передають до аптечної мережі та в ЛПЗ області. У територіальній ДІКЯ створюють базу даних субстандартних, фальсифікованих та незареєстрованих ЛЗ, виявлених за результатами державного контролю. Здійснюють заборону (призупинення) та вилучення з обігу ЛЗ відповідно до наданої інформації ДІКЯ МОЗ та за результатами досліджень ЛЗ щодо його відповідності нормативним документам згідно з затвердженою стандартною процедурою. ЛПЗ та суб’єкти господарської діяльності повідомляють ДІКЯ МОЗ про виявлені субстандартні, фальсифіковані ЛЗ і представляють документацію про вжиті заходи (знищення, повернення постачальнику). Ця інформація фігурує в тижневих звітах ДІКЯ МОЗ. Таким чином, під час проведення вхідного контролю якості безпосередньо в аптечній мережі та ЛПЗ зазначена вище процедура має спрацьовувати на користь реалізації та застосування якісних і безпечних ліків.
Показовою є динаміка кількості серій фальсифікованих та субстандартних ЛЗ, обіг яких було заборонено в Україні та на території Черкаської області у 2000 р. — першому півріччі 2003 р. (рис. 1, 2).
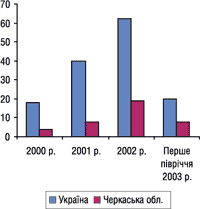 |
Рис. 1. Кількість серій фальсифікованих ЛЗ, обіг яких було заборонено в Україні і на території Черкаської області в 2000 р. — першому півріччі 2003 р.
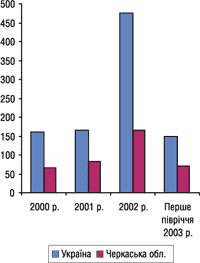 |
Рис. 2. Кількість серій субстандартних ЛЗ, обіг яких було заборонено в Україні та на території Черкаської області в 2000 р.— першому півріччі 2003 р.
Кількість субстандартних ЛЗ, щодо яких було прийнято рішення ДІКЯ МОЗ у першому півріччі 2002 р. перевищило аналогічний показник 2001 р. Причина такого збільшення лежить, напевне, в більш ефективному обміні інформацією між територіальними інспекціями, ДІКЯ МОЗ і суб’єктами господарської діяльності. Таким чином, можна зробити висновок, що запроваджена система запрацювала ефективно.
Практика свідчить, що ймовірніше побічні дії та ПР ЛЗ з’являються у разі застосування субстандартних та фальсифікованих ліків. Саме цей факт мають враховувати лікарі під час призначення лікування. Часто вони дають інформацію про недостатній терапевтичний ефект у разі застосування відомих ЛЗ, прояв нетипової побічної дії та частоту алергічних реакцій. Це, звичайно, пов’язують з неправильним підбором препарату і дозуванням, резистентністю флори (у випадках з антибіотиками), схильністю хворого до алергії. При цьому більшість лікарів, а разом з ними і пацієнтів (для яких основним критерієм залишається вартість ліків), не замислюються про оригінальність препарату, вважаючи, що в разі придбання його в аптеці якість гарантована.
Тому для ЛПЗ дуже важливою є проблема накопичення баз даних щодо виявлених субстандартних та фальсифікованих ЛЗ і розроблення плану термінових дій для своєчасного вилучення з обігу їх та тих ЛЗ, які спричинюють побічні дії. Така інформація може бути важливим чинником у прийнятті остаточних рішень щодо побічної дії чи ПР ЛЗ, а також про включення того чи іншого ЛЗ до схеми лікування.
Аналізуючи дані, наведені в таблицях 1 і 2, можна зробити висновок, що діяльність уповноважених осіб потребує вдосконалення, підвищення ефективності, відповідальності за якість ЛЗ, на які вони дають дозвіл до реалізації. Аналізуючи роботу ДІКЯ в Черкаській області у І–ІІІ кварталах 2003 р., потрібно зазначити, що інспекторами було виявлено 35 найменувань субстандартних ЛЗ, з яких вимогам АНД за показником «опис» не відповідають 16 (визначено візуально), при тому, що уповноваженими особами суб’єктів господарської діяльності було виявлено всього 15 найменувань субстандартних ЛЗ (інспекторів ДІКЯ було 3, уповноважених осіб суб’єктів господарської діяльності — 125).
Таблиця 1
Загальні результати державного контролю
якості ЛЗ та вхідного контролю суб’єктами господарської діяльності в Черкаській області
за 2001 р. — 8 міс 2003 р.
|
Показник |
Кількість забракованих зразків |
||
|
2001 р. |
2002 р. |
8 міс 2003 р. |
|
|
Загальна кількість забракованих зразків |
80 |
166 |
125 |
Таблиця 2
За результатами лабораторного контролю якості ЛЗ в Черкаській області за 2001 р. — 8 міс 2003 р.
|
Показник |
Кількість забракованих зразків |
||
|
2001 р. |
2002 р. |
8 міс 2003 р. |
|
|
Субстандартні ЛЗ, виявлені під час інспектування |
23 |
77 |
35 |
|
Субстандартні ЛЗ, виявлені уповноваженими особами СГД за приписами ДІКЯ МОЗ |
55 |
12 |
15 |
Яких позитивних результатів можна очікувати від взаємодії управління охорони здоров’я, ЛПЗ та аптечних закладів, ДІКЯ з питань якості ЛЗ? Користь для пацієнтів — вилучення з обігу субстандартних і фальсифікованих ЛЗ. Це стане попередженням виникнення ПР ЛЗ. Користь для Управління охорони здоров’я — розширення джерел повідомлень про ПР ЛЗ за рахунок аптечних працівників і пацієнтів та відфільтровування повідомлень, пов’язаних із субстандартними та фальсифікованими ЛЗ. Користь для ДІКЯ — розширення джерел інформації про субстандартні і фальсифіковані ЛЗ.
Відповідно до стандартів належної аптечної практики (GPP) кожний елемент аптечної послуги був орієнтований на окремого споживача, чітко визначений та ефективно доведений до кожного спеціаліста закладів охорони здоров’я.
Олександр Дудник у своєму виступі порушив питання організації фармаконагляду в Черкаській області. Зокрема, він зазначив, що в області, починаючи з літа 2002 р., діє наказ Управління охорони здоров’я обласної державної адміністрації № 237, згідно з яким відповідальність за забезпечення надання закладами охорони здоров’я інформації про ПР ЛЗ до ДФЦ МОЗ було покладено на головного терапевта управління, відповідальність за збір інформації — на заступників головних лікарів з лікувальної роботи. За наказом уся інформація надходить до головного терапевта і після аналізу направляється до ДФЦ МОЗ. З часу виходу наказу розпочалося впровадження системи фармаконагляду в області. За 6 міс поточного року до відділу фармакологічного нагляду ДФЦ МОЗ було направлено 51 повідомлення, а в 2002 р. — всього-на-всього 12. Значно розширився перелік закладів, які надають інформацію про ПР ЛЗ: якщо у 2002 р. — всього 5, то в 2003 р. — 21. За цей період налагоджено взаємодію з обласною ДІКЯ, управлінням охорони здоров’я та регіональним відділенням фармакологічного нагляду. Під час аналізу даних про ПР ЛЗ підтверджується аксіома, що чим більше призначається ліків одному пацієнту, тим вищий ризик виникнення ПР ЛЗ. Тільки у 12 випадках із 51 ПР виникла у хворих, які отримували один ЛЗ.
Своїм досвідом про здійснення фармаконагляду в Черкаській обласній лікарні і Тальнівській районній лікарні з учасниками конференції поділилися Світлана Журба та Анатолій Майсюк.
Конференція стала важливим етапом освоєння знань з питань ПР ЛЗ та організації фармаконагляду для широкого загалу спеціалістів Черкаської області.
Микола Холоденко
Фото автора


Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим