
 Науково-освітній департамент «Щотижневика АПТЕКА» продовжує публікацію авторського циклу статей професорів Національного фармацевтичного університету Івана Матвійовича Перцева та Олени Анатоліївни Рубан, присвячених допоміжним речовинам (початок див.: «Щотижневик АПТЕКА» № 2 (973) від 19.01.2015).
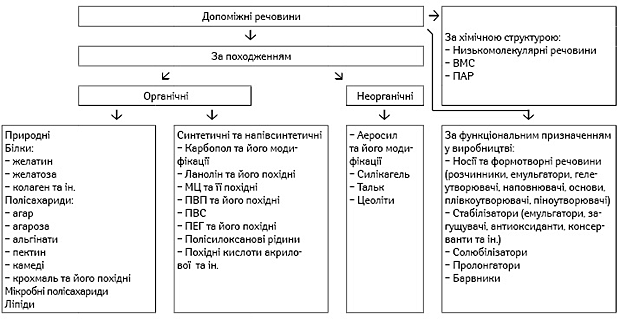
Науково-освітній департамент «Щотижневика АПТЕКА» продовжує публікацію авторського циклу статей професорів Національного фармацевтичного університету Івана Матвійовича Перцева та Олени Анатоліївни Рубан, присвячених допоміжним речовинам (початок див.: «Щотижневик АПТЕКА» № 2 (973) від 19.01.2015).При виробництві фармацевтичних препаратів використовується численний асортимент допоміжних речовин, і для полегшення їх вибору бажано мати чітку систематизацію. Однак через різну їх природу, хімічну структуру та різноплановість впливу на властивості активних фармацевтичних інгредієнтів (АФІ), а, отже, і фармакотерапевтичні характеристики ліків, різне функціональне призначення у виробництві ліків, а також відсутність їх виробництва на підприємствах єдиної галузі ускладнюють їх чітку класифікацію. Зазвичай допоміжні речовини класифікують за походженням (органічні, неорганічні, виділяючи синтетичні речовини), за хімічною структурою та за функціями, які вони виконують при виробництві фармацевтичних препаратів (рис. 1). За походженням допоміжні речовини поділяють на природні (органічні та неорганічні), виділяючи в окрему групу синтетичні та напівсинтетичні. Ця група речовин характеризується високою біологічною індиферентністю, користується великим попитом у виробників фармацевтичних препаратів. Проте природні допоміжні речовини (полісахариди, білки, ліпіди) швидко псуються, особливо при мікробній контамінації, що вимагає додавання консервантів, антиоксидантів тощо. Синтетичні та напівсинтетичні допоміжні речовини знаходять більш широке, порівняно з природними, застосування при виробництві ліків (70%). Цьому сприяють їх доступність, стабільність, вища ефективність та можливість отримувати селективно бажані властивості. За хімічною структурою допоміжні речовини можуть бути низькомолекулярними та високомолекулярними сполуками (ВМС), що мають молекулярну масу не менше 10 000 і здатні утворювати розчини різної в’язкості залежно від концентрації або мають поверхнево-активні властивості. З цими властивостями й пов’язано їх основне використання у виробництві фармацевтичних препаратів, де ВМС використовують в основному як носії, загусники, стабілізувальні, пролонгувальні та коригувальні компоненти, а також пакувальні й закупорювальні матеріали. Завдяки використанню ВМС були отримані багатошарові таблетки пролонгованої дії, полімерні плівки різного призначення (офтальмологічні, стоматологічні та ін.), спансули, мікрокапсули, терапевтичні системи тощо. Широке застосування у виробництві фармацевтичних препаратів одержала окрема група ВМС, що мають поверхнево-активні властивості, — поверхнево-активні речовини (ПАР). Їх поділяють на аніонні, катіонні, амфотерні, неіоногенні, які мають виражену спорідненість до води завдяки дисоціації або гідратації. На особливу увагу заслуговують неіонні ПАР — сполуки, які у водних розчинах не піддаються електролітичній дисоціації і знайшли широке застосування у фармації завдяки найнижчій токсичності, що не подразнює слизові оболонки і тканини. Цей клас речовин найчастіше представлений:
- поліоксіетиленовими етерами вищих жирних кислот:
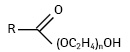 ;
;
- поліоксіетиленовими етерами вищих жирних спиртів:
R – (OC2H4)nOH;
- поліоксіетиленовими етерами поліпропіленгліколів:
Н(С2Н4О)х – (С3Н6О)n – (С2Н4О)уОН;
- естерами ангідросорбіту і вищих жирних кислот (спенами):
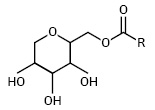 ;
;
- полігліколевими естерами ангідросорбіту і вищих жирних кислот (твінами):
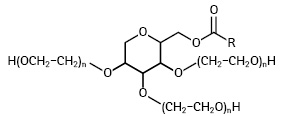 ;
;
- дистеаратом тригліцеролом (емульгатором Т-2) — сумішшю моно- і дигліцеридів кислоти стеаринової з полігліцеролом:
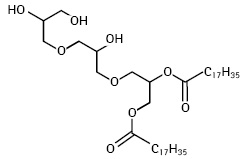 .
.
Використання ПАР у виробництві ліків обумовлено властивостями їх молекул: дифільності (певна величина гідрофільно-ліпофільного балансу — ГЛБ) та поверхневої активності. Під дією ПАР (через дифільну будову їх молекул) помітно змінюються молекулярні властивості тієї поверхні, з якою вони контактують (знижується поверхневий натяг). ПАР впливають і на технологічні характеристики: у розбавлених розчинах ПАР максимально гідратуються, що впливає на створення справжнього розчину. Значний асортимент ПАР, що мають різну природу і будову, надзвичайно утруднює їх вибір для певної мети. Для вирішення цієї проблеми у 1949 р. W. Griffin запропонував класифікувати кожну ПАР за певною величиною — співвідношенням гідрофільної та ліпофільної частини молекули, що одержало назву ГЛБ. З підвищенням значення ГЛБ поліпшуються гідрофільні властивості ПАР, що супроводжуються підвищенням їх розчинності у воді. Практичне значення мають величини ГЛБ від 1 до 20 (табл. 1), що дає можливість обрати необхідну ПАР для певної мети. Біофармацевтичні дослідження підтвердили, що ПАР, змінюючи фізико-хімічні властивості дисперсної системи фармацевтичних препаратів, помітно впливають на їх терапевтичну ефективність. Низькі концентрації ПАР збільшують усмоктування сульфаніламідів, барбітуратів, деяких етерів саліцилової кислоти, гідрокортизону. Високі концентрації багатьох ПАР, навпаки, знижують абсорбцію АФІ із розчинів. Пояснюється це явище появою міцелярної фази, яка може виступати як депо для молекул активної речовини, а також зміною їх коефіцієнта розподілу на межі контактуючих фаз.
| Таблиця 1 | Значення ГЛБ і сфера застосування ПАР |
| Значення ГЛБ | Сфера застосування ПАР |
|---|---|
| 1,5–3,0 | Піногасники |
| 3,0–6,0 | Емульгатори в/о |
| 7,0–9,0 | Зволожувальні речовини |
| 8,0–13,0 | Емульгатори о/в |
| 13,0–15,0 | Мийні, піноутворювальні речовини |
| 15,0–18,0 | Солюбілізатори |
Певне практичне значення при виробництві фармацевтичних систем має поділ допоміжних речовин за їх функціональним призначенням (рис. 2). Однак слід зауважити, що залежно від складу фармацевтичної системи, виду лікарської форми, виробничого процесу та інших чинників можуть значно змінюватися акценти призначення допоміжних речовин, унаслідок чого одна й та сама допоміжна речовина може виконувати різне функціональне призначення при виробництві ліків (стабілізатора, загусника, емульгатора, солюбілізатора тощо) або навіть стати активним фармацевтичним інгредієнтом.
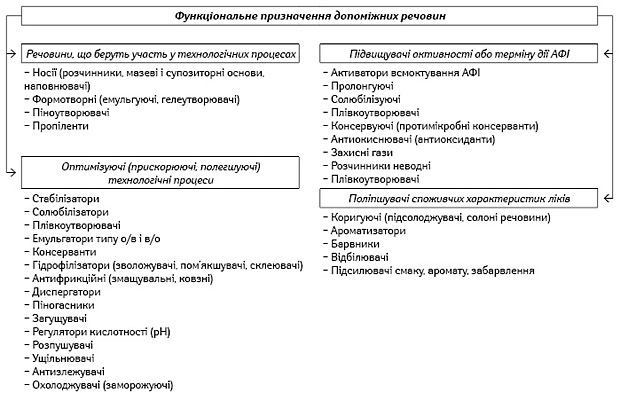
Носії та формоутворювальні допоміжні речовини. Носії та формоутворювальні допоміжні речовини, виходячи з їх назви, зазвичай обумовлюють вид лікарської форми, створюють безперервне дисперсійне середовище різних фармацевтичних систем і входять до складу продукту у великій кількості (до 90% і більше), обумовлюючи основні властивості фармацевтичних препаратів — необхідну масу, об’єм, агрегатний стан, геометричну форму тощо. З цією метою використовується велика номенклатура допоміжних речовин як природного, так і синтетичного походження. До даної групи речовин належать носії-розчинники, що використовуються при виробництві численних різновидів розчинів (для ін’єкцій, внутрішнього та зовнішнього застосування); носії-основи, які використовуються у виробництві ліків з пластично-пружно-в’язкими властивостями (гелі, креми, мазі, лініменти, супозиторії та ін.); наповнювачі при виробництві таблетованих та інших ліків. Носії та формоутворювальні речовини можуть одночасно зумовлювати необхідні технологічні властивості, наприклад, у таблетках поліпшують точність дозування та можливість пресування таблеткової маси, забезпечують механічну міцність, здатність розпадатися й вивільняти АФІ та стабільність таблеток при зберіганні. Наведені приклади наочно демонструють здатність допоміжних речовин виконувати одночасно різні технологічні функції.
Розчинники як носії фармацевтичних систем з рідким дисперсійним середовищем. Розчинники — це індивідуальні хімічні сполуки або їх суміші, здатні розчиняти різні активні речовини, тобто утворювати з ними однорідні (однофазні) системи. У випадку розчинів «рідина — газ» або «рідина — тверде тіло» розчинником вважають рідкий компонент, а у випадку «рідина — рідина» — компонент, який знаходиться в надлишку. Розчинна здатність розчинника визначається головним чином з урахуванням співвідношення полярностей «розчинник — речовина». Дуже полярні розчинники та розчинники, здатні утворювати міцні водневі зв’язки (прості спирти, моноетери, гліколі), більш придатні для розчинення гідрофільних речовин. Неполярні вуглеводні, особливо ароматичні, добре розчиняють рослинні олії, смоли тощо. Деякі розчинники з прихованою розчинністю проявляють свою дію тільки в сумішах зі справжніми розчинниками (рис. 3). Неводні розчинники з хімічної точки зору можна поділити на вуглеводні, спирти, етери, естери, гліколі, кетони, аміди, сульфоксиди і сульфони, олії рослинні (жирні). Олії жирні (лат. Olea Pinguia) є поширеною групою неводних розчинників, що являють собою суміші тригліцеридів вищих жирних насичених і ненасичених кислот (95–97%), фосфатидів, вільних жирних кислот, токоферолів, пігментів та інших речовин. Для фармацевтичних потреб їх одержують холодним пресуванням із свіжого насіння рослин. Кислотне число жирних олій не повинно перевищувати 2,5. Для виробництва ін’єкційних розчинів дозволяється застосовувати мигдалеву, персикову, оливкову, соєву, арахісову, кунжутну, соняшникову, бавовняну і кукурудзяну олії. Вони не повинні містити вологи (можливий ферментний гідроліз тригліцеридів і фосфоліпідів з утворенням вільних кислот, реакційноздатних речовин та вільних радикалів). Для зовнішнього застосування обмежень щодо природи олії немає, але залежно від призначення ліків (парентеральні олійні розчини, для виробництва імплантатів) вимоги до жирних олій можуть змінюватися. При виготовленні гетерогенних дисперсних систем, що складаються із взаємно нерозчинних рідин (найчастіше води та олії), використовують допоміжні речовини, здатні підвищувати в’язкість водного середовища (похідні целюлози, альгінати тощо), та стабілізатори-емульгатори з певним значенням ГЛБ, враховуючи тип емульсії (лецитин, пентол, твін-80, емульгатор Т-2, емульгатор № 1 та ін.), а також використовуються певні технологічні прийоми.
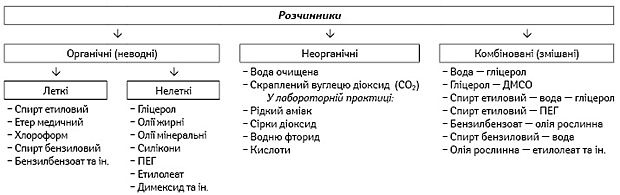
Носії в ліках з пластично-пружно-в’язким дисперсійним середовищем. До цієї неоднорідної групи фармацевтичних систем умовно можна віднести мазі, креми, гелі, лініменти, пасти, вагінальні й ректальні супозиторії, пластирі, трансдермальні й плівкові (очні, стоматологічні) терапевтичні системи, плівкоутворювальні й пінні препарати в аерозольній упаковці, а також фіксовані пов’язки з активними речовинами. До складу цих систем зазвичай входять допоміжні речовини у значній кількості, які й обумовлюють швидкість і повноту вивільнення активних речовин, характер терапевтичної дії (загальна чи місцева), тип дисперсної системи, структурно-механічні та інші властивості. Різне цільове призначення цих ліків вимагає використання різних за своїми фізико-хімічними властивостями носіїв. Ідеального носія не існує, тому, щоб одержати носій з необхідними властивостями, поєднують декілька допоміжних речовин. Так, для виробництва мазей — найбільш численних представників цієї групи, — використовується значна кількість носіїв (мазевих основ), які прийнято поділяти на три групи: гідрофільні, гідрофільно-ліпофільні та гідрофобні (рис. 4). Такий поділ основ є умовним, але дозволяє більш чітко їх охарактеризувати та зробити правильний вибір залежно від фізико-хімічних властивостей активної речовини, передбачити швидкість її вивільнення, абсорбції та характер дії (загальна, місцева, поверхнева тощо), а також можливу технологію мазі. Носії, що використовуються для виробництва сучасних мазей, містять як рідкі, так і тверді компоненти, за допомогою яких досягаються не тільки певна лікувальна ефективність, але й консистенція, споживчі та інші характеристики ліків з урахуванням їх призначення. Важливу роль у виробництві ліків з пружно-в’язким дисперсійним середовищем відіграють ПАР, які забезпечують спрямоване посилення їх лікувальної активності й використовуються як солюбілізатори, емульгатори для одержання емульсій типу о/в (натрію лаурилсульфат, віск емульгувальний, полісорбати, поліоксіетиленгліколеві етери жирних кислот) або емульсій типу в/о (вищі жирні спирти, холестерин, спирти шерстяного воску, спени, гліцерилмоноолеат, гліцерилмоностеарат та ін.). Деякі допоміжні речовини можуть виконувати декілька функцій — одночасно бути пом’якшувальними і зволожувальними добавками, пенетрантами тощо. Деякі з них є сумішами (ланолін водний, віск емульгувальний, віск емульгувальний неіогенний та ін.). Склад носіїв, що найчастіше використовуються у виробництві супозиторних ліків, наведений у табл. 2.
| Таблиця 2 | Склад і характеристика деяких супозиторних основ |
| Основа | Склад і характеристика основи | Примітка |
|---|---|---|
| Бутироль | ГЖ* з температурою плавлення 36 °С — 50 ч., парафіну — 20 ч., масла какао — 30 ч. Твердість стосовно масла какао — 66,5%, Тпл. — 37 °С. Рекомендовано для приготування супозиторіїв методом виливання й пресування | *Під назвою «бутироль» використовують сплави гідрогенізованих жирів (ГЖ) різного складу |
| Желатино-гліцеринова основа | Кількісні співвідношення складових компонентів основи можуть змінюватися залежно від мети. Фармакопейний пропис: желатину — 1–2 ч., води — 2 ч., гліцерину — 5 ч. Пружна, легкозастигаюча маса; рекомендована для виливання вагінальних супозиторіїв; нестабільна, але легко вивільняє лікарські речовини й добре всмоктується | – |
| Масло какао | Естер гліцерину переважно олеїнової, пальмітинової й стеаринової кислот. Використовується для приготування супозиторіїв методом викачування | |
| Поліетиленгліколева основа | 1) сплав поліетиленгліколю (ПЕГ) 1500 — 95% з ПЕГ 400 — 5%; 2) сплав ПЕГ 6000 — 60%, ПЕГ 400 — 20% і ПЕГ 1500 — 20%. Тверді за консистенцією, легко вивільняють лікарські речовини, стабільні, придатні для пресування й виливання супозиторних ліків |
Можуть використовуватися в субтропічних районах. Недолік — зневоднюють слизову оболонку прямої кишки, викликають дискомфорт; розплави мають недостатню в’язкість і можуть витікати |
| Сплав ГБО-5Т | Гідрогенізованої бавовняної олії — 95%, емульгатора Т-2 — 5%. За структурними особливостями не поступається маслу какао, але стабільніший, легко поглинає водні розчини завдяки наявності емульгатора. Використовується для виливання супозиторіїв | – |
| Сплав ГАО-ЗТ | Гідрогенізованої арахісової олії — 97%, емульгатора Т-2 або пропіленгліколю моностеарату — 3%. Має такі самі властивості, як і ГБО-5Т | – |
| Твердий жир | Має два склади: 1) ланолю — 60 г, твердого жиру — 20 г, парафіну — 20 г; 2) ланолю — 80 г, твердого жиру — 40 г, парафіну — 10 г. Твердий жир являє собою суміш тригліцеридів високого заміщення жирних кислот (від С18Н17СООН до С18Н37СООН) у різних пропорціях та моно- і дигліцеридів. Промислово виробляються три основних марки: Massa estarinum, Suppocire та Witepsol, які відрізняються за своїми властивостями. |
Ланоль — суміш етерів фталієвої кислоти з високомолекулярними спиртами кашалотового жиру |

Допоміжні речовини у твердих дисперсних системах. Допоміжні речовини у виробництві таблеток призначені для надання таблетковій масі необхідних технологічних властивостей, що забезпечують точність дозування, механічну міцність, розпадання, а також стабільність у процесі зберігання. За призначенням допоміжні речовини фармацевтичної системи у формі таблеток поділяються на розріджувачі (наповнювачі), стабілізатори, плівкоутворювачі, зв’язувачі (склеювачі), розпушувачі, антифрикційні (ковзні, змащувальні), барвники та коригенти.
Наповнювачі (розріджувачі) — речовини, які вводяться до складу системи з метою досягнення необхідної маси кожної дози таблетованих ліків з малим вмістом (зазвичай 0,01–0,001 г) АФІ (буряковий і молочний цукри, натрію хлорид, глюкоза, крохмаль, натрію гідрокарбонат). З появою методу прямого пресування асортимент наповнювачів для таблеток розширився за рахунок таких речовин, як похідні целюлози, модифіковані крохмалі, кальцію фосфат двозаміщений, кальцію сульфат, кальцію окис, гідрокарбонат і магнію карбонат основний, манітол, сорбітол, сечовина та ін. Наповнювачі визначають технологічні властивості таблеткової маси, фізико-хімічні властивості таблеток. Доведена доцільність застосування як наповнювачів для таблеток похідних целюлози, зокрема мікрокристалічної (авіцел). Найкращим наповнювачем для прямого пресування таблеток із саліциламідом, натрій саліцилатом, тетрацикліну гідрохлоридом є целюлоза мікрокристалічна. Для одержання таблеток етмозину та фторазину — кальцію фосфат двозаміщений. Останнім часом при виробництві таблеток використовують крохмалі модифіковані (целутаб і карбоксиметилкрохмаль) з додаванням 1% магнію стеарату. Наприклад, при введенні карбоксиметилкрохмалю до складу таблеток кетофенілбутазону відзначається помітне подовження часу їх розпадання та пролонгується терапевтичний ефект субстанції.
Зволожувачі (склеювачі) — речовини, що збільшують взаємне зчеплення окремих часток таблеткової маси й обумовлюють міцність гранул або таблеток, визначають їх технологічні властивості, тобто поведінку при пресуванні, а також властивості готової таблетки (зовнішній вигляд, міцність і розпадання). Частинки більшості активних речовин мають невелику силу зчеплення й для їх таблетування необхідно використовувати високий тиск, що часто є причиною одержання неякісних таблеток і передчасного зношування прес-інструмента. Для досягнення необхідної сили зчеплення при порівняно невисоких тисках до таблеткової маси додають зволожувальні речовини, які, заповнюючи простір між частинками, збільшують їх контактну поверхню й когезійну здатність. Особливу роль відіграють склеювальні речовини при пресуванні складних порошків, які в процесі роботи таблеткової машини можуть розшаровуватися й призводити до отримання таблеток з різним вмістом окремих інгредієнтів. Раціональність застосування склеювальних речовин і їх кількість залежать від фізико-хімічних властивостей суміші речовин, що підлягають пресуванню. Функції зволожувальних речовин можуть виконувати вода, спирт етиловий, сироп цукровий, клейстер крохмальний, розчини ВМС (желатину, спирту полівінілового, полівінілпіролідону, метилцелюлози, оксипропілметилцелюлози, карбоксиметилцелюлози, натрій-карбоксиметилцелюлози, натрію альгінату та ін.). Так, наприклад, воду застосовують у випадках, коли звичайне зволоження забезпечує належне гранулювання порошкоподібної маси; спирт використовують для гранулювання порошків гігроскопічних і найчастіше — коли до складу таблеткової маси входять сухі екстракти з рослинної сировини, які з водою та водними розчинами утворюють клейку, плинну масу, що погано гранулюється. Концентрація спирту зазвичай тим вища, чим гігроскопічніший порошок. Для порошків, які утворюють з водою й спиртом розсипчасті (що не гранулюються) маси, застосовують розчини ВМС, зволожувальна здатність яких визначається не тільки їх концентрацією й в’язкістю, але й розмірами молекули. Різні речовини-зволожувачі істотно впливають на розчинність і вивільнення АФІ з таблеток. Так, оптимальна розчинність і вивільнення цефалексину моногідрату з таблеток відмічають при застосуванні полівінілпіролідону. При прямому пресуванні таблеток з кислотою аскорбіновою, левоміцетином, тетрацикліну гідрохлоридом, комплексом вітамінів групи В належне розпадання й розчинність виявляються при використанні ПЕГ 6000. Таблетки парацетамолу, виготовлені методом вологої грануляції, легше вивільняють субстанцію, мають кращі фармацевтичні параметри (масу, твердість) при використанні натрію альгінату (4%) у порівнянні з крохмалем, карбоксиметилцелюлозою, желатином і камеддю аравійською.
Розпушувачі — речовини, що забезпечують механічне руйнування (розпадання) таблетки в шлунку або кишечнику при контакті з травними соками; вводяться в таблеткову масу з метою швидшого вивільнення активних речовин. Розпушувачі додають до складу таблеткової маси тоді, коли АФІ нерозчинний у воді, коли таблетка «цементується» під час зберігання або у випадках, коли при пресуванні різко зменшується пористість і утруднюється проникнення рідини всередину таблетки. Відомо, що терапевтична ефективність таблеток, які вводяться в організм, залежить від часу й характеру їх розпадання. За механізмом руйнівної дії розпушувачі поділяють на три групи.
1. Такі, що адсорбують воду і розривають таблетку за рахунок набрякання (крохмаль і його похідні, агар, кислота альгінова та її солі, похідні целюлози, поліметакрилат, амілопектин, ультраамілопектин та ін.).
2. Такі, що руйнують таблетку за рахунок газоутворення (суміші натрію гідрокарбонату з кислотою лимонною або виннокам’яною). Застосовуються в основному при одержанні «шипучих» таблеток. При проникненні води або травних соків у масу таблетки, що містить суміш зазначених речовин, відбувається реакція взаємодії компонентів суміші, що супроводжується виділенням вуглецю діоксиду, який руйнує таблетку. Взагалі всі розпушувальні речовини забезпечують руйнування таблеток на дрібні часточки при їх контакті з рідиною, внаслідок чого відбувається різке збільшення сумарної поверхні часток, що сприяє вивільненню та всмоктуванню активних речовин.
3. Такі, що поліпшують змочуваність і водопроникність таблетки (ПАР — спени, натрію лаурилсульфат, твін-80). ПАР застосовують у десятих частках відсотка стосовно АФІ у поєднанні із крохмалем як капіляроутворювальною і розпушувальною речовиною, що набрякає у воді. Комбінація розпушувача і ПАР діє синергічно на розпадання таблетки, обумовлюючи механізм змочування, капілярності й здатності до набрякання.
Належний розпушувальний ефект у таблетках з гідрофобними речовинами забезпечують композиції допоміжних речовин, які мають капіляроутворювальні та гідрофілізуючі властивості й здатні до набрякання. Так, нині виробляють таблетки, які швидко розпадаються, з використанням твіну-80 і крохмалю. У більшості випадків здатність таблеток розпадатися є чинником, який істотно впливає на процес вивільнення активної речовини і в кінцевому підсумку — на її біологічну доступність. Серед проблем виробництва фармацевтичних препаратів у формі таблеток є одержання задовільної плинності грануляту в живильних пристроях (лійках, бункерах). Отримані гранули або порошки мають шорсткувату поверхню. Це ускладнює їх надходження до матричних гнізд. Крім того, гранули можуть прилипати до стінок матриць і пуансонів унаслідок тертя, що розвивається в контактних зонах частинок із прес-інструментом таблеткової машини. Для уникнення або зменшення вираженості цих небажаних явищ застосовують антифрикційні речовини, які за механізмом дії поділяються на три групи: речовини, що поліпшують сипкість грануляту (ковзні), мають адгезійні властивості (змащувальні), до речовин змішаного типу належать стеарати (кальцію, магнію й алюмінію). Як ковзні речовини застосовують високодисперсні порошки тальку, висушеного крохмалю картопляного, каоліну, аеросилу, целюлози мікрокристалічної. Кількість тальку та каоліну у таблетковій масі повинна бути не більше 3%, аеросилу — 10%, оскільки вони подразнюють слизові оболонки. Ковзні речовини, адсорбуючись на поверхні часток (гранул), усувають або зменшують їх шорсткість, підвищуючи таким чином плинність. Найвищу ефективність плинності мають частинки зі сферичною формою. До змащувальних речовин належать жири, жирні кислоти та їх солі (кислота стеаринова, кальцію й магнію стеарати), вуглеводні (олія вазелінова) і деякі ВМС (твін-80, ПЕГ 4000), кількість яких не повинна перевищувати 1%, а також тальк. Тальк — один із представників типу пластинчастих силікатів, в основі яких лежать шари найщільнішої гексагональної упаковки, зв’язані один з одним залишковими вандерваальсовими силами, найслабшими з усіх хімічних зв’язків. Завдяки цій властивості та високій дисперсності частинок вони здатні до деформації й належного ковзання. Змащувальні речовини не тільки знижують тертя на контактних ділянках, але й значною мірою полегшують деформацію частинок унаслідок їх адсорбції (за рахунок проникнення в мікрощілини). Основна функція змащувальних речовин полягає в усуненні сили тертя між гранулами й стінкою матриці та спресованою таблеткою й стінкою матриці в момент її виштовхування. Таким чином, застосування ковзних і змащувальних речовин забезпечує краще ковзання часток, створює тонку поверхневу плівку на внутрішніх стінках матриці й зменшує силу тиску, що забезпечує необхідну міцність таблеток. Вибір оптимальних допоміжних речовин при виробництві фармацевтичних систем у формі таблеток є одним із найважливіших чинників, які визначають їх максимальний терапевтичний ефект; його необхідно здійснювати з урахуванням їх впливу на фізико-механічні властивості грануляту, що пресується, на стабільність активних речовин і біофармацевтичні характеристики готового фармацевтичного продукту. Так, ароматизатори при виробництві таблеток і гумок доцільно додавати у вигляді розчинів безпосередньо до гранул, якщо ліки застосовуються для лікування ротової порожнини або верхніх дихальних шляхів (крім аерозолів). Барвники вводять до складу таблеток, насамперед, для надання їм товарного вигляду, з метою позначення терапевтичної групи активних речовин, наприклад, снодійних, отруйних (меркурію дихлорид). Крім того, деякі барвники є стабілізаторами світлочутливих активних речовин.
Солюбілізація як технологічний процес. Солюбілізатори. У фармацевтичній технології підвищення розчинності гідрофобних речовин можна досягнути різними шляхами:
- використанням гідрофілізуючих комплексоутворювачів (ПВП, амінокислоти, протеїни, сечовина, натрій саліцилат);
- використанням співрозчинників (бензилбензоат, спирт бензиловий, пропіленгліколь, ПЕГ, ДМСО, етилцелозольв та ін.);
- використанням солюбілізаторів (НПАР та їх похідні: твіни, жироцукри та ін.).
На сьогодні вивчення процесу солюбілізації (підвищення розчинності важкорозчинних або практично нерозчинних АФІ) цікаве не тільки з теоретичного, але й практичного боку, оскільки відкриває нові можливості використання нерозчинних і важкорозчинних у воді речовин, що дозволяє:
- підвищити ефективність активних речовин;
- знизити дозу використання активних речовин, наприклад, гідрокортизону, преднізолону, синестролу, барбітуратів, антибіотиків та ін.;
- змінити природу розчинника, особливо це важливо при виробництві розчинів для ін’єкцій, наприклад, використання водного розчину камфори замість олійного, який погано розсмоктується і нерідко призводить до утворення пухлин;
- змінити один шлях уведення ліків на інший, більш безпечний та зручний для хворого, наприклад, замінити таблетки протигрибкового антибіотика гризеофульвіну (зазвичай використовують протягом тривалого часу при захворюваннях шкіри) на солюбілізований розчин для місцевого застосування, що призводить до зниження загрози кандидомікозу (виникає при тривалому пероральному використанні антибіотика).
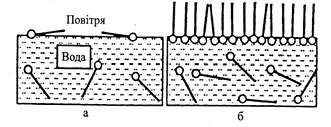
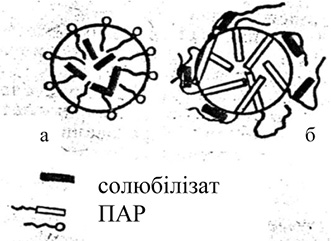
Солюбілізовані активні речовини з огляду на терапевтичну ефективність мають значно більшу абсорбцію, що зумовлено не тільки їх високою дисперсністю, але й впливом ПАР на проникність клітинних мембран. Солюбілізація як технологічний процес являє собою самоплинний перехід нерозчинної у воді речовини в розчин НПАР з утворенням термодинамічно стійкої системи. Механізм солюбілізувальної дії НПАР пов’язаний зі здатністю цих молекул у певних концентраціях утворювати додаткову міцелярну фазу, яка для деяких речовин може бути фазою розчинення. Такі речовини НПАР називають солюбілізаторами. У водних розчинах молекули ПАР мають тенденцію накопичуватися на поверхні водної фази доти, доки поверхня не буде повністю покрита молекулами ПАР — критична концентрація міцелоутворення (ККМ) (рис. 5). При концентрації розчину ПАР вище ККМ надлишок ПАР створює міцели, тобто нову (колоїдну) фазу. Внаслідок зчеплення вуглеводневих ланцюгів молекул ПАР вандерваальсовими силами утворюються міцели, які мають гідрофільну оболонку з полярних груп та неполярне ядро (рис. 6а). Утворена міцелярна фаза може бути додатковою фазою для розчинення АФІ шляхом фіксації молекул неполярних речовин. У неводних розчинах структура міцели протилежна, тобто вуглеводневі ланцюги молекули ПАР орієнтуються назовні, а полярні групи знаходяться в ядрі міцели (рис. 6б). Отже, внутрішню частину міцели можна розглядати як своєрідну полярну мікрофазу. Такі системи мають здатність солюбілізувати полярні речовини. Крім прямого типу солюбілізації, використовується й зворотний тип для отримання ліків пролонгованої дії, наприклад, олійних розчинів ціанокобаламіну. Збільшення довжини аліфатичного ланцюга ПАР сприяє міцелоутворенню (цією властивістю обумовлена солюбілізація оліофільних сполук). Дуже розбавлені розчини неіоногенних ПАР подібні до розчинів звичайних електролітів. Однак при підвищенні їх концентрації до ККМ різко змінюються різні фізико-хімічні характеристики (електропровідність, поверхневий натяг, осмотичний тиск, в’язкість та ін.), а такі показники ПАР, як поверхнева активність, ККМ і ГЛБ є визначальними для їх солюбілізувальних властивостей. Метод солюбілізації використовують для підвищення стійкості активних речовин, наприклад, аніоноактивні ПАР зменшують швидкість гідролізу дикаїну в 10 разів, новокаїну гідрохлориду — в 4 рази. Солюбілізовані розчини (іхтіол, мильно-крезолові препарати та ін.) у фармацевтичній практиці використовують давно. У наш час солюбілізатори використовують у виробництві розчинів для місцевого, внутрішнього та ін’єкційного застосування для різних груп нерозчинних АФІ (вітамінів А, D, Е і К, барбітуратів та інших речовин, у тому числі антибіотики, цитостатики, гормони). З використанням твіну-80 як солюбілізатора отримані розчини для ін’єкцій високоефективного цитостатика фенестерину, гормонів синестролу та октестролу, а також етерних олій для виготовлення ароматних вод.
Далі буде!
Національний фармацевтичний університет

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим