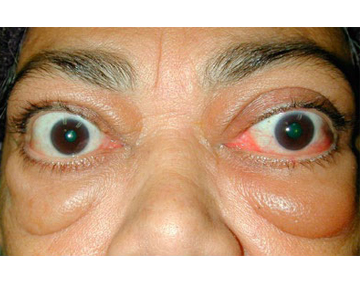
 Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) 21 января выдало разрешение на маркетинг препарата Tepezza (тепротумумаб- trbw) для лечения эндокринной офтальмопатии – поражения глаз, характерного для тиреотоксикоза (повышенной активности гормонов щитовидной железы). Данное одобрение – первое для лечения у взрослых этого аутоиммунного заболевания, проявляющегося патологическими изменениями в мягких тканях орбиты с последующим вовлечением тканей глаза.
Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) 21 января выдало разрешение на маркетинг препарата Tepezza (тепротумумаб- trbw) для лечения эндокринной офтальмопатии – поражения глаз, характерного для тиреотоксикоза (повышенной активности гормонов щитовидной железы). Данное одобрение – первое для лечения у взрослых этого аутоиммунного заболевания, проявляющегося патологическими изменениями в мягких тканях орбиты с последующим вовлечением тканей глаза.
Препарат тепротумумаба- trbw был одобрен на основании результатов 2 исследований с участием 170 пациентов с острыми проявлениями эндокринной офтальмопатии. Из получавших препарат пациентов 71% в 1-м и 83% – во 2-м исследовании продемонстрировали уменьшение выраженности проптоза (протрузии глазного яблока) более чем на 2 мм, тогда как среди получавших плацебо таковых было 20 и 10% соответственно.
Разрешение на маркетинг по ускоренной процедуре в качестве орфанного препарата для прорывной терапии получила компания «Horizon Therapeutics Ireland DAC».
По материалам www.fda.gov; фото: www.sgh.com.sg

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим