У 2012 р. у світі зареєстровано 14,1 млн вперше діагностованих онкологічних захворювань, 8,2 млн випадків смерті та ще 32,6 млн осіб, у яких раніше було діагностовано онкозахворювання у 5-річний період. Онкологічні хвороби займають 2-ге місце у структурі смертності у всьому світі, що становить близько 13% усіх випадків смерті щорічно.
Наукове розуміння онкологічної патології швидко розвивається, що, в свою чергу, зумовлює поліпшення профілактики, діагностики та лікування хвороб цього профілю. Вдосконалення розуміння розвитку онкологічних захворювань на молекулярному рівні викликало появу нових багатообіцяючих сполук для лікування багатьох видів злоякісних новоутворень.
Таргетне лікування, імуноспрямована терапія і сучасна діагностика дають надію на поліпшення результатів виживаності, якості життя та визначення пацієнтів, що найбільше піддаються лікуванню. Проте, як і інші складові лікування онкозахворювань, ці препарати є дуже дороговартісними.
Підходи до оцінки технологій охорони здоров’я
Збільшення кількості пацієнтів з онкологічними захворюваннями, які потребують лікування і довгострокового супроводу, відповідно підвищує і навантаження на систему охорони здоров’я. Під тиском необхідності скорочення витрат і досягнення при цьому максимальної ефективності ці системи повинні ретельно розподіляти свої обмежені ресурси на лікування різних хвороб.
У більшості національних систем охорони здоров’я розвинених країн світу використовують метод оцінки технологій охорони здоров’я (Health Technology Assesment — HTA) для раціонального розподілу дефіцитних ресурсів, у тому числі рівня відшкодування витрат на інноваційні препарати.
Існує два основних підходи HTA: один з них базується більшою мірою на клінічній ефективності терапії. Другий ґрунтується в основному на ефективності витрат, що означає витрати на 1 рік збереженого життя з урахуванням його якості (вартість за quality adjusted life year — QALY, або cost per quality-adjusted life year — CPQ). QALY — кількість якісних років життя, які отримав пацієнт унаслідок лікування, а CPQ — витрати на одну одиницю корисності кожного методу лікування.
При цьому якістю життя вважається рівень благополуччя і задоволеності життям (фізичним, психологічним, соціальним станом), на які впливають хвороба, нещасний випадок та їх лікування, а також оцінка хворим тих негативних змін, що відбулися чи можуть відбутися в результаті цих захворювань.
Методологія із використанням CPQ
У CPQ-методології використовують стандартизований показник вартості для визначення розміру реімбурсації при лікуванні усіх хвороб.
Цей показник, як правило, відповідає співвідношенню витрати-ефективність у запропонованій ціні виробника. Оцінка ефективності витрат вимагає аналізу клінічної, соціальної та/або економічної цінності лікування; визначення відповідності заявленої ціни виробника соціально чи економічно прийнятому порогу допустимих витрат на одиницю вартості.
Основною умовою CPQ-методології є те, що гроші, витрачені, наприклад, на препарати онкологічного профілю, не будуть доступні ні для чого іншого.
Методології без використання CPQ
Методології без використання CPQ, насамперед, оцінюють клінічну ефективність нового препарату і поліпшення здоров’я пацієнтів. Лікувальні заклади за допомогою такої методології розраховують розміри витрат, бюджет та ефективність витрат опосередковано, а не порівнюючи переваги для здоров’я з чітко визначеним та встановленим порогом рентабельності.
Клінічна ефективність у такому разі визначається або в ході процедури отримання ліцензії на маркетинг, або в ході іншого процесу. Такі рішення приймають, наприклад, Управління з контролю за харчовими продуктами та лікарськими засобами США (Food and Drug Administration — FDA), Європейське агентство з лікарських засобів (European Medicines Agency — EMA) та інші національні регуляторні органи. Рівень реімбурсації потім погоджується між платниками (державними чи приватними) та виробниками лікарських засобів.
Де ж доступність онкопрепаратів вища?
П’ять країн, що використовують CPQ, і п’ять країн, які не використовують цей показник, були відібрані для вивчення ефективності реімбурсації вартості нових онкологічних препаратів (табл. 1).
| Таблиця 1 | Країни, які включено у дослідження |
| З використанням CPQ | Без використання CPQ |
|---|---|
| Австралія | Франція |
| Канада | Німеччина |
| Англія* | Італія |
| Шотландія* | Іспанія |
| Швеція | США |
Ці країни були визначені як ті, що мають передові системи охорони здоров’я та використовують новітні підходи щодо прийняття рішень при відшкодуванні вартості лікарських засобів.
У дослідженні проаналізовано препарати, які були затверджені EMA у період з 1 січня 2009 р. по 31 березня 2012 р. (рис. 1 та табл. 2), зокрема онкопрепарати та лікарські засоби для лікування інших захворювань, для визначення доступності терапії онкопатології порівняно з іншими захворюваннями. Так, усі фільтри пройшли лише 9 онкопрепаратів та 17 препаратів для лікування інших захворювань.
| Схвалення EMA |
| Усі 143 нові лікарські препарати, що отримали ліцензію на маркетинг від EMA у 2009–2012 рр. |
 |
| Визначення інтересів |
| Виключено 33 продукти з короткочасними ефектами, вакцини та комбінації фіксованих доз, що не є новими хімічними субстанціями |
 |
| Оцінка NICE* |
| Виключено 79 продуктів з відсутньою опублікованою технологічною оцінкою NICE |
 |
| Схвалення FDA |
| Виключено 5 продуктів, що не отримали схвалення FDA |
Методологія відбору
| Таблиця 2 | Препарати, включені в дослідження |
| Бренд | Призначення | Виробник |
|---|---|---|
| Онкологічні лікарські засоби | ||
| Афінітор® (еверолім) | Рак нирки | Novartis |
| Halaven (ерібулін) | Рак молочної залози | Eisai Europe Ltd |
| Вотрієнт® (пазопаніб) | Рак нирки | GlaxoSmithKline |
| Jevtana (кабазітаксел) | Рак передміхурової залози | Sanofi-Aventis |
| Zytiga (абіратерону ацетат) | Рак передміхурової залози | Janssen |
| Yervoy (іпілумаб) | Меланома | Bristol-Myers Squibb |
| Зелбораф® (вемурафініб) | Меланома | Roche |
| Арзерра® (офатумумаб) | Хронічний лімфолейкоз | GlaxoSmithKline |
| Xgeva (деносумаб) | Метастатичний рак кісток | Amgen |
| Неонкологічні лікарські засоби | ||
| Актемра® (тосілізумаб) | Ревматоїдний артрит | Roche |
| Cimzia (цертолізумаб пегол) | Ревматоїдний артрит | UCB Pharma |
| Сімпоні® (голімумаб) | Ревматоїдний артрит | Janssen (Merck in EU) |
| Стелара® (устекінумаб) | Псоріаз | Janssen |
| Виктреліс® (боцепревір) | Гепатит С | Merck |
| Інсиво®/Incivek (телапревір) | Гепатит С | Janssen |
| Гіленія® (фінголімод) | Розсіяний склероз | Novartis |
| Nplate (роміплостін) | Ідіопатична тромбоцитопенічна пурпура (хвороба Верльгофа) | Amgen |
| Promacta/ Revolade (елтромбопаг/елтромбопагу оламін) | Ідіопатична тромбоцитопенічна пурпура (хвороба Верльгофа) | GlaxoSmithKline |
| Еффієнт® (прасургел) | Гострий коронарний синдром | Eli Lilly |
| Victoza (ліраглутид) | Цукровий діабет ІІ типу | Novo Nordisk |
Більшість країн в обох групах відшкодовують вартість препаратів, що застосовуються для лікування неонкологічних захворювань.
У всіх країнах, які не використовують CPQ, вартість 9 онкологічних лікарських засобів відповідно до цього аналізу відшкодовується, за винятком Арзерри® (офатумумаб) в Іспанії. 4 з 5 країн, що використовують CPQ, відмовилися відшкодовувати вартість принаймні 3 з 9 онкопрепаратів. З іншого боку, 100% показника реімбурсації усіх категорій лікарських засобів досягли такі країни, як Швеція, США, Німеччина.
Дані, наведені в табл. 3, демонструють, що для обох категорій препаратів (зазначених у табл. 2) середній час між отриманням ліцензії на маркетинг та прийняттям рішення про реімбурсацію значно більший у країнах, що використовують CPQ.
| Таблиця 3 | Час між маркетинговим затвердженням препаратів та прийняттям рішення про реімбурсацію |
| Медіана часу для всіх країн в цілому (в днях) | |
|---|---|
| Онкопрепарати в країнах, що використовують CPQ | 407 |
| Онкопрепарати в країнах, що не використовують CPQ | 167 |
| Інші лікарські засоби в країнах, що використовують CPQ | 261 |
| Інші лікарські засоби в країнах, що не використовують CPQ | 245 |
| Таблица 4 | Витрати на лікування онкозахворювань (в євро) за типом використаних ресурсів на душу населення |
| Стаціонарне лікування | Лікарські засоби | Первинна медична допомога | Амбулаторне лікування | Відділення невідкладної допомоги | Всього | ||
|---|---|---|---|---|---|---|---|
| Усі онкозахворювання | Великобританія | 47,00 | 17,00 | 2,00 | 17,00 | 1,00 | 84,00 |
| Швеція | 44,00 | 25,00 | 5,00 | 26,00 | 4,00 | 104,00 | |
| Франція | 58,00 | 47,00 | 2,00 | 3,00 | 0,30 | 110,30 | |
| Німеччина | 119,00 | 33,00 | 9,00 | 21,00 | 0,40 | 182,40 | |
| Італія | 69,00 | 28,00 | 8,00 | 8,00 | 2,00 | 115,00 | |
| Іспанія | 28,00 | 33,00 | 17,00 | 7,00 | 5,00 | 90,00 | |
| Рак молочної залози | Великобританія | 3,77 | 3,58 | 0,18 | 1,83 | 0,06 | 9,40 |
| Швеція | 2,47 | 5,27 | 0,54 | 2,58 | 0,43 | 11,18 | |
| Франція | 4,47 | 9,80 | 0,23 | 0,37 | 0,05 | 14,91 | |
| Німеччина | 14,86 | 9,49 | 1,25 | 2,97 | 0,02 | 28,60 | |
| Італія | 3,21 | 5,80 | 0,73 | 0,68 | 0,17 | 10,57 | |
| Іспанія | 1,39 | 6,91 | 1,74 | 0,76 | 0,46 | 11,28 | |
| Рак легень | Великобританія | 4,92 | 0,61 | 0,16 | 1,70 | 0,06 | 7,46 |
| Швеція | 4,41 | 0,86 | 0,43 | 2,15 | 0,32 | 8,17 | |
| Франція | 5,21 | 1,67 | 0,12 | 0,20 | 0,02 | 7,23 | |
| Німеччина | 11,70 | 1,51 | 0,92 | 2,20 | 0,05 | 16,37 | |
| Італія | 6,68 | 1,00 | 0,71 | 0,66 | 0,17 | 9,20 | |
| Іспанія | 2,72 | 1,18 | 0,54 | 0,24 | 0,15 | 4,84 | |
| Рак передміхурової залози | Великобританія | 2,04 | 3,70 | 0,08 | 0,83 | 0,03 | 6,68 |
| Швеція | 3,76 | 5,48 | 0,54 | 2,69 | 0,43 | 12,91 | |
| Франція | 4,22 | 10,17 | 0,14 | 0,22 | 0,03 | 14,78 | |
| Німеччина | 9,91 | 9,10 | 0,66 | 1,59 | 0,01 | 21,28 | |
| Італія | 2,91 | 6,01 | 0,42 | 0,40 | 0,10 | 9,84 | |
| Іспанія | 0,89 | 7,19 | 1,07 | 0,48 | 0,28 | 9,91 | |
У країнах, що використовують CPQ, в меншій кількості представлені онкологічні лікарські засоби, а їх включення до рутинної практики займає більше часу. Ухвалення сучасних онкологічних препаратів починається пізніше в країнах, що використовують CPQ, і малоймовірно, що там зможуть досягти рівня доступності, характерного для країн, що не використовують CPQ.
На сьогодні не існує єдиної стандартизованої та об’єктивної CPQ-методології, що була б прийнята більшістю країн світу. Це призводить до великих розбіжностей при прийнятті рішень щодо реімбурсації. Так, CPQ-показник у досліджуваних країнах може відрізнятися більше ніж у 20 разів.
Лікарські засоби є лише однією з багатьох статей витрат на лікування пацієнтів з онкологічними захворюваннями. Їх частка в загальній сумі варіює залежно від країни та типу онкологічної патології (рис. 2), а кожна система охорони здоров’я має свою політику щодо лікування, яка визначається національними перевагами та пріоритетами.
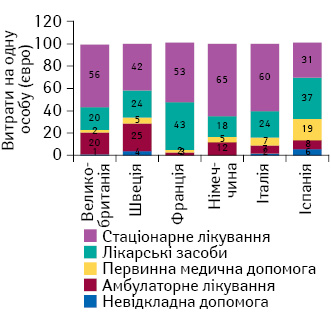
Витрати на лікарські засоби для лікування злоякісних новоутворень молочної залози та передміхурової залози (рис. 3–4) вищі порівняно з іншими, оскільки пухлини, що повільно прогресують, часто вимагають декількох років медикаментозної терапії. Вартість лікування злоякісних новоутворень легені (рис. 5) в цілому порівняно нижча, що пов’язано з численними оперативними втручаннями та коротким періодом виживаності, а також високими затратами на стаціонарне лікування.
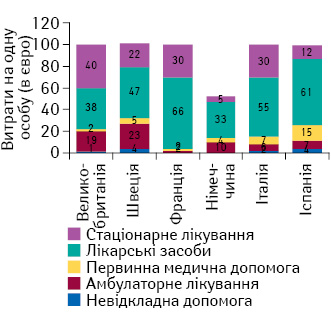
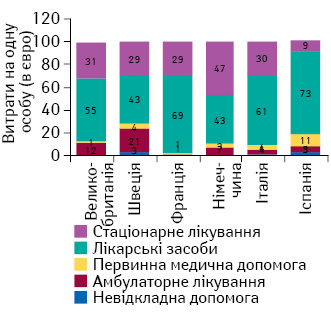
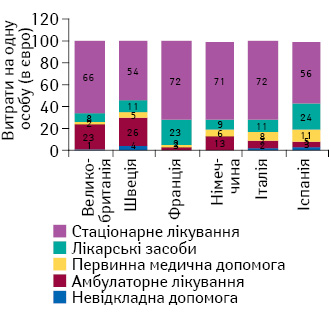
У країнах, що використовують CPQ, застосовують менше новітніх лікарських засобів, а зменшення загальних витрат на терапію знижує її ефективність. Так, наприклад, витрати Великобританії в даному дослідженні лише трохи менші за витрати інших країн ЄС, проте значно поступаються за отриманими результатами лікування. Крім того, Іспанія та Італія досягають більш високих результатів в лікуванні раку передміхурової залози, витрачаючи не набагато більше коштів порівняно з іншими досліджуваними країнами. У лікуванні раку легені Франція та Італія, витрачаючи трохи більше коштів, отримують значно кращі результати.
Англія і Шотландія витрачають не набагато менше, ніж інші країни ЄС, на лікування більшості онкологічних захворювань. Таким чином, кошти, заощаджені на реімбурсації лікарських засобів, спрямовують на інші аспекти терапії.
Обмеження при дослідженні
Дане дослідження має ряд обмежень:
- у дослідження включено лише 10 країн та 9 онкологічних препаратів;
- аналізи, представлені у дослідженні, демонструють кореляцію даних, але не доводять причинно-наслідковий зв’язок;
- аналізи ефективності лікування різними лікарськими засобами мають багато невизначеностей та суперечностей.
Висновок
Підсумовуючи основні результати цього дослідження, слід зазначити, що у 5 країнах, в яких використовують CPQ, нові онкопрепарати менш доступні, ніж в інших 5 країнах, що не використовують CPQ при прийнятті рішення про реімбурсацію. Також в країнах, що використовують CPQ, прийняття рішення про реімбурсацію займає більше часу, а нові онкологічні лікарські засоби вводять у рутинну практику набагато довше.
Незважаючи на важливість, тяжкість та поширеність онкозахворювань порівняно з багатьма іншими хворобами, доступність препаратів, що застосовують у лікуванні останніх, у досліджуваних країнах майже однакова.
Крім того, CPQ-методологія має багато невизначеності та протиріч. Деякі дані також свідчать про низький рівень виживаності при онкозахворюваннях в країнах, що використовують CPQ, і системи охорони здоров’я цих країн, таким чином, створюють менше можливостей для своїх пацієнтів. Відмінності і в доступності сучасного лікування, і в рівні виживаності від онкохвороб є особливо помітними при порівнянні Великобританії та інших країн. Багато підходів, що не використовують CPQ, не особливо визнають цінність наукових інновацій, навіть якщо ця цінність може бути критичною для конкретного препарату чи випадку в певний момент часу.
Реімбурсація нових дороговартісних ліків дає змогу продовжувати розвиток та дослідження в цьому напрямку і, таким чином, «купує» майбутні варіанти боротьби з онкозахворюваннями.
На жаль, питання онкотерапії та доступності ліків для неї не втрачає своєї актуальності і потребує подальших досліджень та пошуку нових методів лікування і сучасних лікарських засобів. Кореляція між реімбурсацією вартості нових онкологічних препаратів і виживаністю при онкозахворюваннях піднімають декілька важливих питань стосовно доступності та ефективності терапії, які потребують подальших досліджень. Такими питаннями, зокрема, є наступні:
- чи використання методології з урахуванням CPQ при прийнятті рішень про відшкодування вартості нових онкопрепаратів істотно погіршує наслідки онкологічних захворювань;
- чи існує надійна, об’єктивна, стандартизована методологія, що може бути використана для інформування про прийняті рішення щодо реімбурсації;
- чи призводить до зниження загальної вартості терапії злоякісних новоутворень витрачання меншої кількості коштів на онкологічні препарати;
- чи не призведе це до зниження ефективності інших аспектів лікування раку? І чи зберігаються гроші в цілому у довгостроковій перспективі?

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим