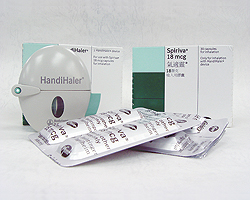
 14 января Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) объявило об окончании проведения обзора безопасности Spiriva®/Спирива® (тиотропия бромид, «Pfizer»/«Boehringer Ingelheim»). По мнению управления, имеющиеся данные исследований не поддерживают теорию, ассоциирующую применение данного препарата с высоким риском инсульта, сердечного приступа или наступления летального исхода вследствие кардиоваскулярных событий.
14 января Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) объявило об окончании проведения обзора безопасности Spiriva®/Спирива® (тиотропия бромид, «Pfizer»/«Boehringer Ingelheim»). По мнению управления, имеющиеся данные исследований не поддерживают теорию, ассоциирующую применение данного препарата с высоким риском инсульта, сердечного приступа или наступления летального исхода вследствие кардиоваскулярных событий.
Такое заключение было сделано после того, как были проанализированы результаты четырехлетнего исследования UPLIFT с участием около 6000 пациентов с хронической обструктивной болезнью легких, которые проходили терапию Spiriva или плацебо. Обзор безопасности применения препарата был инициирован в 2008 г., когда данные метаанализа предположили существование невысокого риска инсульта при применении препарата по сравнению с плацебо. Затем были отмечены две публикации, в которых сообщалось о возможности более высокого риска сердечного приступа, летального исхода или инсульта среди пациентов, применяющих Spiriva или другие препараты с подобным механизмом.
По материалам
;

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим