|
Недавний инцидент с поставками украинского зерна в Бразилию наглядно отражает суть рассматриваемой проблемы. Обнаруженный карантинными службами Бразилии микроскопический грибок Alternaria Triticina (на наличие которого контроль в Украине не проводился, хотя и поступили сведения из Бразилии о новых требованиях к импорту сельскохозяйственной продукции) поставил под угрозу новый рынок сбыта и имидж страны в целом [1].
Проблема, рассматриваемая далее, затрагивает интересы отечественных производителей фармацевтической продукции и заключается в том, что результаты контроля качества нерастворимых ЛС по показателю «Микробиологическая чистота», полученные методом мембранной фильтрации с использованием предфильтров, утвержденным в Государственной Фармакопее Украины [2], являются недостоверными и (или) ложноположительными. Проводя параллель с причинами упомянутого инцидента, следует отметить, что ни в одной фармакопее стран Европы, США, Японии при контроле микробиологических показателей качества ЛС не используется метод мембранной фильтрации с предфильтрами. Поэтому, выходя на внешний рынок, отечественные производители могут оказаться в аналогичной ситуации, когда качественный в соответствии с национальными требованиями лекарственный препарат будет при контроле забракован другим методом, согласно требованиям государства-импортера.
Государственной инспекцией по контролю качества лекарственных средств МЗ Украины ранее поднималась проблема использования предфильтров, а именно АР 15, и акцентировалось внимание на некорректности использования самого принципа предварительной фильтрации. Однако наше мнение не нашло поддержки среди специалистов и в журнале «Фармаком» № 4 за 2002 г. была опубликована статья сотрудников ГП «Научно-экспертный фармакопейный центр» «Изучение пригодности метода мембранной фильтрации с предфильтрами для контроля микробиологической чистоты нестерильных лекарственных средств», доказывающая пригодность материала адсорбционных подложек для использования в качестве предфильтров. Проведенная коллегами работа бесспорно заслуживает внимания, но используемые модели препаратов, искусственно контаминированных тест-микроорганизмами, не отражают условий естественного загрязнения ЛС в процессе их производства. Разница заключается в том, что при искусственной контаминации мелкие частицы предварительно растертого нерастворимого лекарственного препарата, суспендированного в буферном растворе, и внесенные в него микроорганизмы будут находиться отдельно друг от друга. При естественной контаминации ЛС на разных этапах его производства микроорганизмы, находящиеся в воздухе, в воде, наполнителях и т.п., будут сорбированы внутри частичек, до размеров которых может быть растерт препарат. Добиться полного высвобождения микроорганизмов возможно только при достижении степени помола препарата, равной их размерам (от 0,5 мкм), что может повредить живую клетку и, следовательно, недопустимо в данных условиях испытаний.
Таким образом, при предварительной фильтрации искусственно контаминированного образца через адсорбционную подложку, используемую в качестве предфильтра, нерастворимые частички препарата задерживаются на его поверхности, а микроорганизмы (некоторые частично) проникают на поверхность фильтра. Предфильтр с нерастворенными частичками препарата удаляется, а фильтр помещается на питательную среду, после инкубации которой проводят подсчет выросших колоний микроорганизмов. После проведения аналогичной процедуры для естественно контаминированных препаратов сорбированные в частичках микроорганизмы будут вместе с ними задержаны на поверхности предфильтра и удалены после окончания фильтрации. Поэтому результаты количественного определения содержания микроорганизмов в нерастворимых ЛС (таблетки, капсулы, драже, мази), полученные при использовании метода мембранной фильтрации с любым типом предфильтров, предназначенным улавливать крупные частицы, недостоверны и значительно ниже их реального значения. Следует отметить, что при повышении степени разведения препарата разница между числом колониеобразующих единиц (КОЕ) микроорганизмов, полученных методом прямого посева (действительное количество) и методом мембранной фильтрации с предфильтром, уменьшается в пределах приблизительно от 100 до 10 раз.
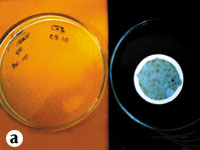
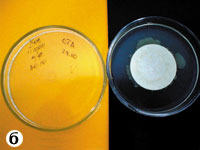
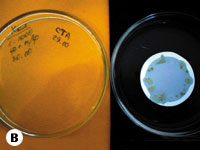
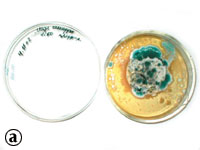
Результаты исследований, проведенных в Центральной лаборатории по анализу качества лекарственных средств МЗ Украины таблеток Холензим методом мембранной фильтрации с использованием предфильтров (адсорбционных подложек), свидетельствуют о том, что при содержании бактерий 42 000 КОЕ/г выявлено 950 КОЕ/г, что в 44 раза меньше действительного значения. По результатам посевов таблеток Холензим и мази «Календула» выявлен рост микроорганизмов на поверхности как фильтра, так и предфильтра, что доказывает задержку на их поверхности микроорганизмов и, следовательно, получение недостоверных результатов (рис. 1, 2).
|
Таблетки Холензим; разведение 1:1000.
Таблетки Холензим; разведение 1:1000.
Таблетки Холензим; разведение 1:1000. |
Рис. 1. Результаты контроля таблеток Холензим методом мембранной фильтрации без и с использованием предфильтров
|
Мазь «Календула»; разведение 1:50.
Мазь «Календула»; разведение 1:50. |
Рис. 2. Результаты контроля мази «Календула» методом мембранной фильтрации без и с использованием предфильтров
Подробное описание исследований, доказывающих непригодность предфильтров (адсорбционных подложек) для проведения испытаний нерастворимых препаратов методом мембранной фильтрации, будет позднее опубликовано в прессе.
Применение такого метода, что отражено в государственном стандарте — Государственной Фармакопее Украины, делает напрасными все усилия и материальные вложения, затрачиваемые на внедрение правил GMP в производственную практику отечественных фармацевтических предприятий. Микробиологический контроль (начиная с сырья и заканчивая готовой продукцией) с использованием данного метода не позволяет выявить достоверную степень микробного загрязнения, что может непосредственно нанести вред здоровью человека или в результате разрушительного влияния продуктов жизнедеятельности микроорганизмов снизить эффективность препарата.
С нашей позиции — позиции защиты здоровья потребителей, эта проблема требует немедленного рассмотрения и принятия соответствующих мер. Однако инертность производителей, заинтересованность которых в качестве своей продукции должна быть максимальной, создает своеобразный вакуум, не позволяющий проникать голосу разума. Так как в течение года с момента поднятия вопроса о корректности использования обсуждаемого метода не было принято надлежащего решения, в новых разработках контроля микробиологической чистоты препаратов в соответствии с требованиями ГФУ продолжает применяться метод мембранной фильтрации с использованием предфильтров, не позволяющий получать достоверные результаты. При этом в случае выявления брака или невоспроизводимости методов контроля препарата не разработчик методик, а производитель несет ответственность за качество своей продукции и терпит моральный и материальный ущерб.
Центральной лабораторией по анализу качества лекарственных средств МЗ Украины проведено достаточно много исследований, подтверждающих непригодность метода предварительной фильтрации нерастворимых ЛС, воспроизводимость эксперимента может быть обеспечена и в условиях микробиологических лабораторий фармацевтических производств.
Остается добавить, что только совместными усилиями можно решить данную проблему и множество других вопросов микробиологического контроля ЛС и тем самым гарантировать их качество в соответствии с европейскими стандартами.
В.Г. Варченко, первый заместитель Главного государственного инспектора
Украины по контролю качества лекарственных средств
|
ЛИТЕРАТУРА |
|
|


Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим