|
|
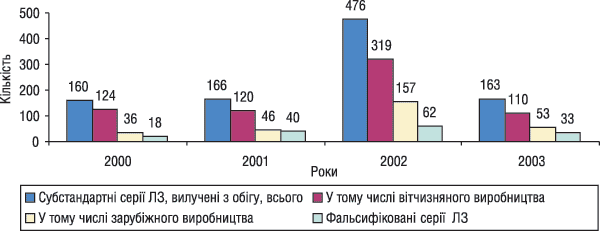
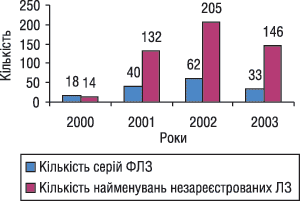
Виступаючи з доповіддю на семінарі, Сергій Сур звернув увагу присутніх на етапи розвитку фармацевтичного ринку України починаючи з 1992 р. Він зазначив, що з розвитком української фармації і насиченням українського ринку фармацевтичними препаратами, стрімким ростом фармацевтичної інфраструктури все більшого поширення набувають субстандартні фальсифіковані та незареєстровані ЛЗ (рис. 1, 2).
Заступник Головного державного інспектора зазначив, що проблема фальсифікації ЛЗ не може бути вирішена тільки за рахунок упровадження вимог належних практик, оскільки виробництво підроблених ліків здійснюється в обхід правового поля, тобто боротьба з виготовленням та поширенням ЛЗ потребує спеціальних комплексних підходів на законодавчому рівні, взаємодії із силовими структурами, об’єднання зусиль усіх легальних суб’єктів фармацевтичного ринку.
С. Сур підкреслив, що організації, діяльність яких спрямована на боротьбу з ФЛЗ, діють відповідно до таких нормативних документів: постанова Кабінету Міністрів України № 1075 від 17.07.2003 р. «Про затвердження Програми боротьби з виробництвом та розповсюдженням фальсифікованих лікарських засобів на 2003–2008 роки»; наказ МОЗ України № 411 від 04.09.2003 р. «Про забезпечення виконання Програми боротьби з виробництвом та розповсюдженням фальсифікованих лікарських засобів на 2003–2008 роки»; наказ Державної інспекції з контролю якості лікарських засобів МОЗ України № 48 від 25.09.2003 р. «Про затвердження Плану заходів Державної інспекції з контролю якості лікарських засобів МОЗ України».
|
Заступник Головного державного інспектора приділив увагу наказам МОЗ України, затвердженим у Міністерстві юстиції України, які визначають роботу Уповноважених осіб аптечних установ: № 436 від 30 жовтня 2001 р. «Про затвердження Інструкції про порядок контролю якості лікарських засобів під час оптової та роздрібної торгівлі», що регламентує роботу Уповноважених осіб, а також № 497 від 12 грудня 2001 р. «Про затвердження Порядку заборони (зупинення) та вилучення з обігу лікарських засобів на території України».
|
С. Сур докладно охарактеризував основні аспекти Програми боротьби з виробництвом та розповсюдженням фальсифікованих лікарських засобів:
· розробка і затвердження порядку вилучення з обігу, конфіскації та знищення ФЛЗ
· розробка проекту постанови Кабінету Міністрів України «Про забезпечення державного контролю за ввезенням лікарських засобів в Україну, їх подальшим транспортуванням, зберіганням, реалізацією та медичним застосуванням»;
· розробка та внесення змін до Ліцензійних умов провадження господарської діяльності з виробництва лікарських засобів, оптової, роздрібної торгівлі ЛЗ відповідно до законодавчих актів, прийнятих на виконання Програми;
· створення міжвідомчої бази даних про юридичних та фізичних осіб, стосовно яких є інформація про ввезення, виробництво, реалізацію ФЛЗ, у тому числі про суб’єктів господарської діяльності, ліцензія яких анульована, а також є інформація про причетність їх до фактів фальсифікації та щодо діяльності яких необхідно в установленому порядку вживати додаткових заходів контролю.
|
С. Сур зазначив, що фальсифікація ЛЗ — не лише проблема фармацевтичного ринку, а й усієї української спільноти, оскільки несе в собі значну загрозу для здоров’я, а іноді й життя людини. Саме тому необхідно якнайшвидше розробити законодавчу базу і створити робочу групу в складі працівників МОЗ, СБУ, МВС України для ефективної боротьби із цим явищем (рис. 2).
Характеризуючи ситуацію, що склалася з виготовленням та поширенням ФЛЗ на Черкащині, начальник Державної інспекції в Черкаській області Надія Шульга повідомила, що якість роботи цього відомства залежить насамперед від рівня підготовки та компетенції персоналу і відповідної матеріально-технічної бази.
У Державній інспекції в Черкаській області працює 11 спеціалістів, 70% із них мають практичний досвід роботи в системі контролю 15 і більше років, 7 спеціалістів — кваліфікаційні категорії.
Н. Шульга зазначила, що сьогодні на фармацевтичному ринку Черкащини працюють 130 суб’єктів господарювання, які здійснюють виробництво, оптову, роздрібну торгівлю ЛЗ, у тому числі 97 суб’єктів зареєстровано на території області. Крім цього, на фармацевтичному ринку області працюють 12 філій, 16 аптек лікувально-профілактичних закладів, 5 заводів-виробників, 538 точок з реалізації ЛЗ, із них 108 — сільські аптеки. Серед міських аптек — 45 комунальної форми власності, 104 — приватної.
Звітуючи про результати роботи Державної інспекції, Н. Шульга сказала, що протягом минулого року перевірками було охоплено 100% суб’єктів господарювання та 90% місць реалізації ЛЗ, а також усі лікарняно-профілактичні заклади області, які отримують ЛЗ за рахунок державного бюджету. Контроль за лікувально-профілактичними закладами області був одним із пріоритетних завдань Державної інспекції.
|
Контроль лікувально-профілактичних закладів щодо дотримання умов зберігання, терміну придатності здійснювався систематично, тому під час останніх перевірок (у 2003 р.) суттєвих порушень не виявлено.
Стосовно суб’єктів господарювання, в діяльності яких виявлено порушення законодавства, за результатами перевірок у 2003 р. надано 87 приписів. Кількість порушень порівняно з 2002 р. зменшилася на 10%.
Так, протягом 2003 р. інспекторами Державної інспекції складено 46 протоколів та винесено 46 постанов (на суму 3740 грн.) за ст. 167, 168, 168-1, 170, 188-10 Кодексу України про адміністративні правопорушення; 20 постанов винесено за реалізацію субстандартних ЛЗ, недоброякісність яких визначалася Уповноваженими особами візуально, а також 8 постанов щодо виявлених субстандартних ЛЗ, обіг яких було заборонено згідно з приписами Державної інспекції. Зважаючи на попередні дані, виникла необхідність у підвищенні якості вхідного контролю ЛЗ суб’єктами господарювання.
Матеріали перевірок стосовно 19 суб’єктів господарювання було направлено до органу ліцензування, 17 — до місцевих органів виконавчої влади, 24 — до місцевих правоохоронних органів.
Протягом 2003 р. в лабораторії Державної інспекції в Черкаській області проаналізовано 4949 зразків ЛЗ. Кількість лабораторних показників, за якими проводилося тестування, збільшилася до 7–11 порівняно з 4–5 у 2000 р., а навантаження на одного фахівця лабораторії протягом року збільшилося до 1025 досліджень, у 2000 р. — 660.
За результатами лабораторного контролю 106 зразків ЛЗ промислового виробництва не відповідали вимогам АНД, з них 77 вітчизняних та 29 зарубіжних, що становить 5,74% від загальної кількості проаналізованих.
Н. Шульга зазначила, що в рамках Програми боротьби з виробництвом та розповсюдженням фальсифікованих лікарських засобів відповідно до наказів МОЗ України Державною інспекцією в Черкаській області було проведено таку роботу:
— затверджено план заходів та визначено відповідальних осіб;
— складено та погоджено план спільних заходів Державної інспекції в Черкаській області, Управлінь МВС, СБУ та Черкаської державної митниці щодо виконання Програми;
— розроблено проект Положення про постійно діючу комісію за участю представників УМВС, СБУ, митниці та прокуратури;
— зроблено стенд із зразками фальсифікованих ЛЗ, виявлених на території області;
— створено атлас ФЛЗ, вилучених на території області під час перевірок;
Протягом 2003 р. та І кварталу 2004 р. здійснено 33 спільні перевірки аптечних закладів з представниками УМВС, СБУ та фахівцями Черкаської державної митниці.
За словами Н. Шульги, той факт, що держава розпочала активну боротьбу з виробниками та розповсюджувачами фальсифікованих ЛЗ, дає надію на те, що з часом кількість їх на фармацевтичному ринку України зменшиться.n
|
ДОВІДКА |
|
|
Сергій Сахацький



Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим