ПОДАННЯ
Проекту Постанови Верховної Ради України
«Про звіт Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі»
Відповідно до статті 93 Конституції України, статті 12 Закону України «Про статус народного депутата України» та статті 89 Регламенту Верховної Ради України в порядку законодавчої ініціативи вноситься на розгляд Верховної Ради України проект Постанови Верховної Ради України «Про звіт Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі».
На пленарному засіданні Верховної Ради України даний проект Постанови доповідатиме народний депутат України Дирів А.Б.
Додаток: 1. Проект Постанови на __ арк.
2. Пояснювальна записка до проекту Постанови на __ арк.
3. Звіт Тимчасової слідчої комісії на __ арк.
4. Електронні файли вищезазначених документів.
| Голова Тимчасової слідчої комісії — народний депутат України | Дирів А.Б. |
| Члени Тимчасової слідчої комісії — народні депутати України | Іонова М.М. Гелевей О.І. Донець Т.А. Лабунська А.В. Спіріна І.Д. Петренко П.Д. |
ПОЯСНЮВАЛЬНА ЗАПИСКА
до проекту Постанови Верховної Ради України
«Про звіт Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі»
1. Обґрунтування необхідності прийняття проекту Постанови
Відповідно до Постанови Верховної Ради України від 15 травня 2013 року № 236-VII утворено Тимчасову слідчу комісію Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі (далі — Тимчасова слідча комісія).
Згідно з вказаною Постановою на Тимчасову слідчу комісію покладено обов’язки з’ясувати обставини і розслідувати факти порушення Конституції України та законів України при скороченні існуючої мережі закладів охорони здоров’я, що призвело до масових звільнень медичних працівників, а також стосовно неналежного виконання державних цільових програм і комплексних заходів з охорони здоров’я, незадовільного стану реалізації проекту щодо запровадження екстреної медичної допомоги, поширення обігу та застосування небезпечних та фальсифікованих лікарських засобів, порушення законодавства України при здійсненні державних закупівель, неефективного використання державних коштів та зловживання службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі.
2. Мета та завдання проекту Постанови
Метою прийняття проекту Постанови є підведення у відповідності до статті 88 Регламенту Верховної Ради України результатів роботи Тимчасової слідчої комісії.
Проект Постанови передбачає заслуховування звіту Тимчасової слідчої комісії Верховною радою України та направлення його Президенту України та Прем’єр-міністру України, а також Генеральній прокуратурі України, Службі безпеки України, Міністерству внутрішніх справ України, Міністерству доходів і зборів України, Антимонопольному комітету України, Державній інспекції України з контролю за цінами, Державній фінансовій інспекції України для його вивчення та відповідного реагування.
3. Загальна характеристика і основні положення проекту Постанови
Постанова містить пропозиції Тимчасової слідчої комісії про те, яким чином мають бути використані висновки, до яких дійшла комісія за результатами проведеного розслідування, а саме: взяти до відома висновки і пропозиції Тимчасової слідчої комісії, викладені у звіті тимчасової слідчої комісії; направити звіт тимчасової слідчої комісії Президенту України та Прем’єр-міністру України, а також Генеральній прокуратурі України, Службі безпеки України, Міністерству внутрішніх справ України, Міністерству доходів і зборів України, Антимонопольному комітету України, Державній інспекції України з контролю за цінами, Державній фінансовій інспекції України для його вивчення та відповідного реагування.
Одночасно пропонується Генеральній прокуратурі України, Службі безпеки України та Міністерству внутрішніх справ України дати належну правову оцінку діям посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі у зв’язку з обставинами, викладеними у звіті Тимчасової слідчої комісії, та вжити відповідних заходів реагування.
Також передбачається звернутися до Президента України з пропозицією звільнити з займаної посади Міністра охорони здоров’я України Богатирьову Р.В.
4. Стан нормативно-правової бази у сфері правового регулювання
Основними нормативно-правовими актами, що регулюють відносини у даній сфері правового регулювання є Конституція України, Закон України «Про статус народного депутата України».
Прийняття проекту не потребує внесення змін до чинного законодавства України.
5. Фінансово-економічне обґрунтування проекту Постанови
Прийняття проекту цієї Постанови не потребуватиме додаткових витрат з Державного бюджету України.
6. Очікувані правові та соціально-економічні наслідки прийняття проекту Постанови
Прийняття проекту Постанови дозволить Верховній Раді України розглянути Звіт Тимчасової слідчої комісії та прийняти відповідні рішення щодо викладених у ньому висновків і пропозицій, а також сприятиме напрацюванню та розгляду законопроектів, необхідних для врегулювання існуючих прогалин та недоліків законодавства у сфері охорони здоров’я.
| Голова Тимчасової слідчої комісії — народний депутат України | Дирів А.Б. |
| Члени Тимчасової слідчої комісії — народні депутати України | Іонова М.М. Гелевей О.І. Донець Т.А. Лабунська А.В. Спіріна І.Д. Петренко П.Д. |
Проект від 07.10.2013 р. реєстр. № 3360
вноситься народними депутатами України –
членами Тимчасової слідчої комісії Верховної Ради України
з питань розслідування фактів порушень законодавства при здійсненні
державних закупівель, неефективного використання державних коштів
та зловживань службовим становищем з боку посадових осіб
Міністерства охорони здоров’я України,
інших державних підприємств, установ та організацій
у сфері охорони здоров’я та фармацевтичної галузі
ПОСТАНОВА
ВЕРХОВНОЇ РАДИ УКРАЇНИ
Про звіт Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі
Заслухавши та обговоривши звіт Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі, Верховна Рада України постановляє:
1. Звіт Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі (далі — Тимчасова слідча комісія) взяти до відома.
2. Направити звіт Тимчасової слідчої комісії Президенту України та Прем’єр-міністру України, а також Генеральній прокуратурі України, Службі безпеки України, Міністерству внутрішніх справ України, Міністерству доходів і зборів України, Антимонопольному комітету України, Державній інспекції України з контролю за цінами, Державній фінансовій інспекції України для його вивчення та відповідного реагування.
3. З огляду на критичну ситуацію, яка склалась у сфері охорони здоров’я України, звернутися до Президента України з пропозицією звільнити з займаної посади Міністра охорони здоров’я України Богатирьову Р.В.
4. Генеральній прокуратурі України, Службі безпеки України та Міністерству внутрішніх справ України дати належну правову оцінку діям посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі у зв’язку з обставинами, викладеними у звіті Тимчасової слідчої комісії, та вжити відповідних заходів реагування.
5. Генеральній прокуратурі України, Службі безпеки України та Міністерству внутрішніх справ України проінформувати Верховну Раду України за наслідками розгляду матеріалів Тимчасової слідчої комісії у 2-тижневий термін.
6. Припинити повноваження Тимчасової слідчої комісії.
7. Опублікувати Звіт Тимчасової слідчої комісії у газеті «Голос України».
8. Ця Постанова набирає чинності з дня її прийняття.
| Голова Верховної Ради України |
ЗВІТ
Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі
Тимчасова слідча комісія Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі (далі — Тимчасова слідча комісія) утворена Постановою Верховної Ради України від 15 травня 2013 року № 236-VII, відповідно до частини четвертої статті 89 Конституції України, статті 85 Регламенту Верховної Ради України.
Відповідному рішенню передували численні факти неналежного виконання державних цільових програм і комплексних заходів з охорони здоров’я, обігу та застосування неякісних та фальсифікованих лікарських засобів, що призвели до смерті пацієнтів та інших тяжких наслідків, необґрунтованого завищення цін на лікарські засоби та вироби медичного призначення, вчинення корупційних правопорушень при здійсненні державних закупівель, неефективного та нецільового використання державних коштів та майна, а також зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі.
Тимчасову слідчу комісію було утворено у складі таких народних депутатів України:
- Дирів Анатолій Борисович (голова);
- Гелевей Олег Іванович (заступник голови);
- Ващук Катерина Тимофіївна;
- Донець Тетяна Анатоліївна;
- Журавський Віталій Станіславович;
- Іонова Марія Миколаївна;
- Лабунська Анжеліка Вікторівна;
- Мисик Володимир Юрійович;
- Момот Олександр Іванович;
- Петренко Павло Дмитрович;
- Поляченко Юрій Володимирович;
- Спіріна Ірина Дмитрівна;
- Шипко Андрій Федорович.
23.05.2013 року проведено перше засідання Тимчасової слідчої комісії, під час якого було затверджено порядок та план роботи комісії, а також обрано секретаря комісії, а саме: народного депутата України Поляченка Юрія Володимировича, розподілено роботу між членами комісії, спрямовану на виявлення та розслідування фактів порушень Конституції та законів України, скорочення існуючої мережі закладів охорони здоров’я, що потягнуло масове звільнення медичного персоналу, неналежного виконання державних цільових програм і комплексних заходів з охорони здоров’я, незадовільного стану реалізації проекту запровадження екстреної медичної допомоги, поширення обігу та застосування небезпечних та фальсифікованих лікарських засобів, фактів корупційних діянь при здійсненні державних закупівель, неефективного та нецільового використання державних коштів та майна, а також зловживань службовим становищем, допущених посадовими особами Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі.
06.06.2013 року проведено друге засідання Тимчасової слідчої комісії, під час якого було обговорено поточний стан дотримання законодавства про охорону здоров’я в регіонах України. У засіданні прийняли участь представники Антимонопольного комітету України, Головного управління по боротьбі з організованою злочинністю МВС України, Генеральної прокуратури України, Державної служби статистки України, Державної фінансової інспекції України, Рахункової палати. За результатами засідання було прийнято рішення визнати незадовільним стан дотримання законодавства про охорону здоров’я в регіонах України, а також направити відповідні звернення до територіальних управлінь охорони здоров’я в областях, м. Києві та Севастополі щодо інформування комісії про стан усунення недоліків та порушень, виявлених правоохоронними органами.
19.06.2013 року проведено третє засідання Тимчасової слідчої комісії, під час якого було піднято проблему закупівлі за завищеними цінами лікарських засобів та виробів медичного призначення за бюджетні кошти. Окрім того, було обговорено питання формування цін на лікарські засоби та вироби медичного призначення, що імпортуються на митну територію України.
04.07.2013 року проведено четверте засідання Тимчасової слідчої комісії, під час якого було обговорено стан виконання державних цільових програм у сфері охорони здоров’я.
05.09.2013 року проведено п’яте засідання Тимчасової слідчої комісії, під час якого було обговорено проблемні питання, які виникають під час проведення закупівель лікарських засобів, виробів медичного призначення та іншої медичної продукції за бюджетні кошти.
Чергове засідання Тимчасової слідчої комісії, що відбулось 19.09.2013 року, було присвячено підведенню підсумків роботи комісії, опрацюванню звіту комісії, розробці проекту Постанови Верховної Ради України про затвердження даного звіту, а також обговоренню подальших напрямків роботи Комісії. За результатами даного засідання було враховано розроблені та погоджені висновки і пропозиції до звіту Тимчасової слідчої комісії, а також проект Постанови Верховної Ради України «Про звіт Тимчасової слідчої комісії Верховної Ради України з питань розслідування фактів порушень законодавства при здійсненні державних закупівель, неефективного використання державних коштів та зловживань службовим становищем з боку посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі».
Таким чином, на виконання поставлених завдань Тимчасовою слідчою комісією проведено 6 засідань.
За період своєї роботи Тимчасовою слідчою комісією направлено 320 запитів щодо надання матеріалів та інформації, необхідних для роботи комісії, до Міністерства охорони здоров’я України, Міністерства охорони здоров’я АР Крим, структурних підрозділів з питань охорони здоров’я обласних (міських) державних адміністрацій, Міністерства доходів і зборів України, Міністерства економічного розвитку і торгівлі України, Міністерства внутрішніх справ України та його територіальних підрозділів, Генеральної прокуратури України та регіональних прокуратур, Служби безпеки України, Антимонопольного комітету України, Рахункової палати, Державної служби України з лікарських засобів, Державної служби статистки України, Державної інспекції України з контролю за цінами, Державної фінансової інспекції України, Фонду державного майна України, ДП «Державний експертний центр Міністерства охорони здоров’я України».
За результатами опрацювання, аналізу і узагальнення отриманих відповідей Тимчасова слідча комісія дійшла до наступних висновків.
I. СУЧАСНИЙ СТАН У СФЕРІ ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ
Медико-демографічна ситуація в Україні продовжує залишатися надзвичайно складною і такою, що загрожує національній безпеці держави. Незадовільний стан здоров’я населення проявляється у низькій народжуваності, порівняно з високим рівнем смертності, насамперед чоловіків працездатного віку, від’ємному природному прирості населення, скороченні середньої очікуваної тривалості життя, а також високому рівні поширеності хронічних неінфекційних захворювань.
Станом на 1 січня 2013 року чисельність населення України становила 45 553,0 тисяч осіб. При цьому протягом минулого року чисельність населення скоротилась на 83,6 тисяч осіб. Коефіцієнт природного скорочення населення у 2012 році в Україні становив 3,1%. Найбільшими коефіцієнтами природного зменшення населення характеризувалися Чернігівська, Сумська, Полтавська, Черкаська, Луганська, Донецька, Кіровоградська області. В 2012 році коливання природного скорочення населення в них було від 6,3% до 9,9%.
Динаміка чисельності наявного населення України у 1991–2013 роках (млн. осіб)
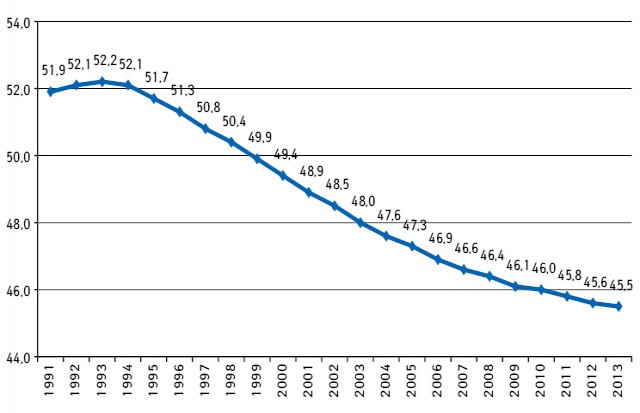
Середня очікувана тривалість життя при народженні в Україні у 2012 році становила лише 71 рік (66 років для чоловіків та 75,9 років для жінок). Між тим, за даними Всесвітньої організації охорони здоров’я, середній показник очікуваної тривалості життя при народженні в більшості країнах Європейського Союзу становить майже 76 років, а в окремих з них (Франція, Швеція, Іспанія, Норвегія) — більше 80 років.
Демографічною проблемою України є вкрай високий рівень смертності населення. Так, у минулому році померло понад 663 тисячі громадян, третина з яких — це люди працездатного і репродуктивного віку.
Регіональна диференціація смертності в Україні у 2012 році
| Адміністративно-територіальна одиниця | Кількість померлих на 1000 осіб | ||
| Все населення | Міське населення | Сільське населення | |
| Автономна Республіка Крим | 13,7 | 13,8 | 13,7 |
| Область | |||
| Вінницька | 15,4 | 11,1 | 19,7 |
| Волинська | 13.2 | 10,6 | 16,0 |
| Дніпропетровська | 15,5 | 14,9 | 18,5 |
| Донецька | 16,1 | 15,8 | 18,7 |
| Житомирська | 16,3 | 13,0 | 20,8 |
| Закарпатська | 11,8 | 11,3 | 12,1 |
| Запорізька | 14,8 | 13,7 | 18,3 |
| Івано-Франківська | 12,2 | 9,6 | 14,1 |
| Київська | 15,8 | 12,2 | 21,6 |
| Кіровоградська | 16,5 | 14,8 | 19,4 |
| Луганська | 16,0 | 15,6 | 18,8 |
| Львівська | 12,5 | 10,7 | 15,2 |
| Миколаївська | 14,7 | 13,7 | 16,9 |
| Одеська | 14,1 | 12,6 | 17,0 |
| Полтавська | 16,4 | 13,9 | 20,5 |
| Рівненська | 12,4 | 9,5 | 15,0 |
| Сумська | 16,6 | 13,9 | 22,3 |
| Тернопільська | 13,8 | 9,8 | 16,9 |
| Харківська | 14,6 | 13,5 | 18,9 |
| Херсонська | 14,7 | 14,5 | 15,1 |
| Хмельницька | 15,5 | 10,7 | 21,3 |
| Черкаська | 16,2 | 13,2 | 20,2 |
| Чернівецька | 12,5 | 10,2 | 14,2 |
| Чернігівська | 18,6 | 13,7 | 27,2 |
| Місто | |||
| Київ | 9,8 | 9,8 | – |
| Севастополь | 13,7 | 13,7 | 12,9 |
| Україна | 14,5 | 13,1 | 17,7 |
Загальний коефіцієнт смертності в Україні становив 14,5 на 1000 осіб проти 6,7 в країнах-членах ЄС.
У загальній структурі причин смертності основне місце займає смертність від серцево-судинних захворювань, показник якої є одним з найвищих у світі, та становить близько 65,8% (957,5 на 100 тисяч осіб).
Особливого занепокоєння викликає рівень онкологічної смертності, який лише за останній рік зріс майже на 4,5% та становить 14% у загальній структурі смертності (203,2 на 100 тисяч осіб). На даний час рівень онкологічної смертності чоловіків працездатного віку в Україні перевищує такий у розвинутих країнах на 40%, а жінок — на 20%.
Таким чином, фактично ці два класи хвороб визначають майже 80% щорічних втрат населення країни.
Одним з найвідчутніших індикаторів якості системи охорони здоров’я є показник смертності дітей віком до одного року. Доводиться констатувати, що рівень смертності немовлят в Україні у минулому році майже удвічі перевищував показники розвинутих європейських країн та становив 8,5%. При цьому в окремих областях України за підсумками 2012 року спостерігалось суттєве зростання кількості випадків малюкової смертності у порівнянні з 2011 роком: Хмельницькій (майже на 50%), Донецькій (на 12%), Дніпропетровській (на 8%) областях.
Смертність населення за причинами смерті в Україні у 2011–2012 роках (на 100 тисяч осіб)
| Причини смерті | 2011 рік | 2012 рік | 2012 рік% до 2011 року |
| Всього померлих | 1454,0 | 1454,5 | 100,0 |
|
Деякі інфекційні та паразитарні хвороби, у т.ч. – туберкульоз – ВІЛ |
30,415,312,2 | 30,215,212,0 | 99,399,398,4 |
| Новоутворення | 194,5 | 203,2 | 104,5 |
| Хвороби крові й кровоносних органів та окремі порушення із залученням імунного механізму | 0,6 | 0,6 | 100,0 |
| Ендокринні хвороби, розлади харчування та порушення обміну речовин | 5,5 | 5,5 | 100,0 |
|
Розлади психіки та поведінки, у т.ч. – розлади психіки та поведінки внаслідок вживання алкоголю |
3,11,8 | 3,42,0 | 109,7111,1 |
| Хвороби нервової системи | 13,4 | 13,0 | 97,0 |
| Хвороби системи кровообігу | 963,4 | 957,5 | 99,4 |
|
Хвороби органів дихання, у т.ч. – грип і пневмонія |
38,910,6 | 37,211,6 | 95,6109,4 |
|
Хвороби органів травлення, у т.ч. – алкогольні хвороби печінки |
55,25,1 | 60,85,7 | 110,1111,8 |
| Хвороби шкіри та підшкірної клітковини | 1,0 | 1,3 | 130,0 |
| Хвороби кістково-м’язової системи та сполучної тканини | 1,3 | 1,3 | 100,0 |
| Хвороби сечостатевої системи | 6,4 | 6,9 | 107,8 |
| Вагітність, пологи та післяпологовий період | 0,2 | 0,2 | 100,0 |
| Окремі стани, що виникають в перинатальному періоді | 5,1 | 5,1 | 100,0 |
| Вроджені вади розвитку, деформації та хромосомні аномалії | 4,2 | 4,0 | 95,2 |
| Зовнішні причини смерті | 91,5 | 90,0 | 98,4 |
Необхідно також звернути увагу на динаміку показників поширеності хвороб серед населення України, яка протягом останніх років має тенденцію до зростання. Так, за період 2008–2012 років рівень поширеності хвороб зріс на 2,29% і становив у минулому році 185,46 тисяч випадків на кожні 100 тисяч населення. Найвищі рівні поширеності хвороб у 2012 році зареєстровані в місті Києві (240929,8), Вінницькій (212424,7), Дніпропетровській (206361,6), Київській (201893,0), Черкаській (200511,3) областях.
Структура поширеності хвороб за класами серед всього населення України у 2012 році (%)
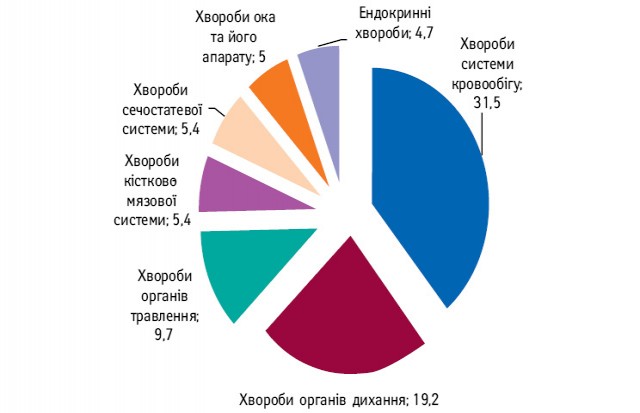
Основну частину структури поширеності захворювань становили хвороби системи кровообігу (31,5%), органів дихання (19,2%), органів травлення (9,7%), кістково-м’язової системи та сполучної тканини (5,4%), сечостатевої системи (5,4%), хвороб ока та його придаткового апарату (5,0%), ендокринних хвороб, порушень обміну речовин (4,7%).
Динаміка показників поширеності хвороб за основними класами у 2008, 2010, 2011 рр. (на 100 тис. всього населення)
| Клас хвороб | Показник | Рік | |||
|---|---|---|---|---|---|
| 2008 | 2011 | 2012 | |||
| Хвороби системи кровообігу | на 100 тис. | 55315,5 | 57967,2 | 58 385,7 | |
| питома вага | 30,51% | 30,98% | 31,48% | ||
| Хвороби органів дихання | на 100 тис. | 36005,1 | 37602,0 | 35 642,0 | |
| питома вага | 19,86% | 20,10% | 19,22% | ||
| Хвороби органів травлення | на 100 тис. | 17696,3 | 18025,3 | 18 058,1 | |
| питома вага | 9,73% | 9,63% | 9,74% | ||
| Хвороби сечостатевої системи | на 100 тис. | 9736,9 | 10074,9 | 10 007,7 | |
| питома вага | 5,37% | 5,36% | 5,40% | ||
| Хвороби кістково-м’язової системита сполучної тканини | на 100 тис. | 10031,7 | 10068,6 | 9956,4 | |
| питома вага | 5,53% | 5,38% | 5,37% | ||
| Хвороби ока та його придаткового апарату | на 100 тис. | 8954,5 | 9 246,3 | 9 240,3 | |
| питома вага | 4,94% | 4,94% | 4,98% | ||
| Ендокринні хвороби, розлади харчування та порушення обміну речовин | на 100 тис. | 8049,6 | 8541,0 | 8669,1 | |
| питома вага | 4,44% | 4,57% | 4,69% | ||
| Травми, отруєння та деякі інші наслідки дії зовнішніх чинників | на 100 тис. | 5181,1 | 4985,3 | 4 997,0 | |
| питома вага | 2,86% | 2,66% | 2,69% | ||
| Хвороби шкіри та підшкірної клітковини | на 100 тис. | 4934,7 | 4 918,1 | 4879,7 | |
| питома вага | 2,72% | 2,63% | 2,63% | ||
| Хвороби нервової системи | на 100 тис. | 4868,7 | 4 898,5 | 4 864,4 | |
| питома вага | 2,69% | 2,62% | 2,62% | ||
| Розлади психіки та поведінки | на 100 тис. | 4769,9 | 4 649,1 | 4 660,3 | |
| питома вага | 2,65% | 2,48% | 2,51% | ||
| Новоутворення | на 100 тис. | 3858,0 | 4159,4 | 4 262,7 | |
| питома вага | 2,13% | 2,22% | 2,30% | ||
| Деякі інфекційні та паразитарні хвороби | на 100 тис. | 4157,3 | 4174,3 | 4057,5 | |
| питома вага | 2,29% | 2,23% | 2,19% | ||
| Хвороби вуха та соскоподібного відростка | на 100 тис. | 3412,0 | 3502,1 | 3 504,9 | |
| питома вага | 1,88% | 1,87% | 1,89% | ||
| Хвороби крові й кровотворних органів та окремі порушення із залученням імунного механізму | на 100 тис. | 1726,7 | 1757,2 | 1729,5 | |
| питома вага | 0,95% | 0,94% | 0,93% | ||
| Природжені вади розвитку, деформації та хромосомні аномалії | на 100 тис. | 608,3 | 670,0 | 683,3 | |
| питома вага | 0,34% | 0,36% | 0,37% | ||
За останні п’ять років поширеність хвороб серед всього населення зросла на 31,1%. Найбільшими темпами зростала поширеність вроджених аномалій — 12,3% (з 608,3 — 2008 р. до 683,3 — 2012 р.), новоутворень — 10,5% (з 3858,0 — 2008 р. до 4262,7 — 2012 р.), хвороб ендокринної системи — 8,1% (з 8049,6 — 2008 р. до 8699,1 — 2012 р.), хвороб системи кровообігу — 5,6% (з 55315,5 — 2008 р. до 58385,7 — 2012 р.).
Динаміка поширеності деяких хвороб серед всього населення України
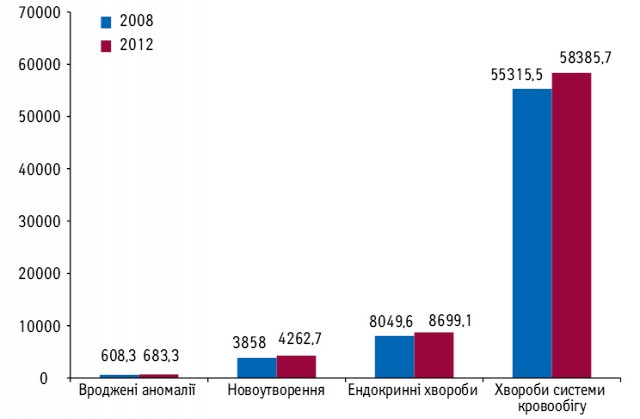
Вкрай критичною є ситуація, яка склалась у сфері протидії виникненню і поширенню захворювання на туберкульоз. Так, у 2012 році на активний туберкульоз захворіло 30958 осіб. Показник захворюваності становив 68,1 на 100 тисяч населення, що на 1,3% більше у порівнянні з 2011 роком. При цьому в 1995 році, коли за висновками Всесвітньої організації охорони здоров’я в Україні була визнано наявність епідемії туберкульозу, захворюваність на всі форми туберкульозу становила лише 41,6 випадків на 100 тисяч населення. Збільшується захворюваність на мультирезистентну форму туберкульозу. Так, за даними Всесвітньої організації охорони здоров’я, Україна займає друге місце серед країн Європи за темпами поширення даної форми туберкульозу та четверте місце у світі за темпами її поширення у хворих із вперше виявленим туберкульозом.
Загалом, від 12 до 14 мільйонів жителів країни хворіють на серцево-судинні хвороби, у понад 1 мільйона українців діагностовано новоутворення, ще більш як 1 мільйон 200 тисяч осіб хворіють на цукровий діабет, при цьому майже 200 тисяч з них є інсулінозалежними.
Таким чином, за станом здоров’я громадян Україна посідає одне з найнижчих рейтингових місць у Європейському регіоні.
Слід констатувати, що одним з основних факторів, що визначає такий негативний стан справ, є вкрай низька якість медичного обслуговування та нерівність громадян у доступі до послуг охорони здоров’я.
Вказане частково підтверджується результатами вибіркового опитування, проведеного органами Державної служби статистики України у жовтні 2012 р.
| Критерій оцінки | Показник |
|---|---|
|
Кількість домогосподарств, у яких хто-небудь із членів протягом останніх 12 місяців потребував медичної допомоги, придбання ліків та медичного приладдя: тисяч відсотків до загальної кількості |
16542,0 97,4 |
|
Кількість домогосподарств, у яких хто-небудь із членів протягом останніх 12 місяців при потребі не зміг отримати медичну допомогу, придбати ліки та медичне приладдя: тисяч відсотків до кількості домогосподарств, у яких хто-небудь із членів протягом останніх 12 місяців потребував медичної допомоги, придбання ліків та медичного приладдя |
2761,1 16,7 |
|
Кількість домогосподарств (тисяч), у яких хто-небудь із членів при потребі не зміг придбати ліки: у тому числі з причин (%): занадто висока вартість не змогли знайти інше |
2307,3
95,5 4,1 0,4 |
|
Кількість домогосподарств (тисяч), у яких хто-небудь із членів при потребі не зміг придбати медичне обладнання: у тому числі з причин (%): занадто висока вартість не змогли знайти інше |
314,1
94,2 4,4 1,4 |
|
Кількість домогосподарств (тисяч), у яких хто-небудь із членів при потребі не зміг відвідати лікаря: у тому числі з причин (%): черга була занадто довгою відсутність медичного спеціаліста необхідного профілю занадто висока вартість послуг |
1363,8
15,0 14,3 70,7 |
|
Кількість домогосподарств (тисяч), у яких хто-небудь із членів при потребі не зміг провести медичне обстеження: у тому числі з причин (%): черга була занадто довгою відсутність медичного спеціаліста необхідного профілю занадто висока вартість послуг |
1221,7
3,2 9,6 96,6 |
|
Кількість домогосподарств (тисяч), у яких хто-небудь із членів при потребі не зміг отримати лікувальні процедури: у тому числі з причин (%): черга була занадто довгою відсутність медичного спеціаліста необхідного профілю занадто висока вартість послуг |
697,7
0,8 3,8 95,4 |
|
Кількість домогосподарств (тисяч), у яких хто-небудь із членів при потребі не зміг отримати лікування у стаціонарі: у тому числі з причин (%): черга була занадто довгою відсутність медичного спеціаліста необхідного профілю занадто висока вартість послуг |
643,8
2,9 2,9 94,2 |
Звертаємо увагу на те, що з усіх зазначених у вибірковому опитуванні потреб українських громадян, причиною 71–97% відмов від надання медичної допомоги, відвідування лікаря, придбання ліків або виробів медичного призначення стала їх занадто висока вартість. І якщо вартість ліків та медичного обладнання може опосередковано регулюватись державою, то відвідування лікаря, отримання лікувальних процедур або лікування у стаціонарі у державних установах за Конституцією України взагалі повинні надаватись безкоштовно.
Окремо варто відзначити, що суттєве зростання поширеності хвороб серед всього населення України зумовлено неналежним визначенням Міністерством охорони здоров’я України кількості хворих, що потребують відповідного лікування. Так, за даними Центру медичної статистки Міністерства охорони здоров’я України, а також за уточненою інформацією з регіонів, станом на 01.01.2013 року потребують відповідного лікування: 610 дітей з муковісцидозом; 11747 дітей-інвалідів з спастичними формами дитячого церебрального паралічу; 24 дитини, хворих на мукополісахаридози; 91 дитина з первинними (вродженими) імунодефіцитами; 20455 хворих на розсіяний склероз.
Водночас Паспортом бюджетної програми на 2013 рік «Забезпечення медичних заходів окремих державних програм та комплексних заходів програмного характеру» передбачено, що в межах відповідного бюджетного фінансування передбачено забезпечення медикаментами: 236 дітей з муковісцидозом (38,6% від реальної потреби); 990 дітей з дитячим церебральним паралічем (8,42% від реальної потреби); 8 дітей, хворих на мукополісахаридози (33,3% від реальної потреби); 24 дитини з первинними (вродженими) імунодефіцитами (26,3% від реальної потреби); 8533 хворих на розсіяний склероз (41,7% від реальної потреби).
З вказаної інформації вбачається, що значна кількість хворих у цьому році не буде забезпечена необхідними медикаментами у межах бюджетного фінансування відповідних програм.
Оцінюючи сучасний стан у сфері охорони здоров’я, необхідно звернути увагу на рівень забезпеченості населення закладами охорони здоров’я.
Так, незважаючи на приписи статті 49 Конституції України, відповідно до якої існуюча мережа державних і комунальних закладів охорони здоров’я не може бути скорочена, в 2012 році спостерігалось скорочення кількості лікарняних закладів та зменшення кількості лікарів усіх спеціальностей та середнього медичного персоналу.
Статистична інформація щодо динаміки кількості лікарняних закладів, лікарняних ліжок та лікарів усіх спеціальностей у 2012 році
| Адміністративно-територіальна одиниця | Кількість лікарняних закладів | Кількість лікарняних ліжок | Кількість лікарів усіх спеціальностей | Кількість середнього медичного персоналу |
|---|---|---|---|---|
| Автономна Республіка Крим | +1 | +100 | -500 | -800 |
| Область | ||||
| Вінницька | -4 | -700 | -300 | -700 |
| Волинська | -4 | – | -100 | -500 |
| Дніпропетровська | +1 | -700 | -700 | -1500 |
| Донецька | -20 | -900 | -900 | -1800 |
| Житомирська | +3 | -100 | -200 | -600 |
| Закарпатська | -2 | -400 | -100 | -500 |
| Запорізька | -7 | -200 | -200 | -1000 |
| Івано-Франківська | – | -300 | +200 | -300 |
| Київська | +3 | -200 | -300 | -600 |
| Кіровоградська | -7 | -500 | -200 | -600 |
| Луганська | -4 | -300 | -400 | -1100 |
| Львівська | – | -100 | -600 | -1200 |
| Миколаївська | -13 | -200 | -300 | -600 |
| Одеська | -10 | -500 | -300 | -900 |
| Полтавська | -6 | -100 | -300 | -700 |
| Рівненська | -4 | -100 | -100 | -500 |
| Сумська | -2 | -500 | -200 | -600 |
| Тернопільська | -3 | -200 | -200 | -500 |
| Харківська | +5 | – | -500 | -1000 |
| Херсонська | -5 | -200 | – | -400 |
| Хмельницька | -5 | -100 | -100 | -300 |
| Черкаська | -7 | -200 | -200 | -600 |
| Чернівецька | -3 | – | – | -100 |
| Чернігівська | -2 | -200 | -200 | -500 |
| Місто | ||||
| Київ | -8 | -500 | -200 | – |
| Севастополь | -1 | – | -100 | -200 |
| Україна | -104 | -7100 | -7000 | -18100 |
Одночасно варто звернути увагу на особливо важливе значення Державної санітарно-епідеміологічної служби України. Діяльність цієї служби тісно пов’язана з профілактичною медициною та спрямована на недопущення негативного впливу на людину небезпечних факторів середовища її життєдіяльності, що можуть стати причиною виникнення інфекційних та неінфекційних хвороб. Згідно з Положенням про Державну санітарно-епідеміологічну службу України Держсанепідслужба є центральним органом виконавчої влади, діяльність якого спрямовується і координується Кабінетом Міністрів України через Міністра охорони здоров’я України. Держсанепідслужба України входить до системи органів виконавчої влади у галузі охорони здоров’я та утворюється для забезпечення реалізації державної політики у сфері санітарного та епідемічного благополуччя населення.
Водночас доводиться констатувати, що нинішнє реформування санітарно-епідеміологічної служби, що активно впроваджується у 2012–2013 роках, несе в собі надзвичайні ризики для всієї системи охорони здоров’я України. За рахунок створення міжрайонних органів кількість структурних підрозділів, відповідальних за санітарно-епідеміологічну ситуацію на місцевому рівні, скоротилась майже в 2 рази (за рахунок міських та сільських районів). Штат працівників територіальних органів Держсанепідслужби України передбачає скорочення на 40%, і такі скорочення наразі масові в державі та часто здійснюються з порушеннями норм чинного трудового законодавства.
Реформування Держсанепідслужби України детально не опрацьоване на предмет можливих наслідків послаблення санітарно-епідеміологічного контролю, призводить до втрати державного впливу на основні фактори виникнення та передачі захворювань. При цьому новостворені головні управління Держсанепідслужби України працюють в хаотичному режимі, оскільки Міністерство охорони здоров’я України належним чином не опрацювало та не підготувало нормативних документів, необхідних для повноцінного функціонування реформованої служби.
Таким чином, можна констатувати, що медико-демографічна ситуація в Україні продовжує залишатися надзвичайно складною і такою, що загрожує національній безпеці держави.
II. ВИКОНАННЯ ДЕРЖАВНИХ ЦІЛЬОВИХ ПРОГРАМ У СФЕРІ ОХОРОНИ ЗДОРОВ’Я
З метою підвищення ефективності здійснення загальнодержавних заходів з профілактики діагностики та лікування хворих, запобігання та зниження рівня захворюваності на різного роду захворювання, збільшення тривалості та поліпшення якості життя хворих шляхом підвищення рівня та забезпечення доступності медичної допомоги в Україні затверджено низку державних цільових програм у сфері охорони здоров’я.
Так, у 2012 році в Україні виконувались наступні державні цільові програми у сфері охорони здоров’я:
- Загальнодержавна цільова соціальна програма протидії захворюванню на туберкульоз на 2012 — 2016 роки (затверджена Законом України 16 жовтня 2012 року № 5451-VI);
- Загальнодержавна програма забезпечення профілактики ВІЛ-інфекції, лікування, догляду та підтримки ВІЛ-інфікованих і хворих на СНІД на 2009 -2013 роки (затверджена Законом України від 19 лютого 2009 року № 1026-VI);
- Загальнодержавна програма боротьби з онкологічними захворюваннями на період до 2016 року (затверджена Законом України від 23 грудня 2009 року № 1794-VI);
- Загальнодержавна програма імунопрофілактики та захисту населення від інфекційних хвороб на 2009 — 2015 роки (затверджена Законом України від 21 жовтня 2009 року № 1658-VI);
- Загальнодержавна програма «Національний план дій щодо реалізації Конвенції ООН про права дитини» на період до 2016 року (затверджена Законом України від 5 березня 2009 року № 1065-VI);
- Державна цільова соціальна програма «Трансплантація» на період до 2012 року (затверджена постановою Кабінету Міністрів України від 8 жовтня 2008 року № 894);
- Державна програма «Репродуктивне здоров’я нації» на період до 2015 року (затверджена постановою Кабінету Міністрів України від 27 грудня 2006 року № 1849);
- Державна цільова програма «Цукровий діабет» на 2009–2013 роки (затверджена постановою Кабінету Міністрів України від 19 серпня 2009 року № 877).
Водночас у минулому році не було забезпечено повного виконання вищезгаданих цільових програм, у результаті чого окремі якісні та кількісні показники даних програм на 2012 рік не були досягнуті. Подібна ситуація негативно відобразилась на рівні захворюваності на окремі хвороби та загальному стані здоров’я населення.
Стан виконання Загальнодержавної цільової соціальної програми протидії захворюванню на туберкульоз на 2012 — 2016 роки
Туберкульоз є другою за значимістю причиною смерті від інфекційних хвороб, поступаючись лише ВІЛ-інфекції/СНІДУ.
Серед держав Європейського регіону Україна посідає друге місце після Російської Федерації за рівнем захворюваності на туберкульоз. Стрімко збільшується захворюваність на мультирезистентну форму туберкульозу. Так, за оцінкою Всесвітньої організації охорони здоров’я, Україна займає 2-ге місце серед країн Європи за темпами поширення даної форми туберкульозу та 4-те місце у світі за її поширенням у хворих із вперше виявленим туберкульозом. Загалом, мультирезистентний туберкульоз мають 16 відсотків хворих, яким вперше встановлено такий діагноз, та 44 відсотки хворих з повторними випадками туберкульозу.
Неприпустимо високою є кількість помилок із встановлення діагнозу туберкульозу в спеціалізованих протитуберкульозних закладах (спеціалізованих структурних підрозділах закладів охорони здоров’я). Тому необхідне навчання лікарів, середніх медичних працівників, лаборантів протитуберкульозної служби та загальної мережі.
В Україні належним чином не функціонує національний і регіональні електронні реєстри хворих на туберкульоз та їх моніторинг. Значну частину інформації досі не внесено до відповідних реєстрів. Вкрай незадовільна матеріально-технічна база протитуберкульозних закладів, їх забезпечення сучасним обладнанням.
Особливої уваги потребує захворюваність на туберкульоз серед медичних працівників. До 1990 року щорічно реєструвалося до 40 таких випадків, натомість у 2012 році на туберкульоз вже захворіло 525 медиків.
Саме тому Загальнодержавною цільовою соціальною програмою протидії захворюванню на туберкульоз на 2012 — 2016 роки констатовано, що поширення туберкульозу становить загрозу національній безпеці країни, є однією з причин втрати працездатності, здоров’я, інвалідності та смертності населення.
Аналіз результатів виконання у минулому році заходів з протидії захворюванню на туберкульоз, відповідальним за виконання яких є Міністерство охорони здоров’я України, свідчить про те, що частина з них не виконана у запланованому обсязі.
| Найменування заходу | Найменування показника | Запланований показник на 2012 рік | Фактичний показник |
|---|---|---|---|
| Проведення закупівлі обладнання та витратних матеріалів для діагностики туберкульозу методом мікроскопії мазка мокротиння та посіву на тверде поживне середовище | Кількість хворих на туберкульоз, яким проведено діагностику методом мікроскопії мазка мокротиння та посіву на тверде поживне середовище, відсотків | 95 | 88,23 |
| Здійснення туберкулінодіагностики | Кількість дітей віком від чотирьох до 14 років, які охоплені туберкулінодіагностикою, відсотків | 90 | 72,5 |
| Організація роботи кабінетів контрольованого лікування у лікувально-профілактичних закладах та надання ДОТ-послуг на рівні первинної медико-санітарної допомоги хворим на туберкульоз першої — четвертої категорії | Кількість хворих на туберкульоз першої — четвертої категорії, які пройшли контрольоване лікування на амбулаторному етапі, відсотків | 70 | 59 |
| Забезпечення доступу хворих на ко-інфекцію (туберкульоз/ВІЛ-інфекція/СНІД) до лікування опортуністичних інфекцій | Кількість хворих, що проходять профілактичне лікування котримоксазолом відповідно до потреби, відсотків | 75 | 46,5 |
| Забезпечення доступу хворих на ко-інфекцію (туберкульоз/ВІЛ-інфекція/СНІД) до антиретровірусної терапії | Кількість хворих на ко-інфекцію (туберкульоз/ВІЛ-інфекція/СНІД), які проходять антиретровірусну терапію, відсотків | 70 | 45,2 |
| Проведення навчальних семінарів для лікарів первинної ланки, психологів та соціальних працівників з питань профілактики, діагностики та лікування туберкульозу | Кількість лікарів первинної ланки, які пройшли навчання з питань профілактики, діагностики та лікування туберкульозу | 2830 | 390 |
Слід відзначити, що у рамках виконання даної загальнодержавної програми здійснювалась централізована закупівля медикаментів для лікування туберкульозу та подальший їх розподіл до регіональних закладів охорони здоров’я. Водночас внаслідок відсутності дієвого моніторингу з боку Міністерства охорони здоров’я України щодо забезпечення регіональних закладів охорони здоров’я протитуберкульозними препаратами та належного контролю за їх розподілом в окремих регіональних закладах охорони здоров’я утворилися залишки препаратів, що забезпечать їх потребу від 3 до 6 років, і враховуючи термін їх придатності, не можуть бути використаними, тоді як в інших регіонах такі препарати відсутні.
Наприклад, прогнозований запас препарату ІЗОНІАЗИД табл. по 100 мг (з терміном використання 5 років) Полтавської області становив 686,4 тис. таблеток, що забезпечує фактичну потребу у вказаному препараті до 6,5 років, разом з тим у Харківській, Чернівецькій областях та м. Севастополі вказаний запас забезпечує їх потребу від 3 до 5 місяців. У Дніпропетровській області на 01.12.2012 року залишок препарату ГАТИФЛОКСАЦИН р-н для ін’єкцій фл. 400 мг (з терміном придатності 2 роки) становить 20,3 тис. фл., що забезпечує потребу до 3 років, водночас його залишки у Івано-Франківській, Сумській та Харківській областях забезпечують 2–4 місячну потребу. У Рівненській області на 01.12.2012 року залишок препарату ЛЕВОФЛОКСАЦИН драже, капс., табл. 500 мг (з терміном придатності 2 роки) становить 149,8 тис. табл., що забезпечує його потребу до 3 років, водночас у м. Києві та АР Крим залишок забезпечує потребу від 2 до 3 місяців.
Міністерством охорони здоров’я України також не забезпечено своєчасного розподілу медикаментів для лікування туберкульозу. Так, у 2012 році в порушення умов договору доручення від 04.05.2012 року, який передбачав надання Міністерством розподілів у десятиденний термін з дня підписання договорів, фактично розподіл протитуберкульозних препаратів I та II ряду, закуплених за рахунок коштів Державного бюджету України на 2012 рік, було затверджено лише 19.09.2012 року (наказ № 721) — через 26 днів після підписання договорів (договори укладено 23.08.2012 року).
У 2012 році в порушення умов договору доручення від 04.05.2012 року № 39/21–24, якими передбачалося здійснити поставку препаратів до закладів охорони здоров’я згідно з розподілом Міністерства охорони здоров’я України у термін, що не перевищує 30 календарних днів з моменту отримання їх на склад, ДУО «Політехмед» здійснило поставку протитуберкульозних препаратів на суму 2,8 млн. гривень до закладів через 31–54 дні після їх поставки на склад. Наприклад, на склад ДУО «Політехмед» постачальником ВАТ «Київмедпрепарат» поставлено препарат КАНАМІЦИН 05.09.2012 року (договір No71Т/211/21–24 від 23.08.2012 року). Розподіл цього препарату затверджено Міністерством 19.09.2012 року (наказ № 721) — через 14 днів після здійсненої поставки. Проте, на базу спеціального медичного постачання Головного управління охорони здоров’я КМДА препарат (51580 од.) на суму 158,9 тис. гривень було поставлено 16.10.2012 року — через 41 день після поставки його на склад ДУО «Політехмед».
Таким чином, внаслідок невчасного здійснення Міністерством охорони здоров’я України розподілу медикаментів для лікування туберкульозу, відсутності у регіонах графіків поставок відповідні медичні заклади не були забезпечені в достатній кількості цими препаратами, що спричинило переривання курсу лікування хворих на туберкульоз.
Неефективні управлінські рішення Міністерства охорони здоров’я України призвели до несвоєчасного проведення процедур закупівель протитуберкульозних препаратів і виробів медичного призначення для діагностики туберкульозу, що одночасно з необґрунтованим продовженням термінів постачання вказаних товарів стало причиною недостатнього забезпечення ними регіональних органів охорони здоров’я: у 2012 році — на рівні 60–75 відсотків.
Загалом, у 2012 році Міністерство охорони здоров’я України не забезпечило ефективного використання коштів державного бюджету, виділених на виконання заходів з профілактики та лікування захворювань на туберкульоз. Через відсутність належної співпраці Міністерства охорони здоров’я України як державного замовника державних цільових програм щодо подолання епідемії туберкульозу з Державною службою України з питань протидії ВІЛ-інфекції/СНІДу та інших соціально небезпечних захворювань, органами місцевого самоврядування і громадськими організаціями, які виконують відповідні заходи коштом місцевих бюджетів та Глобального фонду по боротьбі зі СНІДом, туберкульозом та малярією в Україні, не забезпечено дієвої координації їх виконання.
Високий рівень захворюваності на туберкульоз і поширення його мультирезистентних форм обумовлено, насамперед, недостатньою ефективністю заходів, спрямованих на переривання ланцюга передачі туберкульозної інфекції, і несвоєчасним виявленням хворих на заразні форми, недотриманням схем лікування та кадровими проблемами.
Вказані недоліки в організації роботи Міністерства охорони здоров’я України підтверджуються висновками Рахункової палати, які містяться в Звіті про результати аудиту використання коштів державного бюджету, виділених Міністерству охорони здоров’я України, та гуманітарної допомоги громадських організацій на виконання заходів з профілактики та лікування захворювань на туберкульоз (Звіт затверджено постановою Колегії Рахункової палати від 23.01.2013 року № 1–5).
З цього приводу слід відзначити, що 25.03.2013 року Солом’янським районним управлінням ГУМВС України в місті Києві відомості щодо можливих неправомірних дій службових осіб Міністерства охорони здоров’я України, що призвели до неефективного використання коштів державного бюджету, виділених на виконання заходів з профілактики та лікування захворювань на туберкульоз, внесено до Єдиного реєстру досудових розслідувань та розпочато досудове розслідування в кримінальному провадженні № 12013110090003954 з попередньою правовою кваліфікацією кримінального правопорушення за частиною 1 статті 364 (Зловживання владою або службовим становищем) Кримінального кодексу України.
На зростання рівня захворюваності на туберкульоз у 2012 році вплинуло також скорочення мережі протитуберкульозних закладів. Так, у минулому році реорганізовано 4 протитуберкульозні диспансери у Запорізькій, Миколаївський та Одеській областях, а кількість закладів, що мають фтизіатричні кабінети, зменшилась на 11. Окрім того, було скорочено ліжковий фонд протитуберкульозних диспансерів на 335 ліжок, на 200 ліжок скорочено ліжковий фонд у туберкульозних лікарнях. Показово, що скорочення ліжкового фонду відбулось, у тому числі, в Херсонській області (скорочено 50 ліжок), яка є абсолютним лідером серед усіх регіонів за рівнем захворюваності на туберкульоз.
Загалом, неналежний стан виконання Загальнодержавної цільової соціальної програми протидії захворюванню на туберкульоз у минулому році негативним чином відзначився на показниках захворюваності на туберкульоз. Так, офіційні дані Державної служби статистики України свідчать про зростання показників захворюваності на туберкульоз — у минулому році на активний туберкульоз захворіло 30958 осіб (у 2011 році — 30659), показник захворюваності становив 68,1 на 100 тис. населення, що на 1,3% більше у порівнянні з 2011 роком.
Захворюваність населення України на активний туберкульоз у 2011–2012 роках
| Адміністративно-територіальна одиниця | Всього | ±% до 2011 року | |||
|---|---|---|---|---|---|
| Абсолютні числа | На 100 тис. населення | ||||
| 2011 | 2012 | 2011 | 2012 | ||
| Автономна Республіка Крим | 1491 | 1497 | 76,3 | 76,6 | +0,4% |
| Область | |||||
| Вінницька | 895 | 899 | 54,8 | 55,3 | +0.9% |
| Волинська | 537 | 534 | 51,9 | 51.6 | -0.6% |
| Дніпропетровська | 3179 | 3082 | 95,4 | 92,9 | -2,6% |
| Донецька | 3231 | 3148 | 73,1 | 71,7 | -1.9% |
| Житомирська | 920 | 880 | 71,9 | 69.1 | -3.9% |
| Закарпатська | 711 | 726 | 57,1 | 58,2 | +1,9% |
| Запорізька | 1185 | 1243 | 65,8 | 69,4 | +5.5% |
| Івано-Франківська | 905 | 959 | 65,7 | 69,6 | +5,9% |
| Київська | 964 | 1168 | 56,3 | 68,2 | +21,1% |
| Кіровоградська | 795 | 775 | 79,2 | 77,8 | -1,8% |
| Луганська | 1828 | 1795 | 79,9 | 79,1 | -1,0% |
| Львівська | 1630 | 1680 | 64,5 | 66,6 | +3,3% |
| Миколаївська | 1056 | 1028 | 89,3 | 87,3 | -2.2% |
| Одеська | 2087 | 2235 | 87,8 | 94,0 | +7,1% |
| Полтавська | 817 | 889 | 55,2 | 60,5 | +9,6% |
| Рівненська | 720 | 710 | 62,5 | 61,6 | -1,4% |
| Сумська | 663 | 651 | 57,2 | 56,6 | -1,0% |
| Тернопільська | 585 | 561 | 54,1 | 52,1 | -3,7% |
| Харківська | 1492 | 1359 | 54,5 | 49,8 | -8,6% |
| Херсонська | 1070 | 1167 | 98,5 | 107,9 | +9,5% |
| Хмельницька | 694 | 680 | 52,4 | 51,6 | -1,5% |
| Черкаська | 733 | 800 | 57,2 | 62,8 | +9,8% |
| Чернівецька | 440 | 438 | 48,8 | 48,5 | -0,6% |
| Чернігівська | 722 | 675 | 66,3 | 62,5 | -5,7% |
| Місто | |||||
| Київ | 1073 | 1143 | 38,9 | 41,2 | +5.9% |
| Севастополь | 236 | 236 | 62,3 | 62,2 | -0.2% |
| Україна | 30659 | 30958 | 67,2 | 68,1 | +1,3% |
Одним з важливих проблемних питань у контролі за туберкульозом в Україні є постійне зростання захворюваності від поєднаної інфекції туберкульоз/ВІЛ. Так, у 2012 році в порівнянні з 2011 роком має місце підвищення рівня захворюваності на активний туберкульоз у поєднанні з хворобою, зумовленою ВІЛ-інфекцією, на 14%. Показник захворюваності складає 10,4 на 100 тис. населення. Найбільший рівень захворюваності на поєднану патологію має місце у Дніпропетровській (23,5 на 100 тис. населення), Одеській (23,4 на 100 тис. населення), Донецькій (21,0 на 100 тис. населення) та Миколаївській (20,4 на 100 тис. населення) областях. Найбільше зростання рівня захворюваності на туберкульоз/ВІЛ відзначається у Львівській (+40,7%), Харківській (+40,7%), Сумській (+36,4%) та Івано-Франківській (+35,3%) областях.
Смертність від туберкульозу за підсумками минулого року залишається на рівні 2011 року та становить 15,2 на 100 тис. населення. Найвищий рівень смертності зареєстровано у Дніпропетровській (21,6 на 100 тис. населення), Кіровоградській (20,9 на 100 тис. населення), Луганській (20,6 на 100 тис. населення), Херсонській (20,2 на 100 тис. населення) та Донецькій (20,0 на 100 тис. населення) областях.
Стан виконання Загальнодержавної програми забезпечення профілактики ВІЛ-інфекції, лікування, догляду та підтримки ВІЛ-інфікованих і хворих на СНІД на 2009 -2013 роки
Світовий досвід свідчить, що поширення ВІЛ-інфекції/СНІДу призводить до зменшення тривалості життя, зростання потреби в медичних послугах, загострення проблем бідності, соціальної нерівності та сирітства, подолання яких потребує постійного збільшення видатків з державного бюджету.
За даними офіційної статистичної інформації, загальна кількість зареєстрованих випадків ВІЛ-інфекції серед громадян України станом на 01.01.2013 року становила 223530 осіб (з них 36830 дітей до 14 років), зокрема 56382 осіб із захворюванням на СНІД, у тому числі 1224 дітей до 14 років.
За січень–червень 2013 року в Україні офіційно зареєстровано 10727 випадків ВІЛ-інфекції, у тому числі 5162 випадків захворювання на СНІД. За перше півріччя цього року від СНІДу померло 1 803 особи.
Кількість ВІЛ-інфікованих осіб, які перебувають під медичним наглядом у закладах охорони здоров’я, становить понад 129 тис. осіб, показник поширеності ВІЛ-інфекції — 283,6 особи на 100 тис. населення, у більш як 24 тис. ВІЛ-інфікованих осіб хвороба досягла кінцевої стадії — СНІДу. Показник поширеності СНІДу становить 52,9 особи на 100 тис. населення. За оціночними даними, на початку 2012 року в державі проживало 230 тис. осіб віком від 15 років і старші, які живуть з ВІЛ, що становить 0,58 відсотка всього населення в зазначеній віковій категорії.
Залишається високим показник темпів приросту нових випадків ВІЛ-інфекції (в 2011 році — 3,6%), а також частка випадків захворювання на ВІЛ-інфекцію у віковій групі від 15 до 24 років (4,7%).
Як і раніше, існує значна різниця у рівнях захворюваності на ВІЛ-інфекцію по регіонах України. Найвищі рівні захворюваності в показниках на 100 тисяч населення у 2012 році зареєстровано в Дніпропетровській (103,4), Одеській (96,2), Миколаївській (96,0), Донецькій (85,3) областях. При цьому середній показник захворюваності на ВІЛ-інфекцію в Україні становить 45,5 випадків на 100 тисяч населення. Тенденцію збільшення кількості нових зареєстрованих випадків ВІЛ-інфекції в минулому році відмічено в 14 з 27 регіонів країни.
Кількість зареєстрованих випадків ВІЛ-інфекції щороку збільшується, при цьому рівень доступу до послуг з лікування, особливо серед представників груп підвищеного ризику щодо інфікування ВІЛ, є низьким.
Загальнодержавною програмою забезпечення профілактики ВІЛ-інфекції, лікування, догляду та підтримки ВІЛ-інфікованих і хворих на СНІД на 2009 — 2013 роки передбачалось здійснення профілактичних, лікувальних та організаційних заходів, а також заходів з догляду та підтримки ВІЛ-інфікованих і хворих на СНІД.
Разом з тим, очікувані показники по окремим запланованим заходам, відповідальним за виконання яких є Міністерство охорони здоров’я України, у минулому році не були досягнуті.
| Найменування заходу | Найменування показника | Запланований показник на 2012 рік | Фактичний показник |
|---|---|---|---|
| Здійснення заходів з виявлення та профілактичного лікування інфекцій, що передаються статевим шляхом, серед представників груп ризику | Представники груп ризику, обстежені та охоплені профілактичним лікуванням (відсотків) | 60 | 34,3 |
| Забезпечення доступу ВІЛ-інфікованих дітей і дорослих до безперервної антиретровірусної терапії шляхом централізованої закупівлі препаратів для антиретровірусної терапії | Кількість дітей, охоплених лікуванням (відсотків) | 100 | 96,4 |
| Розширення сфери застосування методу замісної підтримувальної терапії з метою зменшення ризику ВІЛ-інфікування та формування позитивного ставлення до антиретровірусної терапії серед споживачів ін’єкційних наркотиків | Кількість осіб | 15300 | 7339 |
| Створення системи лабораторного моніторингу резистентності ВІЛ до антиретровірусних препаратів | Кількість досліджень | 550 | 80 |
Також слід відзначити, що станом на 01.01.2013 року 4246 осіб, які потребують антиретровірусної терапії, не отримують її. При цьому вказаний показник не відображає реальної потреби в зазначеній терапії, оскільки враховує тільки тих пацієнтів, які перебувають під активним диспансерним спостереженням та зареєстровані в Системі моніторингу лікування.
Вкрай низьким є рівень забезпечення лабораторного супроводження антиретровірусної терапії та моніторингу перебігу ВІЛ-інфекції у хворих на ВІЛ-інфекцію/СНІД. Так, протягом 2012 року ВІЛ-інфікованим та хворим на СНІД пацієнтам, які знаходяться на диспансерному обліку, здійснено наступні дослідження:
- гематологічні — 1773849, що становить 45,5% від активної диспансерної групи;
- біохімічні — 1218774, що становить 25,02% від активної диспансерної групи;
- визначення рівня СД4 лімфоцитів — 145009, що становить 37,2% від активної диспансерної групи;
- визначення вірусного навантаження — 95655, що становить 32,7% від активної диспансерної групи.
Загалом, можна констатувати, що розвиток епідемії ВІЛ-інфекції/СНІДу зумовлений такими факторами, як:
- виявлення ВІЛ-інфекції на пізній стадії захворювання;
- недостатній рівень охоплення диспансеризацією;
- низький рівень доступу населення, представників груп підвищеного ризику щодо інфікування ВІЛ і людей, що живуть з ВІЛ, до послуг з профілактики, медичної та соціальної допомоги, в тому числі паліативної і хоспісної;
- недостатньо розвинута інфраструктура для надання медичної і соціальної допомоги, особливо на місцевому рівні;
- поступове збільшення кількості дітей, народжених ВІЛ-інфікованими матерями, та збільшення кількості ВІЛ-інфікованих жінок дітородного віку;
- недостатній рівень державного фінансування заходів протидії ВІЛ-інфекції/СНІДу.
Стан виконання Загальнодержавної програми боротьби з онкологічними захворюваннями на період до 2016 року
Злоякісні новоутворення є однією з найнебезпечніших медико-біологічних і соціально-економічних проблем. Рівень захворюваності та смертність від цієї хвороби постійно підвищується.
Україна відрізняється високим рівнем онкозахворюваності і входить до першої десятки країн світу за цим показником, маючи більше 160 тисяч захворілих на рік. За прогнозами до 2020 року кількість онкохворих в Україні може зрости до 200 тисяч осіб щорічно.
Вже четвертий рік в Україні виконується Загальнодержавна програма боротьби з онкологічними захворюваннями на період до 2016 року, метою якої є підвищення ефективності здійснення загальнодержавних заходів з профілактики злоякісних новоутворень, підвищення якості профілактики онкологічних захворювань, доступності медичної допомоги для онкологічно хворих, підвищення показника одужання, зниження рівня смертності онкологічно хворих, які помирають протягом року після встановлення діагнозу, і смертності від злоякісних новоутворень деяких локалізацій (рак молочної залози, шийки матки, передміхурової залози).
Водночас доводиться констатувати, що стан онкологічної допомоги населенню у 2012 році є вкрай незадовільним. Підтвердженням цьому є суттєве зростання показників захворюваності та смертності від новоутворень.
Так, у минулому році зареєстровано близько 433 тисяч випадків виявлення новоутворень, що на 2,3% більше порівняно з 2011 роком.
Кількість уперше зареєстрованих випадків захворювань на новоутворення за регіонами у 2011–2012 роках
| Адміністративно-територіальна одиниця | Кількість уперше зареєстрованих випадків захворювань | На 100 тисяч населення | ||
|---|---|---|---|---|
| 2011 | 2012 | 2011 | 2012 | |
| Автономна Республіка Крим | 15765 | 16029 | 807 | 820 |
| Область | ||||
| Вінницька | 16454 | 15366 | 1009 | 946 |
| Волинська | 7714 | 8067 | 745 | 778 |
| Дніпропетровська | 42980 | 43184 | 1293 | 1304 |
| Донецька | 37494 | 37633 | 851 | 860 |
| Житомирська | 10215 | 10409 | 800 | 818 |
| Закарпатська | 8054 | 7865 | 646 | 629 |
| Запорізька | 16863 | 17374 | 939 | 972 |
| Івано-Франківська | 10300 | 11127 | 748 | 807 |
| Київська | 11725 | 12464 | 685 | 727 |
| Кіровоградська | 9054 | 9886 | 906 | 996 |
| Луганська | 17953 | 18658 | 788 | 826 |
| Львівська | 19821 | 23999 | 785 | 951 |
| Миколаївська | 11395 | 11525 | 966 | 981 |
| Одеська | 19591 | 20664 | 824 | 868 |
| Полтавська | 11881 | 12473 | 806 | 852 |
| Рівненська | 8715 | 8516 | 756 | 738 |
| Сумська | 11662 | 12286 | 1010 | 1072 |
| Тернопільська | 6673 | 6510 | 618 | 605 |
| Харківська | 36818 | 37917 | 1347 | 1390 |
| Херсонська | 12579 | 13674 | 1160 | 1267 |
| Хмельницька | 9710 | 9231 | 735 | 703 |
| Черкаська | 13034 | 13101 | 1020 | 1032 |
| Чернівецька | 5129 | 5531 | 569 | 612 |
| Чернігівська | 9246 | 9179 | 852 | 854 |
| Місто | ||||
| Київ | 37417 | 35924 | 1353 | 1288 |
| Севастополь | 4333 | 4372 | 1143 | 1149 |
| Україна | 422575 | 432964 | 928 | 953 |
При цьому слід наголосити на зростанні захворюваності та поширеності новоутворень як серед дорослого населення, так і серед дітей.
Динаміка захворюваності та поширеності новоутворень серед дорослого населення України у 2008–2012 роках (на 100 тис. дорослого населення)
| Показник | Рік | ||||
|---|---|---|---|---|---|
| 2008 | 2009 | 2010 | 2011 | 2012 | |
| Захворюваність | 1003,5 | 1007,8 | 1036,6 | 1051,0 | 1078,2 |
| Поширеність | 4528,8 | 4620,8 | 4761,7 | 4859,1 | 4976,2 |
Динаміка захворюваності та поширеності новоутворень серед дітей віком до 17 років у 2008–2012 роках (на 100 тис. відповідного населення)
| Показник | Рік | ||||
| 2008 | 2009 | 2010 | 2011 | 2012 | |
| Захворюваність | 807 | 823 | 856 | 873 | 908 |
| Поширеність | 315 | 323 | 335 | 343 | 362 |
Особливого занепокоєння викликає рівень онкологічної смертності, який лише за минулий рік зріс майже на 4,5% та становить 14% у загальній структурі смертності (203,2 на 100 тисяч осіб). Загалом, в 2012 році в Україні від онкологічних захворювань померло близько 93 тисяч осіб.
Смертність від новоутворень за регіонами у 2011–2012 роках
| Адміністративно-територіальна одиниця | Кількість уперше зареєстрованих випадків захворювань | На 100 тисяч населення | ||
|---|---|---|---|---|
| 2011 | 2012 | 2011 | 2012 | |
| Автономна Республіка Крим | 3434 | 3785 | 174,9 | 192,7 |
| Область | ||||
| Вінницька | 3032 | 3126 | 185,1 | 191,7 |
| Волинська | 1422 | 1437 | 137,0 | 138,3 |
| Дніпропетровська | 7090 | 7820 | 213,0 | 236,0 |
| Донецька | 10116 | 10295 | 229,0 | 234,5 |
| Житомирська | 2361 | 2374 | 185,0 | 186,8 |
| Закарпатська | 1861 | 1975 | 149,0 | 157,7 |
| Запорізька | 4374 | 4628 | 243,5 | 258,8 |
| Івано-Франківська | 2184 | 2269 | 158,3 | 164,3 |
| Київська | 3541 | 3726 | 206,0 | 216,5 |
| Кіровоградська | 2140 | 2329 | 212,7 | 233,2 |
| Луганська | 4654 | 4636 | 203,9 | 204,7 |
| Львівська | 4008 | 4397 | 157,6 | 173,1 |
| Миколаївська | 2207 | 2205 | 186,9 | 187,5 |
| Одеська | 4624 | 4745 | 193,6 | 198,4 |
| Полтавська | 3244 | 3354 | 218,8 | 227,8 |
| Рівненська | 1786 | 1781 | 154,8 | 154,1 |
| Сумська | 2450 | 2608 | 211,8 | 227,2 |
| Тернопільська | 1848 | 1971 | 170,8 | 182,7 |
| Харківська | 5833 | 6172 | 212,2 | 225,0 |
| Херсонська | 2093 | 2181 | 192,8 | 201,8 |
| Хмельницька | 2541 | 2580 | 192,0 | 192,9 |
| Черкаська | 2430 | 2450 | 189,6 | 192,4 |
| Чернівецька | 1595 | 1667 | 176,3 | 184,0 |
| Чернігівська | 2101 | 2218 | 192,0 | 204,8 |
| Місто | ||||
| Київ | 4930 | 5171 | 175,6 | 182,7 |
| Севастополь | 1058 | 1036 | 277,7 | 271,0 |
| Україна | 8857 | 92896 | 194,6 | 203,2 |
Вкрай низькими є показники стану діагностики та лікування хворих на злоякісні новоутворення. Так, за інформацією Національного канцер-реєстру, в 2012 році на профілактичних оглядах було виявлено 30,6% онкологічних хворих (від 18,7% — в Кіровоградській області до 64,8% — в м. Київ). Дані цифри красномовно свідчать про формальне ставлення до цієї проблеми.
Окремим питанням завжди була дитяча онкологія. Питання ранньої діагностики цього контингенту хворих найбільш актуальне. У дитячого населення коефіцієнт смертність-захворюваність досягає в Україні 30,7%, а максимальні показники серед хлопчиків у Закарпатській області 90,9%, Кіровоградській — 83,3%, а серед дівчаток — в Миколаївській — 62,5%. І це при тому, що у дитячого населення на профілактичних оглядах виявлено лише 12,6% хворих.
Недостатньо ефективним було виявлення на профілактичних оглядах пухлин візуальних локалізацій (злоякісні новоутворення губи, шкіри, шийки матки, молочної залози, прямої кишки), які в ряді областей активно виявлялися лише у 5,1–30,6% хворих (у Херсонській, Закарпатській, Івано-Франківській областях), що свідчить про низьку ефективність роботи мамологічних кабінетів, кабінетів патології шийки матки, оглядових жіночих та чоловічих кабінетів. Відсутність онкологічної настороженості у стоматологів призвела до того, що рівень виявлення на профоглядах злоякісних новоутворень ротової порожнини у Закарпатській області склав 5,6%, Херсонській — 5,2%.
Низькою була ефективність виявлення під час профілактичних оглядів випадків захворювання на злоякісні новоутворення трахеї, бронхів та легень.
Інтенсивне зростання захворюваності на злоякісні новоутворення передміхурової та щитовидної залози потребує особливої уваги до діагностики цих захворювань, рівень активного виявлення яких складало в Чернівецькій — 3,4%, Хмельницькій — 6,3%, Львівській — 5,4%, Кіровоградській — 7,3%. Низькою є ефективність виявлення на профілактичних оглядах випадків захворювання на злоякісні новоутворення трахеї, бронхів та легенів в Україні — 22,4%, а у Закарпатській, Херсонській областях і в м. Севастополь цей показник не досягав 10%, що, перш за все, зумовлено недоліками в роботі флюорографічної служби.
Розподіл усіх виявлених в 2012 році нових випадків злоякісних новоутворень за стадіями (згідно класифікації TNM діючого в областях перегляду) показав, що 52,5% з них були виявлені на 1–2-й стадії розвитку пухлини, 17,5% — на 3-й стадії і 14,5% — на 4-й стадії. У 5,7% випадків стадію за TNM не було визначено у зв‘язку з порушенням правил стадіювання за системою TNM. Найбільшу кількість таких випадків зареєстровано у Полтавській (12,7%) і Сумській (10,3%) областях та у м. Київ (11,5%). Найбільше число хворих із занедбаною стадією хвороби — 20,9–24,5% — було зареєстровано у Полтавській та Херсонській областях.
Вказані статистичні дані доводять, що в Україні значною проблемою є низький рівень діагностики на ранніх стадіях, при цьому високий показник хворих із занедбаною стадією хвороби, що призводить до високої смертності.
В 2012 році спеціальне лікування отримали 68,7% первинних хворих, від 60,2% — в Дніпропетровській області, до 78,3% — в Одеській. Найменший показник охоплення спеціальним лікуванням було зареєстровано серед хворих на злоякісні новоутворення підшлункової залози (27,3%), легені (42,5%), шлунка (46,1%), стравоходу (50,7%). Таким чином, за даними Національного канцер-реєстру в Україні від 37% до 60% усіх хворих при різних локалізаціях злоякісних новоутворень не отримали спеціального лікування, що безумовно впливає на рівень смертності та летальності.
Загрозливо високою залишається питома вага хворих, які не прожили 1 року з моменту встановлення діагнозу захворювання на злоякісні новоутворення. Так, по Україні серед осіб, що захворіли на рак у 2011 році, не прожили року 32,5% хворих — від 28,4% в Автономній Республіці Крим до 37,7% в Чернівецькій та Закарпатській областях. При візуальних локалізаціях пухлини показник хворих, що не прожили 1-го року, усе ще залишався високим: від 8,2% при злоякісних новоутвореннях губи до 31,1% при злоякісних новоутвореннях прямої кишки. Найбільший відсоток хворих, що не прожили року, було зареєстровано серед захворілих на злоякісні новоутворення підшлункової залози — 77,0% та стравоходу — 68,6%. Посмертно було встановлено захворювання у 2288 осіб, що складало 1,4% усіх захворілих на рак в 2011 році, при цьому найбільший відсоток хворих із посмертно встановленим діагнозом було зареєстровано у Запорізькій (3,8%), Кіровоградській і Миколаївській (3,1%) областях та у м. Севастополь (3,7%).
Варто звернути увагу на незабезпеченості матеріально-технічної бази онкологічної служби. Наприклад, в минулому році в загальній лікувальній мережі зареєстровано 1979 оглядових кабінетів, що на 169 менше порівняно з 2011 роком.
Через неналежну організацію роботи з боку Міністерства охорони здоров’я України, Міністерством охорони здоров’я АР Крим, структурними підрозділами з питань охорони здоров’я обласних (міських) державних адміністрацій (крім м. Києва та Сумської області) не виконується наказ Міністерства охорони здоров’я України від 30.12.1992 року № 208, яким рекомендувалося довести забезпеченість ліжками онкологічних закладів до 3,5 на 10 тис. населення або 123,5 на 1000 вперше захворівши. Згідно із бюлетенем Національного канцер-реєстру забезпеченість такими ліжками в середньому становила 2,8 та 77,7 ліжок. Як і раніше, неприпустимо низький рівень забезпеченості ліжками залишається в Житомирській (2,0), Київській (1,7), Рівненській (2,0) областях, що постраждали від аварії на ЧАЕС, та Харківській області (1,9 на 10 тисяч населення). Окрім того, станом на 31.12.2012 року не укомплектовано посади лікарів-онкологів у 95 центральних районних лікарнях, в основному Херсонської, Кіровоградської, Миколаївської та Полтавської областей.
Фактично, при щорічному збільшенні кількості онкологічних хворих, кількість онкологічних ліжок залишається практично незмінною та спостерігається їх дефіцит, що затримує своєчасну госпіталізацію хворих до онкологічного закладу і зволікає з початком лікування, як наслідок, частина онкохворих вимушена проходити лікування в закладах загально-лікарняної мережі, де не завжди дотримуються стандартів і протоколів лікування онкологічних хворих.
Доводиться також констатувати, що Міністерство охорони здоров’я України не забезпечило своєчасного розподілу закуплених препаратів, що зумовило порушення графіків їх постачання до регіонів.
Так, за умовами договору доручення № 39/21–24 від 04.05.2012 року Міністерство охорони здоров’я України має надавати до ДУО «Політехмед» розподіли лікарських засобів у десятиденний термін з дня підписання договорів. Однак, не дотримуючись вказаних умов договорів, 7 наказів про розподіл лікарських засобів (від 26.07.2012 року № 563, від 26.07.2012 року № 564, від 05.10.2012 року № 781, від 31.10.2012 року № 862, від 20.11.2012 року № 937 та від 17.12.2012 року № 1063 і № 1064) у 2012 році затверджені від дванадцяти днів до майже двох місяців після підписання договорів. Наприклад, договір № 79Т/249/21–24 на поставку препарату НЕУЛАСТИМ з постачальником ТОВ «Фармадіс» укладений 07.09.2012 року. На склад ДУО «Політехмед» препарат поставлено 19.09.2012 року. Проте, розподіл вказаного препарату затверджено Міністерством охорони здоров’я України 05.10.2012 (наказ № 781) або майже через місяць після укладання договору та через 16 днів після їх поставки на склад ДУО «Політехмед». Також за умовами договорів доручень, укладених Міністерством охорони здоров’я України із ДУО «Політехмед», у 2012–2013 роках постачання до закладів охорони здоров’я централізовано закуплених препаратів має здійснюватися ДУО «Політехмед» у термін, що не перевищує 30 календарних днів з моменту отримання товару на його склад. Фактично, у 2012 та січні-лютому 2013 року ДУО «Політехмед» здійснило поставку лікарських засобів на суму 4621,8 тис. гривень до регіональних закладів охорони здоров’я через 33–227 днів після їх поставки на склад.
При цьому не доведення Міністерством охорони здоров’я України і ДУО «Політехмед» графіків поставок до закладів охорони здоров’я лікарських засобів за договорами 2012 року, відсутність залишків хіміотерапевтичних препаратів і препаратів супроводу в установах та закупівля і поставка у різні терміни препаратів, що використовуються при лікуванні одночасно, стало наслідком закупівлі лікарських засобів хворими за власні кошти.
Наприклад, згідно інформації Територіального управління Рахункової палати по Вінницькій, Житомирській, Кіровоградській та Хмельницькій областях від 17.06.2013 року № 30–15/375, при перевірці медичних карток за 2012 рік 16 онкологічних хворих, яким медична допомога надавалась у Вінницькому обласному клінічному диспансері, встановлено, що 87,3% витрат на лікарські засоби, які використані на їх лікування, проведено за рахунок власних коштів хворих.
З приводу вищезгаданого слід відзначити, що у 2013 році, за дорученням Генеральної прокуратура України, прокуратурою Вінницької області було проведено перевірку, за результатами якої установлено, що усупереч вимогам Закону України «Про охорону дитинства» 229 онкохворих мешканців області не забезпечено в повному обсязі ліками за рахунок централізованих закупівель, проведених Міністерством охорони здоров’я України на виконання Загальнодержавної програми боротьби з онкологічними захворюваннями на період до 2016 року. Перевіркою встановлено, що через неналежне формування Міністерством охорони здоров’я України номенклатури лікарських засобів та заявок на них, несвоєчасне придбання та їх постачання, потреби регіону в цих препаратах задоволено у 2012 році на 81%, а станом на червень 2013 року — на 16%. Окремі засоби, визначені протоколами лікування, не закуповувались взагалі. За результатами перевірки прокуратурою Вінницької області через Генеральну прокуратуру України внесено подання Міністру охорони здоров’я України.
Окрім того, непоодинокими є випадки, коли лікарські засоби для лікування онкологічних та онкогематологічних хворих, закуплені у централізованому порядку за кошти Державного бюджету України, надходили в аптечну мережу та придбавались пацієнтами власним коштом. Наприклад, 29.04.2013 року слідчим відділом Шевченківського районного управління ГУМВС України в місті Києві за фактом реалізації в аптечній мережі лікарських засобів, придбаних у централізованому порядку за кошти Державного бюджету України, внесено відомості до Єдиного реєстру досудових розслідувань за № 12013110100007638 та розпочато досудове розслідування.
Як передбачено наказами Міністерства охорони здоров’я України від 03.04.2012 року № 235 та від 22.03.2013 року № 232, ДУО «Політехмед» залучено до виконання у 2012 та 2013 роках державних цільових програм і комплексних заходів з охорони здоров’я, та за результатами проведених конкурсних процедур державних закупівель повинно забезпечити:
- супровід укладення договорів про закупівлю, контроль за виконанням постачальниками своїх договірних зобов’язань та участь у претензійній та позовній роботі у разі недотримання постачальниками умов договорів.
- постачання, зберігання, монтаж, пусконалагодження або організацію постачання лікарських засобів, виробів медичного призначення та інших товарів.
Разом з тим, робота ДУО «Політехмед» у даному напрямку є неефективною та не забезпечує повноцінного виконання поставлених завдань. Наприклад, ПАТ «Фармстандарт-Біолік» на виконання договорів від 07.09.2012 року № 80Т/248/21–24 та 06.09.2012 року № 82Т/240/21–24, якими передбачено здійснити поставку товару на склад уповноваженого підприємства до 30.11.2012 препарати ВІНБЛАСТИН-ЛЕНС у кількості 11118 фл. (по 5 мг) на суму 322,8 тис. гривень та ДАКАРБАЗИН-ЛЕНС у кількості 13646 фл. (по 200 мг) на суму 996,2 тис. гривень, поставлено до ДУО «Політехмед» лише 28.03.2013 року або майже на 4 місяці пізніше встановленого терміну. Станом на 01.07.2013 року ДУО «Політехмед» нараховано штрафні санкції у сумі 249,7 тис. гривень, які ПАТ «Фармстандарт-Біолік» не сплачено. Проте, не дотримуючись пункту 1.1.4 договору доручення від 04.05.2012 № 39/21–24, ДУО «Політехмед» не направлено до суду позови про стягнення з ПАТ «Фармстандарт-Біолік» штрафних санкцій.
Також згідно інструкцій про застосування 64 лікарських засобів, що закуплені Міністерством охорони здоров’я України у 2012–2013 роках, їх зберігання та транспортування здійснюється при температурі від +2 до +8°С. Разом з тим, у вказаному періоді ДУО «Політехмед» не здійснювало контроль за дотриманням температурних умов при надходженні препаратів для лікування онкологічних захворювань від постачальників та поставці їх до закладів охорони здоров’я. Зокрема, у ДУО «Політехмед» відсутнє документальне підтвердження за яких температурних умов у 2012–2013 роках здійснювалася доставка до постачальників та закладів охорони здоров’я наступних препаратів для лікування онкологічних захворювань: ІНТРОН 30 млн. МО (закупленого за договором від 10.07.2012 № 31Т/113/21–24); РИТУКСИМ 100 мг (дог. від 08.11.2012 № 99/316/21–24; від 05.12.2012 № 105/354/21–24); РИТУКСИМ 500 мг (дог. від 05.12.2012 № 105/354/21–24 та від 10.07.2012 №36Т/108/21–24); ТЕВА ГРАСТИМ 30 млн. МО (дог. від 05.12.2012 № 104/353/21–24); ТРАСТУМАМ 150 мг (дог. від 17.07.2012 № 51/126/21–24); АТГАМ 250мг (дог. від 10.07.2012 № 27Т/82/21–24); ГРАНОЦИТ 33,6 млн. МО (дог. від 10.07.2012 № 31Т/113/21–24); АСПАРАГІНАЗА 10000 МО (дог. від 07.09.2012 №98/320/21–24); ЛЕЙКОФОЗИН 30 мг (дог. від 06.07.2012 № 23Т/83/21–24); ДОКСОЛІК 10 мг (дог. від 24.06.2012 № 18Т/85/21–24); ДОКСОЛІК 50 мг (дог. від 24.06.2012 № 18Т/85/21–24); ЕЛІГАРД 22,5 мг (дог. від 06.07.2012 № 26Т/82/21- 24). Загальна вартість зазначених препаратів складає 42770,99 тис. гривень.
Таким чином, за відсутності належного контролю з боку Міністерства охорони здоров’я України за виконанням умов договорів-доручень укладених з ДУО «Політехмед» (на приймання централізовано закуплених лікарських засобів і організацію їх поставки до закладів охорони здоров’я) не забезпечено доказовості дотримання належних температурних умов на всіх ланках постачання та зберігання централізовано закуплених препаратів для лікування онкологічних захворювань, що має забезпечувати їх якість.
Загалом, можна констатувати, що неналежне виконання Загальнодержавної програми боротьби з онкологічними захворюваннями на період до 2016 року у минулому році унеможливило проведення ефективної роботи щодо попередження та зниження онкологічної захворюваності в Україні, впровадження методів профілактики та ранньої діагностики і надання медичної допомоги онкологічним хворим в необхідному обсязі.
Стан виконання Загальнодержавної програми імунопрофілактики та захисту населення від інфекційних хвороб на 2009 — 2015 роки
Інфекційні хвороби залишаються небезпечними для людства, займають провідне місце в структурі захворюваності населення, призводять до зниження якості життя, тимчасової втрати працездатності, інвалідності та смертності населення.
У структурі поширеності хвороб у дітей інфекційні хвороби в Україні посідають 7 місце, а серед вперше зареєстрованих у житті хвороб — 3 місце після захворювань органів дихання та хвороб шкіри. Інфекційні та паразитарні захворювання посідають одне з провідних місць у структурі смертності дітей в Україні. Щорічно від інфекцій помирає 300 — 350 дітей.
Щороку на інфекційні хвороби хворіють від 600 тис. до 1 млн. наших громадян (без урахування грипу та ГРВІ). Захворюваність на інфекційні хвороби перевищує відповідні показники у провідних країнах Європи в десятки, а за окремими нозологіями — і в сотні разів. До того ж, в Україні обов’язковій реєстрації підлягають лише 53 нозології із понад 2 000 відомих інфекцій.
Загалом, доводиться констатувати, що епідемічна ситуація щодо найпоширеніших інфекцій залишається напруженою. На такі інфекційні хвороби, як дифтерія, вірусні гепатити, кір, краснуха, епідемічний паротит, кашлюк та гемофільна інфекція, припадає близько 90 відсотків усіх зареєстрованих випадків. Окремі з них (краснуха та вірусний гепатит B) є причиною більшості уроджених аномалій та вад розвитку, що вкрай негативно позначається на здоров’ї населення та його генофонді.
Подібну ситуацію зумовлюють проблеми, пов’язані з організацією імунопрофілактики та захисту населення від інфекційних хвороб, здійсненням медичного контролю за проведенням щеплень, дотриманням правил імунізації та моніторингом післявакцинальних реакцій та ускладнень, що негативно впливають на стан імунопрофілактики населення.
Сьогодні дуже непокоїть зростання захворюваності на деякі керовані інфекції, яке відбувається одночасно зі зниженням обсягів профілактичних щеплень. Досвід вакцинопрофілактики вірусних інфекцій свідчить, що стійке зниження захворюваності можливе лише у разі охоплення щепленнями понад 95% населення. Саме такий показник і закладається як найважливіший серед заходів з імунізації населення, в інакшому випадку — заходи є недостатніми.
Водночас, аналіз результатів виконання у минулому році заходів з імунізації населення, відповідальним за виконання яких є Міністерство охорони здоров’я України, свідчить про те, що частина з них не виконана у запланованому обсязі.
| Найменування заходу | Найменування показника | Запланований показник на 2012 рік | Фактичний показник |
|---|---|---|---|
| Забезпечення своєчасного охоплення щепленнями дітей за станом здоров’я згідно з Календарем щеплень | Охоплення профілактичними щепленнями дітей до 1 року проти дифтерії, правця, кашлюку, не менше (відсотків) | 95 | 75,5 |
| Охоплення профілактичними щепленнями дітей до 1 року проти гемофільної інфекції типу b, не менше (відсотків) | 95 | 82,7 | |
| Охоплення профілактичними щепленнями дітей до 1 року проти поліомієліту не менше (відсотків) | 95 | 73,7 | |
| Охоплення профілактичними щепленнями дітей до 1 року проти кору, краснухи, не менше (відсотків) | 95 | 78,8 | |
| Охоплення профілактичними щепленнями дітей до 1 року проти гепатиту B, не менше (відсотків) | 95 | 46,1 | |
| Продовження впровадження стратегії Всесвітньої організації охорони здоров’я щодо елімінації кору, зниження захворюваності на епідемічний паротит, краснуху та запобігання синдрому вродженої краснухи | Доведення показників розповсюдженості епідемічного паротиту, кашлюку, кору до рівня менш як 1 на 100 тис. | менш як 1 на 100 тис. | Епідемічний паротит (1,75 на 100 тис.) Кашлюк (5,01 на 100 тис.) Кір(27,95 на 100 тис.) |
Слід відзначити, що через неповне забезпечення потреби регіонів вакцинами для профілактики кору, краснухи та епідемічного паротиту у 2012 році значно зменшились обсяги вакцинації та ревакцинації. Це призвело до епідемічного підйому кору — захворюваність на кір порівняно з 2011 роком зросла майже в 10 разів, інтенсивний показник становив 27,95 на 100 тис. Хворіли переважно діти та молодь, епідемічний процес супроводжувався спалахами в дитячих навчально-виховних закладах серед дітей та підлітків, а також серед студентів вищих начальних закладів.
Відмічалась нестабільна епідемічна ситуація щодо краснухи. Так, в окремих регіонах (Вінницькій, Волинській, Чернігівській областях та м. Києві) спостерігався підйом захворюваності у 2–3 рази, особливо серед молоді віком 15–17 років.
Аналогічна ситуація спостерігалась щодо захворюваності на епідемічний паротит. Високі показники та ріст захворюваності зафіксовані у 8 регіонах серед вікової групи 1–4 роки, показники коливались у межах від 11,54 на 100 тис. населення (м. Київ) до 27,16 на 100 тис. населення (Кіровоградська область) та в 10 регіонах серед дітей 5–9 років: від 12,74 на 100 тис. населення (Івано-Франківська область) до 47,54 на 100 тис. населення (Миколаївська область).
У минулому році не було припинено місцеву передачу вірусу кору та краснухи. Віруси кору та краснухи продовжують циркуляцію на території України. Захворюваність на кір реєструвалась в усіх регіонах: всього 12746 випадків. Випадки краснухи реєструвались в усіх регіонах, за винятком м. Севастополь: всього 1952 випадки.
В 2012 році зареєстровано 139 випадків бактеріальних менінгітів, що на 53 випадки більше порівняно з 2011 роком.
Загалом, у минулому році відсоток охоплення населення України профілактичними щепленнями складав:
- вакцинація БЦЖ першого року життя — 95,4%;
- вакцинація БЦЖ 7 років — 63,8%;
- вакцинація поліомієліту до року — 73,7%;
- ревакцинація поліо- 18 міс. — 72,0%;
- ревакцинація поліо старше 2-х років — 63,2%;
- ревакцинація поліо — 6 років — 82,4%
- ревакцинація поліо — 14 років — 85,6%;
- вакцинація АКДП до року — 75,6%;
- ревакцинація АКДП 18 міс. — 69,1%;
- ревакцинація АКДП старше 2 років — 55,4%;
- ревакцинація АДП 6 років — 74,4%;
- ревакцинація АДП старше 6 років — 50,7%;
- ревакцинація АДП-м 14 років — 86,6%;
- ревакцинація АДП-м старше 14 років — 63,3%;
- ревакцинація АДП-м 18 років — 52,7%;
- ревакцинація АДП-м дорослі — 30,1%
- вакцинація гепатиту В-1 до року — 82,6%;
- вакцинація гепатиту В-3 до року — 46,1%;
- вакцинація КПК в 1 рік — 78,8%;
- ревакцинація КПК в 6 років — 83,7%;
- вакцинація КПК 2 роки і старше — 61,6%;
- ревакцинація КПК 7 років і старше — 56,6%;
- вакцинація Хіб-2 до року — 82,7%;
- ревакцинація Хіб 18 міс. — 26,7%.
Слід відзначити, що Законом України «Про Державний бюджет України на 2012 рік» в межах бюджетної програми за КПКВК 2301400 «Забезпечення медичних заходів окремих державних програм та комплексних заходів програмного характеру» на виконання Загальнодержавної програми імунопрофілактики та захисту населення від інфекційних хвороб на 2009 — 2015 роки було передбачено видатки у сумі 302110,9 тис. гривень на централізовану закупівлю імунобіологічних препаратів для проведення імунопрофілактики населення. Водночас внаслідок відсутності дієвого моніторингу з боку Міністерства охорони здоров’я України щодо забезпечення регіональних закладів охорони здоров’я різними вакцинами та належного контролю за їх розподілом, в окремих регіонах утворилися залишки препаратів, тоді як в інших регіонах такі препарати відсутні в необхідній кількості.
Наприклад, вакциною для профілактики туберкульозу Тернопільська область забезпечена на 133,9%, Кіровоградська — 108,7%. Водночас Запорізька область забезпечена даною вакциною на 52,5%, Херсонська — 65,7%.
Комбінованою вакциною проти кору, паротиту та краснухи для вакцинації дітей Чернігівська область забезпечена на 120%, Кіровоградська — 112,7%, Львівська — 110,4%. Разом з тим, Івано-Франківська область забезпечена даною вакциною на 83,6%, Рівненська — 85,6%.
Чернігівська область забезпечена вакциною проти поліомієліту на 153%, Миколаївська — 104,8%. Рівень забезпечення даною вакциною в Кіровоградській області становить 68,6%.
Миколаївська область забезпечена вакциною проти дифтерії, правця, кашлюку на 180%, Запорізька — 120,9%. Водночас потреби Кіровоградської області у даній вакцині задоволені на рівні 72,6%, Херсонської — 62,1%.
Чернігівська область забезпечена вакциною проти дифтерії та правця для щеплення дітей у віці 14 і 18 років та дорослих на 121,7%, натомість забезпеченість даної вакцини в Кіровоградській області становить 79,6%.
До такої ситуації призвело те, що придбання та розподіл імунобіологічних препаратів в розрізі адміністративно-територіальних одиниць здійснено Міністерством охорони здоров’я України пропорційно до кількості населення у віці від 0 до 17 років, без врахування даних про народжуваність та кількості осіб у певній віковій групі.
Міністерством охорони здоров’я України також не забезпечено своєчасного розподілу імунобіологічних препаратів. Так, умовами договору-доручення від 04.05.2012 року № 30/21–24, укладеного Міністерством охорони здоров’я України з ДП «Укрвакцина», визначено, що державне підприємство зобов’язується забезпечити доставку товару до закладів охорони здоров’я згідно розподілу у строк, що не перевищує 30 календарних днів з моменту отримання товару на склад, при наявності затвердженого розподілу. Однак, накази про розподіл імунобіологічних препаратів у 2012 році загалом на суму 35959,2 тис. гривень надані Міністерством охорони здоров’я України через 7–28 днів після їх поставки на склад ДП «Укрвакцина», чим створено умови затримки їх постачання до закладів охорони здоров’я. Наприклад, імунобіологічні препарати, які закуплено у 2012 році за продовженими договорами від 09.06.2011 року № 47/21–24 та № 48/21–24 поставлено на склад ДП «Укрвакцина» 18.04.2012 року на суму 6304,0 тис. гривень та на суму 51,1 тис. гривень відповідно. Водночас розподіли вказаних імунобіологічних препаратів затверджено наказом Міністерства охорони здоров’я України від 16.05.2012 року № 362 або через 28 днів після їх поставки на склад уповноваженого державного підприємства. До закладів охорони здоров’я вказані препарати поставлено лише у період 33 до 51 дня після поставки на склад ДП «Укрвакцина».
Внаслідок невчасного здійснення Міністерством охорони здоров’я України розподілу імунобіологічних препаратів, відсутності у регіонах графіків поставок, відповідні заклади охорони здоров’я не були забезпечені в достатній кількості відповідними вакцинами, що спричинило зниження рівня охоплення профілактичними щепленнями.
Таким чином, у 2012 році Міністерство охорони здоров’я України не забезпечило ефективного використання коштів державного бюджету, виділених на виконання заходів з імунопрофілактики та захисту населення від інфекційних хвороб. Наприклад, в минулому році з державного бюджету було виділено 924,6 тис. гривень на централізовану закупівлю виробів для забезпечення умов температурного контролю імунобіологічних препаратів. Разом з тим, обладнання для дотримання оптимальних умов «холодового ланцюга» під час зберігання, транспортування, використання імунобіологічних препаратів централізовано не закупалось, оскільки відповідні торги не відбулись.
З цього приводу слід відзначити, що 25.03.2013 року Солом’янським районним управлінням ГУМВС України в місті Києві відомості щодо можливих неправомірних дій службових осіб Міністерства охорони здоров’я України, що призвели до неефективного використання коштів державного бюджету, виділених на виконання заходів з імунопрофілактики та захисту населення від інфекційних хвороб, внесено до Єдиного реєстру досудових розслідувань та розпочато досудове розслідування в кримінальному провадженні № 12013110090003954 з попередньою правовою кваліфікацією кримінального правопорушення за частиною 1 статті 364 (Зловживання владою або службовим становищем) Кримінального кодексу України.
Вищезгадані проблеми в організації роботи Міністерства охорони здоров’я України та підпорядкованих йому структур підтверджуються висновками Рахункової палати, які містяться в Звіті про результати аудиту ефективності використання коштів державного бюджету на виконання заходів Загальнодержавної програми імунопрофілактики та захисту населення від інфекційних хвороб (Звіт затверджено постановою Колегії Рахункової палати від 24.10.2012 року № 20–1).
Більше того, Генеральною прокуратурою України за участі спеціалістів Державної фінансової інспекції України, Антимонопольного комітету України та Міністерства економічного розвитку і торгівлі України проведено перевірку додержання Міністерством охорони здоров’я України вимог чинного законодавства під час закупівлі та застосування у 2012 році вакцин, за результатами якої виявлені грубі порушення Законів України «Про здійснення державних закупівель», «Про захист населення від інфекційних хвороб».
Перевіркою встановлено, що у порушення вимог законодавства (статті 27 Закону України «Про захист населення від інфекційних хвороб») дітям не забезпечено проведення у повному обсязі обов’язкових профілактичних щеплень. Найнижчий рівень охоплення щепленнями дітей у Вінницькій, Волинський, Житомирській, Закарпатській, Івано-Франківській та Київській областях. Водночас, згідно з інформацією ДП «Укрвакцина», станом на 01.01.2013 року в залишку знаходиться імунобіологічних препаратів майже на 60 млн. гривень. Зокрема, не використаними залишилось 734,9 тис. доз вакцини для профілактики поліомієліту 1, 2, 3 типів на суму 1,5 млн. гривень, 140,5 тис. доз вакцини ІНФАНРИКС для профілактики дифтерії, правця, кашлюку на суму 16,8 млн. гривень, 181,3 тис. доз вакцини ТРИВОМАКС для профілактики кору, епідемічного паротиту та краснухи на суму 6,9 млн. гривень.
Необхідно також враховувати, що неналежний стан вакцинації дітей негативно впливає на додержання їх прав на дошкільну та загальну освіту, оскільки згідно з вимогами статті 15 Закону України «Про захист населення від інфекційних хвороб» дітям, які не отримали профілактичних щеплень згідно Календарем щеплень, відвідування дитячих закладів забороняється.
Загалом, виявлені порушення стали можливими через ігнорування вимог законодавства службовими особами Міністерства охорони здоров’я України, відсутність контролю за діяльністю підлеглих з боку керівників міністерства та неналежної взаємодії структурних підрозділів.
Стан виконання Загальнодержавної програми «Національний план дій щодо реалізації Конвенції ООН про права дитини» на період до 2016 року
Метою даної Програми є забезпечення оптимального функціонування цілісної системи захисту прав дітей в Україні відповідно до вимог Конвенції ООН про права дитини та з урахуванням цілей розвитку, проголошених Декларацією тисячоліття ООН, і стратегії Підсумкового документа Спеціальної сесії в інтересах дітей Генеральної Асамблеї ООН «Світ, сприятливий для дітей». Зокрема, передбачається створення умов для народження здорової дитини, збереження здоров’я кожної дитини протягом усього періоду дитинства, забезпечення доступу до високоякісних медичних послуг.
Водночас у минулому році в діяльності Міністерства охорони здоров’я України, регіональних органів охорони здоров’я виявлені суттєві порушення законодавства щодо охорони життя і здоров’я дітей.
По-перше, не вживається дієвих заходів, спрямованих на збереження здоров’я дітей та попередження їх інвалідності, у т.ч. шляхом своєчасного забезпечення кваліфікованою медичною допомогою та безоплатними ліками.
Так, за рахунок централізованих закупівель, проведених Міністерством охорони здоров’я України упродовж 2012 року, забезпечено необхідними лікарськими засобами: 20% дітей з дитячим церебральним паралічем, з хворобою Гоше; 25% дітей, хворих на первинні вроджені імунодефіцити; 40% дітей, хворих на муковісцидоз, хронічну ниркову недостатність; 50% дітей, хворих на гемофілію; 75% дітей з гіпофізарним нанізмом; 90% дітей віком до 3 років з фенілкетонорією.
Зокрема, в Донецьку область поставлено препаратів для лікування онкологічних захворювань на 39% від потреби, в Автономну Республіку Крим — на 70%, церебрального паралічу — відповідно на 14,5% та 30%. Волинську область забезпечено ліками для онкохворих на 40%, новонароджених з дихальними розладами — на 25%.
Всього в Автономній Республіці Крим, Дніпропетровській, Кіровоградській, Луганській, Миколаївській, Одеській, Рівненській, Тернопільській, Харківській, Хмельницькій областях та місті Севастополі виявлено майже 10 тис. дітей пільгових категорій, яких не забезпечено медикаментами в повному обсязі.
У порушення вимог статті 7 Бюджетного кодексу України при формуванні бюджетних запитів та заявок на закупівлю лікарських засобів органами охорони здоров’я не забезпечено ґрунтовного вивчення реальних потреб з урахуванням кількості хворих, переліку препаратів, їх вартості тощо. Зокрема, в Хмельницькій області до заявки на 2012 рік включено лікарські засоби для онкохворих дітей, частина яких — на суму 180 тис. гривень — взагалі не використана, більшість інших — застосована для дорослих. При цьому діти необхідними ліками не забезпечені.
Окрім того, Міністерство охорони здоров’я України не забезпечило масового скринінгу новонароджених на адреногенітальний синдром та муковісцидоз, оскільки у минулому році відповідні обстеження проведені лише у 75% новонароджених.
По-друге, не додержуються права дітей на отримання медикаментів за пільговими рецептами, що суперечить вимогам статті 54 Закону України «Основи законодавства України про охорону здоров’я». Так, у Миколаївській області закладами охорони здоров’я третини районів не видано жодного безоплатного рецепта для дітей-інвалідів та малюків у віці до трьох років. Такі ж факти виявлено в Автономній Республіці Крим, Житомирській, Харківській, Херсонській областях, місті Києві. У лікувальних установах Автономної Республіки Крим, Волинської, Донецької, Житомирської, Запорізької, Київської, Миколаївської, Сумської, Харківської, Херсонської, Чернівецької, Чернігівської областей стягується плата за надання медичної допомоги, у т.ч. під виглядом благодійних внесків.
По-третє, вжиті Міністерством охорони здоров’я України та органами охорони здоров’я заходи щодо попередження смертності новонароджених і дітей першого року життя є недостатніми. Торік у віці до 1 року померло 4,4 тисячі малюків. Найвищі показники смертності у Дніпропетровській, Донецькій, Кіровоградській, Черкаській областях. Основними причинами такого становища є неякісна медична допомога, неналежна матеріально-технічна база лікувальних установ, відсутність кваліфікованих фахівців, регулярного патронажу новонароджених за місцем їх проживання.
По-четверте, не вирішено проблему санаторно-курортного лікування дітей-інвалідів. Унаслідок неналежної організації цієї роботи Міністерством охорони здоров’я України та органами охорони здоров’я на місцях торік його отримали 6,1 тис. дітей-інвалідів (або 3%). Наприклад, Макарівською центральною районною лікарнею Київської області у 2012 році із 316 безоплатних путівок дітям-інвалідам виділено 8. При цьому жодної письмової відмови їх законних представників від санаторного лікування немає. Негативно впливає на реалізацію прав дітей-інвалідів відсутність у санаторіях необхідної кількості ліжок «матері і дитини» для розміщення супроводжуючих осіб. Так, на обліку в Деснянському районі міста Києва перебуває 21 хвора на дитячий церебральний параліч дитина, яка не може себе обслуговувати. Проте, 15 таких дітей не отримували путівок жодного разу, оскільки кошти для супроводжуючих осіб не виділялися. Через відсутність путівок за профілем захворювання не оздоровлено 46 дітей з цукровим діабетом.
Вкрай неналежною є робота лікарсько-консультативних комісій лікувальних закладів. Зокрема, усупереч вимогам статей 7, 23 Закону України «Про реабілітацію інвалідів в Україні» цими комісіями не всім дітям-інвалідам складено індивідуальні програми реабілітації — єдиний документ, на підставі якого вони отримують необхідні соціальні гарантії та пільги (забезпечення засобами пересування, реабілітації, освітою тощо). Більшість розроблених програм є формальними, своєчасно не переглядаються, їх виконання не контролюється. Більш того, непоодинокими є випадки внесення медичними працівниками неправдивих відомостей до даних документів — відміток про отримання дітьми протезних виробів, санаторно-курортного лікування, якими вони фактично не забезпечувалися.
Варто звернути увагу на незабезпеченості матеріально-технічної бази закладів охорони здоров’я, які надають медичні послуги дітям. Так, відсутність необхідних приміщень, обладнання та профільних спеціалістів встановлено в закладах охорони здоров’я Житомирської, Закарпатської, Львівській, Миколаївської, Рівненської, Тернопільської, Херсонської, Черкаської, Чернігівської областей та міста Києва. Одночасно має місце неефективне використання наявного медичного обладнання. Наприклад, у Черкаській реабілітаційно-оздоровчій поліклініці «Астра» для лікування дітей з дитячим церебральним паралічем застосовуються пристрої, які втратили своє функціональне призначення у зв’язку з повним зношенням. Водночас на складі Волинського обласного дитячого територіального медичного об’єднання більше року зберігається без використання 35 комплектів пристроїв «Гравітон» на суму 260 тис. гривень, закуплених Міністерством охорони здоров’я України за кошти Державного бюджету України.
Одночасно мають місце розтрати бюджетних коштів. Наприклад, на даний час щодо службових осіб Міністерства охорони здоров’я України, які не забезпечили кваліфікованого лікування дітей за кордоном, незаконно перерахували кошти бюджету в сумі понад 2 млн. гривень установі, яка має ознаки фіктивності, розпочато досудове розслідування в кримінальному провадженні з попередньою правовою кваліфікацією кримінального правопорушення за частиною 2 статті 367 (Службова недбалість) Кримінального кодексу України.
Загалом, такий стан склався внаслідок неналежної організації виконання Міністерством охорони здоров’я України вимог чинного законодавства щодо охорони життя і здоров’я дітей, невжиття дієвих заходів, спрямованих на вирішення проблемних питань у сфері реалізації прав дітей на охорону здоров’я та реабілітацію.
Стан виконання Державної цільової соціальної програми «Трансплантація» на період до 2012 року
З метою підвищенні якості надання спеціалізованої медичної допомоги хворим, що потребують проведення операцій з трансплантації органів та інших анатомічних матеріалів, продовження строку життя людини без втрати працездатності і зниження рівня смертності шляхом широкого впровадження новітніх медичних технологій починаючи з 2008 року в Україні реалізовувалась Державна цільова соціальна програма «Трансплантація» на період до 2012 року, якою передбачено поетапно реформувати трансплантологію, розширити можливості з надання спеціалізованої медичної допомоги особам з незворотніми захворюваннями та удосконалити процес їх реабілітації.
Разом з тим, аналіз результатів виконання у минулому році комплексних заходів щодо надання послуг належної якості у сфері трансплантації, відповідальним за виконання яких є Міністерство охорони здоров’я України, свідчить про те, що частина з них не виконана у запланованому обсязі.
Зокрема, лікувально-профілактичні заклади не були забезпечені у необхідній кількості лікарськими засобами для проведення імуносупресії.
Окрім того, матеріально-технічна база основних медичних центрів, що здійснюють трансплантацію органів, тканин і клітин, залишається на вкрай низькому рівні.
Одночасно доводиться констатувати, що Міністерство охорони здоров’я України не забезпечило належного внутрішнього контролю за закладами охорони здоров’я, що призводило до порушення встановленого законом порядку трансплантації органів або тканин людини та чинного законодавства про поховання. Підтвердженням цьому є низка кримінальних справ та проваджень, що перебували у провадженні правоохоронних органів упродовж 2011–2012 років.
Так, у провадженні УСБУ в Чернігівській області перебуває кримінальне провадження, відомості про яке внесено до Єдиного реєстру досудових розслідувань, за частиною 5 статті 143 Кримінального кодексу України за фактом порушення встановленого законом порядку трансплантації тканин людини працівниками першого міського відділення комунального закладу «Чернігівське обласне патологоанатомічне бюро». Крім того, у провадженні УСБУ в Миколаївській області у 2012 році перебувала кримінальна справа стосовно судово-медичного експерта відділу експертиз трупів Миколаївського обласного бюро СМЕ за частиною 1 статті 143 Кримінального кодексу України за фактом порушення встановленого законом порядку трансплантації тканин людини. У провадженні слідчого управління УМВС України в Івано-Франківській області перебувала кримінальна справа, порушена за частиною 5 статті 143 Кримінального кодексу України щодо працівників Івано-Франківського обласного бюро СМЕ, які всупереч чинному законодавству проводили вилучення анатомічних утворень, тканин та їх компонентів. Відомості про кримінальне правопорушення у вищезгаданій справі внесено до Єдиного реєстру досудових розслідувань. За результатами розслідування обвинувальний акт щодо п’яти осіб направлено до суду для розгляду по суті.
Також Слідчим управлінням ГУМВС України в Київській області протягом 2011 року розслідувано та направлено до суду для розгляду по суті три кримінальні справи стосовно трьох працівників Києво-Святошинського відділення Київського обласного бюро СМЕ, Києво-Святошинської ЦРЛ та Броварського відділення Київського обласного бюро СМЕ, які всупереч чинному законодавству проводили вилучення очних яблук у померлих.
Стан виконання Державної програми «Репродуктивне здоров’я нації» на період до 2015 року
Результати аналізу змін населення за останні 10 — 15 років свідчать про те, що Україна перебуває у стані глибокої демографічної кризи, зумовленої депопуляцією, збільшенням питомої ваги осіб похилого віку і зменшенням середньої тривалості життя.
Особливе занепокоєння викликає стан репродуктивного здоров’я, яке є невід’ємною складовою частиною здоров’я нації в цілому і має стратегічне значення для забезпечення сталого розвитку суспільства.
Рівні материнської та дитячої смертності залишаються високими і значно перевищують середньоєвропейські показники.
Такий стан справ зумовлює необхідність подальшого здійснення комплексу заходів, спрямованих на поліпшення репродуктивного здоров’я населення.
З метою створення умов для безпечного материнства, формування репродуктивного здоров’я у дітей та молоді, удосконалення системи планування сім’ї, збереження репродуктивного здоров’я населення починаючи з 2006 року в Україні реалізується Державна програма «Репродуктивне здоров’я нації» на період до 2015 року.
Водночас аналіз результатів виконання у минулому році завдань, спрямованих на поліпшення репродуктивного здоров’я населення як важливої складової загального здоров’я, відповідальним за виконання яких є Міністерство охорони здоров’я України, свідчить про те, що частина з них не виконана у запланованому обсязі.
| Найменування завдання | Найменування показника | Запланований показник на 2012 рік | Фактичний показник |
|---|---|---|---|
| Знизити рівень анемії серед вагітних | На 100 вагітних | 23,5 | 24,7 |
| Знизити рівень гемолітичної хвороби новонароджених | На 1000 народжених вагою 1000 грамів та більш | 7,1 | 7,2 |
| Збільшити кількість дітей, які перебувають на грудному вигодовуванні до шести місяців | Відсотків | 56 | 54 |
| Знизити рівень запальних захворювань статевих органів у підлітків 15 — 17 років | На 10000 дівчат 15 — 17 років | 60 | 123 |
| Знизити рівень захворюваності на рак шийки матки | На 100000 населення | 16 | 23,8 |
У подібній ситуації особливо показово, що Державна програма «Репродуктивне здоров’я нації» на період до 2015 року була профінансована з державного бюджету України у повному обсязі.
Таким чином, невжиття Міністерством охорони здоров’я України дієвих заходів, спрямованих на вирішення проблемних питань репродуктивного здоров’я населення, зумовили невиконання запланованих завдань у межах даної державної цільової програми.
Стан виконання Державної цільової програми «Цукровий діабет» на 2009–2013 роки
Діабет на сьогодні є однією з найпоширеніших хвороб в Україні, що посідає третє місце серед причин смертності після серцево-судинних та онкологічних хвороб. Загроза діабету не лише в його поширеності, а й у тому, що він призводить до розвитку багатьох тяжких ускладнень. Це одна з головних причин ураження нирок і ниркової недостатності, ризику розвитку інфаркту міокарда, інсульту. Смертність від серцево-судинних захворювань у хворих на діабет у 2–3, а за даними деяких досліджень і у 6 разів, більша, ніж у людей, які не хворіють на цю недугу.
За даними Інституту ендокринології та обміну речовин ім. В.П. Комісаренка, кількість хворих на цукровий діабет в різних країнах світу коливається від 6,6% до 8% чисельності населення. Водночас, за даними офіційної статистики станом на 01.01.2013 року в Україні зареєстровано близько 1 млн. 331 тис. хворих на цукровий діабет, що становить 2,9% всього населення країни. Подібні статистичні показники свідчать про недостатній рівень охоплення населення скринінговими обстеженнями на своєчасне виявлення ранніх стадій цукрового діабету.
Захворюваність на цукровий діабет серед населення України у 2012 році (зареєстровано вперше вжитті) становить 121352, що складає 267,0 на 100 тис. населення.
Останніми роками невпинно збільшується розповсюдженість інсулінозалежного цукрового діабету.
Смертність від цукрового діабету залишається на вкрай високому рівні, що зумовлено ускладненнями цукрового діабету діабетичною гангреною, діабетичною нефропатією, діабетичними комами внаслідок несвоєчасного діагностування. Загалом, у минулому році від цукрового діабету та його ускладнень померло 2205 осіб або 4,9 на 100 тис. населення. При цьому в окремих регіонах спостерігається підвищений рівень смертності від цукрового діабету — Закарпатській, Луганській та Львівській областях (7,1 на 100 тис. населення), Одеській області (7,9 на 100 тис. населення).
На ситуацію, що склалася, негативно впливають такі фактори:
- збільшення кількості осіб з хронічними серцево-судинними захворюваннями (гіпертонічна хвороба, атеросклероз) як групи ризику розвитку цукрового діабету;
- відсутність налагодженого механізму проведення у закладах охорони здоров’я обов’язкового профілактичного огляду населення з метою виявлення та діагностики цукрового діабету, його ускладнень і диспансеризації хворих;
- низький рівень оснащення закладів охорони здоров’я медичним обладнанням для діагностики та лікування хворих;
- відсутність ефективної системи забезпечення хворих лікарськими засобами та виробами медичного призначення, їх медико-соціальної реабілітації;
- обмеженість можливостей із забезпечення санаторно-курортним лікуванням.
З метою запобігання та зниження рівня захворюваності на цукровий діабет починаючи з 2009 року в Україні реалізується Державна цільова програма «Цукровий діабет» на 2009–2013 роки, якою передбачено створити і забезпечити належне функціонування системи профілактики захворювання на цукровий діабет. Термін виконання Державної програми добігає кінця у 2013 році.
Водночас аналіз результатів виконання у минулому році завдань, спрямованих на профілактику, діагностику та лікування хворих на цукровий діабет, відповідальним за виконання яких є Міністерство охорони здоров’я України, свідчить про те, що частина з них не виконана у запланованому обсязі.
| Найменування завдання | Найменування показника | Запланований показник на 2012 рік | Фактичний показник |
|---|---|---|---|
| Розроблення нормативно-правових та організаційно-структурних засад удосконалення надання медичної допомоги хворим на цукровий діабет та його ускладнення | Зниження рівня первинного виходу у працездатному віці на інвалідність внаслідок ускладнень, зумовлених захворюванням на цукровий діабет (кількість випадків на 10 тис. населення) | 1,1 | 1,5 |
| Створення умов для ефективного функціонування закладів охорони здоров’я з метою підвищення рівня та якості надання медичної допомоги хворим на цукровий діабет | Зменшення кількості випадків ампутацій стопи, зумовлених захворюванням на цукровий діабет (кількість випадків на 100 тис. населення) | 5,5 | 7,4 |
| Створення умов для ефективного функціонування закладів охорони здоров’я з метою підвищення рівня та якості надання медичної допомоги хворим на цукровий діабет | Збільшення питомої ваги дітей, хворих на цукровий діабет, які пройшли оздоровлення у спеціалізованих санаторіях та оздоровчих центрах (питома вага дітей, які оздоровлені, щороку, відсотків) | 40 | 10,9 |
Одним з показників незадовільного стану виконання Державної цільової програми «Цукровий діабет» на 2009–2013 роки є вкрай високий показник випадків ампутацій стопи, зумовлених захворюванням на цукровий діабет. Загалом, у минулому році зафіксовано 3370 випадків ампутацій стопи або 7,4 випадки на 100 тис. населення. При цьому в окремих регіонах вказаний показник коливався від 3,7 на 100 тис. населення (Житомирська область) до 11,0 на 100 тис. населення (Вінницька область). Перевищення середнього показника по країні зафіксовано в 12 регіонах (Автономна Республіка Крим — 8,2; Вінницька — 11,0; Волинська — 7,7; Дніпропетровська — 9,4; Донецька — 8,7; Київська — 9,1; Луганська — 9,6; Одеська — 10,0; Харківська — 9,6; Черкаська — 9,3; Чернівецька — 7,8; м. Севастополь — 7,6).
Слід відзначити, що з метою запобігання та зниження рівня захворюваності на цукровий діабет Міністерство охорони здоров’я України, а також розпорядники бюджетних коштів нижчого рівня здійснювали закупівлю препаратів для забезпечення лікування хворих на діабет. Як передбачено постановою Кабінету Міністрів України від 13.08.2012 року № 794 «Питання декларування зміни оптово-відпускних цін на лікарські засоби і вироби медичного призначення, які закуповуються за рахунок коштів державного та місцевих бюджетів», заклади і установи охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів, закуповують лікарські засоби і вироби медичного призначення за цінами, які не перевищують рівень задекларованих оптово-відпускних цін з урахуванням мита, податку на додану вартість та граничних постачальницько-збутових та торговельних (роздрібних) надбавок.
Міністерство охорони здоров’я України здійснює декларування зміни оптово-відпускних цін на лікарські засоби, які закуповуються за рахунок бюджетних коштів, відповідно до Положення про Міністерство охорони здоров’я України, затвердженого Указом Президента України від13.04.2011 року №467/2011, та за Порядком декларування зміни оптово-відпускних цін на лікарські засоби і вироби медичного призначення, що закуповуються за рахунок коштів державного та місцевих бюджетів, затвердженим постановою Кабінету Міністрів України від 13.08.2012 року № 794.
Разом з тим, Міністерство охорони здоров’я України не створило умови для ефективного використання бюджетних коштів, оскільки не забезпечило проведення завчасного визначення оптово-відпускних цін на лікарські засоби для лікування хворих на діабет. Зокрема, відповідні накази про декларування змін оптово-відпускної ціни на лікарські засоби приймались протягом 2012 року, при цьому частина з цих наказів була прийнята уже після укладення розпорядниками договорів на постачання ліків.
Має місце нерозуміння службовими особами Міністерства охорони здоров’я України ключових завдань та мети затвердження Державної програми. Адже лише 10% коштів, що виділяються, витрачається на закупівлю препаратів для хворих на діабет, 10% — на профілактичні заходи, а 80% — на лікування ускладнень. І це при тому, що навіть якщо діагноз цукровий діабет вже встановлено, на початковому етапі шляхом раціональної дієтотерапії та адекватних навантажень можна не лише запобігти розвитку ускладнень діабету, а й сприяти зворотному розвитку хвороби.
Негативно впливає на лікування цукрового діабету і той факт, що один з основних вітчизняних виробників інсуліну ПрАТ «По виробництву інсулінів «Індар», для виготовлення інсуліну закупляє генно-інженерну субстанцію в компанії Tonghua Dongbao (Китай) сумнівної якості, і лише розфасовує її по флаконам та картриджам.
Адекватне лікування цукрового діабету має бути направлене на зниження ризику розвитку ускладнень. Доведено, що всебічний підхід до лікування уможливлює зниження ризику розвитку інфаркту, інсульту і смертності серед хворих на діабет більш ніж у 2 рази.
За даними Асоціації ендокринологів України, лише 7% хворих на цукровий діабет хоча б раз вимірювали рівень глікованого гемоглобіну. А зниження рівня глікованого гемоглобіну лише на 1% зменшує ризик розвитку інфаркту на 14%, серцевої недостатності — на 14%.
Тобто левова частка витрат бюджету повинна направлятись на профілактичні заходи з ранньої діагностики діабету та створення умов для зупинення розвитку щойно виявленого захворювання, що в перспективі знизить ризики розвитку ускладнень, які і спричинюють зростання смертності українських пацієнтів.
Натомість нерозуміння важливості таких заходів призводить до постійного зростання кількості хворих на діабет, зростання рівня смертності та постійного збільшення витрат державного бюджету України на лікування ускладнень, спричинених цукровим діабетом.
Зокрема, Міністерство охорони здоров’я України досі не затвердило давно розроблені та подані Положення про кабінети діабетичної стопи, кабінети навчання хворих методам самоконтролю, Програми підготовки середнього медичного персоналу, який працюватиме в таких кабінетах. Профілактичні кабінети діабетичної стопи в багатьох регіонах працюють вже понад 10 років, проте Міністерство охорони здоров’я України досі нормативно не визначилось щодо введення штатних одиниць лікаря і медсестри кабінетів, офіційного виділення для них приміщень на усіх рівнях та мінімального їх оснащення. Таким чином, існування кабінетів можливе виключно за рахунок ентузіастів серед лікарів, медсестер та керівників амбулаторно-поліклінічних закладів, перші з яких працюють безоплатно «на громадських началах», другі — виділяють приміщення на власний розсуд і ризик.
Досі не створений Національний реєстр хворих на цукровий діабет, розробкою якого опікується Інститут ендокринології та обміну речовин ім. В.П. Комісаренка. Для його ефективного функціонування необхідне фінансування та координація дій між Міністерством охорони здоров’я України та Національною Академією медичних наук України, чого наразі немає.
Загалом, виявлені порушення стали можливими через ігнорування вимог законодавства службовими особами Міністерства охорони здоров’я України, відсутність контролю за діяльністю підлеглих з боку керівників міністерства та неналежної взаємодії структурних підрозділів.
III. ОБІГ ЛІКАРСЬКИХ ЗАСОБІВ ТА ВИРОБІВ МЕДИЧНОГО ПРИЗНАЧЕННЯ
Як передбачено статтею 3 Закону України «Про лікарські засоби», державна політика у сфері створення, виробництва, контролю якості та реалізації лікарських засобів спрямовується, зокрема, на розвиток виробництва високоефективних та безпечних лікарських засобів, забезпечення потреб населення ліками належної якості та в необхідному асортименті.
Разом з тим, в Україні наявні системні проблеми із забезпеченням потреб населення, державних і комунальних закладів охорони здоров’я лікарськими засобами належної якості та в необхідному асортименті, а також відсутністю ефективного механізму протидії виробництву і обігу фальсифікованих та неякісних лікарських засобів, ввезенню таких засобів в Україну.
Протягом останніх декількох років суттєво збільшився обсяг неякісних та фальсифікованих лікарських засобів, застосування яких становить реальну загрозу життю та здоров’ю людини. Так, лише за офіційними даними у 2011 році на внутрішньому ринку України було вилучено з обігу та утилізовано більше 3,5 млн. упаковок неякісних, фальсифікованих та незареєстрованих лікарських засобів на загальну суму більше 35 млн. гривень, що на 1 млн. упаковок більше, ніж у 2010 році. При цьому у 2009 році було виявлено та утилізовано лише 230 тис. упаковок.
Яскравим прикладом існуючої проблеми обігу фальсифікованих лікарських засобів на вітчизняному фармацевтичному ринку є результати позапланової перевірки, проведеної Службою безпеки України. Так, 14 травня 2013 року в м. Васильків (Київська область) було виявлено підпільне виробництво ліків під виглядом продукції відомої європейської фармацевтичної корпорації Біологіше Хайльміттель Хеель ГмбХ (Німеччина). Встановлено, що понад 60 найменувань лікарських препаратів ввозилися в Україну вантажним транспортом і у подальшому без будь-яких дозвільних документів фасувалися та реалізовувалися під виглядом продукції компанії Хеель через аптечні мережі. Було виявлено нерозфасовані та незареєстровані лікарські засоби з маркуванням німецькою мовою, упаковки українською мовою без зазначення номерів серій та термінів придатності, інструкції, та запаковані лікарські засоби з маркуванням українською мовою, а також 300 тисяч упаковок прострочених медичних препаратів, на яких було підроблено дати випуску та терміни придатності. Загалом, на складах було виявлено майже 3,9 мільйонів упаковок лікарських засобів на загальну суму майже 30 мільйонів євро.
Загалом, за оцінками експертів 5% медичних препаратів на фармацевтичному ринку України є фальсифікованими та неякісними.
На вказаній проблемі наголошено в рішенні Ради національної безпеки і оборони України від 25 травня 2012 року «Про забезпечення населення якісними та доступними лікарськими засобами», введеного в дію Указом Президента України від 30 серпня 2012 року № 526.
На підтвердження масштабності проблеми обігу фальсифікованих лікарських засобів варто відзначити, що лише протягом минулого року Державна служба України з лікарських засобів (далі — Держлікслужба України) надала 507 розпоряджень про заборону реалізації (торгівлі), зберігання та застосування лікарських засобів:
- 120 розпоряджень про заборону обігу 137 серій 99 найменувань та 58 розпоряджень про заборону всіх серій 58 найменувань неякісних лікарських засобів;
- 262 розпорядження про заборону обігу 322 найменувань незареєстрованих лікарських засобів;
- 67 розпоряджень про заборону обігу 67 серій 41 найменувань фальсифікованих лікарських засобів;
- 99 розпоряджень про тимчасову заборону реалізації (торгівлі) та застосування лікарських засобів на підставі надходження повідомлень щодо можливих побічних реакцій внаслідок застосування серії або серій лікарських засобів.
- За перше півріччя 2013 року Держлікслужба України надала 307 розпоряджень про заборону реалізації (торгівлі), зберігання та застосування лікарських засобів:
- 98 розпоряджень про заборону обігу 145 серій 78 найменувань неякісних лікарських засобів (у тому числі 16 розпоряджень про заборону обігу всіх серій);
- 149 розпоряджень про заборону обігу 199 найменувань незареєстрованих лікарських засобів;
- 36 розпоряджень про заборону обігу 47 серій 25 найменувань фальсифікованих лікарських засобів;
- 24 розпорядження про тимчасову заборону реалізації (торгівлі) та застосування лікарських засобів на підставі надходження повідомлень щодо можливих побічних реакцій внаслідок застосування серії або серій лікарських засобів.
Окрім того, за період 2012 року на підставі повідомлень про летальні випадки внаслідок застосування серій лікарських засобів Держлікслужба України надала 40 розпоряджень про тимчасову заборону обігу серій лікарських засобів (у тому числі 24 розпорядження про тимчасову заборону обігу вакцин). Загалом, відповідні розпорядження були надані щодо таких лікарських засобів: ПЕНТАКСИМ (Комбінована вакцина для профілактики дифтерії, правця, кашлюку (ацелюлярний компонент), поліомієліту та захворювань, спричинених Haemophilus influenzae типу b), вакцина туберкульозна (БЦЖ), вакцина для профілактики гепатиту В рекомбінантна рідка, ЦЕФТРІАКСОН, АУГМЕНТИН, вакцина для профілактики поліомієліту 1,2,3 типів, АКДП-Біолік, ПРІОРИКС, алерген туберкульозний очищений, ІНФАНРИКС, ОКСИТОЦИН, КОНТИКАЛ 10 000, БІЦИЛІН-5, ЦЕФТРІАКСОН-БХМЗ, НОВОКАЇН, ЛІДОКАЇНУ ГІДРОХЛОРИД, ІНФАНРИКС ГЕКСА, НІТРОГЛІЦЕРІН, НАТРІЮ ХЛОРИД, КСЕФОКАМ РАПІД, МІДОКАЛМ, ЦЕФОТАКСИМ, РИБОКСИН-ДАРНИЦЯ.
Досліджуючи окремі випадки обігу неякісних та фальсифікованих лікарських засобів, слід звернути особливу увагу на численних летальних випадках після застування вакцини для профілактики гепатиту В виробництва ПАТ «ФАРМСТАНДАРТ-БІОЛІК». Зокрема, лише у минулому році було надано сім розпоряджень про тимчасову заборону обігу даної вакцини у зв’язку з повідомленнями про летальні випадки при її застосуванні (від 20.12.2012 № 28823–1.3/2.1/17–12, від 23.11.2012 № 26010–1.3/2.1/17–12, від 23.11.2012 № 26008–1.3/2.1/17–12, від 14.09.2012 № 19446–1.3/2.1/17–12, від 20.08.2012 № 17610–1.2/2.1/17–12, від 09.08.2012 № 16859–1.3/2.1/17–12, від 10.04.2012 № 7294–1.3/2.1/17–12). Станом на 1 липня 2013 року зафіксовано ще один летальний випадок після застосування вакцини для профілактики гепатиту В, в результаті чого Держлікслужба України надала розпорядження про тимчасову заборону обігу серії даної вакцини (розпорядження від 24.07.2013 № 16262–1.1/2.0/17–13).
Необхідно також звернути увагу на випадки смерті пацієнтів після застування препарату ПЕНТАКСИМ (комбінована вакцина для профілактики дифтерії, правця, кашлюку, поліомієліту) виробництва ТОВ «Фармекс груп». Так, лише в минулому році Держлікслужбою України було надано п’ять розпоряджень про тимчасову заборону обігу серій даного лікарського засобу (від 25.12.2012 № 29261–1.3/2.1/17–12, від 06.12.2012 № 27357–1.2/2.0/17–12, від 19.04.2012 № 7988–1.1/2.0/17–12, від 06.04.2012 № 7023–1.3/2.1/17–12, від 05.01.2012 № 235–1.3/2.1/17–12). Водночас, незважаючи на вжиття зазначених заходів, летальні випадки внаслідок застосування імунобіологічного препарату ПЕНТАКСИМ були виявлені також і в 2013 році.
Як вже зазначалось, летальні випадки серед пацієнтів були зафіксовані після застосування імунобіологічного препарату ІНФАНРИКС (вакцина для профілактики дифтерії, правця, кашлюку ацелюлялрна очищена інактивована рідка) виробництва ТОВ «Фарма Лайф». У зв’язку з цим необхідно зауважити, що в минулому році Рахунковою палатою було проведено аудит ефективності використання коштів державного бюджету на виконання заходів Загальнодержавної програми імунопрофілактики та захисту населення від інфекційних хвороб. За його результатам було встановлено, що Міністерство охорони здоров’я України не забезпечило дієвого контролю за підпорядкованим йому ДП «Укрвакцина», яке, порушуючи умови договору, укладеного з ТОВ «Фарма Лайф», прийняло на склад вакцину для профілактики дифтерії, правця, кашлюку ацелярну очищену інактивовану рідку ІНФАНРИКС — вартістю 16184,6 тисяч гривень, термін придатності якої був на 3–6,5 місяці менший, ніж визначений у договорі. Таким чином, вказана обставина у подальшому могла зумовити летальний випадок після застосування імунобіологічного препарату ІНФАНРИКС.
Одним з кричущих прикладів заподіяння тяжких наслідків у зв’язку з обігом фальсифікованої медичної продукції є летальний випадок пацієнтки у ДЗ «Клінічна лікарня ДТГО «Львівська залізниця» у результаті застосування препарату МЕТОТРЕКСТАТ. При цьому, згідно даних, представлених в картці-повідомленні про вказаний смертельний випадок, серія та виробник даного лікарського засобу були невідомі. У зв’язку з цим Держлікслужба України ще у вересні 2012 року звернулась до ДП «Державний експертний центр МОЗ України» з вимогою надати інформацію про виробника та серію препарату МЕТОТРЕКСТАТ з метою тимчасової заборони його обігу. Водночас станом на кінець березня 2013 року запитувані дані до Держлікслужби України не надходили.
Необхідно також відзначити, що застосування неякісних та фальсифікованих лікарських засобів може призводити також до інших серйозних побічних реакцій, не пов’язаних з летальними наслідками. При цьому останнім часом почастішали випадки фіксації виникнення побічних реакцій від застосування лікарських засобів. Так, за 2012 рік до бази даних побічних реакцій ДП «Державний експертний центр МОЗ України» було введено 11674 випадків побічних реакцій, пов’язаних з застосуванням лікарських засобів. Серед них випадки серйозних побічних реакцій (за виключенням тих, що мали летальні наслідки) — 1242. За перше півріччя 2013 року усього до бази даних побічних реакцій було введено вже 6784 випадків побічних реакцій, пов’язаних з застосуванням лікарських засобів. Серед них випадки серйозних побічних реакцій (за виключенням тих, що мали летальні наслідки) — 581.
В аспекті вищевказаного слід відзначити, що згідно Закону України «Про лікарські засоби» у разі підтвердження факту фальсифікації лікарського засобу, інформацію та матеріали щодо відстеження шляхів надходження та розповсюдження такого лікарського засобу Держлікслужба України направляє до територіальних підрозділів Міністерства внутрішніх справ України та Служби безпеки України, на території яких знаходяться суб’єкти господарювання. Так, за 2012–2013 роки (станом на 01.06.2013 року) Держлікслужбою України до правоохоронних органів направлено 116 листів, отримано 41 відповідь з інформацією щодо розгляду отриманих листів.
Водночас доводиться констатувати, що правоохоронні органи здебільшого не вживають необхідних заходів реагування у зв’язку з надходженням повідомлень про фальсифікацію лікарського засобу, поверхнево підходять до проведення перевірок та обмежуються формальними відписками. Наведене підтверджується наступним. Так, Держлікслужбою України направлено низку листів до територіальних управлінь МВС України щодо фальсифікації лікарського засобу L-ЛІЗИНУ ЕСЦИНАТ ®, розчин для ін’єкцій, 1 мг/мл по 5 мл в ампулах № 10, з маркуванням виробника «Галичфарм». У цьому плані показовою є постанова, винесена оперуповноваженим СДСБЕЗ Фрунзенського РВ ХМУ ГУ МВС України в Харківській області від 06.04.2012 р., якою відмовлено у порушенні кримінальної справи стосовно фальсифікації L-ЛІЗИНУ ЕСЦИНАТ ® з тих підстав, що «не було встановлено місце знаходження директора» однієї з компаній, яка розповсюджувала фальсифікований лікарський засіб.
Ще однією відмовою у порушенні кримінальної справи закінчився розгляд звернення Держлікслужби України до ГУ МВС України у Донецькій області щодо реалізації фальсифікованого лікарського засобу ГЛОДУ НАСТОЙКА, настойка по 100 мл у флаконах, з маркуванням виробника Дочірнє підприємство «Агрофірма «Ян» приватного підприємства «Ян», Україна. У даному випадку підставою для відмови у порушенні кримінальної справи згідно Постанови старшого оперуповноваженого ОГ СБЕЗ Макіївського ГУ УМВС України у Донецькій області від 21.06.2012 року стало закінчення строків проведення дослідчої перевірки та неможливість отримання необхідної інформації у ці строки.
Протягом 2012–2013 років у Харківській, Донецькій, Чернівецькій, Дніпропетровській областях були виявлені численні випадки розповсюдження фальсифікованого лікарського засобу АНАФЕРОН ДИТЯЧИЙ, таблетки № 20 (20х1) у блістері в картонній коробці, з маркуванням виробника ТОВ «НВФ «Матеріал Медика Холдинг», Російська Федерація.
Проте правоохоронними органами не було порушено жодної кримінальної справи за фактом фальсифікації даного препарату. Більше того, Постановою оперуповноваженого СД СБЕЗ Ленінського РВ ДМУ ГУ МВС України в Дніпропетровській області від 26.10.2012 року було відмовлено у порушенні кримінальної справи за статтею 321–1 (Фальсифікація лікарських засобів або обіг фальсифікованих лікарських засобів) Кримінального кодексу України, хоча сам факт фальсифікації лікарського засобу АНАФЕРОН ДИТЯЧИЙ був встановлений.
Під час проведення перевірки та підтвердження факту фальсифікації розчину спиртового для зовнішнього застосування по 100 мл у флаконах МЕДАСЕПТ у кількості 97 упаковок, з маркуванням виробника ДП «Межерицький вітамінний завод ДАК «Укрмедпром», Україна, Головним управлінням МВС України у Миколаївській області також безпідставно відмовлено у порушенні кримінальної справи.
Аналогічна ситуація склалася і щодо лікарського засобу ІМПАЗА, таблетки гомеопатичні № 20, з маркуванням виробника ТОВ «НВФ «Матеріал Медика Холдинг», Російська Федерація. Начальник Шевченківського РУГУ МВС України у м. Києві також не знайшов підстав для порушення кримінальної справи за фактом розповсюдження фальсифікату вказаного лікарського засобу.
Лише після направлення депутатських звернень щодо неналежного розгляду органами внутрішніх справ повідомлень Держлікслужби України при виявлення фактів розповсюдження фальсифікованих лікарських засобів було розпочато ряд досудових розслідувань в кримінальних провадженнях. Так, 22.05.2013 року Заводським РВ Миколаївського МУ розпочато досудове розслідування за фактом реалізації фальсифікованого лікарського засобу МЕДАСЕПТ з попередньою правовою кваліфікацією за частиною 1 статті 321–1 (Фальсифікація лікарських засобів або обіг фальсифікованих лікарських засобів) Кримінального кодексу України. 24.05.2013 року Ленінським РВ Дніпропетровського МУ розпочато досудове розслідування за фактом реалізації фальсифікованого лікарського засобу АНАФЕРОН ДИТЯЧИЙ з попередньою правовою кваліфікацією за частиною 1 статті 321–1 (Фальсифікація лікарських засобів або обіг фальсифікованих лікарських засобів) Кримінального кодексу України.
Окрім того, ГУ МВС України в Донецькій області матеріали про відмову в порушенні кримінальної справи за фактом реалізації фальсифікованого лікарського засобу ГЛОДУ НАСТОЙКА надіслано до прокуратури міста Макіївки Донецької області для розгляду питання щодо скасування постанови про відмову в порушенні кримінальної справи. Також ГУ МВС України в місті Києві матеріали про відмову в порушенні кримінальної справи за фактом реалізації фальсифікованого лікарського засобу ІМПАЗА надіслано до прокуратура Шевченківського району міста Києва для розгляду питання щодо скасування постанови про відмову в порушенні кримінальної справи.
Слід також констатувати, що на даний час в Україні не створено дієвої системи контролю за утилізацією та знищенням фальсифікованих, неякісних лікарських засобів, у тому числі тих, термін придатності яких закінчився.
Так, у разі виявлення неякісних, фальсифікованих, підозрілих щодо фальсифікації та незареєстрованих лікарських засобів, Держлікслужба України відповідно до «Порядку встановлення заборони (тимчасової заборони) та поновлення обігу лікарських засобів на території України» своїми розпорядженнями забороняє обіг таких лікарських засобів. Згідно п. 2.9. Ліцензійних умов провадження господарської діяльності з виробництва лікарських засобів, оптової, роздрібної торгівлі лікарськими засобами суб’єкти господарювання зобов’язані забезпечити виконання наказів Держлікслужби України щодо зупинення виробництва, торгівлі, вилучення із торгівлі лікарських засобів і вжиття відповідних організаційних заходів щодо повернення продавцю (виробнику) зазначених лікарських засобів або їх знищення та утилізації.
Водночас, незважаючи не вищевказані вимоги, суб’єкти господарювання зазвичай ігнорують відповідні вимоги Держлікслужби України. Так, в 2012 році в різних областях України були виявлені сотні випадків, коли в роздрібній мережі реалізовувались лікарські засоби, на відповідні серії яких були надані розпорядження щодо тимчасової заборони їх обігу.
Варто відзначити, що станом на 04 жовтня 2013 року в Україні зареєстровано 13244 лікарських засобів, що охоплюють усі фармакологічні групи. З них: 3913 — лікарські засоби вітчизняного виробництва та 9331 — іноземного виробництва. Серед них: звичайних лікарських засобів — 12817 найменувань (3755 вітчизняного та 9062 іноземного виробництва), імунобіологічних препаратів — 427 найменувань (158 вітчизняного та 269 іноземного виробництва).
Разом з тим, у 2012 році у багатьох випадках реєстрація лікарських засобів проводилась з порушенням вимог чинного законодавства. Так, всупереч положенням статті 9 Закону України «Про лікарські засоби», третина із зареєстрованих препаратів не має підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики.
При цьому Міністерство охорони здоров’я України неодноразово проводило реєстрацію окремих лікарських засобів, незважаючи на отримання з Держлікслужби України інформації про виробників, яким відмовлено у видачі сертифікатів відповідності. Зокрема 10.08.2012 року зареєстровано лікарські засоби КЛАФАР 250, КЛАФАР 500 виробництва компанії Екюмс Драгс енд Фармасьютикалс Лтд. (Індія), а у вересні 2012 року — лікарський засіб ГАТИЛИН виробництва компанії Євролайф Хелткеар Пвт. Лтд. (Індія). Між тим, обом цим виробникам відмовлено у видачі сертифікату в зв’язку з виявленням недостовірних відомостей у документах, що додавались до заяви на видачу сертифіката (накази від 11.07.2012 № 583 та від 21.08.2012 № 723).
Окрім того, Міністерством охорони здоров’я України не вжито заходів до припинення дії реєстраційних посвідчень лікарських засобів тих виробників, яким Держлікслужбою України відмовлено у видачі сертифікатів відповідності умов виробництва лікарських засобів вимогам належної виробничої практики. Наприклад, подібна ситуація стосується виробників Наброс Фарма Пвт. Лтд. (Індія) та Дженом Біотек Пвт. Лтд. (Індія), яким відмовлено у видачі сертифікату відповідності в зв’язку з наявністю критичних і суттєвих порушень вимог належної виробничої практики (накази від 06.09.2012 № 758 та від 06.03.2013 № 292).
Слід відзначити, що відповідно до п.8 Порядку державної реєстрації (перереєстрації) лікарських засобів, затвердженого постановою Кабінету Міністрів України від 26 травня 2005 р. № 376, Міністерство охорони здоров’я України може прийняти у визначеному порядку рішення про повну або тимчасову заборону застосування лікарського засобу шляхом припинення дії реєстраційного посвідчення без повернення збору за державну реєстрацію цього засобу у разі виявлення невідомих раніше небезпечних його властивостей, зокрема, якщо лікарський засіб не був введений в обіг на території України протягом двох років з моменту його державної реєстрації (перереєстрації), якщо це не зумовлено специфікою виробництва та/або застосування такого лікарського засобу.
Водночас, незважаючи на те, що лікарські засоби цієї категорії становлять близько десятої частини від усіх зареєстрованих, протягом 2012 року не прийнято жодного рішення про повну або тимчасову заборону застосування лікарських засобів, які не були введені в обіг на території України протягом двох років з моменту їх державної реєстрації (перереєстрації).
Через недостатній контроль посадових осіб Міністерства охорони здоров’я України від лікувальних закладів не завжди своєчасно надходять повідомлення про виявлені небезпечні побічні реакції при застосуванні ліків. Так, лише 25.07.2011 року до управління післяреєстраційного нагляду ДП «Державний експертний центр Міністерства охорони здоров’я України» надійшло повідомлення з Бєршадської центральної районної лікарні (Вінницька область) про випадок смерті, який стався ще 18.07.2010 після застосування лікарського засобу МІЛДРОНАТ (AT «Санітас», Литва), що не дозволило своєчасно розглянути питання про заборону його обігу.
Не в усіх випадках додержуються вимоги статті 9 Закону України «Про лікарські засоби» та пунктів 3–5 Порядку державної реєстрації (перереєстрації) лікарських засобів щодо державної реєстрації лікарських засобів за умови проведення необхідних досліджень для вивчення специфічної активності та безпечності, а також встановлення або підтвердження ефективності та нешкідливості лікарського засобу.
Наприклад, в березні 2013 року Солом’янським районним управлінням ГУМВС України в місті Києві розпочато досудове розслідування в кримінальному провадженні, відкритому за фактом порушення посадовими особами. Міністерства охорони здоров’я, ДП «Державний експертний центр МОЗ України» вимог законодавства про лікарські засоби за ознаками кримінального правопорушення, передбаченого частиною 1 статті 140 (Неналежне виконання професійних обов’язків медичним або фармацевтичним працівником) Кримінального кодексу України.
Більше того, у 2012 році були виявлені численні випадки, коли доклінічне вивчення і клінічне випробування лікарського засобу проводилось з грубим порушенням вимог чинного законодавства.
Зокрема, за результатами клінічного аудиту клінічного випробування у відділені дитячої ендокринної патології державної установи «Інститут ендокринології та обміну речовин ім. В.П.Комісаренка Національної академії медичних наук України» щодо вивчення ефективності і переносимості препарату ДЖІНТОПРІН (Генесайнс Фармасьютікалс Ко. Лтд, Китай) установлено, що 26 пацієнтів брали участь у клінічному випробуванні після закінчення строку, визначеного страховим договором. Крім того, усупереч статті 8 Закону України «Про лікарські засоби» інформаційні згоди 9 пацієнтів підписані лише одним із батьків. Окрім того, у відділенні дитячої кардіології (вроджених вад серця) державної установи «Науково-дослідний медичний центр дитячої кардіології та кардіохірургії МОЗ України» при дослідженні препарату БОСЕНТАН виявлені випадки неповідомлення органів опіки і піклування про участь у клінічному випробуванні одного із пацієнтів, а самі клінічні випробування проводилися без акредитаційного сертифікату закладу охорони здоров’я. За вказаним фактом 25.03.2013 року слідчим відділом Подільського РУ ГУМВС України в м. Києві розпочато кримінальне провадження з попередньою правовою кваліфікацією за частиною 1 статі 142 (Фальсифікація лікарських засобів або обіг фальсифікованих лікарських засобів) Кримінального кодексу України, досудове розслідування наразі триває.
Міністерством охорони здоров’я України в минулому році також не дотримано вимог статті 9 Закону України «Про лікарські засоби», яка встановлює десятиденний строк для видачі реєстраційного посвідчення про державну реєстрацію (перереєстрацію) лікарського засобу. Зокрема, майже через три місяці після проведення реєстрації 12.06.2012 року видано посвідчення на лікарський засіб ІРЕССА. Через півроку після реєстрації видано посвідчення на препарати АЛКЕРАН ТМ, ЛАВІС, ЛЕЙКЕРОН ТМ. Більше місяця не видавалося посвідчення на лікарський засіб ЕТАНОЛ 70, зареєстрований 03.02.2012 року. На лікарський засіб ІМАЗОЛ КРЕМПАТА зареєстрований 31.01.2012 року, посвідчення видано лише 06.06.2012, а на препарат КАТАДОЛОГ, зареєстрований 23.05.2012 року, реєстраційне посвідчення видано 05.06.2012 року.
Основними причинами виявлених порушень є неналежне виконання службовими особами Міністерства охорони здоров’я України, ДП «Державний експертний центр МОЗ України» своїх посадових обов’язків. Умовою їх вчинення є відсутність достатнього контролю за діяльністю посадових осіб з боку керівництва Міністерства охорони здоров’я України.
Виявлені факти обігу неякісних лікарських засобів, невжиття заходів реагування до їх усунення зумовлений також неналежним розподілом повноважень між відповідними органами виконавчої влади. Зокрема, існуюча ситуація, коли державна реєстрація (перереєстрація) лікарського засобу віднесена до компетенції Міністерства охорони здоров’я України, а сертифікація виробництва лікарських засобів на відповідність вимогам належної виробничої практики віднесена до компетенції Держлікслужби України, не перешкоджає обігу неякісних ліків та створює поле для зловживань з боку Міністерства охорони здоров’я України. На підтвердження цього можна навести низку прикладів, коли Міністерство охорони здоров’я України неодноразово проводило реєстрацію окремих лікарських засобів, незважаючи на отримання з Держлікслужби України інформації про виробників, яким відмовлено у видачі сертифікатів відповідності. Саме тому з метою забезпечено належного та ефективного державного контролю якості лікарських засобів, повноваження щодо державної реєстрації (перереєстрації) лікарського засобу мають бути передані до виключної компетенції Держлікслужби України.
IV. ЦІНОУТВОРЕННЯ НА ФАРМАЦЕВТИЧНУ ПРОДУКЦІЮ
Відповідно до рекомендацій Всесвітньої організації охорони здоров’я, доступність лікарських засобів є основним фактором, що визначає доступність системи охорони здоров’я для пацієнта.
Одним з ключових елементів доступності лікарських засобів є забезпечення справедливої, економічної обґрунтованої ціни на лікарські засоби, недопущення необґрунтованого та неконтрольованого зростання цін на ці засоби.
Слід відзначити, що чинним законодавством України встановлені окремі механізми регулювання цін на лікарські засоби і вироби медичного призначення на вітчизняному фармацевтичному ринку. Так, постановою Кабінету Міністрів України від 17.10.2008 року № 955 встановлено регулювання цін у вигляді граничних розмірів торговельних надбавок:
1) на лікарські засоби і вироби медичного призначення, які включені до Національного переліку основних лікарських засобів і виробів медичного призначення (крім наркотичних, психотропних лікарських засобів, прекурсорів та медичних газів) та обов’язкового мінімального асортименту (соціально орієнтованих) лікарських засобів і виробів медичного призначення для аптечних закладів, визначеного Міністерством охорони здоров’я, граничні постачальницько-збутові надбавки не вище ніж 10 відсотків оптово-відпускної ціни та граничні торговельні (роздрібні) надбавки, виходячи із закупівельної ціни, що не перевищують такі розміри:
| Закупівельна ціна, грн. | Торговельна (роздрібна) надбавка до закупівельної ціни,% |
|---|---|
| До 100 включно | 25 |
| Більше 100 до 300 включно | 23 |
| Більше 300 до 500 включно | 20 |
| Більше 500 до 1000 включно | 15 |
| Більше 1000 | 10 |
2) на лікарські засоби (крім наркотичних, психотропних лікарських засобів, прекурсорів та медичних газів) і вироби медичного призначення, оптово-відпускні ціни на які внесені до реєстру оптово-відпускних цін на лікарські засоби і вироби медичного призначення, які придбаваються повністю або частково за рахунок коштів державного та місцевих бюджетів, граничні постачальницько-збутові надбавки не вище ніж 10 відсотків до задекларованої зміни оптово-відпускної ціни з урахуванням мита, податку на додану вартість та граничні торговельні (роздрібні) надбавки не вище ніж 10 відсотків до закупівельної ціни з урахуванням податку на додану вартість. При цьому фактичний розмір оптово-відпускної ціни на кожну лікарську форму, дозування, споживчу упаковку лікарського засобу, усі типи, види, марки виробів медичного призначення не повинен перевищувати розміру внесеної до зазначеного реєстру оптово-відпускної ціни у гривнях.
Лікарські засоби і вироби медичного призначення вітчизняного виробництва, оптово-відпускна ціна яких нижча ніж 12 гривень за одну упаковку, не підлягають державному регулюванню, крім тих, що придбаваються за рахунок коштів державного та місцевих бюджетів (п. 1 постанови Кабінету Міністрів України від 17.10.2008 року № 955).
Порядок формування цін на лікарські засоби і вироби медичного призначення, щодо яких запроваджено державне регулювання, затверджено постановою Кабінету Міністрів України від 25.03.2009 року № 333. Даний Порядок визначає механізм формування цін на лікарські засоби і вироби медичного призначення, щодо яких запроваджено державне регулювання, для реалізації суб’єктом господарювання на внутрішньому ринку з урахуванням граничних постачальницько-збутових і торговельних (роздрібних) надбавок.
Відповідно до п. 2 Порядку гранична постачальницько-збутова надбавка є максимально допустимим її розміром, який може враховуватися суб’єктом господарювання, що здійснює оптову торгівлю, при визначенні ціни товару. Гранична постачальницько-збутова надбавка не повинна перевищувати її встановленого розміру незалежно від кількості здійснених суб’єктами господарювання операцій з реалізації товару.
Відповідно до п. 3 Порядку гранична торговельна (роздрібна) надбавка є максимально допустимим її розміром, який може враховуватися суб’єктом господарювання при реалізації товару через аптечну мережу.
Таким чином, відповідно до норм чинного законодавства, регулювання граничного розміру надбавки до цін встановлено на лікарські засоби і вироби медичного призначення, які:
- включені до Національного переліку основних лікарських засобів і виробів медичного призначення, затвердженого постановою Кабінету Міністрів України від 25.03.2009 року № 333;
- включені до Обов’язкового мінімального асортименту (соціально орієнтованих) лікарських засобів і виробів медичного призначення для аптечних закладів, затвердженого наказом Міністерства охорони здоров’я України від 29.12.2011 року № 1000.
Тобто аптеки можуть встановити торговельну надбавку вищу, ніж граничні торговельні надбавки, передбачені постановою № 955, на лікарські засоби і вироби медичного призначення, не включені у вищезазначені переліки (в тому числі лікарські засоби і вироби медичного призначення вітчизняного виробництва, оптово-відпускна ціна яких нижча, ніж 12 гривень за одну упаковку), а також на супутні товари, перелік яких затверджений наказом МОЗ від 06.07.2012 р. № 498.
Окрім того, в минулому році розпочато впровадження підходів щодо регулювання цін на лікарські засоби через встановлення референтних цін. Зокрема, на підставі постанови Кабінету Міністрів України від 25 квітня 2012 року № 340 ініційовано пілотний проект щодо встановлення референтних цін на лікарські засоби для лікування осіб з гіпертонічною хворобою.
Разом з тим, вищевказані механізми регулювання цін на лікарські засоби і вироби медичного призначення не можуть забезпечити реалізацію свого основного призначення — формування справедливих цін на фармацевтичну продукції, недопущення зловживань з боку суб’єктів господарювання, які суттєво завищують ціни на лікарські засоби та вироби медичного призначення, що реалізуються у торговельній (роздрібній) мережі.
Так, останнім часом відбувається зростання цін на лікарські засоби, що пов’язано не з підвищенням ефективності, безпеки та якості цих засобів, а викликано діями суб’єктів ринку лікарських засобів, спрямованими на максимізацію прибутку. Необґрунтоване та неконтрольоване зростання цін на лікарські засоби, інші проблеми у цій сфері зумовлюють погіршення стану системи охорони здоров’я і соціального захисту населення, що може спровокувати небезпечне погіршення стану здоров’я населення і, як наслідок, призвести до створення загрози національним інтересам і національній безпеці України.
Як наслідок, непоодинокими є випадки, коли в Україні окремі лікарські засоби та вироби медичного призначення коштують в 2–3 рази дорожче, ніж в країнах ЄС та СНД.
Вказана проблема є особливо гострою, враховуючи вартісні показники вітчизняного фармацевтичного ринку. Так, за підсумками минулого року обсяг фармацевтичного ринку склав 31,65 млрд. гривень за 1,43 млрд. упаковок лікарських засобів.
Обсяг роздрібних продажів вітчизняних лікарських засобів становив 8,39 млрд. гривень за 0,83 млрд. упаковок лікарських засобів, імпортних — 18,66 млрд. гривень за 0,44 млрд. упаковок лікарських засобів.
Середня вартість упаковки лікарського засобу українського виробництва в 2012 році становила 10,2 гривні, іноземного — 42,2 гривні, тобто упаковка лікарського засобу вітчизняного виробництва в 4 рази дешевше імпортного.
Необхідно також враховувати, що проблема необґрунтованого та неконтрольованого зростання цін негативно впливає на добробут окремих категорій пацієнтів, лікування яких здійснюється виключно лікарськими засобами іноземного виробництва. Так, за офіційними даними Міністерства охорони здоров’я України імпортними є 88% препаратів для хворих на СНІД, 87% ліків від туберкульозу, 90% для онкохворих і 100% медикаментів для трансплантології. Окрім того, вітчизняні аналоги (за міжнародними непатентованими назвами) відсутні у 609 лікарських засобів, які імпортувались до України впродовж 2011–2012 років.
На вказаній проблемі, зокрема, наголошується у рішенні Ради Національної безпеки і оборони України «Про забезпечення населення якісними та доступними лікарськими засобами» від 25 травня 2012 року, що було введено в дію Указом Президента України від 30 серпня 2012 року № 526/2012.
На підтвердження фактів обігу на вітчизняному фармацевтичному ринку лікарських засобів та виробів медичного призначення за суттєво завищеними цінами можна навести результати порівняльного аналізу роздрібних цін на окремі лікарські засоби в Україні, Білорусії та Російській Федерації, проведеного Державною інспекцією України з контролю за цінами.
Проведений аналіз свідчить, що роздрібні ціни на окремі лікарські засоби в України перевищують ціни на відповідні товари в Білорусії та Російській Федерації (у перерахунку на гривню) більше ніж на 60%.
Зокрема, істотне завищення роздрібних цін можна продемонструвати на наступних прикладах:
| № з/п | Назва лікарського засобу | Дозування | Виробник | Роздрібна ціна в Україні | Роздрібна ціна в Білорусії | % | Роздрібна ціна в Російській Федерації | % |
|---|---|---|---|---|---|---|---|---|
| 1 | АКТОВЕГИН | 40 мг/мл 10 мл амп. №5 | Takeda (Японія) | 319,5 | 274,0 | -14.2 | 145,0 | -54,6 |
| 2 | ЕССЕНЦІАЛЕ ФОРТЕ Н | З00 мг №30 | Sanofi-Aventis (Франція) | 82,0 | 70,0 | -14,6 | 82,0 | 0 |
| 3 | КАРДІОМАГНІЛ | 75 мг №30 | Takeda (Японія) | 26,51 | 21 | -20,8 | 21 | -20,8 |
| 4 | НО-ШПА | р-р 40 мг амп. 2 мл № 25 | Sanofi-Aventis (Франція) | 71,79 | 51 | -29,0 | 54 | -24,8 |
| 5 | ЦЕРАКСОН | р-р 1000 мг 4 мл №5 | Ferrer International (Японія) | 440,0 | 345,0 | -21,6 | 170,0 | -61,4 |
| 6 | СПАЗМАЛГОН | р-р амп. 2мл №5 | Sopharma іActavis (Болгарія) | 39,5 | 39.0 | -1,3 | 29 | -29,1 |
| 7 | КЕТАНОВ | р-р 30 мг/мл. амп 1 мл № 10 | Bionorica (Індія) | 68,27 | 51,0 | -25,3 | 24 | -64,8 |
| 8 | ЛАЗОЛВАН | табл. 30 мг №50 | Boehringer Ing (Німеччина) | 53,85 | 49,0 | -9,0 | 51,0 | -5,3 |
| 9 | КАНЕФРОН | драже №60 | Bionorica (Німеччина) | 69,9 | 63,0 | -9,9 | 70,0 | 0,1 |
| 10 | КАРСІЛ | 22,5 мг №80 | Sopharma (Болгарія) | 45,06 | 37,0 | -17,9 | 33,0 | -26,8 |
| 11 | СУМАМЕД | капс. 500 мг №3 | TEVA (Ізраїль) | 128,24 | 125,0 | -2,5 | 112,0 | -12,7 |
| 12 | ПЛАВІКС | табл. п/о 75 мг, № 28 | Sanofi-Aventis (Франція) | 789,0 | 700,0 | -11,3 | 580,0 | -26,5 |
| 13 | КАРСИЛ ФОРТЕ | 90 мг №30 | Sopharma (Болгарія) | 60,6 | 49,0 | -19,1 | 53,0 | -12,5 |
| 14 | ДІАБЕТОН МR | табл. 60 мг №30 | Servier (Франція) | 63,79 | 76,0 | 19,1 | 42,0 | -34,2 |
| 15 | НУРОФЕН | табл. 200 мг № 24 | Reckett Benckiser (Великобританія) | 27,2 | 14,0 | -48,5 | 23,0 | -15,4 |
| 16 | ГЕПТРАЛ | табл. 400 мг № 20 | Abbott Labs (Німеччина) | 374,57 | 299,00 | -20,2 | 321,0 | -14,3 |
| 17 | ГЕПТРАЛ | пор. с раств 400 мг + 5 мл №5 | Abbott Labs (Німеччина) | 461,0 | 365,0 | -20,8 | 368,0 | -20,2 |
| 18 | ДОЛАРЕН | табл. № 100 | Dr. Reddy’s (Індія) | 89,2 | 59,0 | -33,9 | 71,0 | -20,4 |
| 19 | ЦЕРЕБРОЛІЗІН | р-р 10 мл №5 | EBEWE (Австрія) | 326,5 | 293,0 | -10,3 | 284,0 | -13,0 |
| 20 | КОНКОР | табл. 5 мг №50 | Takeda (Японія) | 87,8 | 87,0 | -0,9 | 66,0 | -24,8 |
| 21 | КОНКОР | табл. 10 мг №50 | Takeda (Японія) | 144,0 | 136,0 | -5,6 | 113,0 | -21,5 |
| 22 | ГЕРБІОН 3 ПЕРВОЦВІТОМ | сироп 150 мл | KRKA (Словенія) | 34,5 | 25,0 | -27,5 | 25,0 | -27,5 |
| 23 | ЛОРАКСОН | пор. 1000 мг № 12 | Exir (Іран) | 292,8 | 59,0 | -79,8 | 59,0 | -79,8 |
| 24 | ЛОРАКСОН | пор. 500 мг № 12 | Exir (Іран) | 142,8 | 45,0 | -68,5 | 45,0 | -68,5 |
| 25 | ФАРІНГОСЕПТ ЛИМОН | табл. 10 мг № 20 | Ranbaxy (Індія) | 26,5 | 24,0 | -9,4 | 18,0 | -31,1 |
| 26 | ФАРІНГОСЕПТ | табл. 10 мг № 20 | Ranbaxy (Індія) | 26,65 | 24,0 | -9,4 | 18,0 | -31,1 |
| 27 | ДІПРОСПАН | амп. 1 мл №5 | Merck&Co (США) | 349,73 | 272,0 | -22,2 | 349,0 | -0,2 |
| 28 | КЛЕКСАН | шприц преднап. 4000, № 10 | Sanofi-Aventis (Франція) | 834,43 | 747,0 | -10,5 | 61,0 | -92,7 |
| 29 | ЛАНТУС СОЛОСТАР | шприц з картр. №5 | Sanofi-Aventis (Франція) | 936,15 | 590,0 | -37,0 | 815,0 | -12,9 |
Як можна пересвідчитись з наведеної інформації, жоден з вищевказаних лікарських засобів не виробляється в Білорусії або Російській Федерації, тобто всі ці товари імпортуються з інших країн, зокрема, Франції, Німеччини, Словенії, Австрії, Великобританії тощо. Таким чином, вказані товари мають реалізовуватись в Україні за приблизно подібними цінами. Між тим, у 2012 році має місце суттєве перевищення вартості вказаних препаратів при їх реалізації в роздрібній (аптечній) мережі України, порівняно з роздрібними цінами на ці ж саме препарати в Білорусії та Російській Федерації.
| № з/п | Назва лікарського засобу | Кількість упаковок (шт.) | Сума (тис. грн.) | Мінімальна роздрібна ціна в країнах СНД (грн.) | Переплата (тис. грн.) |
|---|---|---|---|---|---|
| 1 | АКТОВЕГИН | 178 490 | 57 483 | 145,0Російська Федерація | 31 601 |
| 2 | ЕССЕНЦІАЛЕ ФОРТЕ Н | 1 743 948 | 143 070 | 70,0Білорусія | 20 993 |
| 3 | КАРДІОМАГНІЛ | 2 239 383 | 58 666 | 21,0Російська Федерація, Білорусія | 11 639 |
| 4 | НО-ШПА | 281 302 | 26 137 | 51,0Білорусія | 11 791 |
| 5 | ЦЕРАКСОН | 59 150 | 24 016 | 170,0Російська Федерація | 13 961 |
| 6 | СПАЗМАЛГОН | 30 798 | 1 476 | 29,0Російська Федерація | 583 |
| 7 | КЕТАНОВ | 467 519 | 30 217 | 24,0Російська Федерація | 18 997 |
| 8 | ЛАЗОЛВАН | 234 590 | 12 213 | 49,0Білорусія | 719 |
| 9 | КАНЕФРОН | 909 886 | 69 999 | 63,0Білорусія | 12 676 |
| 10 | КАРСІЛ | 2 372 831 | 98 557 | 33,0Російська Федерація | 20 254 |
| 11 | СУМАМЕД | 231 402 | 33 131 | 112,0Російська Федерація | 7 214 |
| 12 | ПЛАВІКС | 24 560 | 20 052 | 580,0Російська Федерація | 10 315 |
| 13 | КАРСИЛ ФОРТЕ | 141 492 | 9 250 | 49,0Білорусія | 2 317 |
| 14 | ДІАБЕТОН МR | 1 212 353 | 86 075 | 42,0Російська Федерація | 35 156 |
| 15 | НУРОФЕН | 285 094 | 7 740 | 14,0Білорусія | 3 749 |
| 16 | ГЕПТРАЛ | 110 004 | 42 107 | 299,0Білорусія | 9 216 |
| 17 | ГЕПТРАЛ | 101 359 | 37 983 | 365,0Білорусія | 987 |
| 18 | ДОЛАРЕН | 470 848 | 44 663 | 59Білорусія | 16 883 |
| 19 | ЦЕРЕБРОЛІЗІН | 48 997 | 18 877 | 284,0Російська Федерація | 4 962 |
| 20 | КОНКОР | 275 658 | 25 655 | 66,0Російська Федерація | 7 462 |
| 21 | КОНКОР | 100 400 | 15 219 | 113,0Російська Федерація | 3 874 |
| 22 | ГЕРВІОН 3 ПЕРВОЦВІТОМ | 778 536 | 24 459 | 25,0Білорусія,Російська Федерація | 4 996 |
| 23 | ЛОРАКСОН | 157 795 | 44 375 | 59,0Білорусія,Російська Федерація | 35 066 |
| 24 | ЛОРАКСОН | 12 941 | 1 935 | 45,0Білорусія,Російська Федерація | 1 352 |
| 25 | ФАРІНГОСЕПТ ЛИМОН | 403 568 | 10 729 | 18,0Російська Федерація | 3 465 |
| 26 | ФАРІНГОСЕПТ | 1 304 221 | 34 446 | 18,0Російська Федерація | 10 971 |
| 27 | ДІПРОСПАН | 127 553 | 44 543 | 272,0Білорусія | 9 849 |
| 28 | КЛЕКСАН | 20 886 | 18 592 | 61,0Російська Федерація | 17 318 |
| 29 | ЛАНТУС СОЛОСТАР | 15 808 | 15 395 | 590,0Білорусія | 6 069 |
| 1 057 060 | 334 435 |
З вказаної інформації можна зробити висновок, що лише при купівлі в аптечній (роздрібній) мережі вказаних 29 препаратів українці переплатили у минулому році близько 335 мільйонів гривень.
Як вбачається зі зведеної статистичної інформації митних органів України, у минулому році 26 суб’єктів зовнішньоекономічної діяльності імпортували в Україну 111 тонн лікарських засобів не дозованих і не фасованих для роздрібної торгівлі (товарна позиція згідно з УКТЗЕД 3003) загальною вартістю 4,5 млн. дол. США. Окрім того, 336 суб’єктів зовнішньоекономічної діяльності імпортували в Україну 35,3 тис. тонн лікарських засобів дозованих або фасованих для роздрібної торгівлі (товарна позиція згідно з УКТЗЕД 3004) загальною вартістю 2,9 млрд. дол. США.
У зв’язку з цим слід відзначити, що необґрунтоване та неконтрольоване зростання цін на лікарські засоби та вироби медичного призначення зумовлено, у першу чергу, завищенням митної вартості таких товарів при їх ввезенні на митну територію України.
Відповідно до частини 4 статті 58 Митного кодексу України митною вартістю товарів, які ввозяться на митну територію України відповідно до митного режиму імпорту, є ціна, що була фактично сплачена або підлягає сплаті за товари, якщо вони продаються на експорт в Україну.
Митна вартість товарів, що переміщуються через митний кордон України, визначається декларантом відповідно до норм Митного кодексу України. Декларант або уповноважена ним особа, які заявляють митну вартість товару, зобов’язані подавати митному органу достовірні відомості про визначення митної вартості, які повинні базуватись на об’єктивних, документально підтверджених даних, що піддаються обчисленню.
Водночас, як доводить практика останніх років, імпорт лікарських засобів та виробів медичного призначення на митну територію України здійснюється, переважно, не на основі прямих зовнішньоекономічних договорів з зарубіжними підприємствами-виробниками лікарських засобів та виробів медичного призначення, а через суб’єктів зовнішньоекономічної діяльності, зареєстрованих у країнах із спрощеною системою звітності та оподаткування. При цьому постачання товарів через ланцюг компаній-посередників здійснюється фіктивно, рух товару відбувається лише «на папері» та без фактичного перетину митного кордону відповідної країни.
У результаті використання подібних посередницьких операцій декларант або уповноважена ним особа на законних підставах може заявляти таку митну вартість лікарських засобів та виробів медичного призначення, яка суттєво перевищує ціни підприємства-виробники.
Слід також враховувати, що Податковим кодексом України для операцій з поставки лікарських засобів та виробів медичного призначення визначено пільговий режим оподаткування. Так, підпунктом 197.1.27 пункту 197.1 статті 197 операції з постачання лікарських засобів, дозволених для виробництва і застосування в Україні та внесених до Державного реєстру лікарських засобів, а також виробів медичного призначення за переліком, затвердженим Кабінетом Міністрів України, звільняються від оподаткування податком на додану вартість. До набрання чинності Податковим кодексом України зазначені операції також звільнялись від оподаткування податком на додану вартість відповідно до Закону України від 02.04.1997 року № 168/97-ВР «Про податок на додану вартість».
У зв’язку з цим доводиться констатувати, що запровадження такого пільгового режиму оподаткування жодним чином не досягло свого основного призначення — здешевлення вартості лікарських засобів та виробів медичного призначення для кінцевих споживачів. Навпаки, це зумовило значні втрати бюджету, не привело до здешевлення вартості ліків, а торгова націнка на зазначені товари в окремих випадках сягає сотень відсотків. Втрати бюджету від застосування платниками податку на додану вартість пільгового режиму оподаткування операцій з поставки лікарських засобів та виробів медичного призначення становили у 2010 році 3,1 млрд. грн., у 2011 році — 3,4 млрд. грн.
Окрім того, зважаючи на пільговий режим оподаткування, імпортери лікарських засобів, завищуючи митну вартість лікарських засобів та виробів медичного призначення, отримують можливість для тіньового виведення коштів за межі держави та штучної мінімізації власних податкових зобов’язань.
Факти завищення митної вартості лікарських засобів та виробів медичного призначення підтверджуються результатами діяльності митних органів України. Так, у минулому році митними органами було направлено до митних адміністрацій іноземних країн-експортерів 46 запитів з метою перевірки автентичності документів, поданих для підтвердження заявленої митної вартості лікарських засобів та виробів медичного призначення. Станом на 01.03.2013 року отримані відповіді на 19 запитів. Надана у 8 відповідях інформація свідчить про те, що ціна товару у виробника у 2–4 рази менша від вартості товару, зазначеної в документах (рахунках-фактурах) фірм-посередників, зареєстрованих у країнах із спрощеною системою обліку й оподаткування, які надавались митним органам при митному оформленні імпорту зазначених товарів.
Окрім того, на підставі укладених Україною міжнародних угод, митними органами України у 2012 році до митних адміністрацій іноземних країн-експортерів направлено 227 запитів про надання взаємної адміністративної допомоги у проведенні перевірок законності ввезення в Україну лікарських засобів та виробів медичного призначення. За результатами опрацювання отриманих відповідей заведено 6 справ про порушення митних правил. Наприклад, як вбачається з однієї із відповідей, фактурна вартість товару (лікарські засоби) при експорті з Індії становила 583962,5 дол. США. Між тим, українським суб’єктом зовнішньоекономічної діяльності заявлено митну вартість цього самого товару в розмірі 1179402,5 дол. США, тобто вдвічі більше, ніш фактурна вартість товару при експорті.
Яскравим прикладом використання фіктивних посередницьких операцій з метою завищення митної вартості товарів можна назвати схему ввезення на митну територію України лікарських засобів, виявлену у минулому році підрозділом податкової міліції м. Києва Державної податкової служби України.
Як було встановлено, громадянин іноземної держави зареєстрував на території України низку підприємств — TOB «Абрил формулейшнз» (код ЄДРПОУ 34726658) та TOB «Абрил» (код ЄДРПОУ 37144155), а також придбав підприємство-нерезидент з ознаками «фіктивності» STALLION BIOSKIENCE LLC. У подальшому, використовуючи печатку підприємства-нерезидента з ознаками «фіктивності», вказана особа складала завідомо неправдиві фінансово-господарські документи щодо продажу нібито компанією STALLION BIOSKIENCE LLC лікарських засобів підприємствам TOB «Абрил формулейшнз» та TOB «Абрил» та подавала вказані фіктивні документи до митних органів України, на підставі яких формувалася ціна на ввезені лікарські засоби. В дійсності ж зазначені лікарські засоби по прямим зовнішньоекономічним контрактам між заводами-виробниками, що знаходяться в Індії, та TOB «Абрил формулейшнз» і TOB «Абрил» поставлялися безпосередньо на територію України без будь-якої участі компанії STALLION BIOSKIENCE LLC.
Імпортовані лікарські засоби в подальшому реалізовувались на адресу ЗAT «АЛЬБА УКРАЇНА», TOB «БАДМ», TOB «Оптима фарма», TOB «Прогресфарм», TOB «Фірма «Лакас». При цьому вказані підприємства неодноразово брали участь у конкурсних (тендерних) торгах, що проводились Міністерством охорони здоров’я України, його структурними підрозділами та територіальними управліннями (відділами) охорони здоров’я, щодо закупівель лікарських засобів за державні кошти та були їх переможцями, внаслідок чого реалізовували лікарські засоби по завищеним цінам, завдаючи при цьому збитки держави в особливо великих розмірах.
Загалом, TOB «Абрил формулейшнз» та TOB «Абрил» перераховано грошових коштів на розрахункові рахунки заводів-виробників — 192 млн. гривень, та на розрахункові рахунки STALLION BIOSKIENCE LLC — 97 млн. гривень. Попередньо орієнтовна сума збитків, завданих Державному бюджету України у результаті такої схеми склала понад 95 млн. гривень.
Іншим суттєвим фактором, що зумовлює необґрунтоване та неконтрольоване зростання цін на лікарські засоби та вироби медичного призначення, є зловживання монопольним (домінуючим) становищем на загальнодержавному та регіональних ринках торгівлі лікарських засобами, антиконкуренті узгоджені дії великооптових дистриб’юторів лікарських засобів, суб’єктів господарювання, які функціонують на регіональних ринках роздрібної торгівлі лікарськими засобами.
Подібна ситуація зумовлена тим, що на загальнодержавному ринку послуг з оптової реалізації лікарських засобів наявні суб’єкти господарювання, становище яких має ознаки монопольного (домінуючого). Зокрема, у 2012 році на ринку оптової реалізації лікарських засобів функціонувало 4 суб’єкти господарювання, сукупна частка яких у вартісних та кількісних показниках становила більше 70 відсотків.
Монопольне (домінуюче) становище суб’єктів господарювання відзначається також і на регіональних ринках роздрібної торгівлі лікарськими засобами. Так, у 2012 році органами Антимонопольного комітету України завершено дослідження 138 регіональних ринків роздрібної торгівлі лікарськими засобами, за результатами яких встановлено, що на переважній більшості регіональних ринків (110 ринків) існують суб’єкти господарювання, становище яких має ознаки індивідуальної чи колективної монополії.
В ході проведення зазначених досліджень Антимонопольним комітетом України надано близько 1500 рекомендацій операторам ринків лікарських засобів з метою запобігання вчиненню порушень конкуренційного законодавства, а також розглянуто 57 справ про порушення законодавства про захист економічної конкуренції у вигляді:
8 — зловживання монопольним (домінуючим) становищем на ринку;
3 — антиконкурентних дій органів державної влади, органів місцевого самоврядування;
1 — антиконкурентних узгоджених дій;
17 — недобросовісної конкуренції;
28 — інших видів порушень.
Порушення на ринках послуг охорони здоров’я, лікарських засобів та виробів медичного призначення, виявлені у минулому році органами Антимонопольного комітету України, складали 6,96 відсотка порушень законодавства про захист економічної конкуренції. Кількість виявлених порушень у вигляді зловживання монопольним (домінуючим) становищем на ринках послуг охорони здоров’я, лікарських засобів та виробів медичного призначення становила 8,65 відсотка загальної кількості порушень цього виду.
Слід відзначити, що у минулому році економічно необґрунтоване зростання цін на окремі лікарські засоби було спричинено також зловживанням монопольним (домінуючим) з боку окремих виробників. Наприклад, Антимонопольним виявлені факти реалізації ПАТ «Монфарм» лікарського засобу ПАРАЦЕТАМОЛ (супозиторії ректальні, 0,17 г, № 10) та ПАТ «Фармак» лікарського засобу НАФТИЗИН (0,1%, 10 мл, в п/е фл.) на внутрішньому ринку за цінами значно вищими, ніж ціни реалізації на експорт. У зв’язку з цим розпочато розгляд справ про порушення законодавства зазначеними виробниками у вигляді зловживання монопольним (домінуючим) становищем на ринку шляхом встановлення таких цін реалізації товару, які неможливо було б встановити за умов значної конкуренції на ринку.
Також має місце сезонне зростання оптово-відпускних та закупівельних цін на лікарські засоби та вироби медичного призначення, ціни на які підлягають державному регулюванню. Що особливо загрозливо, зростання цін спостерігається на профілактичні та лікарські засоби і засоби індивідуального захисту проти поширення гострих респіраторних вірусних інфекцій та грипу в осінньо-зимовий період, коли вказані захворювання мають найбільшу поширеність серед населення України.
Так, на виконання підпункту 3 пункту 8 протоколу засідання Кабінету Міністрів України № 74 від 26.09.2012 року «Про стан забезпечення закладів охорони здоров’я вакцинами та сироватками з метою запобігання виникненню та розповсюдженню інфекційних захворювань» Державною інспекцією України з контролю за цінами проведено аналіз рівня цін 173 суб’єктів господарювання, які здійснюють виробництво, оптову та роздрібну торгівлю лікарськими засобами та виробами медичного призначення для профілактики, лікування гострих респіраторних вірусних інфекцій та грипу, які внесені до Національного переліку лікарських засобів та виробів медичного призначення та Обов’язкового мінімального асортименту (соціально орієнтованих) лікарських засобів і виробів медичного призначення для аптечних закладів. Дослідженням охоплено 22043 цінові пропозиції на лікарські засоби та вироби медичного призначення. Станом на 01.04.2013 року у порівнянні з 01.03.2012 року підвищення цін відбулося на 25,7 відсотків товарних позицій. Аналіз рівня оптово-відпускних цін, проведений у основних вітчизняних виробників лікарських засобів, свідчить про те, що у порівнянні з березнем 2013 ринку на ринку виробництва спостерігається зростання оптово-відпускних цін на лікарські засоби, які застосовуються для профілактики та лікування гострих респіраторних вірусних інфекцій і грипу. Зростання цін до 21 відсотків на препарати вітчизняного виробництва відбувається в основному за рахунок підвищення оптово-відпускних цін українськими фармацевтичними підприємствами, а саме: ВАТ «Київмедпрепарат», ПАТ «Фармак», ПрАТ «Технолог», ТОВ «Здоров’я», ТОВ «СТИРОЛ БІОФАРМ», ЗАТ «Лекхім-Харків», ПАТ НВЦ «Борщагівський хіміко-фармацевтичний завод» на препарати: АМОКСИЛ, ЦИПРОФЛОКСАЦИН, АМБРОКСОЛ, ЦЕФАЗОЛІН, АМІЗОН, АСКОРБІНОВА КИСЛОТА.
Разом з тим, на оптовому ринку реалізації лікарських засобів спостерігається коливання цін на досліджувану групу препаратів до 30 відсотків, причинами яких є зміна закупівельних цін (митної вартості) імпортерами. За цих умов відбувається зростання роздрібних цін до 40 відсотків в основному на лікарські засоби, які використовуються для лікування грипу та гострих респіраторних захворювань, а саме: АЦЦ, ЛАЗОЛВАН, ФЛЕМОКЛАВ СОЛЮТАБ, АМОКСИКЛАВ, ПАНАДОЛ ЕКСТРА, зокрема, у Волинській, Луганській, Київській, Одеській областях та м. Києві.
Також зафіксоване застосування високого рівня постачальницько-збутових та торговельних надбавок на лікарські засоби та вироби медичного призначення вітчизняного виробництва, оптово-відпускна ціна яких є нижчою від 12 гривень, тобто на ті, які не підлягають державному регулюванню, але користуються попитом у найбільш соціально незахищених верств населення. Зокрема, на такі лікарські засоби як АСКОРБІНОВА КИСЛОТА, ПАРАЦЕТАМОЛ, АЦЕТИЛСАЛІЦИЛОВА КИСЛОТА, ОКСОЛІНОВА МАЗЬ, ЦЕФТРІАКСОН, ЦИПРОФЛОКСАЦИН, ДОКИЦИКЛІН, ФАРМАЗОЛІН застосовані торговельні надбавки до 57 відсотків, що зафіксовано у Волинській, Кіровоградській, Тернопільській, Харківській, Львівській, Полтавській, Чернівецькій, Херсонській областях та м. Києві.
Загалом, незважаючи на вищевказані результати діяльності контролюючих органів, слід стверджувати, що вони не забезпечили дотримання цінової дисципліни з боку виробників лікарських засобів, великооптових дистриб’юторів та аптечних мереж у загальнодержавному масштабі.
Економічно необґрунтована ціна на лікарські засоби негативно відображається на добробуті громадян, оскільки вони змушені переплачувати за ліки. Більш того, завищені ціни призводять до того, що найменш соціально захищені верстви населення взагалі не мають можливості придбати необхідні ліки у потрібній їм кількості. Таким чином, існуюча ситуація із суттєвим завищенням цін на лікарські засоби та вироби медичного призначення є прикладом невиконання державою соціальних гарантій населенню щодо забезпечення доступності лікарських засобів.
V. ДЕРЖАВНІ ЗАКУПІВЛІ МІНІСТЕРСТВА ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ
У 2012 році Міністерством охорони здоров’я України укладено 306 договорів із застосуванням процедур закупівлі (процедура відкритих торгів і процедура закупівлі в одного учасника) на суму близько 1,9 млрд. гривень.
Як передбачено статтею 3 Закону України «Про здійснення державних закупівель», одним з основних принципів, за яким здійснюються державні закупівлі, є максимальна економія та ефективність.
З цього приводу слід відзначити, що на виконання наказу Міністерства охорони здоров’я України від 31.10.2011 року № 711 наказом ДП «Державний експертний центр МОЗ України» у складі центру створено відділ моніторингу цін на лікарські засоби і вироби медичного призначення. Моніторингу цін підлягають лікарські засоби, що відносяться до Переліку лікарських засобів вітчизняного та іноземного виробництва, які можуть закуповувати заклади охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів, затвердженого постановою Кабінету Міністрів України від 05.09.1996 року № 1071, в частині збору даних щодо задекларованих оптово-відпускних цін в Україні, а також відповідних цін в зарубіжних країнах.
При проведенні моніторингу цін здійснюється порівняння з цінами доступних для використання аналогічних реєстрів цін наступних країн: Російська Федерація, Болгарія, Молдова, Польща, Словацька Республіка, Угорщина та Чехія. Інформація по кожному з вказаних реєстрів в перерахунку цін за поточним курсом на гривні щоквартально (до 27.03.2013 року — щотижнево) подається до Міністерства охорони здоров’я України (Управління моніторингу державних цільових програм та державних закупівель та Управління лікарських засобів та медичної продукції), як інформаційно-довідковий матеріал для відповідного використання.
Разом з тим, незважаючи на наявність вичерпної інформації щодо цін на лікарські засоби в зарубіжних країнах, у 2012 році Міністерство охорони здоров’я України у рамках здійснення державних закупівель неодноразово закуповувало імунобіологічні препарати, лікарські засоби, вироби медичного призначення і обладнання за суттєво завищеними цінами, що призвело до розтрати бюджетних коштів в особливо великих розмірах.
| Найменування товару | Виробник | Постачальник | Дата та номер договору | Поставлено | Мінімальна заявлена ціна за кордоном | Можлива економія | ||
|---|---|---|---|---|---|---|---|---|
| Міжнародна непатентована назва | Торговельна назва | К-ть | Ціна за од., грн. | |||||
| Тейкопланін, амп., фл., шпр. 400 мг | ТАРГОЦИД® | Группо Лепетіт С.р.Л., Італія | ТОВ «Людмила-Фарм» | 2Т/59/21–24 від 13.06.2012 | 2925 | 628,98 | 377,62(Болгарія) | 735228,00 |
| Цитарабін, амп., фл., шпр. 1000 мг | ЦИТОЗАР® | Пфайзер Італія С.р.л., Італія; Актавіс Італія С.п.А., Італія | ТОВ «Людмила-Фарм» | 2Т/59/21–24 від 13.06.2012 | 1938 | 245,00 | 157,10(Російська Федерація) | 170350,2 |
| Ганцикловір, амп., фл., шпр. 500 мг | ЦИМЕВЕН | Ф.Хоффманн-Ля Рош Лтд, Швейцарія | ТОВ «Фармадіс» | 5Т/50/21–24 від 13.06.2012 | 1292 | 317,60 | 38,04 (Болгарія) | 361191,52 |
| Вориконазол, амп., фл., шпр. 200 мг | ВІФЕНД | ДСМ Фармасютикалс Інк, США; Пфайзер Айленд Фармасьютікалз Лімітед, Ірландія; Пфайзер Пі.Джі.Ем., Франція | ТОВ «Людмила-Фарм» | 6Т/55/21–24 від 13.06.2012 | 5129 | 1153,20 | 968,51(Болгарія) | 947275,01 |
| Етопозид, амп., фл., шпр. 200 мг | ЕТОПОЗИД-ТЕВА | Фармахемі Б.В., Нідерланди | ТОВ «Фра-М» | 9Т/53/21–24 від 13.06.2012 | 3431 | 185,00 | 139,51 (Чехія) | 156076,00 |
| Метотрексат, амп., фл., шпр. 5000 мг | МЕТОТРЕКСАТ «ЕБЕВЕ» | ЕБЕВЕ Фарма Гес.М.б.Х. Нфг. КГ, Австрія | ТОВ «Фра-М» | 11Т/56/21–24 від 13.06.2012 | 522 | 1351,60 | 748,32 (Чехія) | 314912,00 |
| Флударабін, амп., фл., шпр. 50 мг | ФЛУДАБІН | Сіндан Фарма СРЛ, Румунія | ТОВ «Фра-М» | 11Т/56/21–24 від 13.06.2012 | 120 | 1071,11 | 516,92(Болгарія) | 66503,00 |
| Епоетин-альфа, амп., фл., шпр. 40000 МО | ЕПРЕКС | Сілаги АГ, Швейцарія | ТОВ «Людмила-Фарм» | 12Т/51/21–24 від 13.06.2012 | 786 | 4498,00 | 3640,77 (Угорщина) | 673783,00 |
| Посаконазол, амп., фл., шпр. 105 мл (40 мг/мл) | НОКСАФІЛ® | Патеон Інк., Канада та Шерінг-Плау, Франція, власна філія Шерінг-Плау Корпорейшн, США; Патеон Інк., Канада та Шерінг-Плау Лабо Н.В., Бельгія, власна філія Шерінг-Плау Корпорейшн, США | ТОВ «Людмила-Фарм» | 12Т/51/21–24 від 13.06.2012 | 495 | 11630,10 | 5985,05 (Словацька Республіка) | 2794299,75 |
| Пегаспаргаза, амп., фл. шпр. 3750 МО | ОНКАСПАР | Медак ГмбХ, Німеччина | ПрАТ «Ганза» | 13Т/58/21–24 від 13.06.2012 | 129 | 18309,98 | 13558,47 (Польща) | 612944,79 |
| Доцетаксел, амп., фл. шпр. 80 мг | ДОЦЕТ | Вінус Ремедіс Лімітед, Індія | ПрАТ «Альба-Україна» | 19Т/86/21–24 від 06.07.2012 | 634 | 3790,00 | 2847,65 (Молдова) | 597449,90 |
| Доцетаксел, амп., фл. шпр. 80 мг | ТАКСОТЕР® | Авентіс Фарма Дагенхем, Великобританія | ПрАТ «Альба-Україна» | 19Т/86/21–24 від 06.07.2012 | 337 | 3790,00 | 2891,36 (Словацька Республіка) | 302841,68 |
| Етопозид, амп., фл. шпр. 200 мг | ЕТОПОЗИД-ТЕВА | Фармахемі Б.В., Нідерланди | ПрАТ «Альба-Україна» | 19Т/86/21–24 від 06.07.2012 | 9611 | 181,90 | 139,51(Чехія) | 407410,29 |
| Іринотекан, амп., фл. шпр. 100 мг | ІРИНОСИНДАН | Сіндан Фарма СРЛ, Румунія; Актавіс Італія С.п.А., Італія | ТОВ «Фра-М» | 23Т/83/21–24 від 06.07.2012 | 2302 | 530,00 | 368,62(Словацька Республіка) | 371496,76 |
| Кальцію фолінат, амп., фл. шпр. 30 мг | ЛЕЙКОФОЗИН | Сіндан Фарма СРЛ, Румунія; Актавіс Італія С.п.А., Італія | ТОВ «Фра-М» | 23Т/83/21–24 від 06.07.2012 | 26718 | 56,94 | 28,99 (Болгарія) | 746768,10 |
| Лейпроліду ацетат, амп., фл. шпр. 11,25 мг | ЛЮКРИН ДЕПО | Такеда Фармасьютікал Компані Лтд, Японія; Аббот Лабораторіз С.А., Іспанія | ТОВ «Людмила-Фарм» | 26Т/82/21–24 від 06.07.2012 | 437 | 3275,00 | 2101,30 (Словацька Республіка) | 512906,90 |
| Лейпрорелін, амп., фл. шпр. 22,5 мг | ЕЛІГАРД 22,5 мг | МедиГене АГ, Німеччина; Толмар Інк., США; Канджин біоФарма Інк., США | ТОВ «Людмила-Фарм» | 26Т/82/21–24 від 06.07.2012 | 1225 | 4535,01 | 2045,94 (Словацька Республіка) | 3049110,70 |
| Медроксипро гестерону ацетат, амп., фл. шпр. 500 мг | ДЕПО-ПРОВЕРА® | Пфайзер Менюфекчуринг Бельгія Н.В., Бельгія | ТОВ «Людмила-Фарм» | 26Т/82/21–24 від 06.07.2012 | 2873 | 76,20 | 29,07 (Польща) | 135404,49 |
| Бортезоміб, амп., фл. шпр. 3,5 мг | ВЕЛКЕЙД® | Бен Веню Лабораторіз Інк., США; П’єр Фабр Медикамент Продакшн, Франція; Янссен Фармацевтика Н.В., Бельгія | ТОВ «Людмила-Фарм» | 27Т/100/21–24 від 10.07.2012 | 360 | 13526,50 | 9943,80 (Болгарія) | 1289772,00 |
| Епоетин-альфа, амп., фл., шпр. 40000 МО | ЕПРЕКС | Сілаги АГ, Швейцарія | ТОВ «Людмила-Фарм» | 27Т/100/21–24 від 10.07.2012 | 210 | 4498,00 | 3640,77 (Угорщина) | 180018,30 |
| Ертапенем, амп., фл. шпр. 1000 мг | ІНВАНЗ® | «Мерк Шарп і Доум», Франція, Лабораторія Мерк Шарп і Доум-Чібрет (Мірабел), Франція | ТОВ «Людмила-Фарм» | 21Т/113/21–24 від 10.07.2012 | 2658 | 425,00 | 332,27 (Болгарія) | 246476,34 |
| Ідарубіцину гідрохлорид, табл., капс., драже 10 мг | ЗАВЕДОС | Актавіс Італія С.п.А., Італія | ТОВ «Людмила-Фарм» | 31Т/113/21–24 від 10.07.2012 | 938 | 1035,54 | 458,10 (Словацька Республіка) | 541638,72 |
| Інтерферон альфа-2b / шприц-ручка 30 млн. МО | ІНТРОН А® | Шерінг-Плау (Брінні) Компані, Ірландія, власна філія Шерінг-Плау Корпорейшн, США; Шерінг-Плау Лабо Н.В., Бельгія | ТОВ «Людмила-Фарм» | 31Т/113/21–24 від 10.07.2012 | 571 | 2351,25 | 1303,27 (Польща) | 598396,58 |
| Етопозид, амп., фл., шпр. 200 мг | ЕТОПОЗИД-ТЕВА | Фармахемі Б.В., Нідерланди | ТОВ «Фра-М» | 32Т/114/21–24 від 10.07.2012 | 6828 | 181,00 | 139,51 (Чехія) | 283293,72 |
| Флударабіну фосфат, амп., фл. шпр. 50 мг | ФЛУДАРАБІН-ТЕВА | Фармахемі Б.В., Нідерланди | ТОВ «Фра-М» | 36Т/108/21–24 від 10.07.2012 | 1350 | 1129,00 | 838,67 (Польща) | 391945,50 |
| Флударабіну фосфат, амп., фл. шпр. 50 мг | ФЛУДАБІН | Сіндан Фарма СРЛ, Румунія | ТОВ «Фра-М» | 36Т/108/21–24 від 10.07.2012 | 1451 | 1071,11 | 516,92 (Болгарія) | 804129,69 |
| Цитарабін, амп., фл. шпр. 1000 мг | ЦИТОЗАР® | Пфайзер Італія С.р.л., Італія; Актавіс Італія С.п.А., Італія | ТОВ «Людмила-Фарм» | 41Т/101/21–24 від 10.07.2012 | 1040 | 195,70 | 157,10(Російська Федерація) | 40144,00 |
| Гемцитабін, амп., фл. шпр. 1000 мг | ГЕМЦИБІН | Сіндан Фарма СРЛ, Румунія; Актавіс Італія С.п.А., Італія | ПрАТ «Альба-Україна» | 45Т/117/21–24 від 12.07.2012 | 2007 | 1080,00 | 488,53 (Словацька Республіка) | 1187080,30 |
| Гозерелін, депо-шприц 10,8 мг | ЗОЛАДЕКС | АстраЗенека ЮК Лімітед, Великобританія | ПрАТ «Альба-Україна» | 45Т/117/21–24 від 12.07.2012 | 1899 | 3270,00 | 2261,61 (Польща) | 1914932,60 |
| Гемцитабін, амп., фл. шпр. 200 мг | ГЕМЦИБІН | Сіндан Фарма СРЛ, Румунія; Актавіс Італія С.п.А., Італія | ТОВ «Фра-М» | 47Т/116/21–24 від 12.07.2012 | 2990 | 161,00 | 81,88(Словацька Республіка) | 236568,80 |
| Гемцитабін, амп., фл. шпр. 200 мг | ГЕМЦИБІН | Сіндан Фарма СРЛ, Румунія; Актавіс Італія С.п.А., Італія | ТОВ «Фра-М» | 47Т/116/21–24 від 12.07.2012 | 1376 | 159,39 | 81,88(Словацька Республіка) | 106653,76 |
| Гозерелін, депо-шприц 3,6 мг | ЗОЛАДЕКС | АстраЗенека ЮК Лімітед, Великобританія | ТОВ «Компанія Укроптпостач» | 48Т/115/21–24 від 12.07.2012 | 1914 | 1195,00 | 698,89(Польща) | 949554,54 |
| Трипторелін, амп., фл. шпр. 11,25 мг | ДИФЕРЕЛІН® | Іпсен Фарма Біотек, Франція | ТОВ «Людмила-Фарм» | 50Т/125/21–24 від 17.07.2012 | 851 | 3230,00 | 2261,40(Польща) | 824278,60 |
| Цисплатин, амп., фл. шпр. 100 мг | ЦИСПЛАТИН-ТЕВА | Фармахемі Б.В., Нідерланди | ТОВ «Фра-М» | 51Т/126/21–24 від 17.07.2012 | 16833 | 218,00 | 174,72(Польща) | 728532,24 |
| Цетусимаб, амп., фл. шпр. 100 мг | Ербітукс® | Merck KGaA, Німеччина | ПрАТ «Альба-Україна» | 54Т/129/21–24 від 17.07.2012 | 2188 | 3671,00 | 1808,59(Угорщина) | 4074953,10 |
| Мітоміцин, амп., фл. шпр. 10 мг | МІТОМІЦИН-С КІОВА | КіоваХакко Кірін Ко. Лтд, Японія; СВУС Фарма а.с., Чеська Республіка Нордік Фарма с.р.о., Чеська Республіка | ТОВ «Фармадіс» | 58Т/137/21–24 від 19.07.2012 | 780 | 395,00 | 162,04 (Польща) | 181708,80 |
| Мітоміцин, амп., фл. шпр. 20 мг | МІТОМІЦИН-С КІОВА | КіоваХакко Кірін Ко. Лтд, Японія; СВУС Фарма а.с., Чеська Республіка Нордік Фарма с.р.о., Чеська Республіка | ТОВ «Фармадіс» | 58Т/137/21–24 від 19.07.2012 | 2080 | 693,00 | 313,10 (Польща) | 790192,00 |
| Паклітаксел, амп., фл. шпр. 30 мг | НЕОТАКСЕЛ | Напрод Лайф Саінсис Пвт. Лтд., Індія; Вінус Ремедіс Лімітед, Індія | ПрАТ «Альба-Україна» | 59Т/133/21–24 від 19.07.2012 | 965 | 529,00 | 232,35 (Молдова) | 286267,25 |
| Пегфілграстим, шприц-ручка 6 мг/0,6 мл | НЕУЛАСТИМ | Ф. Хоффманн-Ля Рош Лтд, Швейцарія; вторинне пакування: Ф.Хоффманн-Ля Рош Лтд. Швейцарія | ТОВ «Фармадіс» | 79Т/249/21–24 від 07.09.2012 | 101 | 11428,00 | 8508,29 (Польща) | 294890,71 |
| Імуноглобулін проти тимоцитів кролячий, амп., фл. шпр. 25 мг | ТИМОГЛОБУЛІН | Genzyme Polyclonals S.A.S., Франція; Genzyme Ireland Ltd, Ірландія; Genzyme Ltd, Велика Британія | ТОВ «Людмила-Фарм» | 91Т/304/21–24 від 31.10.2012 | 310 | 2050,00 | 1772,23 (Чехія) | 86108,70 |
| Пегфілграстим, шприц-ручка 6 мг/0,6 мл | НЕУЛАСТИМ | Ф. Хоффманн-Ля Рош Лтд, Швейцарія; вторинне пакування: Ф.Хоффманн-Ля Рош Лтд. Швейцарія | ТОВ «Фармадіс» | 93Т/306/21–24 від 31.10.2012 | 220 | 11428,00 | 8508,29 (Польща) | 642336,20 |
| Пегфілграстим, шприц-ручка 6 мг/0,6 мл | НЕУЛАСТИМ | Ф. Хоффманн-Ля Рош Лтд, Швейцарія; вторинне пакування: Ф.Хоффманн-Ля Рош Лтд. Швейцарія | ТОВ «Фармадіс» | 93Т/306/21–24 від 31.10.2012 | 194 | 11313,72 | 8508,29 (Польща) | 544253,42 |
| Філграстим, амп., фл. шпр. 30 млн. МО | ТеваГрастим | Тева Фарма Б.В., Нідерланди; Тева Фармацевтікал Індастріз Лтд., Ізраїль | ТОВ «Компанія Укроптпостач» | 104Т/353/21–24 від 05.12.2012 | 1240 | 420,00 | 336,54 (Польща) | 103490,40 |
| Вориконазол, амп., фл., шпр. 200 мг | ВІФЕНД | ДСМ Фармасютикалс Інк, США; Пфайзер Айленд Фармасьютікалз Лімітед, Ірландія; Пфайзер Пі.Джі.Ем., Франція | ТОВ «Людмила-Фарм» | 107Т/348/21–24 від 05.12.2012 | 447 | 1153,20 | 968,51(Болгарія) | 82556,43 |
| Ботулінічний токсин типу А, порошок для приготування розчину для ін’єкцій, 500 ОД у флаконах № 1 | ДИСПОРТ® | Ipsen Biopharm Limited, Великобританія | ТОВ «Людмила-Фарм» | 1/12/63/21–24 від 14.06.2012 | 629 | 3250,00 | 2693,12(Чехія) | 350277,52 |
| Ботулінічний токсин типу А, порошок для розчину для ін’єкцій, 100 одиниць Аллерган у флаконі | BOTOX® | Аллерган Фармасьютікалз Ірландія, Ірландія | «Оптіма-Фарм, ЛТД» ТОВ | 2/12/62/21–24 від 14.06.2012 | 162 | 1755,00 | 1545,05(Словацька Республіка) | 34011,90 |
| Альтеплазе, амп., фл., шпр. 50 мг | АКТИЛІЗЕ® | Берінгер Інгельхайм Фарма ГмбХ і Ко КГ, Німеччина | ТОВ «Людмила-Фарм» | 6/12/77/21–24 від 05.07.2012 | 2684 | 5000,00 | 3561,75(Болгарія) | 3860263,00 |
| Еноксапарин, амп., фл., шпр. 30000 МО | КЛЕКСАН® 300 | Санофі-Авентіс С.А., Іспанія | ТОВ «Людмила-Фарм» | 6/12/77/21–24 від 05.07.2012 | 36483 | 220,00 | 189,94 (Польща) | 1096679,00 |
| Левосимендан, амп., фл., шпр. 2,5 мг/мл | СИМДАКС | Оріон Корпорейшн, Фінляндія | ТОВ «Людмила-Фарм» | 6/12/77/21–24 від 05.07.2012 | 346 | 7000,00 | 5781,29 (Болгарія) | 421673,66 |
| Кортикостероїди (Метилпреднізолону натрію сукцинат), амп., фл., шпр. 1000 | СОЛУ-МЕДРОЛ | Пфайзер Менюфекчуринг Бельгія Н.В., Бельгія; Фармація Н.В./С.А., Бельгія | ТОВ «Людмила-Фарм» | 11/12/96/21–24 від 10.07.2012 | 4939 | 207,00 | 76,33(Угорщина) | 645379,13 |
| Базиліксимаб, амп., фл., шпр. 10 мг | СІМУЛЕКТ® | Новартіс Фарма Штейн АГ, Швейцарія | ТОВ «Фармадіс» | 17/12/119/21–24 від 16.07.2012 | 98 | 16785,00 | 9663,58 (Чехія) | 697899,16 |
| Іміглюцераза фл., 400 ОД | ЦЕРЕЗИМ® 400 ОД | Джензайм Лтд, Велика Британія; Джензайм Корпорейшн, США; Джензайм Ірланд Лтд, Ірландія | ТОВ «Людмила-Фарм» | 21/12/149/21–24 від 08.08.2012 | 319 | 16610,00 | 13940,15 (Болгарія) | 851682,15 |
| Пегінтерферон альфа-2b, амп., фл., шпр. 50мкг/0,5мл | ПЕГІНТРОН® | Шерінг-Плау (Брінні) Компані, Ірландія, власна філії Шерінг-Плау Корпорейшн, США; Мерк Шарп і Доум Інтернешнл ГмбХ, Сінгапур | ТОВ «Людмила-Фарм» | 61/12/269/21–24 від 24.09.2012 | 744 | 2117,03 | 1522,83 (Молдова) | 442084,80 |
| Пегінтерферон альфа-2b, амп., фл., шпр. 80мкг/0,5мл | ПЕГІНТРОН® | Шерінг-Плау (Брінні) Компані, Ірландія, власна філії Шерінг-Плау Корпорейшн, США; Мерк Шарп і Доум Інтернешнл ГмбХ, Сінгапур | ТОВ «Людмила-Фарм» | 61/12/269/21–24 від 24.09.2012 | 1006 | 2358,00 | 1230,05 (Польща) | 1134717,70 |
| Пегінтерферон альфа-2b, амп., фл., шпр. 100мкг/0,5мл | ПЕГІНТРОН® | Шерінг-Плау (Брінні) Компані, Ірландія, власна філії Шерінг-Плау Корпорейшн, США; Мерк Шарп і Доум Інтернешнл ГмбХ, Сінгапур | ТОВ «Людмила-Фарм» | 61/12/269/21–24 від 24.09.2012 | 662 | 2425,58 | 1645,03(Чехія) | 516724,10 |
| Пегінтерферон альфа-2b, амп., фл., шпр. 120мкг/0,5мл | ПЕГІНТРОН® | Шерінг-Плау (Брінні) Компані, Ірландія, власна філії Шерінг-Плау Корпорейшн, США; Мерк Шарп і Доум Інтернешнл ГмбХ, Сінгапур | ТОВ «Людмила-Фарм» | 61/12/269/21–24 від 24.09.2012 | 193 | 2437,00 | 1845,07(Польща) | 114242,49 |
| Пегінтерферон альфа-2b, амп., фл., шпр. 50мкг/0,5мл | ПЕГІНТРОН® | Шерінг-Плау (Брінні) Компані, Ірландія, власна філії Шерінг-Плау Корпорейшн, США; Мерк Шарп і Доум Інтернешнл ГмбХ, Сінгапур | ТОВ «Людмила-Фарм» | 61/12/269/21–24 від 24.09.2012 | 83 | 2117,03 | 1522,83 (Молдова) | 49318,60 |
| Пегінтерферон альфа-2b, амп., фл., шпр. 80мкг/0,5мл | ПЕГІНТРОН® | Шерінг-Плау (Брінні) Компані, Ірландія, власна філії Шерінг-Плау Корпорейшн, США; Мерк Шарп і Доум Інтернешнл ГмбХ, Сінгапур | ТОВ «Людмила-Фарм» | 61/12/269/21–24 від 24.09.2012 | 71 | 2358,00 | 1230,05 (Польща) | 80084,45 |
| Вакцина для профілактики поліомієліту інактивована | ІМОВАКС ПОЛІО суспензія для ін’єкцій по 0,5 мл (1 доза) у попередньо заповнених шприцах з прикріпленою голкою (або 2-ма окремими голками) № 1 | ТОВ «Фармекс Груп», Україна (фасування з форми «in bulk» фірми-виробника Санофі Пастер С.А., Франція) | ТОВ «Фармекс Груп» | 303/21–24 від 31.10.2012 | 207300 | 65,00 | 31,70(Словацька Республіка) | 6903090,00 |
| Всього: 140 527 787,9 | Можлива економія 47564252,4 | |||||||
Вищевказана інформація підтверджує, що Міністерство охорони здоров’я України здійснювало закупівлю препаратів за цінами, які суттєво перевищують ціни на аналогічні товари в Російській Федерації, Польщі, Болгарії, Чехії, Словацькій Республіці, Угорщині, Молдові. При цьому, якщо б закупівля здійснювалась за мінімальними цінами, приблизна економія бюджетних коштів становила близько 47,5 млн. гривень.
Неефективне використання Міністерством охорони здоров’я України коштів Державного бюджету України при здійсненні державних закупівель підтверджується також результатами закупівель антиретровірусних препаратів за напрямком «Загальнодержавна програма забезпечення профілактики ВІЛ-інфекції, лікування, догляду та підтримки ВІЛ-інфікованих і хворих на СНІД». Зокрема, протягом 2012–2013 років вказані препарати закуповувались за цінами, що на 150–300% перевищують ціни, за якими ці ж самі препарати купували пацієнтські організації, зокрема, ВБО «Всеукраїнська мережа ЛЖВ».
| Основні закупівлі антиретровірусних препаратів у 2012 році | ||||||
|---|---|---|---|---|---|---|
| Препарат | Джерело інформації(дата і номер бюлетеня) | Кількість препарату, закупленого МОЗ України(одиниць) | Ціна за одиницю МОЗ України(грн.) | Ціна за одиницю ЛЖВ (грн.) | Різниця цін за одиницю між МОЗ та ЛЖВ(грн.) | Загальна сума різниці цін(грн.) |
| Зидовудин/Ламівудин, табл., капс., драже, 300 мг/150 мг | Бюлетень№97/2 (699/2) від 13.08.2012, оголошення № 271572 | 17453025 | 1,56 | 1,168 | 0,392 | 6841585,80 |
| Тенофовір+Емтрицитабін, табл., капс., драже, 300 мг/200 мг | Бюлетень№97/2 (699/2) від 13.08.2012, оголошення № 271579 | 1680732 | 7,79 | 3,62 | 4,17 | 7008652,44 |
| Ламівудин, табл., капс., драже, 150 мг | Бюлетень№97/2 (699/2) від 13.08.2012 оголошення № 271572 | 7403547 | 0,56 | 0,31 | 0,25 | 1850886,75 |
| Ефавіренз, табл., капс., драже, 600 мг | Бюлетень№97/2 (699/2) від 13.08.2012 | 7083858 | 3,96 | 1,24 | 2,72 | 19268093,8 |
| Лопінавір/Ритонавір, табл., капс., драже, 200 мг/50 мг | Бюлетень№97/2 (699/2) від 13.08.2012 оголошення № 271572 | 23650764 | 4,11 | 4,05 | 0,06 | 1419045,84 |
| Невірапін, табл., капс., драже, 200 мг | Бюлетень№97/2 (699/2) від 13.08.2012, оголошення № 271579 | 2401600 | 0,84 | 0,55 | 0,29 | 696464,00 |
| Ефавіренз, табл., капс., драже, 200 мг | Бюлетень№97/2 (699/2) від 13.08.2012, оголошення № 271579 | 476629 | 1,25 | 0,636 | 0,614 | 292650,206 |
| Зидовудин/Ламівудин, табл., капс., др. 300 мг/150 мг | Бюлетень№ 136 (738) від 13.12.2012, оголошення №340646 | 440490 | 1,56 | 1,168 | 0,392 | 172672,08 |
| Тенофовір+Емтрицитабін, табл., капс., драже, 300 мг/200 мг | Бюлетень№ 136 (738) від 13.12.2012, оголошення №340646 | 185220 | 7,65 | 3,62 | 4,03 | 746436,60 |
| Ламівудин, табл., капс., драже, 150 мг | Бюлетень№ 136 (738) від 13.12.2012, оголошення №340646 | 437660 | 0,57 | 0,31 | 0,26 | 113791,60 |
| Ефавіренз, табл., капс., драже, 600 мг | Бюлетень№ 136 (738) від 13.12.2012, оголошення №340646 | 223940 | 3,94 | 0,636 | 3,304 | 739897,76 |
| Загальна сума різниці цін по всіх препаратах: | 39150177,00 | |||||
Таким чином, протягом 2012 року Міністерством охорони здоров’я України закуплено антиретровірусних препаратів на загальну суму 233104367,88 гривень, з яких щонайменше 39 мільйонів гривень переплачено, що становить приблизно 16,7%.
| Основні закупівлі антиретровірусних препаратів у 2013 році | ||||||
|---|---|---|---|---|---|---|
| Препарат | Джерело інформації(дата і номер бюлетеня) | Кількість препарату, закупленого МОЗ України(одиниць) | Ціна за одиницю МОЗ України (грн.) | Ціна за одиницю ЛЖВ(грн.) | Різниця цін за одиницю між МОЗ та ЛЖВ(грн.) | Загальна сума різниці цін(грн.) |
| Зидовудин/Ламівудин, табл., капс., драже, 300 мг/150 мг | Бюлетень №36 (779) від 06.05.2013, оголошення № 121880 | 16458432 | 1,24 | 1,1 | 0,14 | 2304180,50 |
| Тенофовір+Емтрицитабін, табл., капс., драже, 300 мг/200 мг | Бюлетень №35 (778) від 02.05.2013, оголошення № 121763 | 1504400 | 5,4 | 3,83 | 1,57 | 2361908,00 |
| Ламівудин, табл., капс., драже, 150 мг | Бюлетень №36 (779) від 06.05.2013, оголошення № 121880 | 9160720 | 0,44 | 0,31 | 0,13 | 1190893,60 |
| Ефавіренз, табл., капс., драже, 600 мг | Бюлетень №35 (778) від 02.05.2013, оголошення № 121763 | 6780530 | 2,05 | 1,11 | 0,94 | 6373698,20 |
| Тенофовір, табл., капс., драже, 300 м | Бюлетень №35 (778) від 02.05.2013, оголошення № 121763 | 2874900 | 3,72 | 2,4 | 1,32 | 3794868 |
| Невірапін, табл., капс., драже, 200 мг | Бюлетень №35 (778) від 02.05.2013, оголошення № 121763 | 1819020 | 0,71 | 0,49 | 0,22 | 400184,40 |
| Загальна сума різниці цін по всіх препаратах: | 16425733,00 | |||||
Отже, лише у першому півріччі 2013 року закупівля Міністерством охорони здоров’я України антиретровірусних препаратів за завищеними цінами призвела до розтрати коштів Державного бюджету України на суму більше 16,4 млн. гривень.
При здійсненні закупівель лікарських засобів і виробів медичного призначення Міністерство охорони здоров’я України систематично не дотримувалось приписів постанови Кабінету Міністрів України від 13.08.2012 року № 794 «Питання декларування зміни оптово-відпускних цін на лікарські засоби і вироби медичного призначення, які закуповуються за рахунок коштів державного та місцевих бюджетів», відповідно до яких заклади і установи охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів, закуповують лікарські засоби і вироби медичного призначення за цінами, які не перевищують рівень задекларованих оптово-відпускних цін з урахуванням мита, податку на додану вартість та граничних постачальницько-збутових та торговельних (роздрібних) надбавок.
Зокрема, у минулому році Міністерство охорони здоров’я України закуповувало лікарські засоби за цінами, що перевищують зареєстровані оптово-відпускні ціни з урахуванням граничних постачальницько-збутових надбавок. Наприклад, за договором від 06.07.2012 року № 17Т/80/21–24 у переможця торгів — ТОВ «Фра-М» (протокол комітету з конкурсних торгів від 06.06.2012 року № 24) придбано препарат ДОЦЕТАКТИН (фл., 20 мг, виробництва Сіндан Фарма СРЛ, Румунія) у кількості 2004 од. за ціною 1350 гривень на суму 2705,0 тис. гривень. При цьому зареєстрована оптово-відпускна ціна з урахуванням 10% граничної постачальницько-збутової надбавки складала 1276,4 гривень, або на 73,6 гривень менше. Загалом, лише при закупівлі 3 препаратів для лікування онкологічних та онкогематологічних хворих (ДОЦЕТАКТИН, ЛЕЙКОФОЗИН, ЕЛІГАРД 22,5 мг) Міністерством охорони здоров’я України неефективно використано кошти загального фонду у сумі 335,9 тис. гривень.
Окрім того, закуповувались лікарські засоби і вироби медичного призначення, оптово-відпускні ціни на які взагалі не були задекларовані/зареєстровані. Наприклад, подібним чином придбано: лікарський засіб ДАУНОЛ (Даунорубіцин, амп., фл., шпр. 20 мг) виробництва компанії ВІНУС РЕМЕДІС ЛІМІТЕД (Індія) на суму 306894,80 гривень; лікарський засіб ГРАНОЦИТ®34 (Ленограстим, амп., фл., шпр. 33,6 млн. МО) виробництва Санофі Вінтроп Індасріа (Франція) на суму 2616973,50 гривень; вакцину для профілактики кору, паротиту та краснухи ТРИМОВАКС виробництва Sanofi Pasteur S.A. (Франція) на суму 20632431,20 гривень. Окрім того, здійснювалась закупівля тих лікарських засобів, оптово-відпускні ціни на які не були задекларовані/зареєстровані на момент укладення відповідного договору про закупівлю. Наприклад, 13.06.2012 року Міністерство охорони здоров’я України уклало договір № 27Т/59/21–24 з ТОВ «Людмила-Фарм» про поставку лікарського засобу ЗОПЕРЦИН® (Піперицилін/Тазобактам, амп., фл., шпр. 4500 мг; виробництва ОРХІД ХЕЛТХЕР, Індія). Водночас, оптово-відпускна ціна на вказаний лікарський засів була зареєстрована Міністерством охорони здоров’я України лише 08.08.2012 (наказ № 626).
Подібну ситуацію підтверджує Рахункова палата у своєму звіті про результати аудиту використання коштів державного бюджету, виділених Міністерству охорони здоров’я України, та гуманітарної допомоги громадських організацій на виконання заходів з профілактики та лікування захворювань на туберкульоз (звіт затверджено постановою Колегії Рахункової палати від 23.01.2013 року № 1–5). Зокрема, наголошується, що у 2012 році із 32 найменувань протитуберкульозних препаратів, закуплених Міністерством охорони здоров’я України, оптово-відпускні ціни на 9 препаратів не були задекларовані/зареєстровані. Окрім того, Рахункова палата у своєму звіті про результати аудиту використання коштів державного бюджету, виділених на виконання заходів з лікування онкологічних захворювань у дорослих (звіт затверджено постановою Колегії Рахункової палати від 13.08.2013 року № 14–1) зазначає про те, що з 82 препаратів для лікування онкологічних та онкогематологічних хворих, включених до номенклатури та закуплених Міністерством охорони здоров’я України, оптово-відпускні ціни 13 препаратів на дату проведення торгів та укладення договорів не були задекларовані/зареєстровані представниками власників реєстраційних посвідчень.
У результаті, система декларування/реєстрації оптово-відпускних цін на лікарські засоби та вироби медичного призначення, запроваджена Кабінетом Міністрів України з метою ефективного використання коштів державного та місцевих бюджетів, фактично не забезпечує отримання достовірних даних та досягнення зазначеної мети.
Окремо слід відзначити, що у минулому році Міністерство охорони здоров’я України неодноразово закуповувало імунобіологічні препарати та лікарські засоби, належна якість яких не була підтверджена. Наприклад, у ТОВ «Центрофарм» було закуплено лікарський засіб ПАС (кислота парааміносаліцилова, порошок, гран. кишково-розчинні, 1000 мг) на суму 23187882,0 гривень (договір № 73Т/215/21–24 від 23.08.2012 року) та 10475450,0 гривень (договір № 113Т/376/21–24 від 18.12.2012 року). Виробником вказаного лікарського засобу є компанія Вівімед Лабс Лтд (адреса провадження діяльності — Д-125–128, Фаза-ІІІ, ІДА, Джедіметла, Хайдерабад, Андра Прадеш-500055, Індія). Водночас Держлікслужба України двічі відмовляла цьому виробнику у видачі сертифікату відповідності вимогам належної виробничої практики в зв’язку з наявністю критичних і суттєвих порушень вимог належної виробничої практики (накази про відмову у видачі сертифікату відповідності вимогам належної виробничої практики від 06.07.2012 року № 545 та від 01.07.2013 року № 846).
Аналогічним чином, у зв’язку з наявністю критичних і суттєвих порушень вимог належної виробничої практики, Держлікслужба України двічі відмовляла компанії РУП «Бєлмедпрепарати» (адреса провадження діяльності — 220006, Республіка Білорусь, м. Мінськ, вул. Маяковського, 1) у видачі сертифікату відповідності вимогам належної виробничої практики (накази про відмову у видачі сертифікату відповідності вимогам належної виробничої практики від 25.09.2012 року № 814 та від 22.04.2013 року № 590). Між тим, у минулому році Міністерство охорони здоров’я України закупило у ПрАТ «Альба-Україна» лікарський засіб РИФАМПІЦИН (Рифімпіцин, табл., капс., драже 150 мг) виробництва РУП «Бєлмедпрепарати» у кількості 9466130 одиниць на загальну суму 2461196,4 гривень (договір №95Т/321/21–24 від 13.11.2012 року).
Окрім того, незважаючи на своєчасне отримання інформації та копій розпоряджень Держлікслужби України з лікарських засобів від 21.12.2012 року про заборону реалізації (торгівлі), зберігання та застосування вакцин виробництва ПАТ «Фармстандарт-Біолік» № 27914–1.3/2.0/17–12, 27915–1.3/2.1/17–12, 27918–1.3/2.1/17–12, 27919–1.3/2.0/17–12, 27922–1.3/2.1/17–13 та 27924–1.3/2.1/17–12, Міністерство охорони здоров’я України 20.12.2012 року проведено попередню оплату за імунобіологічні препарати виробництва ПАТ «Фармстандарт-Біолік» на загальну суму 6,48 млн. гривень.
Аналізуючи державні закупівлі, замовником яких у 2012 році виступало Міністерство охорони здоров’я України, слід звернути увагу на низку інших порушень Закону України «Про здійснення державних закупівель», які призвели до дискримінації окремих учасників конкурсних торгів та не забезпечили об’єктивної, неупередженої оцінки пропозицій конкурсних торгів.
Зокрема, 03.12.2012 року за результатами процедури закупівлі в одного учасника було укладено договір з дочірнім підприємством «БіоЛайн Україна» щодо закупівлі реагентів та витратних матеріалів для визначення кількості СД4+ лімфоцитів у ВІЛ-інфікованих пацієнтів (реагенти та витратні матеріали до проточного цитофлюориметру «Becton Dickinson» — 1734 од., 9 найменувань) на загальну суму 5,59 млн. гривень. Між тим, у подальшому Міністерством економічного розвитку і торгівлі України було проведено моніторинг зазначеної закупівлі на предмет наявності підстав для застосування замовником процедури закупівлі в одного учасника. За результатами здійснення моніторингу Міністерство економічного розвитку і торгівлі України надало свій висновок (лист від 14.03.2013 року № 3303–05/8899–06), відповідно до якого вищевказана процедура закупівлі в одного учасника застосована Міністерством охорони здоров’я України без наявності умови застосування, передбаченої пунктом 4 частини другої статті 39 Закону України «Про здійснення державних закупівель».
Окрім того службовими особами Комітету з конкурсних торгів Міністерства охорони здоров’я України (Голова Комітету — заступник Міністра — керівник апарату Богачев Р.М., начальник Управління моніторингу державних цільових програм та державних закупівель Довганчин Г.С.) усупереч статей 29 та 30 Закону України «Про здійснення державних закупівель» визнано переможцем процедур закупівель та укладено з ПАТ «Фармстандарт-Біолік» (м. Харків) договори від 04.05.2012, 29.08.2012 та 04.10.2012 про закупівлю вакцин на суму 17,9 млн. гривень.
Так, в усіх процедурах державних закупівель імунобіологічних препаратів учасниками торгів не подано довідок, виданих компетентним державним органом України, щодо відсутності рішення про визнання банкрутом та відкриття відносно них ліквідаційної процедури. Крім того, за висновками Антимонопольного комітету України, документальне підтвердження відповідності пропозицій конкурсних торгів технічним, якісним та іншим вимогам до предмету закупівлі учасниками не подано (процедури державних закупівель згідно з бюлетенем «Вісник державних закупівель» №37/1 (639/1) від 26.03.2012, оголошення № 148309, лоти № 7–10; бюлетень №88/3 (690/3) від 23.07.2012, оголошення № 258051, лот №3; оголошення № 258061, лоти №4 та 6; бюлетень № 106/2 (708/2) від 03.09.2012, оголошення № 283645, лот № 1).
За таких обставин Комітет з конкурсних торгів Міністерства охорони здоров’я України повинен був відхилити пропозиції усіх учасників указаних конкурсних торгів та відмінити їх проведення.
Особливої уваги потребує ситуація, яка склалася навколо ПрАТ «По виробництву інсулінів «Індар». Левову частку бюджетних коштів, виділених на закупівлі лікарських засобів Міністерством охорони здоров’я України, отримав саме ПрАТ «По виробництву інсулінів «Індар», 71% акцій якого належить державі. Зокрема, лише протягом першої половини 2013 року це підприємство стало переможцем державних закупівель лікарських засобів, які здійснювалися Міністерством охорони здоров’я України на загальну суму 279 млн. гривень. Виходячи з інформації, розміщеної у Державному реєстрі лікарських засобів, ПрАТ «По виробництву інсулінів «Індар» не є виробником жодного з препаратів, закупленого Міністерством охорони здоров’я України. Одночасно, згідно інформації, наведеної у журналістських розслідуваннях, даний завод відомий тим, що у 2012 році продав Міністерству охорони здоров’я України вироби медичного призначення (тест-смужки для глюкометрів, які теж ним не виготовляються) на загальну суму 15 млн. гривень, а отримані бюджетні кошти були переведені на рахунки британської компанії «Altona Trade Agency LLP». Варто відмітити, що «Altona Trade Agency LLP» зареєстровано у Лондоні за адресою, де одночасно зареєстровано ще 78000 компаній, а у червні цього року вона оголосила про свою ліквідацію.
Голова Правління ПрАТ «По виробництву інсулінів «Індар» Вишневська Л.В. з невідомих причин у відповідь на депутатські звернення відмовилася надавати інформацію про походження лікарських засобів, які заводом поставлені до Міністерства охорони здоров’я України. За даним фактом Головним управлінням МВС України в м. Києві внесено відомості до Єдиного реєстру досудових розслідувань за № 12013110020009797 за ч. 1 ст. 351 Кримінального кодексу України (Перешкоджання у діяльності народного депутата України).
Разом з тим, факти щодо перерахунку посадовими особами заводу коштів, отриманих від Міністерства охорони здоров’я України, на рахунки компанії з ознаками фіктивності «Altona Trade Agency LLP», потребують окремого розслідування, як і потребують детальної перевірки обставини використання заводом 279 млн. грн., отриманих від Міністерства охорони здоров’я України у 2013 році.
Вказані порушення в діяльності Міністерства охорони здоров’я України стали можливими через ігнорування вимог законодавства його службовими особами, відсутність контролю за діяльністю підлеглих з боку керівників міністерства та неналежної взаємодії структурних підрозділів.
Слід відзначити, що системні факти порушення вимог законодавства з боку Міністерства охорони здоров’я України під час здійснення державних закупівель, що призвели до розтрати бюджетних коштів, встановлені також правоохоронними органами України.
Наприклад, 24.04.2012 та 28.04.2012 Головним слідчим управлінням СБ України порушені кримінальні справи за фактами вчинення невстановленими службовими особами Міністерства охорони здоров’я України розтрати бюджетних коштів, шляхом зловживання своїм службовим становищем, в особливо великих розмірах на загальну суму понад 1,1 та 19,7 млн. гривень при проведенні процедур закупівель за державні кошти лікарських засобів ІМУФЕТ, ПРОГРАФ, АЛУВІА.
12.12.2012 року слідчим управлінням ГУ МВС України у м. Києві внесено відомості до Єдиного реєстру досудових розслідувань та розпочато досудове розслідування в кримінальному провадженні № 12012110000000606 з попередньою правовою кваліфікацією кримінального правопорушення за частиною 5 статті 191 (Привласнення, розтрата майна або заволодіння ним шляхом зловживання службовим становищем) Кримінального кодексу України за фактом розтрати коштів державного бюджету службовими особами Міністерства охорони здоров’я України та ДУО «Політехмед» під час здійснення закупівель автомобілів швидкої медичної допомоги на виконання бюджетної програми КПКВ 2301380 «Розвиток служби екстреної медичної допомоги (придбання медичного автотранспорту) у Вінницькій, Дніпропетровській, Донецькій областях та м. Києві», що спричинило завдання шкоди на загальну суму 56,6 млн. гривень.
Окрім того, 18.04.2013 року слідчим відділом Печерського районного управління ГУМВС України в місті Києві внесено відомості до Єдиного реєстру досудових розслідувань та розпочато досудове розслідування в кримінальному провадженні № 12013110060003630 з попередньою правовою кваліфікацією кримінального правопорушення за частиною 1 статті 364 (Зловживання владою або службовим становищем) Кримінального кодексу України за фактом можливих зловживань службовими особами Міністерства охорони здоров’я України та інших установ медичної галузі під час використання коштів державного бюджету, виділених у 2011–2013 роках на закупівлю лікарських засобів.
Одночасно існує ймовірність, що до подібних випадків нераціонального, непрозорого та неефектного використання державних коштів під час здійснення державних закупівель лікарських засобів та виробів медичного призначення призвели корупційні правопорушення з боку посадових осіб Міністерства охорони здоров’я України. При цьому високий рівень корупції під час здійснення державних закупівель у сфері охорони здоров’я підтверджується висновками Служби безпеки України. Зокрема, наголошується, що протягом 2012–2013 років неодноразово виявлялись факти корупційних правопорушень під час проведення Міністерством охорони здоров’я України та іншими державними підприємствами, установами і організаціями державних закупівель. Порівняння Звітів про стан протидії корупції за 2011 та 2012 роки свідчить про збільшення кількості виявлених кримінальних та адміністративних корупційних правопорушень у сфері охорони здоров’я. Так, якщо у 2011 році всіма правоохоронними органами держави виявлено 47 кримінальних корупційних правопорушень, то у 2012 році — 142. Наявні в Служби безпеки України матеріали свідчать, що ситуація у цій сфері протягом 2013 року кардинальних змін не зазнала. Зокрема, не знижується загальний рівень корупційних ризиків та продовжують мати місце випадки неефективного витрачання бюджетних коштів під час закупівлі медичних товарів, у тому числі в рамках затверджених державних програм.
Загалом, неефективні та непрозорі закупівлі Міністерства охорони здоров’я України протягом 2012–2013 років призвели до розтрати коштів Державного бюджету України в особливо великих розмірах. Окрім того, це унеможливило закупівлю лікарських засобів та виробів медичного призначення в необхідній кількості та належної якості, що негативним чином відобразилось на якості надання медичної допомоги населенню України.
VI. СТАН ДОТРИМАННЯ ЗАКОНОДАВСТВА У СФЕРІ ОХОРОНИ ЗДОРОВ’Я В РЕГІОНАХ УКРАЇНИ
Протягом 2012–2013 років виявлені численні порушення вимог Конституції України, Основ законодавства України про охорону здоров’я, законів України «Про лікарські засоби», «Про наркотичні засоби, психотропні речовини і прекурсори», «Про основи соціальної захищеності інвалідів в України», «Про реабілітацію інвалідів», «Про охорону дитинства», «Про психіатричну допомогу», «Про здійснення державних закупівель», «Про оренду державного та комунального майна», «Про ліцензування певних видів господарської діяльності», «Про благодійництво та благодійні організації», «Про звернення громадян», інших нормативно-правових актів з боку посадових осіб структурних підрозділів з питань охорони здоров’я обласних (міських) державних адміністрацій, закладів охорони здоров’я, інших підприємств, установ та організацій.
По-перше, закладами охорони здоров’я не завжди дотримується принцип безоплатної медичної допомоги, визначений статтею 49 Конституції України.
Зокрема, в лікувальних закладах створюються різноманітні місії, фундації, організації, які відповідно до установчих документів засновані для поліпшення якості надання медичної допомоги. При цьому в порушення вимог статті 1 Закону України «Про благодійництво та благодійні організації» грошові кошти, які вносяться в каси благодійних організацій, в багатьох випадках фактично не є добровільними безкорисливими пожертвами фізичних та юридичних осіб, а сплачуються під прямим чи завуальованим впливом медичних працівників.
Наприклад, у хірургічному відділенні та відділенні хіміотерапії Волинського обласного онкологічного диспансеру хворими при поступленні у лікарню на вимогу медичних працівників сплачувались «благодійні внески» у благодійну організацію «Муніципальна лікарняна каса». Із пояснень хворих вбачається, що сплату таких внесків вони розуміли як обов’язкову, а не добровільну. Крім того, медичний персонал самостійно визначав та повідомляв про суму коштів, яку слід сплатити, що суперечить вимогам статей 1–2 Закону України «Про благодійництво та благодійні організації». Аналогічно у відділенні неврології Волинської обласної дитячої клінічної лікарні медичним персоналом проводився збір коштів у якості «благодійних внесків» з батьків, чиї діти перебували на лікуванні в даному закладі. Такі внески сплачувались не на засадах добровільності, а у порядку примусової сплати фіксованої суми, яка визначалась медичним персоналом відділення. Медичними працівникам Волинської обласної клінічної лікарні, незважаючи на наявності пільг у осіб, на яких поширюється дія законів України «Про статус і соціальний захист громадян, які постраждали внаслідок Чорнобильської катастрофи» та «Про статус ветеранів війни, гарантії їх соціального захисту», проводився збір коштів з інвалідів війни, учасників війни та постраждалих внаслідок Чорнобильської катастрофи під час проходження останніми медичних обстежень та здачі аналізів. У Луцькій центральній лікарні (Волинська область) особи, які не проживають на території району, за оформлення в лікарню в обов’язковому порядку сплачували кошти у фіксованому розмірі як «благодійні внески»: за госпіталізацію в лікарню — 80 гривень, за пологи — 200 гривень, за проведення кесаревого розтину — 350 гривень.
У Запорізькій міській багатопрофільній лікарні №9 виявлено, що пацієнтами цієї лікарні сплачуються у обов’язковому порядку благодійні (добровільні) внески, які у подальшому оприбутковуються в касі лікарні та вносяться на її рахунок. Про факт обов’язковості внесення благодійних внесків свідчать статистичні дані щодо їх стягнення, а саме: з 682 пацієнтів, які перебували на лікування у травматологічному відділенні, благодійний внесок сплатило 80%, з яких понад 30% становлять соціально незахищена верства населення — пенсіонери, інваліди та учасники Великої Вітчизняної Війни. Аналогічно під виглядом благодійних внесків зобов’язують сплачувати оплату за надану медичну допомогу пацієнтів Міської клінічної лікарні № 3 (м. Запоріжжя). Так, пацієнтами при прийманні до хірургічного відділення № 1 пропонувалося сплатити під виглядом благодійного внеску кошти до запорізького міського благодійного фонду «Здорове покоління» за відповідне лікування або на придбання матеріалів для проведення операції та анестезії. При цьому сума, яку необхідно внести на благодійного фонду, заздалегідь визначена затвердженим головним лікарем «прейскурантом цін».
Наведені факти свідчать про те, що якість надання медичної допомоги системно залежить від сплати пацієнтами грошових коштів під виглядом благодійних внесків, які фактично є обов’язковим платежем у цих лікарнях.
Аналогічні випадки зафіксовані в лікувальних закладах інших регіонів країни. Так, Добровеличківською центральною районною лікарнею (Кіровоградська область) отримувались кошти у вигляді благодійних внесків у фіксованому розмірі від громадян, які перебували на стаціонарному та амбулаторному лікування, без зазначення цілей використання коштів.
Посадові особи КРУ «Онкологічний клінічний диспансер», зловживаючи службовим становищем шляхом надання відповідних незаконних розпоряджень підлеглим працівникам, створили умови, за яких громадян, які звертались до зазначеної установи, змушували здійснювати благодійні внески, що варіювались від 30 до 3000 гривень, до Кримського протиракового товариства «Антінео» під загрозою ненадання відповідної медичної допомоги. Вкрай показово, що засновниками даного товариства є керівники КРУ «Онкологічний клінічний диспансер».
У Менській центральній районній лікарні (Чернігівська область) з хворих стягувалась плата за надані медичні послуги, які вносилися нібито в якості «благодійних внесків». Також встановлено, що у Прилуцькій міській дитячій лікарні (Чернігівська область) з батьків стягувались кошти за видачу медичної картки дитини при влаштуванні до шкіл та дитячих садків.
Одночасно мають місце порушення порядку надання платних послуг, які можуть надаватись в державних та комунальних закладах охорони здоров’я. Наприклад, медичними працівниками Баштанської центральної районної лікарні (Миколаївська область) з випускників шкіл району стягувались кошти за проведення медичного огляду при вступі до вищих навчальних закладів у сумі 69,62 гривень. Відповідно до наказу головного лікаря Білогірської центральної районної лікарні (Хмельницька область) починаючи з січня 2013 року стягувалась плата за бактеріологічні обстеження при проходженні періодичних медичних оглядів при прийнятті на роботу. Старосинявською центральною районною лікарнею (Хмельницька область) надавались платні послуги для отримання посвідчення водія за направленням органів державної служби зайнятості, вимагалась оплата вартості сертифікатів наркологічного та психіатричного оглядів. Працівниками Дніпропетровського обласного комунального закладу «Бюро судово-медичної експертизи» у період з 20.11.2012 по 12.02.2013 років було стягнуто плату на загальну суму 99,8 тис. гривень за надання платних послуг у вигляді утримання тіл померлих, транспортних послуг з доставки померлих. Водночас вказані послуги відсутні в Переліку платних послуг, що можуть надаватися в державних та комунальних закладах охорони здоров’я, вищих медичних навчальних закладах та науково-дослідних установах, медичними працівниками, що затверджений постановою Кабінету Міністрів України № 1138 від 17.09.1996 року.
Випадки безпідставного віднесення закладами охорони здоров’я медичних послуг до переліку платних виявлено також в діяльності КЗ КОР «Обласне психіатрично-наркологічне медичне об’єднання» (Київська область). Так, незважаючи на вимоги частини 2 статті 240 Цивільного процесуального кодексу України, відповідно до яких судові витрати, пов’язані з провадженням справи про визнання фізичної особи недієздатною або обмеження цивільної дієздатності фізичної особи, відносяться на рахунок держави, вказаною установою судові-психіатричні експертизи проводились за рахунок фізичних осіб. Так, упродовж 2012 року експертами закладу було проведено 225 судово-психіатричних експертиз, з яких лише 16 — за рахунок державних коштів, а 209 експертиз на загальну суму 44691,41 гривень — за рахунок фізичних осіб.
Також встановлено, що працівники швидкої медичної допомоги КЗ «Молочанська районна лікарня» (Запорізька область) упродовж грудня 2012 — січня 2013 років незаконно вимагали у громадян оплату за виїзд автомобіля невідкладної медичної допомоги. Аналогічні випадки встановлено в діяльності КУ «Міська багатопрофільна клінічна лікарня №9», КУ «Запорізька міська багатопрофільна дитяча лікарня №5», КЗ «Кам’янсько-Дніпровська центральна районна лікарня» (Запорізька область).
Загалом, у результаті вищевказаних дій порушено право громадян на безоплатну медичну допомогу, яке гарантовано Конституцію України.
По-друге, лікувально-профілактичні заклади допускають використання неякісних лікарських засобів, порушують умови зберігання лікарських засобів.
Так, всупереч вимог статті 21 Закону України «Про лікарські засоби», п. 1,5 Правил зберігання та проведення контролю якості лікарських засобів у лікувально-профілактичних закладах, затверджених наказом Міністерства охорони здоров’я України №584 від 16.12.2003 року, у неврологічному, ендокринологічному відділеннях, відділенні реанімації та інтенсивної терапії лікувальних закладів Волинської області використовувались лікарські засоби, термін дії яких минув, зокрема, МЕЗАТОН, ЕУФІЛІН.
Факти зберігання лікарських засобів, термін придатності яких минув, виявлені також у поліклінічному відділенні Галицької центральної районної лікарні (Івано-Франківська область), бактеріологічній лабораторій КУ «Львівській регіональний фтизіопульмонологічний клінічний лікувально-діагностичний центр (препарати ЕТАМБУТОЛ, КАНАМІЦИН, КАПРЕАМІЦИН, ПАСК, ПІРАЗИНАМІД та СТРЕПТОМІЦИН, термін придатності яких минув 01.01.2012 року), ревматологічному відділенні та відділенні лікувань учасників війни КЗ «Міська лікарня №3» (м. Севастополь).
Одночасно мали місце випадки відпуску хворим лікарських засобів, термін придатності яких минув, та які відповідно до вимог статті 23 Закону України «Про лікарські засоби» підлягали утилізації і знищенню. Наприклад, у Нетішинській спеціалізованій медико-санітарній частині №4 МОЗ України препарат інсулін НОВО-МІКС в кількості 5 картриджів терміном придатності до 01.06.2012 року видано пацієнту 01.06.2012 року, тобто з простроченою датою використання. Як вбачається з письмового пояснення вказаного пацієнта, виданий препарат інсуліну у кількості 2 од. ним було використано.
Всупереч Правил зберігання та проведення контролю якості лікарських засобів у лікувально-профілактичних закладах приміщення для зберігання лікарських засобів у Лановецькій центральній районній лікарні (Тернопільська область) не обладнано охоронними та протипожежними засобами. Недоліки при зберіганні лікарських засобів, термін придатності яких минув, встановлені також в інших лікувально-профілактичних закладах Тернопільської області, зокрема, Збаразькій, Зборівській, Чортківській центральних районних лікарнях, Тернопільському територіальному районному медичному об’єднанні.
Порушення правил зберігання лікарських засобів виявлені також у ряді лікувально-профілактичних закладів Черкаської області. Наприклад, приміщення для зберігання лікарських засобів ШМД Канівської центральної районної лікарні не забезпечені термометрами і гідрометрами для спостереження температури та вологості повітря, журнали або картки обліку температури та відносної вологості не ведуться. Спостереження за температурою зберігання лікарських засобів ОКСИТОЦИН, ВАЛІДОЛ, СУЛЬФАЦИЛ не проводилось. У Черкаському обласному кардіологічному центрі порушено умови зберігання лікарських засобів РЕНАЛГАН (300 упаковок), ДЕКСОМЕТАЗОН; у Черкаському обласному шкірно-венерологічному диспансері порушено умови зберігання препарату ХЛОРОФІЛІПТ; у хірургічному відділенні № 2 КЗ «Третя Черкаська міська лікарня» порушено умови зберігання препарату ФЕНІГІДИН.
У приміщеннях для зберігання лікарських засобів ЛПЗ «Обласний центр екстреної медичної допомоги та медицини катастроф» та КЛПЗ «Чернігівського обласного шкірно-венерологічного диспансеру» (Чернігівська область) зберігались лікарські засоби без дотримання температурного режиму.
Всупереч п. 1 наказу Міністерства охорони здоров’я України №59 від 16.09.2011 року «Про порядок проведення профілактичних щеплень в Україні та контроль якості й обігу медичних імунобіологічних препаратів» у хірургічному відділенні КЗ «Міська лікарня №4» (м. Севастополь) вакцина антирабічна зберігалась з порушенням температурних умов.
Слід також відзначити, що в багатьох лікувально-профілактичних закладах країни допускаються грубі порушення умов зберігання наркотичних засобів та прекурсорів, у тому числі ведення їх обліку.
Наприклад, у порушення статті 6 Закону України «Про наркотичні засоби, психотропні речовини та прекурсори» відповідальними особами Галицької центральної районної лікарні (Івано-Франківська область) журнал обліку наркотичних речовин заповнювався неналежним чином, поза обліком виявлено 70 одиниць наркотичних засобів, що може спричинити неконтрольоване використання даних засобів.
Посадовими особами Новгородківської центральної районної лікарні (Кіровоградська область) систематично порушувався строк здачі порожніх ампул, комісією по знищенню порожніх ампул від наркотичних та психотропних препаратів та по прийому використаних ампул наркотичних препаратів не додержувалась встановлена періодичність знищення ампул, у приміщеннях, де зберігались нарковмісні препарати, не проводився облік температури та відносної вологості повітря.
По-третє, допускаються порушення вимог законодавства при здійсненні державних закупівель.
Згідно частини другої статті 39 Закону України «Про здійснення державних закупівель» процедура закупівлі в одного учасника застосовується замовником як виняток. Винятковість процедури закупівлі в одного учасника на відміну від інших процедур закупівлі потребує максимального обґрунтування та об’єктивного документального підтвердження необхідності застосування цієї процедури як єдиноможливої в конкретному випадку за умов, визначених частиною другою статті 39 вищевказаного закону. При цьому рішення про застосування процедури закупівлі в одного учасника замовником має бути обґрунтованим та документально підтвердженим.
Водночас закладами охорони здоров’я допускались порушення при обранні неконкурентної процедури закупівлі в одного учасника. Наприклад, без належних правових підстав комітетом з конкурсних торгів Волинського обласного онкологічного диспансеру прийнято рішення здійснити закупівлю у 2013 році наркотичних засобів на 152 тис. гривень із застосування процедури в одного учасника. Подібним чином безпідставно застосовано у поточному році процедуру закупівлі в одного учасника сполук гетероциклічних та сульфамідів комітетом з конкурсних торгів Волинської обласної клінічної лікарні.
Аналогічним чином без належного обґрунтування Полтавською обласною клінічною лікарнею ім. М. В. Скліфосовського проведено закупівлі за державні кошти робіт з реконструкції приміщень будівлі діагностичного центру в перинатальний центр (оголошення N 319878 в інформаційному бюлетені «Вісник державних закупівель» від 26.11.2012 N 131 (733)), проведеної за процедурою закупівлі в одного учасника у приватної фірми «Лібор». Вказане підтверджується висновком Міністерства економічного розвитку і торгівлі України (лист від 21.01.2013 року № 3303–06/1870–12).
Закладами охорони здоров’я допускались порушення під час розроблення документації з конкурсних торгів, встановлення кваліфікаційних критеріїв для учасників та оцінки їх пропозицій. Так, Управлінням охорони здоров’я Сумської обласної державної адміністрації у жовтні-грудні 2012 року проведені конкурсні торги щодо закупівлі устаткування медичного, хірургічного та ортопедичного для КЗ СОЗ «Обласний клінічний пренатальний центр». Документацією конкурсних торгів замовником встановлені кваліфікаційні вимоги до учасників закупівлі, зокрема, передбачений перелік документів, які вимагаються від учасника для підтвердження його відповідності кваліфікаційним критеріям. Як вбачається з наявних документів, учасниками торгів (ТОВ «МЕД-ІНВЕКСТ» та ТОВ «ТОПСЕРВІС-МЕДТЕХНІКА») не було надано необхідних документів, які могли б підтвердити відповідність учасника кваліфікаційним критеріям. За таких обставин відповідно до статті 29 Закону України «Про здійснення державних закупівель» замовник повинен відхилити пропозицію конкурсних торгів. Незважаючи на викладене, у протоколі розкриття пропозицій конкурсних торгів від 01.12.2012 року зазначено про наявність всіх документів та фактично про відповідність пропозицій зазначених учасників вимогам Закону України «Про здійснення державних закупівель» та документації торгів. Відповідно до протоколу оцінки пропозицій конкурсних торгів від 10.12.2012 року №40 переможцем торгів визнано ТОВ «ТОПСЕРВІС-МЕДТЕХНІКА» із пропозицією закупівель на загальну суму 13,6 млн. гривень, і в цей же день комітетом з конкурсних торгів замовника акцептовано пропозицію даного учасника. Таким чином, члени комітету з конкурсних торгів Управління охорони здоров’я Сумської обласної державної адміністрації, діючи всупереч зазначених вимог закону, в інтересах суб’єкта господарювання ТОВ «ТОПСЕРВІС-МЕДТЕХНІКА» неправомірно сприяли одержанню ним перемоги у конкурсних торгах із закупівлі устаткування медичного, хірургічного та ортопедичного для КЗ СОЗ «Обласний клінічний пренатальний центр».
Також комітетом з конкурсних торгів Департаменту охорони здоров’я Хмельницької обласної державної адміністрації, в порушення вимог статей 5, 22 Закону України «Про здійснення державних закупівель», при затвердженні документації конкурсних торгів щодо закупівлі лікарських засобів (препаратів для корекції фосфатно-кальцієвого обміну та корекції анемічного синдрому) встановлено такі вимоги до предмета закупівлі, які призвели до обмеження конкуренції та дискримінації учасників закупівлі. Так, учасників зобов’язано було пропонувати для закупівлі зазначені препарати виключно у формі розчину для ін’єкцій у передчасно заповнених шприцах. Встановлення таких вимог до предмета закупівлі призвело до подання учасниками скарг на дії комітету з конкурсних торгів замовника до Антимонопольного комітету України, яким дії комітету визнані неправомірними. Як наслідок, медичні установи Хмельницької області у 2012 році залишились незабезпеченими необхідними медичними препаратами.
Слід відзначити, що відповідно до статті 4 Закону України «Про здійснення державних закупівель» закупівля здійснюється відповідно до річного плану. Річний план закупівель та зміни до нього оприлюднюються замовником шляхом розміщення на власному веб-сайті або за його відсутності на веб-сайті головного розпорядника бюджетних коштів протягом п’яти робочих днів з дня їх затвердження. Разом з тим, значна частина закладів охорони здоров’я, не маючи власного веб-сайту, не розміщували свої річні плани закупівель на веб-сайті головного розпорядника коштів.
Вищенаведені факти свідчать про порушення принципів здійснення закупівель щодо створення конкурентного середовища, об’єктивної та неупередженої оцінки пропозицій конкурсних торгів, які визначені у статті 3 Закону України «Про здійснення державних закупівель».
Одночасно мають місце випадки розтрати бюджетних коштів під час закупівлі лікарських засобів та виробів медичного призначення.
Наприклад, відсутність належного контролю з боку Управління охорони здоров’я Житомирської обласної державної адміністрації за рівнем цін закупівлі препаратів інсуліну призвело до закупівлі розпорядниками бюджетних коштів нижчого рівня лікарських засобів за ціною, що в окремих випадках перевищувала оптово-відпускну з врахуванням торговельно-збутової надбавки на 20 відсотків. При цьому закупівля лікарських засобів проводилась у суб’єктів господарювання, які в більшості випадків придбавали дані препарати не у виробників, а в посередників. Так, Житомирською медичною базою укладено договір з ТОВ «Компанія Валіс» (від 26.03.2012 року) щодо закупівлі 4 найменувань препаратів інсуліну (АКТРАПІД, ПРОТАФАН, МІКСТАРД НМ, МІКСТАРД 30 НМ) за цінами, що перевищують зареєстровані граничні оптово-відпускні ціни з урахуванням постачальницько-збутових надбавок на 0,5–5,6% (або від 0,25 грн. до 7,03 гри. за одиницю). При закупівлі за зареєстрованими гранично оптово-відпускними цінами можна було б додатково закупити ліків розрахунково на суму 102,2 тис. гривень. Одночасно слід відзначити, що Житомирською медичною базою у першому півріччі 2012 року здійснювалась закупівля препарату ХАМУЛІН Р за ціною 66,3 гривні за одиницю. Між тим, оптово-відпускна ціна на вказаний препарат зареєстрована Міністерством охорони здоров’я України лише 08.08.2012 року (наказ №626) та становила 39,1 гривень за картридж, або 47,3 гривні з урахуванням граничної націнки. Таким чином, Житомирською медичною базою було закуплено препарат за ціною, що перевищує максимально встановлену на 19,0 гривень, або на 40,2%.
Прикладом неефективного використання бюджетних коштів є закупівля лікарських засобів та виробів медичного призначення, які не відповідають номенклатурі, передбаченій Міністерством охорони здоров’я України. Подібним чином у 2012 році службові особи Управління охорони здоров’я Голосіївського району міста Києва, зловживаючи своїм службовим становищем, здійснили нецільове використання бюджетних коштів під час закупівлі витратних матеріалів.
Слід відзначити, що системні факти порушення вимог законодавства з боку структурних підрозділів з питань охорони здоров’я обласних (міських) державних адміністрацій та закладів охорони здоров’я під час здійснення державних закупівель, що призвели до розтрати бюджетних коштів, встановлені також правоохоронними органами України.
Так, прокуратурою м. Дзержинська Донецької області 18.01.2012 року порушено кримінальну справу за ознаками злочину, передбаченого частиною 1 статті 358 Кримінального кодексу України, за фактом протиправної діяльності посадових осіб станції швидкої медичної допомоги м. Дзержинська, які шляхом підробки звіту про результати відкритих торгів незаконно надали перевагу суб’єкту господарювання в ході здійснення закупівель хірургічного та медичного обладнання за державні кошти у розмірі понад 370 тис. гривень.
Прокуратурою Одеської області 03.02.2012 року порушено кримінальну справу за частиною 2 статті 364 Кримінального кодексу України стосовно посадових осіб Управління охорони здоров’я Одеської міської ради за фактом закупівлі за бюджетні кошти обладнання для потреб медичних установ м. Одеса за завищеною вартістю, що призвело до завдання збитків державі на суму 408,71 тис. гривень.
Слідчим управлінням УМВС України у Дніпропетровській області відкрито кримінальне провадження № 12013040449991187 за ознаками кримінального правопорушення, передбаченого частиною 2 статті 364 Кримінального кодексу України, стосовно службових осіб ОКЗ «База спеціального медичного постачання Головного управління охорони здоров’я Дніпропетровської облдержадміністрації», які діючи всупереч інтересам служби, в інтересах ТОВ «Техкомплект» в порушення вимог конкурсних торгів на закупівлю товарів за державні кошти, здійснили закупівлю легкових автомобілів в кількості 18 штук, які не укомплектовані спеціальним медичним обладнанням, чим завдали збитків бюджету у великих розмірах.
Слідчим управлінням УМВС України у рівненській області 03.01.2013 року відкрито кримінальне провадження № 12013190020000007 за ознаками кримінального правопорушення, передбаченого частиною 5 статті 191 Кримінального кодексу України, за фактом розтрати коштів державного бюджету на суму 655 тис. гривень службовими особами комітету з конкурсних торгів Управління охорони здоров’я Рівненської обласної державної адміністрації.
Слідчим управлінням УМВС України у Львівській області 09.01.2013 року відкрито кримінальне провадження № 12013150010000050 за ознаками кримінального правопорушення, передбаченого частиною 5 статті 191 Кримінального кодексу України, за фактом завдання збитків державі в сумі 1,19 млн. гривень посадовими особами Львівського обласного клінічного діагностичного центру, які здійснили закупівлю медичного обладнання для потреб медичної установи, та в подальшому не забезпечили гарантійного сервісного обслуговування придбаного медичного обладнання.
Красноармійською міжрайонною прокуратурою Донецької області 11.03.2013 року відкрито кримінальне провадження №42013050670000047 за ознаками кримінального правопорушення, передбаченого частиною 5 статті 191 Кримінального кодексу України, за фактом протиправної діяльності Красноармійської районної державної адміністрації та Красноармійської центральної районної лікарні, які допустили розтрату бюджетних коштів у сумі понад 6,3 млн. гривень, виділених на закупівлю медичного обладнання.
Слідчим управлінням УМВС України в Полтавській області 09.04.2013 року відкрито кримінальне провадження № 12013180070000156 за ознаками кримінального правопорушення, передбаченого частиною 2 статті 364 Кримінального кодексу України, за фактом зловживання службовим становищем з боку посадових осіб Полтавського обласного комунального підприємства «Полтавафарм», які впродовж 2012–2013 років у порушення вимог Закону України «Про здійснення державних закупівель», тобто без проведення конкурсних торгів, здійснили закупівлю препаратів інсуліну в рамках програми «Цукровий діабет на 2009–2013 роки» на загальну суму 18829900 гривень.
Слідчим управлінням УМВС України в Житомирській області 20.04.2013 року відкрито кримінальне провадження № 12013060010000084 за ознаками кримінального правопорушення, передбаченого частиною 2 статті 367 Кримінального кодексу України, відносно службових осіб КУ «Обласна база спеціального медичного постачання», яке через неналежні виконання своїх службових обов’язків під час проведення процедури державних закупівель препаратів для лікування цукрового і нецукрового діабету внесли недостовірну інформацію в документацію конкурсних торгів про назву предмету закупівлі, що значно обмежило коло учасників, які мали намір взяти участь у вказаних торгах, та заподіяло збитків бюджету на загальну суму близько 301 тис. грн.
По-четверте, мають місце численні випадки не введення в експлуатацію медичного обладнання, закупленого за бюджетні кошти.
На даний час залишаються не введеними в експлуатацію десятки одиниць медичного обладнання, закупленого за рахунок бюджетних коштів, та отриманого лікувально-профілактичними закладами Вінницької, Волинської, Дніпропетровської, Донецької, Київської, Кіровоградської, Луганської, Одеської, Тернопільської, Харківської, Хмельницької, Чернігівської областей.
Наприклад, у зв’язку з невідповідністю технічних умов приміщень та проведенням ремонтних робіт в 14 лікувальних установах Донецької області залишаються не введеними в експлуатацію 33 одиниці обладнання на суму 57438,0 тис. гривень, а саме: 10 комплексів рентгенівських діагностичних цифрових КРДЦ-00-Альфа вартістю 1640,0 тис. гривень за одиницю, 1 система рентгенівська діагностична REX-650R вартістю 899,9 тис. гривень, 2 системи рентгенівських діагностичних REX-650RF вартістю 1999,5 тис. гривень за одиницю, 1 стерилізатор паровий ВК-75–01 вартістю 14,7 тис. гривень, 1 стерилізатор ОТ 570 вартістю 749,0 тис. гривень, 1 комп’ютерний томограф 16 зрізовий TSX-034A Alexion Super 16 вартістю 6850,0 тис. гривень, 1 апарат рентгенографічний цифровий «Аспект» вартістю 630,0 тис, гривень, 1 томограф комп’ютерний TSX-032A вартістю 6848,3 тис. гривень, 2 флюорографа стаціонарних фірми «Крас» вартістю 629,0 тис. гривень.
У Київській області не введено в експлуатацію 5 одиниць медичного обладнання, придбаного у 2012 році за рахунок коштів субвенціїз державного бюджету, на суму 15 421,3 тис. гривень. Так, у Вишнівській центральній районній лікарні у зв’язку з невідповідністю приміщення технічним вимогам та проведенням ремонтних робіт залишається не встановленим комп’ютерний томограф SOMATOM. 3 аналогічних причин не використовується комплекс рентгенівський діагностичний «МЕДИКС» на 2 робочих місця в Комунальному закладі «Київська обласна психоневрологічна лікарня № 2» та рентгенографічна система в Ірпінській центральній міській лікарні. Крім цього, в Іванківській центральній районній лікарні та в Білоцерківській центральній районній лікарні не введено в експлуатацію два комплекси рентгенівські діагностичні «МЕДИКС» на 2 робочих місця, оскільки на даний час проводяться монтажні роботи.
Центром ядерної медицини Київського міського клінічного онкологічного центру не використовується закуплене за рахунок коштів субвенції з державного бюджету на створення центру із застосуванням ПЕТ-технології для раннього виявлення онкологічних захворювань дороговартісне медичне обладнання на загальну суму 39700,0 тис. гривень. Зокрема, у зв’язку з несправністю з березня 2012 року не використовується лінійний прискорювач № 1 вартістю 35000 тис. гривень; у зв’язку з відсутністю джерел іонізуючого випромінювання з червня 2012 року — обладнання блоку брахітерапії вартістю 4700 тис. гривень.
У Петрівській центральній районній лікарні (Кіровоградська область) не введено в експлуатацію комплекс рентгенівський діагностичний «Медикс» вартістю 695 тис. гривень у зв’язку з невідповідністю технічних умов приміщення для його встановлення. У Комунальному закладі «Обласний центр профілактики та боротьби зі СНІДом» Кіровоградської області не введено в експлуатацію гастрофіброскоп GIF-Е 3 вартістю 180 тис. гривень у зв’язку з необхідністю придбання додаткового електронасосу, штативів та витратних матеріалів для його використання.
В Оріхівській центральній районній лікарні (Запорізька область) не введено в експлуатацію комплекс рентгенівський діагностичний «Медикс» на 3 робочих місця у зв’язку з проведенням ремонту в приміщеннях лікарні.
На даний час в 11 лікувальних закладах охорони здоров’я Харківської області не використовуються 11 комплексів рентгенівських діагностичних «МЕДИКС» на 2 робочих місця на загальну суму 7740,7 тис. гривень. Зокрема, в Комунальному закладі охорони здоров’я «Харківська міська дитяча поліклініка № 2», Комунальному закладі охорони здоров’я «Харківська міська дитяча поліклініка № 12» та Комунальному закладі охорони здоров’я «Харківська міська дитяча поліклініка № 15» вищевказані комплекси не використовуються через невідповідність приміщень для їх монтажу технічним вимогам.
У Тернопільській області не введено в експлуатацію 2 одиниці медичного обладнання інкубатор транспортний модель ІТ-158-ТS на загальну суму 1234240,73 гривень у зв’язку з тим, що габарити транспортного візка не дозволяють встановити обладнання в салон автомобіля, а також відсутністю підігріву та зволоження газової суміші в апараті ШВЛ. Вказані недоліки не дозволяють експлуатувати дане обладнання в умовах відділення інтенсивної терапії новонароджених Тернопільської обласної дитячої клінічної лікарні та надавати медичну допомогу новонародженим дітям області згідно сучасних вимог та клінічних протоколів.
Подібна ситуація зумовлена невідповідністю приміщень для монтажу медичного обладнання технічним вимогам, затягуванням строків проведення будівельних та ремонтних робіт з підготовки приміщень для встановлення, монтажу та введення в експлуатацію обладнання, некомплектністю придбаного медичного обладнання, відсутністю технологічних складових та витратних матеріалів до даного обладнання.
При цьому доводиться констатувати, що вказані порушення мають системний, загальнодержавний характер, оскільки виявлені у більшості регіонах країнах.
Таким чином, незабезпечення Міністерством охорони здоров’я України належного виконання функцій головного розпорядника коштів державного бюджету та невиконання структурними підрозділами з питань охорони здоров’я обласних державних адміністрацій власних повноважень щодо своєчасного введення частини придбаного медичного обладнання в експлуатацію зумовило ненадання частині відповідних областей передбачених законодавством якісних медичних послуг на безоплатній основі.
По-п’яте, виявлено численні факти здійснення медичної практики закладами охорони здоров’я за відсутності акредитаційних сертифікатів та ліцензій.
Згідно статті 9 Закону України «Про ліцензування певних видів господарської діяльності» ліцензуванню підлягають, зокрема, такі види господарської діяльності, як медична практика, переробка донорської крові та її компонентів, виготовлення з них препаратів, крім діяльності банків пуповинної крові, інших тканин і клітин людини, діяльність банків пуповинної крові, інших тканин і клітин людини, а також господарська діяльність з обігу наркотичних засобів, психотропних речовин і прекурсорів.
Водночас у багатьох регіонах України масово функціонують заклади охорони здоров’я за відсутності ліцензій.
Наприклад, у порушення вимог статей 17, 33 Основ законодавства України про охорону здоров’я адміністрацією КЛПЗ «Прилуцька міська лікарня» (Чернігівська область) своєчасно не було вжито всіх необхідних заходів щодо своєчасного отримання ліцензії на зайняття медичною практикою, у результаті чого медичний заклад здійснював діяльність без відповідної ліцензії. Строк дії акредитаційного сертифіката КЗ «Талалаївська центральна районна лікарня» (Чернігівська область) закінчився ще 17.07.2012 року і до кінця 2012 року новий сертифікат не отримано.
Медичний заклад «Млинівська центральна районна лікарня» (Рівненька область) здійснював свою діяльність на підставі ліцензії, строк дії якої закінчився ще в липні 2012 року. При цьому станом на початок 2013 року ліцензія не поновлена.
Посадовими особами Хмельницького обласного протитуберкульозного диспансеру не забезпечено своєчасну подачу документів для продовження ліцензії на здійснення медичної практики, внаслідок чого з 08.11.2012 року установа незаконно проводила діяльність у цій сфері.
Випадки здійснення медичної діяльності без отримання у встановленому порядку ліцензії виявлені також в діяльності закладів охорони здоров’я Кіровоградської області, зокрема, Новоукраїнської центральної районної лікарні та КЗ «Кіровоградський обласний центр профілактики та боротьби зі СНІДом».
Аналогічні випадки виявлені в Миколаївській області. Зокрема, медична діяльність обласним лікувально-фізкультурним диспансером, обласною психіатричною лікарнею № 2, Жовтневою центральною районною лікарнею здійснювалась на підставі ліцензій, терміни яких закінчились 20.12.2012 року, Березнегуватська центральна районна лікарня здійснювала свою діяльність на підставі ліцензій, строк дії якої закінчився 25.02.2012 року.
Встановлено, що в Тернопільській області 11 закладів охорони здоров’я функціонували за наявності ліцензії на провадження господарської діяльності з медичної практики, термін якої минув. Зокрема, Копичинецька комунальна районна лікарня з 27 грудня 2012 року здійснювала діяльність, пов’язану з обігом наркотичних засобів, психотропних речовин і прекурсорів, без наявності відповідної ліцензії. Аналогічно без ліцензії на медичну практику надавалась медична допомога Борщівською, Вишнівецькою, Козівською, Козлівською, Кременецькою, Підволочиською та Скалатською лікарнями.
Згідно зі статтею 16 Основ законодавства України про охорону здоров’я передбачено, що заклади охорони здоров’я підлягають акредитації у випадках та в порядку, визначених Кабінетом Міністрів України.
Згідно Порядку державної акредитації закладу охорони здоров’я, затвердженого постановою Кабінету Міністрів України від 15.07.1997 року № 765, акредитація закладу охорони здоров’я — це офіційне визнання наявності у закладі охорони здоров’я умов для якісного, своєчасного, певного рівня медичного обслуговування населення, дотримання ним стандартів у сфері охорони здоров’я, відповідності медичних працівників єдиним кваліфікаційним вимогам. Пунктом 2 вищевказаного Порядку визначено, що акредитації підлягають всі заклади охорони здоров’я незалежно від форми власності.
Незважаючи на вищевказані вимоги закону, мають місце численні факти здійснення медичної діяльності закладами охорони здоров’я без проходження відповідної державної акредитації.
Наприклад, 97 державних та комунальних закладів охорони здоров’я Запорізької області, з яких 5 обласного підпорядкування, у тому числі КУ «Запорізька обласна клінічна лікарня», яка входить до переліку закладів, яким надано право проводити діяльність пов’язану з трансплантацією органів, здійснювали діяльність без акредитаційних сертифікатів (КУ «Мелітопольський центр з профілактики та боротьби зі СНІДом», КУ «Обласний дитячий багатопрофільний санаторій», КУ «Молочанський дитячий санаторій», КУ «Дитячий спеціалізований санаторій «Бердянський», КУ «Міська дитяча клінічна поліклініка»).
У Вижницькій та Герцаївській центральних районних лікарнях (Чернівецька область) не акредитовано клініко-діагностичні лабораторії, документи для їх акредитації не підготовлено, хоча адміністрацію даних закладів було зобов’язано здійснити акредитацію до грудня 2012 року.
Довгий час в Тернопільській області не акредитовані низка медичних закладів, зокрема, Язлівецький обласний протитуберкульозний санаторій, Кременецький обласний психоневрологічний санаторій, Бережанський обласний дитячий санаторій, Буданівська обласна психіатрична лікарня.
Відсутність у лікувальних закладів дозвільних документів на провадження медичної діяльності свідчить про неналежний рівень забезпечення якісного та своєчасного медичного обслуговування та створює реальну загрозу життю та здоров’ю населення.
Загалом, доводиться констатувати, що усі зазначені порушення створюють умови для поширення захворювань, негативним чином впливають на стан реалізації державної політики у галузі охорони здоров’я на рівні окремого регіону.
Причинами виявлених порушень є неналежне виконання своїх посадових обов’язків службовими особами структурних підрозділів з питань охорони здоров’я обласних (міських) державних адміністрацій та лікувально-профілактичних закладів.
Умовами виявлених порушень є відсутність належного контролю з боку відповідних структурних підрозділів з питань охорони здоров’я обласних (міських) державних адміністрацій за діяльністю підпорядкованих лікувально-профілактичних закладів, а також відсутність належного контролю у галузі охорони здоров’я з боку Міністерства охорони здоров’я України як головного органу у системі центральних органів виконавчої влади у формуванні та забезпеченні реалізації державної політики у сфері охорони здоров’я, формуванні державної політики у сферах санітарного та епідемічного благополуччя населення, створення, виробництва, контролю якості та реалізації лікарських засобів, медичних імунобіологічних препаратів і медичних виробів, протидії ВІЛ-інфекції/СНІДу та іншим соціально небезпечним захворюванням.
VII. ПРОПОЗИЦІЇ ЩОДО УДОСКОНАЛЕНННЯ ЧИННОГО ЗАКОНОДАВСТВА У СФЕРІ ОХОРОНИ ЗДОРОВ’Я
За результатами своєї діяльності Тимчасова слідча комісія відзначає наявність проблем із забезпеченням потреб населення, державних і комунальних закладів охорони здоров’я лікарськими засобами належної якості та в необхідному асортименті, а також відсутність ефективного механізму протидії виробництву і обігу фальсифікованих та неякісних лікарських засобів, ввезенню таких товарів в Україну.
Відбувається зростання цін на лікарські засоби, що пов’язано не з підвищенням ефективності, безпеки та якості цих засобів, а викликано діями суб’єктів ринку лікарських засобів, спрямованими на максимізацію власного прибутку.
Одночасно мають місце численні випадки непрозорого та неефективного використання бюджетних коштів під час здійснення державних закупівель лікарських засобів, виробів медичного призначення та медичної техніки.
Вказані проблеми зумовлюють погіршення стану системи охорони здоров’я і соціального захисту населення, що може спровокувати небезпечне погіршення стану здоров’я населення і, як наслідок, призвести до створення загрози національним інтересам і національній безпеці України.
Доводиться констатувати, що виявлені проблеми у сфері охорони здоров’я зумовлені, у тому числі, недосконалою нормативно-правовою базою.
По-перше, наявні системні проблеми із державною реєстрацією, проведенням експертизи якості, здійсненням ефективного контролю за реалізацією та використанням лікарських засобів.
Як передбачено статтею 4 Закону України «Про лікарські засоби», управління у сфері створення, виробництва, контролю якості та реалізації лікарських засобів у межах своєї компетенції здійснюють центральний орган виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я (Міністерство охорони здоров’я України), центральний орган виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів (Держлікслужба України).
Повноваження щодо державної реєстрації (перереєстрації) лікарських засобів, а також прийняття рішень про повну або тимчасову заборону застосування лікарських засобів шляхом припинення дії їх реєстраційних посвідчень покладені на Міністерство охорони здоров’я України (стаття 9 Закону України «Про лікарські засоби», пункт 9 Порядку державної реєстрації (перереєстрації) лікарських засобів). Натомість, повноваження щодо контролю за якістю лікарських засобів та умовами їх виробництва, а також прийняття рішень про вилучення з обігу та заборону (зупинення) виробництва, реалізації та застосування лікарських засобів, що не відповідають вимогам, визначеним нормативно-правовими актами та нормативними документами, покладені на Держлікслужбу України.
Існуюча ситуація, коли державна реєстрація (перереєстрація) лікарського засобу віднесена до компетенції Міністерства охорони здоров’я України, а сертифікація виробництва лікарських засобів на відповідність вимогам належної виробничої практики віднесена до компетенції Держлікслужби України, не перешкоджає обігу неякісних ліків та створює поле для зловживань з боку Міністерства охорони здоров’я України. На підтвердження цього можна навести низку прикладів, коли Міністерство охорони здоров’я України неодноразово проводило реєстрацію окремих лікарських засобів, незважаючи на отримання з Держлікслужби України інформації про виробників, яким відмовлено у видачі сертифікатів відповідності. Окрім того, не було вжито необхідних заходів щодо припинення дії реєстраційних посвідчень тих лікарських засобів, відносно яких Держлікслужба України надавала свої висновки про наявність шкідливих властивостей та/або відсутність терапевтичної ефективності.
Таким чином, розподіл повноважень між Міністерством охорони здоров’я України та Держлікслужбою України не забезпечує вжиття невідкладних заходів щодо протидії обігу неякісних та фальсифікованих лікарських засобів.
З цього приводу доречно відзначити, що рішенням Ради національної безпеки і оборони України від 25 травня 2012 року «Про забезпечення населення якісними та доступними лікарськими засобами», введеного в дію Указом Президента України від 30 серпня 2012 року N 526, Кабінету Міністрів України було вказано опрацювати питання щодо утворення в установленому порядку центрального органу виконавчої влади з покладенням на такий орган функцій із надання адміністративних послуг у сфері створення, реєстрації, виробництва та реалізації лікарських засобів.
Окрім того, практика країн Європейського Союзу підтверджує, що функції із надання адміністративних послуг у сфері створення та реєстрації лікарських засобів здійснюють окремі уповноважені органи, відокремлені від міністерств охорони здоров’я. Наприклад, реєстрацію препаратів у Польщі проводить Управління з реєстрації лікарських засобів, виробів медичного призначення та біоцидів. Процедура реєстрації лікарських засобів в Угорщині здійснюється національним методологічним центром — Національним інститутом якості та забезпечення розвитку в сфері охорони здоров’я та лікарських засобів.
Також відсутній дієвий механізм відстеження обігу лікарських засобів в режимі реального часу, що ускладнює для Держлікслужби України можливість оперативно отримати інформацію щодо наявності лікарських засобів, припинити реалізацію серії або конкретної упаковки лікарського засобу, контролювати передачу фальсифікованих, неякісних та незареєстрованих лікарських засобів на утилізацію.
Водночас, Директивою Європейського Парламенту та Ради Європи 2011/62/ЕС від 8 червня 2011 року «Про внесення змін до Директиви 2001/83/ЕС кодексу Співтовариства, пов’язаного з лікарськими засобами для застосування людиною, щодо запобігання надходження у легальну мережу постачання фальсифікованих лікарських засобів» передбачені додаткові превентивні механізми потрапляння фальсифікованих та неякісних лікарських засобів в легальну мережу поставок та реалізації товару. Зазначені зміни в законодавстві Європейського Союзу, що вступили в дію з січня 2013 року, встановлюють обов’язкове індивідуальне кодування виробником кожної упаковки лікарського засобу, що дозволить отримати інформацію про те, де, коли і ким вироблений лікарський засіб, кінцевий термін придатності лікарського засобу, оперативно отримати інформацію щодо наявності лікарських засобів та їх походження.
Викликає суттєвого зауваження порядок ввезення в Україну лікарських засобів. Так, відповідно до статті 17 Закону України «Про лікарські засоби» термін придатності лікарських засобів, що ввозяться на територію України, має становити не менше половини терміну, визначеного виробником, за умови, якщо виробник визначив термін менше одного року, або не менш як шість місяців, за умови, якщо виробник визначив термін більше одного року. Вказаний термін придатності лікарські засобів, що можуть ввозитись на територію України, є невиправдано обмеженим та може призвести до поширення фактів реалізації у роздрібній мережі тих лікарських засобів, терміни придатності яких наближаються до закінчення, або взагалі минули.
Дотепер лишаються не врегульованими питання, пов’язані із обліком, використанням та знищенням незареєстрованих лікарських засобів, призначених для проведення клінічних випробувань, доклінічних досліджень.
Отже, Тимчасова слідча комісія рекомендує ухвалити законопроект, метою якого є спрощення процедури реєстрації (перереєстрації) лікарських засобів та приведення вітчизняного законодавства у сфері створення, виробництва, контролю якості та реалізації лікарських засобів у відповідність до стандартів Європейського Союзу.
Даним законопроектом пропонується:
- надати Держлікслужбі України виключні повноваження щодо державної реєстрації (перереєстрації) лікарських засобів, прийняття рішень про повну або тимчасову заборону застосування лікарських засобів шляхом припинення дії їх реєстраційних посвідчень, контролю за цільовим використанням ввезених незареєстрованих лікарських засобів;
- передбачити обов’язкове індивідуальне кодування виробником кожної зовнішньої упаковки лікарського засобу як додатковий елемент захисту від реалізації фальсифікованих лікарських засобів;
- запровадити норму щодо обов’язкової участі посадових осіб Держлікслужби України при здійсненні утилізації або знищення неякісних, фальсифікованих та незареєстрованих лікарських засобів, у тому числі тих, термін придатності яких закінчився, а також обов’язкового інформування суб’єктом господарювання територіального органу Держлікслужби України про здійснення утилізації або знищення таких лікарських засобів;
- передбачити можливість залучення представників саморегулівних організацій фармацевтичної галузі при здійсненні утилізації або знищення неякісних, фальсифікованих та незареєстрованих лікарських засобів, у тому числі тих, термін придатності яких закінчився;
- встановити термін, у який суб’єкт господарювання повинен знищити та утилізувати неякісні, фальсифіковані та незареєстровані лікарські засоби, у тому числі ті, термін придатності яких закінчився;
- підвищити мінімально допустимий термін придатності лікарських засобів, що можуть ввозитись на територію України;
- внести застереження до Закону України «Про основні засади державного нагляду (контролю) у сфері господарської діяльності», яким передбачити, що під час здійснення заходів державного контролю за якістю та безпекою лікарських засобів не застосовуватиметься положення закону щодо необхідності письмового повідомлення суб’єкта господарювання про проведення планового заходу не пізніш як за десять днів до дня здійснення цього заходу. Подібне застереження підвищить ефективність профілактики та попередження потрапляння неякісних та фальсифікованих лікарських засобів на споживчий ринок;
- розширити об’єктивну сторону деяких складів злочинів (статті 305 та 3211 Кримінального кодексу України), що дозволить криміналізувати діяння, пов’язані з контрабандою та обігом неякісних лікарських засобів. Реалізація даного положення сприятиме забезпеченню подальшої гармонізації національної нормативно-правової бази у сфері обігу лікарських засобів із міжнародним та європейським законодавством, недопущенню до обігу неякісних лікарських засобів.
По-друге, система державного регулювання цін на лікарські засоби та вироби медичного призначення не забезпечує формування справедливої, економічно обґрунтованої ціни на вказану продукцію.
Механізм формування цін на лікарські засоби і вироби медичного призначення, щодо яких запроваджено державне регулювання, для реалізації суб’єктом господарювання на внутрішньому ринку з урахуванням граничних постачальницько-збутових і торговельних (роздрібних) надбавок прив’язано до рівня оптово-відпускних цін. Наприклад, закупівельна ціна одиниці товару визначається суб’єктом господарювання, що здійснює оптову торгівлю товаром, для його подальшої реалізації через аптечну мережу, за формулою: оптово-відпускна ціна + постачальницько-збутова надбавка в межах граничного розміру. Роздрібна ціна одиниці товару визначається суб’єктом господарювання, що здійснює реалізацію товару через аптечну мережу, за формулою: закупівельна ціна або оптово-відпускна ціна, встановлена вітчизняним товаровиробником + торговельна (роздрібна) надбавка в межах граничного розміру.
Оптово-відпускна ціна є ціною одиниці імпортованого товару або ціною одиниці товару, що встановлюється в договорі, укладеному між вітчизняним товаровиробником та суб’єктом господарювання, що здійснює оптову торгівлю товаром.
Слід відзначити, що на даний час обґрунтованість рівня оптово-відпускних цін на лікарські засоби та вироби медичного призначення уповноваженими органами не контролюється та не перевіряється, не розраховується граничний рівень оптово-відпускних цін з прив’язкою до цін, що сформувались на аналогічні товари в інших країнах.
За таких обставин суб’єкти господарювання, що здійснюють оптову та роздрібну торгівлю лікарськими засобами та виробами медичного призначення, мають змогу формувати економічно необґрунтовані ціни на такі товари у межах встановлених постачальницько-збутових та торговельних надбавок.
Одночасно слід відзначити, що безпосередньо самі розміри встановлених надбавок є необґрунтованими та спрямовані, у першу чергу, на максимізацію прибутку суб’єктів господарювання. Наприклад, якщо закупівельна ціна на лікарські засоби і вироби медичного призначення становить до 100 гривень, торговельна (роздрібна) надбавка до закупівельної ціни допускається до 25%.
У зв’язку з цим слід відзначити, що у 2012 році серед усього обсягу лікарських засобів, реалізованих в роздрібній (аптечній) мережі (близько 27 млрд. гривень), 75 відсотків складають товари вартістю до 100 гривень.
| Ціновий діапазон (гривень) | Імпортний лікарський засіб | Вітчизняний лікарський засіб | ||
|---|---|---|---|---|
| Кількість упаковок (шт.) | Сума (тис. грн.) | Кількість упаковок (шт.) | Сума (тис. грн.) | |
| до 5 | 31 690 856 | 96 122 | 407 474 743 | 990 654 |
| 5–10 | 22 938 724 | 146 684 | 201 199 196 | 1 310 307 |
| 10–15 | 34 521466 | 401 224 | 51 717 711 | 593 169 |
| 15–20 | 41 727 213 | 657 753 | 67 112 776 | 1 136 465 |
| 20–40 | 134 949 515 | 3 688 105 | 59 987 402 | 1 524 357 |
| 40–60 | 78 044 953 | 3 579 384 | 20 630 028 | 910 576 |
| 60–100 | 60 756 631 | 4 197 674 | 12 812 632 | 917 808 |
| 100–150 | 18 603 201 | 2 064 279 | 5 101 710 | 588 214 |
| 150–200 | 7 796 299 | 1 279 189 | 1430 376 | 238 459 |
| 200–300 | 4 457 465 | 1 024 552 | 587 205 | 137 189 |
| 300–500 | 2 532 648 | 911 863 | 331 105 | 124 652 |
| більше 500 | 552 363 | 430 717 | 138 371 | 110 014 |
| Всього | 438 571 335 | 18 477 545 | 828 523 255 | 8 581 866 |
Отже, слід визнати, що існуюча система надбавок стимулює співробітників аптечних установ реалізовувати покупцеві найбільш дорогі лікарські засоби в межах 100 гривень (які забезпечують установі найвищу надбавку 25%).
З огляду на вищевказане слід звернути увагу на європейський досвід регулювання цін на лікарські засоби, у першу чергу, інструментами прямого регулювання цін. Наприклад, починаючи з 2001 року в Норвегії запроваджена система граничних цін на основі базових цін, що охоплює всі ліки, які відпускаються за рецептом. Виробник, який продає рецептурні ліки на норвезькому ринку, має повідомити про ціни на препарати в «подібних» країнах. До подібних країн відноситься Австрія, Бельгія, Данія, Фінляндія, Німеччина, Ірландія, Нідерланди, Швеція та Великобританія. Якщо відповідний лікарський препарат ще не продається в жодній з вказаних країн, то гранична ціна визначається шляхом переговорів між виробником і регулятором. Середня з трьох найнижчих повідомлених цін стає максимальною внутрішньою оптовою ціною препарату. Після цього визначається максимальна націнка для роздрібних суб’єктів господарювання.
Аналогічний підхід до визначення граничних цін на лікарські засоби застосовується також в Болгарії, відповідно до Положення щодо регулювання і реєстрації цін на лікарські засоби, яке затверджено у 2011 році. Даним положенням передбачено, що під час реєстрації ціни лікарського засобу власник торгової ліцензії подає довідку щодо ціни на даний препарат у Румунії, Франції, Естонії, Греції, Словаччині, Литві, Португалії та Іспанії. Базова ціна на конкретний лікарський засіб в Болгарії не може бути вищою за найменшу ціну виробника на ідентичний лікарських засіб у вищезгаданих країнах.
Україні доцільно також врахувати досвід Бельгії, Угорщини та Словаччини які запровадили механізми державного регулювання цін по відношенню до всіх лікарських засобів, що зареєстровані в країні.
Вказане кореспондується з положеннями Директиви Європейського Парламенту та Ради Європи 89/105/ЕС (Директива прозорості), яка вимагає від країн — членів Європейського союзу забезпечення прозорості ціноутворення на продукцію медичного призначення.
Отже, Тимчасова слідча комісія рекомендує ухвалити законопроект, метою якого є приведення вітчизняного законодавства щодо державного регулювання цін на лікарські засоби у відповідність до стандартів Європейського Союзу, запобігання штучному завищенню цін на лікарські засоби та вироби медичного призначення для населення, забезпечення ефективного використання бюджетних коштів під час закупівлі лікарських засобів і виробів медичного призначення.
Даним законопроектом пропонується запровадити прозорий механізм декларування цін на лікарські засоби та вироби медичного призначення, який передбачатиме:
- подання власником реєстраційного посвідчення на лікарський засіб або свідоцтва про державну реєстрацію виробу медичного призначення розрахунку оптово-відпускної ціни на лікарський засіб або виріб медичного призначення;
- визначення уповноваженим органом граничного рівня оптово-відпускних цін на лікарські засоби або вироби медичного призначення з урахуванням порівняльних (референтних) цін в референтних країнах
- проведення перевірки правильності розрахунку оптово-відпускної ціни на лікарський засіб або виріб медичного призначення, яка здійснюватиметься центральним органом виконавчої влади, що реалізує державну політику з контролю за цінами.
Вказаним законопроектом одночасно пропонується зменшити граничний рівень торговельних (роздрібних) надбавок.
По-третє, існуючий пільговий режим оподаткування операцій з постачання лікарських засобів та виробів медичного призначення не забезпечує досягнення свого основного призначення — здешевлення вартості таких товарів для кінцевих споживачів.
Податковим кодексом України для операцій з поставки лікарських засобів та виробів медичного призначення визначено пільговий режим оподаткування. Так, підпунктом 197.1.27 пункту 197.1 статті 197 операції з постачання лікарських засобів, дозволених для виробництва і застосування в Україні та внесених до Державного реєстру лікарських засобів, а також виробів медичного призначення за переліком, затвердженим Кабінетом Міністрів України, звільняються від оподаткування податком на додану вартість.
Застосування даного режиму оподаткування не забезпечило здешевлення вартості лікарських засобів та виробів медичного призначення для населення.
Парадоксально, але в Україні ціни на окремі лікарські засоби є набагато дорожчими від цін на аналогічні товари в тих країнах, де ставка податку на додану вартість на операції з постачання лікарських засобів складає до 10%.
Окрім цього, це зумовило значні втрати бюджету, які становили у 2010 році 3,1 млрд. гривень, у 2011 році — 3,4 млрд. гривень.
Яскравим підтвердженням подібної ситуації є те, що останніми роками обсяг роздрібного фармацевтичного ринку України зростає у грошовому вираженні набагато більшими темпами, ніж у натуральному. Наприклад, у 2012 році у порівнянні з 2011 роком ринок у грошовому вираженні зріс на 17,4%, а в натуральному — лише на 5,5%. У 2011 році порівняно з 2010 роком показники зростання становили — 17,0% у грошовому вираженні та 1,3% у натуральному.
З цього приводу окремо варто відзначити, що імпорт лікарських засобів та виробів медичного призначення на митну територію України здійснюється, переважно, не на основі прямих зовнішньоекономічних договорів з зарубіжними підприємствами-виробниками лікарських засобів та виробів медичного призначення, а через суб’єктів зовнішньоекономічної діяльності, зареєстрованих у країнах із спрощеною системою звітності та оподаткування. При цьому постачання товарів через ланцюг компаній-посередників здійснюється фіктивно, рух товару відбувається лише «на папері» та без фактичного перетину митного кордону відповідної країни. У результаті використання подібних посередницьких операцій декларант або уповноважена ним особа на законних підставах може заявляти таку митну вартість лікарських засобів та виробів медичного призначення, яка суттєво перевищує ціни підприємства-виробника.А враховуючи, що операції з поставки лікарських засобів та виробів медичного призначення звільняються від оподаткування податком на додану вартість, імпортери лікарських засобів, завищуючи митну вартість товару, тим самим отримують можливість для тіньового виведення коштів за межі держави та штучної мінімізації власних податкових зобов’язань. При цьому вони не несуть жодних податкових зобов’язань зі сплати податку на додану вартість.
Тобто недобросовісні постачальники штучно завищують митну вартість лікарських засобів на етапі їх імпорту на територію України для подальшого виведення валютної виручки за кордон, переважно в офшорні зони.
З метою подолання вказаних недоліків Тимчасова слідча комісія рекомендує ухвалити законопроект, метою якого є недопущення штучного завищення цін на лікарські засоби та вироби медичного призначення для населення, а також створення законодавчих перешкод для тіньового виведення капіталу з України та штучної мінімізації податкових зобов’язань вітчизняних суб’єктів господарювання, які здійснюють ввезення лікарських засобів та виробів медичного призначення на територію України.
Проектом пропонується запровадити знижену ставку податку на додану вартість (на рівні 5–8%) на операції з ввезення на митну територію України лікарських засобів, дозволених для виробництва і застосування в Україні та внесених до Державного реєстру лікарських засобів та виробів медичного призначення за переліком, затвердженим Кабінетом Міністрів України.
За таких обставин постачальнику лікарських засобів стане економічно не вигідно штучно завищувати митну вартість товару, оскільки з вказаної ціни він буде змушений сплатити податок до бюджету.
З цього приводу доречно відзначити, що у більшості країн Європейського Союзу встановлена знижена ставка податку на додану вартість на операції з постачання фармацевтичної продукції: в Австрії — 10% (стандартна ставка — 20%), Угорщині — 5% (стандартна ставка — 25%), Іспанії — 4% (стандартна ставка — 18%), Латвії — 10% (стандартна ставка — 21%), Польщі — 7% (стандартна ставка — 22%), Чехії — 10% (стандартна ставка — 20%).
По-четверте, система державних закупівель лікарських засобів та виробів медичного призначення не забезпечує закупівлі якісних товарів та за економічно обґрунтованими цінами.
Так, у минулому році Міністерство охорони здоров’я України при здійсненні закупівель лікарських засобів і виробів медичного призначення систематично не дотримувалось приписів постанови Кабінету Міністрів України від 13.08.2012 року № 794 «Питання декларування зміни оптово-відпускних цін на лікарські засоби і вироби медичного призначення, які закуповуються за рахунок коштів державного та місцевих бюджетів», відповідно до яких заклади і установи охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів, закуповують лікарські засоби і вироби медичного призначення за цінами, які не перевищують рівень задекларованих оптово-відпускних цін з урахуванням мита, податку на додану вартість та граничних постачальницько-збутових та торговельних (роздрібних) надбавок.
Зокрема, закуповувались лікарські засоби за цінами, що перевищують зареєстровані оптово-відпускні ціни з урахуванням граничних постачальницько-збутових надбавок. Одночасно мали місце випадки закупівлі лікарських засобів і виробів медичного призначення, оптово-відпускні ціни на які взагалі не були задекларовані/зареєстровані. Як наслідок, не забезпечується максимальна економія та ефективність використання державних коштів, які спрямовуються на закупівлю в рамках державних та місцевих програм у сфері охорони здоров’я. У результаті зменшується кількість хворих, яких буде забезпечено лікарськими засобами, виробами медичного призначення, що призводить до погіршення якості надання медичної допомоги.
Одночасно потребує удосконалення система державного контролю якості та безпеки лікарських засобів, які закуповуються за державні кошти для потреб державних та комунальних закладів охорони здоров’я.
Отже, Тимчасова слідча комісія рекомендує ухвалити законопроект, метою якого є запровадження прозорих закупівель у сфері охорони здоров’я, посилення контролю за якістю та безпечністю лікарських засобів та виробів медичного призначення, що закуповуються за бюджетні кошти, недопущення закупівлі медичних препаратів за завищеними цінами.
Законопроектом пропонується:
- встановити застереження щодо неможливості закупівлі лікарських засобів та виробів медичного призначення за цінами, які перевищують рівень задекларованих оптово-відпускних цін з урахуванням граничних постачальницько-збутових та торговельних (роздрібних) надбавок, а також неможливості закупівлі тих лікарських засобів або виробів медичного призначення, оптово-відпускні ціни на які не задекларовані;
- врегулювати порядок здійснення контролю якості лікарських засобів та виробів медичного призначення під час державних закупівель.
Одночасно проектом пропонується передбачити, що з 2015 року державні закупівлі, замовником яких виступатиме Міністерство охорони здоров’я України, проводитимуться за процедурою електронного реверсивного аукціону.
Тимчасова слідча комісія також звертає увагу на необхідності доопрацювання чинного законодавства стосовно посилення відповідальності співробітників аптечних установ у разі порушення порядку відпуску рецептурних лікарських засобів. Наразі відзначається практично вільний доступ пацієнтів до рецептурних препаратів будь-якої групи. За виключенням препаратів предметно-кількісного обліку, рецепти за якими підлягають обліку та перевірці відповідних контролюючих органів, купівля решти рецептурних лікарських засобів на практиці не вимагає від пацієнта наявності рецепта.
Крім того, є актуальним посилення відповідальності співробітників лікувально-профілактичних закладів у разі порушення ними порядку проведення доклінічних вивчень та клінічних випробувань лікарських засобів.
Так, у 2012 році були виявлені випадки, коли доклінічні вивчення та клінічні випробування лікарських засобів проводилось з грубим порушенням вимог чинного законодавства. Як наслідок, існують сумніви щодо достовірності результатів таких випробувань, що не може гарантувати обіг виключно ефективних та безпечних лікарських засобів з визнаною доказовою базою. Це також становило суттєву загрозу для життя та здоров’я пацієнтів.
Тимчасова слідча комісія звертає увагу на необхідності обмеження реклами лікарських засобів, медичної техніки, методів профілактики, діагностики, лікування і реабілітації у засобах масової інформації.
Враховуючи вищевикладене, Тимчасовою слідчою комісією прийнято рішення рекомендувати:
1. Звернути увагу органів державної влади та органів місцевого самоврядування усіх рівнів на наявність численних порушень вимог статей 3, 22, 49 Конституції України, вимог відповідних міжнародних договорів України і міжнародних зобов’язань України у частині забезпечення належної реалізації невід’ємного права кожної людини на рівний та справедливий доступ до охорони здоров’я та якісної і своєчасної медичної допомоги, та вжити відповідних заходів для припинення цих порушень.
2. Верховній Раді України:
2.1. Звіт Тимчасової слідчої комісії взяти до відома.
2.2. Направити звіт Тимчасової слідчої комісії Президенту України та Прем’єр-міністру України, а також Генеральній прокуратурі України, Службі безпеки України, Міністерству внутрішніх справ України, Міністерству доходів і зборів України, Антимонопольному комітету України, Державній інспекції України з контролю за цінами, Державній фінансовій інспекції України для його вивчення та відповідного реагування.
2.3. Сприяти удосконаленню законодавчої бази у сфері охорони здоров’я з урахуванням світового досвіду. Зокрема, щодо формування додаткових правових механізмів недопущення створення, виробництва та реалізації неякісних та фальсифікованих лікарських засобів; запобігання штучному завищенню цін на лікарські засоби та вироби медичного призначення для населення; посилення державного контролю за якістю та безпечністю лікарських засобів та виробів медичного призначення, що закуповуються за бюджетні кошти, недопущення закупівлі медичних препаратів за завищеними цінами.
2.4. Посилити парламентський контроль за виконанням органами виконавчої влади та органами місцевого самоврядування положень зазначених вище статей Конституції України, інших законів України, відповідних міжнародних договорів України, згода на обов’язковість яких надана Верховною Радою України у частині, що стосується охорони здоров’я населення та права особи на охорону здоров’я та медичну допомогу.
3. Кабінету Міністрів України:
3.1. Вжити невідкладних заходів для припинення виявлених порушень законодавства з боку Міністерства охорони здоров’я України та посилити контроль за діяльністю Міністерства охорони здоров’я України. Підготувати та до 1 листопада 2013 року подати на розгляд Верховної Ради України проект Закону України «Про заклади охорони здоров’я та медичну діяльність», врегулювавши у ньому, зокрема, питання особливостей діяльності закладів охорони здоров’я, підвищення якості медичного обслуговування населення закладами охорони здоров’я усіх форм власності, правового статусу та відповідальності медичних (фармацевтичних) працівників, організаційно-правових засад реалізації прав пацієнтів, здійснення громадського контролю за діяльністю закладів охорони здоров’я та професійною діяльністю медичних (фармацевтичних) працівників.
3.2. Опрацювати питання щодо розширення переліку захворювань та номенклатури лікарських засобів, до яких може бути застосований механізм часткового відшкодування пацієнтам вартості лікарських засобів, аналогічний механізму, визначеному у постанові Кабінету Міністрів України від 25 квітня 2012 року № 340 «Про реалізацію пілотного проекту щодо запровадження державного регулювання цін на лікарські засоби для лікування осіб з гіпертонічною хворобою».
3.3. Доручити Міністерству охорони здоров’я України:
- у двотижневий термін розробити та представити на розгляд Кабінету Міністрів України програму заходів та календарний план протягом двох місяців щодо усунення виявлених Тимчасовою слідчою комісією фактів порушення законодавства України;
- удосконалити механізм моніторингу цін на лікарські засоби і вироби медичного призначення, що закуповуються за рахунок коштів державного та місцевих бюджеті, в частині розширення переліку країн для проведення зовнішнього реферування, оприлюднення інформації про оптово-відпускні ціни в референтних країнах;
- удосконалити механізм розподілу лікарських засобів та виробів медичного призначення, закуплених у централізованому порядку, з метою недопущення формування надлишків товарів в одних закладах охорони здоров’я та недостачі цих самих товарів в інших закладах;
- переглянути Національний перелік основних лікарських засобів і виробів медичного призначення з метою приведення його у відповідність до Списку життєво необхідних лікарських засобів Всесвітньої організації охорони здоров’я та включити до нього основні лікарські засоби і вироби медичного призначення, які необхідні для подолання в Україні епідемій соціально-небезпечних захворювань (туберкульозу, гепатитів тощо), з метою встановлення державного регулювання цін на вказані препарати;
- опрацювати питання щодо введення в документацію конкурсних торгів обов’язкової вимоги про надання учасниками сертифікату/висновку GMP, виданого Державною службою України з лікарських засобів;
- опрацювати питання активного залучення відомих іноземних постачальників та виробників лікарських засобів до участі в процедурах закупівель, замовником яких є Міністерство охорони здоров’я України;
- готувати оголошення, документацію конкурсних торгів та, у разі участі у закупівлі нерезидента — всі документи щодо відповідної процедури державних закупівель, українською та англійською мовами;
- розробити для учасників торгів нерезидентів-виробників окремий перелік кваліфікаційних вимог та відповідний пакет підтверджуючих документів, необхідних для участі у процедурах закупівель, з урахуванням підпорядкування нерезидентів іншим правовим системам та технічної неможливості компаній-нерезидентів отримувати деякі офіційні документи в Україні, зокрема такі як, довідка про банкрутство, ліцензія на оптову торгівлю тощо;
- посилити співпрацю із країнами — членами Європейського Союзу, іншими іноземними державами, в тому числі, пострадянського простору, з метою налагодження партнерського діалогу для здійснення спільних закупівель на міждержавному рівні для здешевлення вартості лікарських засобів і виробів медичного призначення, які мають високу ціну через обмежену конкуренцію між фармацевтичними компаніями — виробниками чи невеликим обсягом закупівель для рідкісних (орфанних) захворювань;
- впровадити механізми зниження закупівельних цін на лікарські засоби і вироби медичного призначення шляхом збільшення об’ємів закупівель, їх спільним фінансуванням за рахунок коштів державного та місцевих бюджетів, коштів неурядових організацій (в тому числі, Ініціативою Фонду Клінтона з питань ВІЛ/СНІДу та іншими міжнародними організаціями);
- провести інвентаризацію невведеного в експлуатацію медичного обладнання, закупленого у централізованому порядку, та вжити невідкладних заходів щодо якнайшвидшого введення такого обладнання в експлуатацію;
- забезпечити спільно з іншими центральними органами виконавчої влади розробку єдиних тарифів платних послуг, які можуть надаватися в державних та комунальних закладах охорони здоров’я, вищих медичних навчальних закладах та науково-дослідних установах;
- активізувати претензійно-позовну роботу у зв’язку з несвоєчасним виконанням окремими суб’єктами господарювання договорів про закупівлю, укладених на виконання бюджетних програм 2012 року;
- посилити співпрацю з Всесвітньою організацією охорони здоров’я, іншими міжнародними організаціями та науковими установами з питань управління якістю медичної допомоги.
3.4. Доручити Державній службі інтелектуальної власності України опрацювати питання імплементації гнучких положень Угоди ТРІПС СОТ у сфері охорони здоров’я до законодавства України для забезпечення вільної конкуренції на ринку лікарських засобів з метою зниження цін на лікарські засоби та забезпечення їх загальнодоступності.
3.5. На виконання рішення Ради національної безпеки і оборони України від 25 травня 2012 року «Про забезпечення населення якісними та доступними лікарськими засобами», введеного в дію Указом Президента України від 30 серпня 2012 року N 526, підпорядкувати Державне підприємство «Державний експертний центр Міністерства охорони здоров’я України» Державній службі України з лікарських засобів.
3.6. Доручити Міністерству доходів і зборів України посилити контроль за достовірністю відомостей про визначення митної вартості лікарських засобів та виробів медичного призначення, що ввозяться на митну територію України.
3.7. Доручити Державній інспекції України з контролю за цінами посилити контроль за формуванням, встановленням та застосуванням цін на лікарські засоби та вироби медичного призначення.
4. Антимонопольному комітету України посилити контроль за дотриманням законодавства про захист економічної конкуренції з боку великооптових дистриб’юторів лікарських засобів, які здійснюють господарську діяльність на загальнодержавному ринку торгівлі лікарськими засобами, та суб’єктів господарювання, які здійснюють діяльність на регіональних ринках торгівлі лікарських засобами.
5. Генеральній прокуратурі України, Службі безпеки України та Міністерству внутрішніх справ України дати належну правову оцінку діям посадових осіб Міністерства охорони здоров’я України, інших державних підприємств, установ та організацій у сфері охорони здоров’я та фармацевтичної галузі у зв’язку з обставинами, викладеними у звіті Тимчасової слідчої комісії, та вжити відповідних заходів реагування.
| Голова Тимчасової слідчої комісії — народний депутат України | Дирів А.Б. |
| Члени Тимчасової слідчої комісії — народні депутати України | Іонова М.М. Гелевей О.І. Донець Т.А. Лабунська А.В. Спіріна І.Д. Петренко П.Д. |

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим