Розпорядження
від 29.10.2015 р. № 15210-1.2/2.0/17-15
У відповідності до Конституції України, ст. 15, ст. 22, ст. 55 Закону України «Основи законодавства України про охорону здоров’я», ст. 15, ст. 21 Закону України «Про лікарські засоби», Положення про Державну службу України з лікарських засобів, затвердженого Указом Президента України від 08.04.2011 № 440, п.п. 3.2., 3.2.2. «Порядку встановлення заборони (тимчасової заборони) та поновлення обігу лікарських засобів на території України», затвердженого наказом МОЗ України від 22.11.2011 за № 809 (зі змінами), зареєстрованого Міністерством юстиції України від 30.01.2012 за № 126/20439, «Правил утилізації та знищення лікарських засобів», затверджених наказом МОЗ України від 24.04.2015 за № 242, зареєстрованого Міністерством юстиції України від 18.05.2015 за № 550/26995 та на підставі інформації ТОВ «Медвестснаб» щодо встановлення факту фальсифікації лікарського засобу ЛОРАКСОН, порошок для розчину для ін’єкцій по 1000 мг у флаконах № 12, серії 0320314, з маркуванням виробника «Ексір Фармасьютикал Компані», Іран, ЗАБОРОНЯЮ реалізацію, зберігання та застосування лікарського засобу ЛОРАКСОН, порошок для розчину для ін’єкцій по 1000 мг у флаконах № 12, серії 0320314, з маркуванням виробника «Ексір Фармасьютикал Компані», Іран, який має ознаки фальсифікації:
«Маркування»:
- інформація про серію, дату виготовлення та термін придатності нанесена методом типографського друку (в оригінальному зразку — методом штамповки);
«Упаковка»:
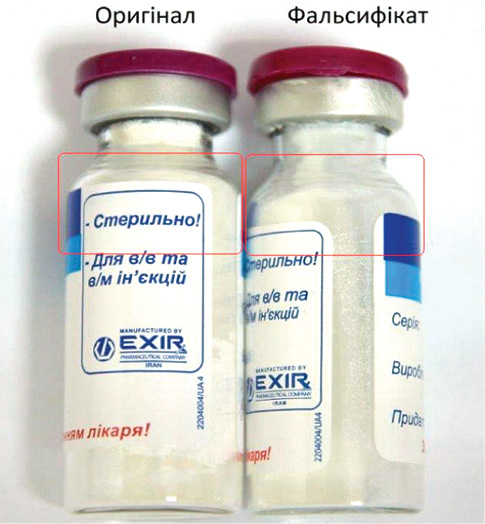
- висота етикетки на флаконі 35 мм (в оригінальному зразку висота етикетки 37 мм) (Фотографія № 1 Додатку);
- пластмасова кришечка на флаконі з нерівними краями і дефектами виплавки, не однорідного кольору (в оригінальному зразку — пластмасова кришечка з чіткими рівними краями, однорідного кольору) (Фотографія № 2 Додатку);
- обкатка алюмінієвого ковпачка виконана не якісно, край не рівний (в оригінальному зразку — обкатка виконана якісно, край рівний) (Фотографія № 3 Додатку);
- форма флакону фальсифікованого лікарського засобу відрізняється від оригінального лікарського засобу (Фотографія № 4 Додатку).
Суб’єктам господарювання, які здійснюють реалізацію, зберігання та застосування лікарських засобів, невідкладно після одержання даного розпорядження перевірити наявність лікарського засобу ЛОРАКСОН, порошок для розчину для ін’єкцій по 1000 мг у флаконах № 12, серії 0320314, з маркуванням виробника Ексір Фармасьютикал Компані, Іран, з вищезазначеними ознаками фальсифікації і вжити заходи щодо його вилучення з обігу шляхом знищення.
У разі наявності вказаного лікарського засобувжити заходи щодо вилучення його з обігу для подальшої передачі на знищення, про що в двотижневий термін поінформувати територіальний орган Держлікслужби України за місцем розташування.
При наступних поставках лікарського засобу суб’єкт господарювання повинен вжити заходів щодо запобігання придбанню, реалізації та застосуванню лікарського засобу, наведеного в даному розпорядженні.
Контроль за виконанням даного розпорядження здійснюють територіальні органи Держлікслужби України за місцем розташування.
Невиконання даного розпорядження тягне за собою відповідальність згідно чинного законодавства України.
| Перший заступник Голови – Голова комісії з реорганізації |
О.А. Алєксєєва |
Додаток
ФОТОГРАФІЯ №1

ФОТОГРАФІЯ №2

ФОТОГРАФІЯ № 3

ФОТОГРАФІЯ № 4

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим