Документ втратив чинність на підставі наказу МОЗ України від 26.09.2016 р. № 996
МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ
НАКАЗ
від 15.06.2007 р. № 325
Зареєстровано в Міністерстві
юстиції України
6 липня 2007 р.
за № 773/14040
Про затвердження Показників якості імунобіологічних препаратів (вакцин та анатоксинів)
Відповідно до Положення про Міністерство охорони здоров’я України, затвердженого постановою Кабінету Міністрів України від 02.11.2006 № 1542 та з метою забезпечення належного рівня якості імунобіологічних препаратів згідно Державної політики у сфері створення, виробництва, контролю якості та реалізації лікарських засобів і у відповідності з рекомендаціями Всесвітньої організації охорони здоров’я (ВООЗ) та на виконання Рішення Комітету з питань охорони здоров’я, материнства та дитинства Верховної Ради України від 12 січня 2006 року № 06-4/4-95 «Про забезпечення населення лікарськими засобами та шляхи подальшого реформування фармацевтичної галузі», доручення Кабінету Міністрів України від 1 лютого 2006 року № 3727/1/1-06 до листа першого заступника голови Комітету з питань охорони здоров’я, материнства та дитинства Верховної Ради України від 27 січня 2006 року № 06-4/4-49 НАКАЗУЮ:
1. Затвердити Показники якості імунобіологічних препаратів (вакцин та анатоксинів), що додаються.
2. Директору Департаменту державного санітарно-епідеміологічного нагляду Пономаренку А.М. забезпечити державну реєстрацію цього наказу в Міністерстві юстиції України.
3. Контроль за виконанням цього наказу покласти на першого заступника Міністра охорони здоров’я, головного державного санітарного лікаря С.П. Бережнова.
| Міністр | Ю.О. Гайдаєв |
ЗАТВЕРДЖЕНО
Наказ Міністерства
охорони здоров’я України
від 15.06.2007 р. № 325
Зареєстровано в Міністерстві
юстиції України
6 липня 2007 р.
за № 773/14040
ПОКАЗНИКИ
якості імунобіологічних препаратів
(вакцин та анатоксинів)
Основними показниками якості імунобіологічних препаратів (вакцин та анатоксинів) є такі загальноприйняті показники – реактогенність, імуногенність та епідеміологічна ефективність. На підставі аналізу даних післямаркетингового моніторингу щодо реактогенності вакцин та анатоксинів Календаря профілактичних щеплень в Україні, затвердженого наказом Міністерства охорони здоров’я України від 03.02.2006 № 48, зареєстрованого в Міністерстві юстиції України 02.06.2006 за № 665/12539 (далі – Календар профілактичних щеплень в Україні), даних клініко-епідеміологічних спостережень за їх реактогенністю та імуногенністю та даних Всесвітньої організації охорони здоров’я щодо їх безпеки та ефективності розроблені ці Показники якості імунобіологічних препаратів (вакцин та анатоксинів) в Україні.
Терміни, які вживаються в цьому документі, мають такі значення:
Показники якості показники, які є обов’язковими для всіх вакцин, що пропонуються до використання в Україні, як на етапі подання документів з метою реєстрації препарату в Україні, так і для використання раніше зареєстрованих.
Вакцини гетерогенний клас антибактеріальних лікарських засобів, що містять антигенні речовини, здатні до стимулювання активного імунітету проти збудника інфекційної хвороби або токсину, або інших важливих антигенних речовин, створених цим збудником. Вакцини для застосування у людини можуть містити: організми, інактивовані хімічним або фізичним засобом, що мають адекватні імуногенні властивості;
живі організми, які від природи є авірулентними або які пройшли обробку для послаблення їхньої вірулентності з одночасним збереженням адекватних імуногенних властивостей;
антигени, з організмів, у яких вони є секретами, або вироблені за допомогою технології рекомбінації ДНК. Антигени можуть використовуватись у своєму природному вигляді або можуть бути детоксифіковані хімічним або фізичним шляхом та можуть бути з’єднані, полімеризовані або зв’язані з носієм для збільшення їх імуногенності (стандарт Європейської фармакопеї 1998:0153).
Вакцинація щеплення за допомогою вакцин або анатоксинів.
Комбіновані препарати, призначені для захисту від декількох вакцини інфекційних хвороб, що можуть бути викликані різними штамами, різними мікроорганізмами чи серотипами мікроорганізмів.
Активна вакцинація, проведена протягом деякого часу імунізація для забезпечення тривалого захисту організму людини.
Імуногенність здатність вакцини утворювати гуморальний (визначені рівні антитіл у відсотках) і/або клітинно-опосередкований імунітет.
Сероконверсія продукування або збільшення концентрації антитіл, що розглядається як перехід від серонегативної до серопозитивної реакції, або як клінічно значиме збільшення заданого рівня антитіл, що демонструє імуногенність вакцини.
Захисний титр титр антитіл, що захищає проти визначених інфекцій.
Реактогенність патологічні явища, що виникають унаслідок вакцинації. Дані явища можуть бути місцевими або загальними. Відсоток реакцій визначається від загальної кількості щеплених даною вакциною.
Епідеміологічна зниження кількості випадків захворювання ефективність інфекційної хвороби після вакцинації порівняно вакцини до кількості випадків захворювання до вакцинації. Ефективність вакцини визначає прямий і непрямий захист (тобто захист не вакцинованих людей вакцинованими). Ефективність вакцинації залежить від рівня охоплення щепленнями, кореляції вакцинного штаму і штаму, що циркулює, дотримання умов «холодового ланцюга».
В Україні для активної імунізації відповідно до Календаря профілактичних щеплень в Україні можуть використовуватись тільки вакцини та анатоксини, що відповідають показникам якості, а саме:
– реактогенність за даними клініко-епідеміологічних досліджень, проведених в Україні, та моніторингу післявакцинальних реакцій та ускладнень повинна становити:
частота місцевих реакцій – не більше 25%;
частота загальних реакцій – не більше 15%;
частота ускладнень розраховується на 100 тис. щеплених та не повинна перевищувати показники, отримані при проведенні клініко-епідеміологічних досліджень;
– імуногенність вакцини (визначення відсотка сероконверсії серед щеплених даною вакциною відповідно до значень захисних титрів антитіл) за даними клініко-епідеміологічних досліджень, має бути більше 90%; для комбінованих вакцин кожен компонент вакцини повинен відповідати даному показнику;
– при наявності даних в Україні не менше ніж за 5 років використання вакцини визначається її епідеміологічна ефективність;
коефіцієнт епідеміологічної ефективності розраховується у відсотках для кожної вікової групи, щепленої вакциною одного виробника за такою формулою:
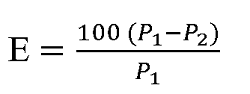
де
E – коефіцієнт, що відображає питому вагу осіб, які були щеплені, захист яких забезпечений вакцинацією;
P1 – кількість захворілих серед не щеплених;
P2 – кількість захворілих серед щеплених;
– наявність даних за динамікою зниження захворюваності щодо інфекції (інфекцій), проти яких призначена дана вакцина, за останні 5 років не менше ніж за 2 країнами, де вона використовувалася.
Застосовуються вакцини та анатоксини які зареєстровані відповідно до наказу Міністерства охорони здоров’я України від 06.12.2001 № 486, зареєстрованого в Міністерстві юстиції України 28.02.2002 за № 204/6492.
| Директор Департаменту державного санітарно-епідеміологічного нагляду | А.М. Пономаренко |

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим