 Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) 23 августа выдало разрешение на экстренное использование (Emergency Use Authorizations — EUA) исследуемой плазмы крови выздоравливающих от COVID-19 для лечения госпитализированных пациентов. На основании имеющихся научных данных FDA пришло к выводу, что этот продукт может быть эффективным в лечении COVID-19 и что известные и потенциальные преимущества перевешивают его известные и потенциальные риски.
Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) 23 августа выдало разрешение на экстренное использование (Emergency Use Authorizations — EUA) исследуемой плазмы крови выздоравливающих от COVID-19 для лечения госпитализированных пациентов. На основании имеющихся научных данных FDA пришло к выводу, что этот продукт может быть эффективным в лечении COVID-19 и что известные и потенциальные преимущества перевешивают его известные и потенциальные риски.
EUA не предназначен для замены рандомизированных клинических исследований, и FDA по-прежнему рекомендует, чтобы планы текущих рандомизированных клинических исследований плазмы крови выздоравливающих от COVID-19 и других терапевтических агентов оставались неизменными, поскольку плазма крови выздоравливающих еще не представляет собой новый стандарт лечения, основанный на имеющихся в настоящее время данных.
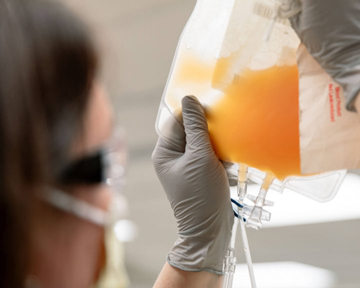
В рамках программы расширенного доступа (Expanded access program) конвалесцентную плазму крови уже применили более 70 тыс. раз в 2780 лечебных учреждениях, как поясняет головная организация — клиника Мэйо (Mayo Clinic), на своем веб-сайте. Первоначальные данные, полученные в результате исследований с использованием плазмы крови реконвалесцентов у пациентов с тяжелым течением COVID-19, свидетельствуют, что однократная доза 200 мл приводит к улучшению у некоторых из них. Однако запасы плазмы ограничены, поскольку ее можно получить только из донорской крови выздоравливающих.
Президент США Дональд Трамп приветствовал EUA для плазмы реконвалесцентов как «исторический прорыв». Ранее он обвинял FDA в препятствовании внедрению вакцин и прочих терапевтических средств по политическим причинам. «Очевидно, они надеются отложить принятие резолюции до 3 ноября. Но нужно действовать быстро и спасать жизни», — написал он комиссару FDA в Twitter.
По материалам www.fda.gov; www.uscovidplasma.org; www.faz.net

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим