Европейское агентство по лекарственным средствам (European Medicines Agency — EMA) 28 июня опубликовало отчет, в котором подводит итоги 15-летних усилий по поддержке малых и средних предприятий (МСП) в ЕС. Основная цель — содействие инновациям и поддержка компаний в разработке новых лекарственных средств для применения у людей и в ветеринарии. Отчет охватывает период 2016–2020 гг.
Для поддержки МСП на всех этапах развития Управление по делам предприятий малого и среднего бизнеса ЕМА (EMA’s Small and Medium-Sized Enterprises (SME) Office) обеспечивает активную регуляторную, финансовую и административную поддержку при их регистрации. В 2019–2020 гг. количество МСП, зарегистрированных ЕМА, достигло рекордного показателя — 1904. Из них 40% приходится на микро-, 34% — малые и 26% — на средние предприятия (таблица).
| Таблица | Характеристики МСП в зависимости от величины бизнеса |
| Характеристики | Микро (Micro) | Малые (Small) | Средние (Medium) |
| Количество сотрудников | <10 | <50 | <250 |
| Годовой оборот или баланс | ≤2 млн евро | ≤10 млн евро | ≤50 млн евро (баланс ≤43 млн евро) |
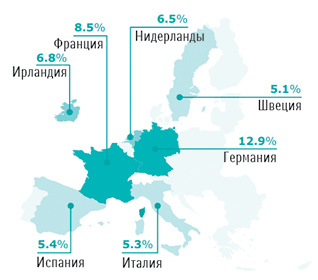
По итогам 2020 г. наибольшее количество компаний базировалось в Германии и Франции. После выхода Великобритании из ЕС наблюдают увеличение количества МСП, зарегистрированных в Ирландии и Нидерландах. Теперь они занимают 3–4-е места по данному показателю (рис. 1).
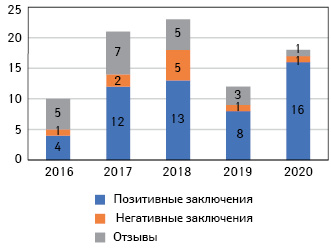
С 2016 г. количество успешных заявок на регистрацию лекарственных средств для человека, подаваемых малыми и средними предприятиями, увеличилось более чем вдвое. Так, в 2016 г. положительную оценку получили 40% лекарств от МСП. В 2020 г. — уже 89% (рис. 2). Только в 2020 г. на МСП приходится 16 рекомендаций по одобрению нового лекарства, что составляет почти 20% всех лекарственных средств для человека, рекомендованных для одобрения EMA в прошлом году. Половина из них нацелена на редкие заболевания.
МСП также оперативно откликнулись на необходимость разработки препаратов для борьбы с COVID-19. Так, 18 из 127 (14%) компаний, получавших научные консультации в ЕМА по данному вопросу, были МСП.
15 лет поддержки малого и среднего бизнеса
Публикация отчета знаменует 15-летнюю годовщину принятия Регламента о МСП (SME Regulation, № 2049/2005 от 15 декабря 2005 г.), которое способствует инновациям и разработке новых лекарств в Европе. МСП являются основным двигателем инноваций в фармацевтической промышленности, и ЕМА предоставляет им доступ к ряду стимулов, включая сниженные сборы за определенные процедуры и помощь со стороны вышеназванного Управления. С момента его создания в 2005 г. более 130 лекарственных препаратов, разработанных МСП, были одобрены в соответствии с рекомендациями EMA и способствуют укреплению здоровья населения и животных.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим