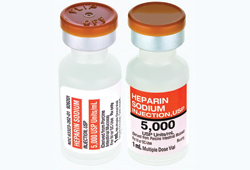
 1 октября Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) заявило в письме к работникам здравоохранения, что изменения в производстве препаратов гепарина приведут к снижению стандартной дозы антикоагулянта по сравнению с ранее представленной на рынке США на 10%. Данное изменение внесено Фармакопеей Соединенных Штатов (United States Pharmacopeia ? USP) и является частью новых действий по управлению производством, предназначенных для того, чтобы гарантировать качество гепарина и принять меры против потенциальной возможности его загрязнения.
1 октября Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) заявило в письме к работникам здравоохранения, что изменения в производстве препаратов гепарина приведут к снижению стандартной дозы антикоагулянта по сравнению с ранее представленной на рынке США на 10%. Данное изменение внесено Фармакопеей Соединенных Штатов (United States Pharmacopeia ? USP) и является частью новых действий по управлению производством, предназначенных для того, чтобы гарантировать качество гепарина и принять меры против потенциальной возможности его загрязнения.
Изменения, принятые USP для стандартной дозы гепарина, которую применяют в Европе в течение многих лет, соответствуют Международному стандарту (International Standard) Всемирной организации здравоохранения, определяющей единицы действия препарата.
Фармацевтические компании «Baxter International Inc.», «Hospira Inc.», «B. Braun Group» и «APP Pharmaceuticals Inc.», которые представляют на рынке США парентеральные гепарины, внесли изменения в способы управления производством по состоянию на 1 октября, однако не будут начинать отгрузку продукта с новой дозировкой до 8 октября, пока все сотрудники сферы здравоохранения не будут осведомлены о принятых изменениях, отмечают в управлении. Джон Дженкинс (John Jenkins), директор департамента новых препаратов (Office of New Drugs) FDA, заявил, что, хотя одобренная FDA маркировка для гепарина не изменилась, включая рекомендуемые дозы, важно, чтобы работники здравоохранения знали о потенциальных отличиях в дозировке старой и новой форм гепарина…
Напомним, что в 2008 г. партии контаминированного гепарина, импортированного из Китая, вызвали сотни побочных явлений в США, включая смерть («Китай защищает своего производителя контаминированного гепарина»), что привело к отзыву препарата с рынка США, а затем и Европы («Отзыв серий гепарина с европейских рынков»).
По материалам ;

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим