ТИФЛОКС: Универсальная комбинациядля лечения смешанных инфекций
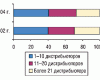
Корреспондент «Еженедельника АПТЕКА» обратился к заведующей аптекой «36,7» (г. Симферополь, ул. Карла Маркса, 14) Оксане Макаровой с просьбой рассказать о динамике продаж препарата ТИФЛОКС в этом аптечном учреждении и перспективах дальнейшего сотрудничества с его производителем — компанией «Торговый дом «Авант».
Сигнальный указатель для аптечных учреждений: Новые аргументы
Установка сигнального указателя в настоящее время является добровольной процедурой. Тем не менее на страницах газеты продолжается дискуссия на эту тему.
Уроки побед и поражений реформы российского здравоохранения
Поделиться с читателем «Еженедельника АПТЕКА» информацией о последних наиболее заметных событиях на фармацевтическом рынке РФ и высказать экспертные оценки последствий этих событий любезно согласился генеральный директор компании «КОМКОН–Фарма», сопредседатель Гильдии специалистов фармацевтического маркетинга «Российская ассоциация фармацевтического маркетинга» Олег Фельдман.
Міністерство охорони здоров’я УкраїниЛист суб’єктам господарської діяльності, які займаються реалізацією лікарських засобів
29 квітня 2005 р. редакція «Щотижневика АПТЕКА» отримала лист МОЗ України щодо продукції, у маркуванні або інструкціях по застосуванню якої вказується на використання для лікування (профілактики) захворювань або симптомів, але яка не зареєстрована як лікарські засоби.
Аптека и дистрибьютор — скованные одной цепью
Мы уже не раз обращались к результатам VIII Всеукраинского рейтинга «Еженедельника АПТЕКА» «ФармЭксперт». В данной публикации мы рассмотрим еще один немаловажный, а возможно, даже один из ключевых аспектов фармацевтического рынка: взаимодействия двух его основных звеньев — дистрибьютора и аптеки.
Рішення № 1381/12-16 від 25.04.2005 р. на № 1007/21 від 13.04.2005 р.
На підставі позитивних висновків додаткової лабораторної перевірки якості зразків лікарського засобу АДРЕНАЛІНУ ГІДРОТАРТРАТ, розчин для ін’єкцій 0,18% в ампулах по 1 мл № 10 серії 110704 виробництва ТОВ «Фармацевтична компанія «Здоров’я», Україна, в тому числі за показником «Механічні включення», у відповідності з вимогами п. 3.4. п. 4.1.7, п. 4.1.8, п. 4.1.12, Порядку заборони (зупинення) та вилучення з обігу лікарських засобів на території України, затвердженого наказом МОЗ України від 12.12.2001 р. № 497 і зареєстрованого в Міністерстві юстиції України 28.12.2001 р. за № 1091/6282, із змінами та доповненнями, затвердженими наказом МОЗ України від 08.07.2004 р. № 348 і зареєстрованими в Міністерстві юстиції України 23.07.2004 р. за № 917/9516, дозволено поновлення обігу вказаного вище лікарського засобу.
Наказ Міністерства охорони здоров’я України від 07.04.2005 р. № 156
ПРО ДЕРЖАВНУ РЕЄСТРАЦІЮ ЛІКАРСЬКИХ ЗАСОБІВ ТА ВНЕСЕННЯ ЗМІН У РЕЄСТРАЦІЙНІ МАТЕРІАЛИ
Рішення про поновлення обігу лікарського засобу від 04.04.2005 р. № 1111/12-19
На підставі позитивних результатів додаткових досліджень на відповідность вимогам аналітичної нормативної документацїї (далі — АНД) до реєстраційного посвідчення № П.05.03/06562, змінам № 5.12-5828/А від 10.08.04 до АНД серії 131004 лікарського засобу Тріомбраст, розчин для ін’єкцій 76% в ампулах по 20 мл № 5 серії 131004 виробництва ВАТ «Фармак», Україна, у відповідності з вимогами п. 3.4. Порядку заборони (зупинення) та вилучення з обігу лікарських засобів на території України, затвердженого наказом МОЗ України від 12.12.2001 р. № 497 і зареєстрованого в Міністерстві юстиції 28.12.2001 р. за № 1091/6282, із змінами, затвердженими наказом МОЗ України від 08.07.2004 р. № 348, дозволено поновлення обігу вказаного вище лікарського засобу.
від 21.04.2005 р. № 1342/12-22
В першому абзаці рішення Державної інспекції з контролю якості лікарських засобів від 04.04.2005 р. № 1111/12-19 про поновлення обігу лікарського засобу Тріомбраст, розчин для ін’єкцій 76% в ампулах по 20 мл № 5 серії 131004 виробництва ВАТ «Фармак» була допущена технічна помилка стосовно АНД, відповідно до якої проводилися додаткові дослідження препарату, та номера реєстраційного посвідчення лікарського засобу.
Рішення від 22.04.2005 р. № 1364/12-16
У зв’язку з внесенням змін в АНД, перереєстрацією препарату та на підставі позитивних результатів державного контролю п’яти серій, у відповідності з вимогами п. 3.4., п. 4.1.7, п. 4.1.8, п. 4.1.12. Порядку заборони (зупинення) та вилучення з обігу лікарських засобів на території України, затвердженого наказом МОЗ України від 12.12.2001 р. № 497 і зареєстрованого в Міністерстві юстиції України 28.12.2001 р. за № 1091/6282, із змінами та доповненнями, затвердженими наказом МОЗ України від 08.07.2004 р. № 348 і зареєстрованими в Міністерстві юстиції України 23.07.2004 р. за № 917/9516, дозволено поновлення обігу лікарського засобу АМІАКУ РОЗЧИН, розчин для зовнішнього застосування 10%, по 40 мл у флаконах, виробництва Фармацевтичної фабрики - підприємство обласної комунальної власності, м. Миколаїв, Україна.