РОЗПОРЯДЖЕННЯ
від 20.05.2025 р. № 313-001.1/002.0/17-25
Відповідно до Конституції України, статей 15, 22, 55 Закону України «Основи законодавства України про охорону здоров’я», статей 15, 17, 21 Закону України «Про лікарські засоби», Положення про Державну службу України з лікарських засобів та контролю за наркотиками, затвердженого постановою Кабінету Міністрів України від 12.08.2015 № 647, Порядку здійснення державного контролю якості лікарських засобів, що ввозяться в Україну, затвердженого постановою Кабінету Міністрів України від 14.09.2005 № 902, пункту 3.2.2 Порядку встановлення заборони (тимчасової заборони) та поновлення обігу лікарських засобів на території України, затвердженого наказом Міністерства охорони здоров’я України від 22.11.2011 № 809 (зі змінами), зареєстрованого Міністерством юстиції України 30.01.2012 за № 126/20439, Порядку контролю якості лікарських засобів під час оптової та роздрібної торгівлі, затвердженого наказом Міністерства охорони здоров’я України від 29.09.2014 № 677, зареєстрованого Міністерством юстиції України 26.11.2014 за № 1515/26292, Правил утилізації та знищення лікарських засобів, затверджених наказом Міністерства охорони здоров’я України від 24.04.2015 № 242, зареєстрованих Міністерством юстиції України від 18.05.2015 за № 550/26995, на підставі міжнародного повідомлення Ref. RPQ/REG/ISF/Alert № 3/2025 та інформації від ДУ «Центр громадського здоров’я МОЗ України» (лист від 15.05.2025 № 04-12/20/3087/25) щодо виявлення в обігу на території Ірану та Туреччини серій BAZR (термін придатності 03.2025), BBEG (термін придатності 12.2025), AVZT (термін придатності 12.2026) фальсифікованого лікарського засобу IMFINZI (durvalumab) injection 500 mg/10 ml, з маркуванням виробника AstraZeneca.
З метою активної протидії поширенню лікарських засобів, шляхи надходження та умови зберігання яких невідомі, визначити якість та безпечність яких неможливо, з огляду на те, що така продукція є небезпечною та може нести потенційну загрозу життю та здоров’ю населення:
ЗАБОРОНЯЮ реалізацію, зберігання та застосування серій BAZR, BBEG, AVZT фальсифікованого лікарського засобу IMFINZI (durvalumab) injection 500 mg/10 ml, з маркуванням виробника AstraZeneca (фото додається).
Суб’єктам господарювання, які здійснюють реалізацію, зберігання та застосування лікарських засобів, невідкладно, після одержання даного розпорядження, перевірити наявність вказаних серій лікарського засобу, вжити заходи щодо вилучення їх з обігу шляхом знищення або повернення постачальнику, про що повідомити територіальний орган Держлікслужби.
У разі знищення відходів зазначених серій лікарського засобу в двотижневий строк направити до територіального органу Держлікслужби копію акта про знищення відходів лікарського засобу.
Контроль за виконанням даного розпорядження здійснюють територіальні органи Держлікслужби на відповідній території.
Невиконання даного розпорядження тягне за собою відповідальність згідно з чинним законодавством України.
ГоловаР. Ісаєнко
| Product Name | IMFINZI (durvalumab) injection 500mg/10ml | ||
| Stated manufacturer | AstraZeneca | ||
| Identified in | Islamic Republic of Iran | Islamic Republic of Iran | Türkiye |
| Lot | BAZR | BBEG | AVZT |
| Expiry date | 03-2025 | 12-2025 | 12-2026 |
| Available Photographs | |||
| Lot BAZR | 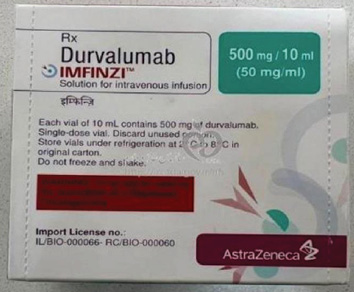 |
||
| Lot BBEG |  |
||

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим