ВЕРХОВНА РАДА УКРАЇНИ
ПОДАННЯ
Відповідно до статті 93 Конституції України в порядку законодавчої ініціативи вносимо на розгляд Верховної Ради України проект Закону України «Зробимо ліки дешевшими!» (про внесення змін до деяких законодавчих актів України щодо комплексного здешевлення ліків для громадян та забезпечення розвитку вітчизняної фармацевтичної галузі).
Доповідати на пленарному засіданні Верховної Ради України буде народний депутат України Галасюк В.В.
Додаток:
1. Проект Закону України на 8 арк.;
2. Пояснювальна записка на 17 арк.;
3. Порівняльна таблиця на 17 арк.;
4. Проект Постанови Верховної Ради України на 1 арк.;
5. Матеріали законопроекту в електронному вигляді.
Народні депутати УкраїниО.В. Ляшко
В.В. Галасюк
В.І. Вовк
О.М. Кириченко
А.В. Кошелєва
М.Ю. Бурбак
В.Л. Заружко
М.В. Довбенко
О.Г. Домбровський
О.В. Кужель
А.М. Гіршфельд
Л.П. Козаченко
Є.Ю. Рибчинський
М.В. Єфімов
А.Ю. Геращенко
О.С. Мусій
В.В. Амельченко
Д.В. Лінько
С.В. Рибалка
ПОЯСНЮВАЛЬНА ЗАПИСКА
до проекту Закону України «Зробимо ліки дешевшими!» (про внесення змін до деяких законодавчих актів України щодо комплексного здешевлення ліків для громадян та забезпечення розвитку вітчизняної фармацевтичної галузі)
1. Обґрунтування необхідності прийняття законопроекту
Ліки в Україні є занадто дорогими та недоступними для українського населення. Низька купівельна спроможність українців, що сформувалась в останні роки, значно загострила проблему економічної доступності ліків. Натомість при формуванні системи обігу лікарських засобів пріоритетом мають бути інтереси пацієнта, які полягають у доступності ліків з доведеною терапевтичною ефективністю.
В Україні, за даними статистичного бюлетеня «Національні рахунки охорони здоров’я України», кінцеве споживання фінансових коштів системи охорони здоров’я забезпечувалося через трьох основних постачальників медичних послуг і товарів (провайдерів): лікарень (35,3% поточних витрат на охорону здоров’я), закладів, що надавали амбулаторні послуги (12,4%), і закладів з роздрібного продажу медичних товарів та інших організацій, що надавали медичні товари (38,2%)1.
1Національні рахунки охорони здоров’я (НРОЗ) України у 2015 році: Статистичний бюлетень/Державна служба статистики України. 2017. C. 10−11.
Згідно результатів загальнонаціонального дослідження «Індекс здоров’я. Україна — 2017», у більшості країн ці витрати покриваються за рахунок коштів бюджету або схем обов’язкового медичного страхування. У країнах ОЕСР ці схеми становлять у середньому 57% від усіх роздрібних фармацевтичних витрат, крім того, 39% покривається населенням за рахунок власних коштів, ще 4% — коштами добровільного медичного страхування2.
В Україні ж витрати із роздрібного продажу медичних товарів майже повністю (99,8%) фінансуються за рахунок коштів домогосподарств. Це лягає важким тягарем на малозабезпечені верстви населення, які не мають належного соціального захисту. Тому пріоритетом для національної системи охорони здоров’я мають бути інтереси пацієнта, які полягають у фізичній і фінансовій доступності ліків.
Також у вказаному дослідженні здійснено аналіз доступності лікарських засобів для українців та виявлено наступні вкрай негативні тенденції:
1) 21,6% опитаних серед тих, хто мав хворобу чи травму і не звертався по медичну допомогу, відмовилися від звернення по неї через її високу вартість. Отримані дані кореспондуються з результатами самооцінки домогосподарств щодо доступності товарів і послуг. Згідно з ними, у 18% від загальної кількості домогосподарств були особи, які повідомили про випадки неможливості придбання необхідних, але занадто дорогих ліків;
| Протягом останніх 12 місяців Вам доводилося через відсутність коштів… | %/N | Всього | Стать | Місце проживання | Вік | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| чоловіки | жінки | місто | село | 18–29 років | 30–44 роки | 45–59 роки | 60 років і старші | |||
| … відмовлятися від лікування? | % | 19,1 | 13,2 | 24,0 | 18,7 | 20,1 | 9,0 | 13,7 | 20,8 | 30,6 |
| N | 1911 | 594 | 1317 | 1289 | 623 | 175 | 385 | 535 | 816 | |
| … відкласти лікування? | % | 18,9 | 12,6 | 24,1 | 18,4 | 19,9 | 8,6 | 15,5 | 19,9 | 29,1 |
| N | 1893 | 568 | 1325 | 1273 | 620 | 170 | 435 | 512 | 776 | |
| … зменшити кількість препаратів? | % | 18,9 | 12,4 | 22,8 | 18,5 | 17,3 | 9,7 | 13,8 | 19 | 27,9 |
| N | 1814 | 559 | 1255 | 1277 | 537 | 190 | 388 | 490 | 746 | |
| … перервати (не закінчити) курс лікування? | % | 9,6 | 6,6 | 12,2 | 9,4 | 10,1 | 4 | 7,2 | 10,4 | 15,6 |
| N | 965 | 298 | 668 | 650 | 315 | 77 | 203 | 267 | 418 | |
2) майже кожен третій респондент віком 60 років і старші (33,4%) відчували тягар витрат на ліки;
3) основною причиною відмови від купівлі призначених лікарем лікарських засобів стала відсутність коштів, про що повідомив майже кожен другий респондент;
4) витрати на лікарські засоби з особистого чи сімейного бюджету впродовж останніх 30 днів становили 610,9 грн.
Згідно іншого дослідження, проведеного в рамках проекту USAID «(Без)коштовна медицина» та виконаного БФ «Пацієнти України»3, встановлено, що кожен другий пацієнт в Україні відмовляється від лікування або відкладає його через брак коштів. Головна проблема, як вважають 94% пацієнтів, що брали участь у фокус-групах, є саме висока вартість препаратів.
2health-index.com.ua/upload/files/+Report%20Health%20Index%202017_web.pdf784933025.pdf
3moz.gov.ua/article/statistic/rezultati-doslidzhennja-bezkoshtovna-medicina
Враховуючи вищенаведені вкрай негативні тенденції в Україні, принциповим повинно стати питання економічної доступності медикаментів для українського населення, особливо для соціально незахищених верств населення.
Отож, для забезпечення економічної доступності медикаментів для населення України слід комплексно вирішити наступні проблеми:
1. За останні роки в Україні склалась тенденція монополізації роздрібних мереж у сфері реалізації населенню лікарських засобів. У звіті Антимонопольного комітету України за результатами дослідження фармацевтичних ринків зазначено, що схильність аптечного сегменту фармацевтичного ринку до консолідації стала загрозливою для добросовісної конкуренції.
Антимонопольний комітет України дійшов висновку, що вже зараз у цьому сегменті ринку з’являються гравці (аптечні мережі), яким притаманні ознаки монопольного (домінуючого) становища на регіональних ринках. Так, у ході дослідження регіональних ринків лікарських засобів були встановлені структурні ознаки монопольного (домінуючого) становища на досліджуваних регіональних ринках 183 суб’єктів господарювання, які здійснюють роздрібну торгівлю лікарськими засобами в форматі аптечної мережі4.
Така тенденція призводить до поглинання сильними гравцями ринку слабкіших конкурентів. При цьому, враховуючи, що аптечний сегмент є практично єдиним каналом збуту лікарських засобів кінцевим споживачам, великі аптечні мережі можуть негативно впливати як на цінову, так і на номенклатурну пропозицію на ринку, а саме можуть обмежувати асортимент лікарських засобів для споживачів, пропонуючи ті препарати, прибутковість від реалізації яких є найбільшою.
За інформацією Об’єднання організації роботодавців медичної та мікробіологічної промисловості України, поряд з вищевказаним, вже декілька років існує некоректна практика нав’язування постачальникам лікарських засобів маркетингових договорів, згідно яких постачальник, у тому числі і вітчизняний виробник, мусить витрачати шалені кошти тільки на те, щоб його препарати просто були у фізичній доступності в аптечному закладі.
Так, на сьогоднішній день ситуація складається таким чином, що монополізація аптечних роздрібних мереж стала суттєво відчутною проблемою для фармацевтичних підприємств. Але ще більше це відчувають безпосередньо кінцеві споживачі — пацієнти, які приходять за вітчизняними якісними лікарськими засобами у аптечну мережу, але не можуть їх придбати. Дана ситуація в першу чергу пов’язана з тим, що вітчизняний виробник не має можливості сплачувати до 30–40 відсотків від вартості лікарського засобу тільки за те, щоб він просто потрапив на полицю аптеки.
З метою подолання даної проблеми, боротьби з недобросовісною конкуренцією, підвищення фізичної та фінансової доступності для населення ефективних і якісних ліків, встановлення чітких та прозорих правил для всіх учасників ринку необхідно запровадити в Україні європейський досвід вирішення цієї проблеми.
Так, згідно інформації, наданої Об’єднанням організації роботодавців медичної та мікробіологічної промисловості України, декілька років тому у Польщі запровадили проект зі зменшення кінцевої вартості лікарських засобів, обмеживши розростання аптечних мереж у монопольні структури. Нині у Польщі існує чітке правило: тільки фармацевт може відкрити аптеку, він повністю відповідає за надану фармацевтичну послугу, за цінову характеристику та за інші складові, які пов’язані з реалізацією лікарських засобів. При цьому, кількість аптек однієї мережі не може перевищувати 1 відсотка від усіх аптечних закладів воєводства (найбільша адміністративна одиниця Польщі), а фізична доступність — становить 3000 осіб на одну аптеку.
В Болгарії, для прикладу, в 2008 році запроваджено новий закон, який надав право створення аптеки будь-кому. До цього часу лише особи з фармацевтичною освітою мали право відкривати аптеки. Але одночасно з цим також заборонено підприємству чи особі володіти більше ніж 4 аптеками. Це повинно обмежити створення аптечних мереж. На Кіпрі кожен фармацевт може володіти однією аптекою, а їх об’єднання не дозволяється.
4www.apteka.ua/article/392373.
Даним законопроектом пропонується з врахуванням європейського досвіду в сфері запобігання зловживань з боку аптечних мереж (протидії встановлення монопольного становища на роздрібному ринку ліків, поглинання та знищення суб’єктів господарювання малого та середнього бізнесу) створити необхідні умови забезпечення економічної та фізичної доступності лікарських засобів та раціонального їх використання. Зокрема, проектом пропонується запровадження чіткого законодавчого тлумачення терміну «Аптечна мережа» та обмеження кількості аптек однієї аптечної мережі не більше 2 відсотків від загальної кількості аптек у регіоні.
2. Частиною 1 статті 21 Закону України «Про лікарські засоби» визначено, що реалізація (відпуск) препаратів громадянам здійснюється за рецептами та без рецептів лікаря. При цьому, в ч. 1 п. 3 Порядку відпуску лікарських засобів і виробів медичного призначення з аптек та їх структурних підрозділів, затвердженого наказом МОЗ України від 19.07.2005 р. № 360, зазначено, що рецепти на лікарські засоби і вироби медичного призначення виписуються лікарями закладів охорони здоров’я незалежно від форм власності та підпорядкування, згідно з видами медичної практики, на які було видано ліцензію МОЗ України, та відповідно до лікарських посад.
Медичні працівники, які мають право виписувати рецепти, є відповідальними за призначення хворому ліків та додержання правил виписування рецептів згідно із законодавством України. Рецепти виписуються хворому за наявності відповідних показів з обов’язковим записом про призначення лікарських засобів чи виробів медичного призначення в медичній документації (історія хвороби, медична карта амбулаторного чи стаціонарного хворого). Рецепти повинні виписуватись на спеціальному рецептурному бланку з вказанням лікарського засобу за міжнародною непатентованою назвою.
Торговельна назва зазначається, якщо лікарський засіб не має міжнародної непатентованої назви, належить до лікарських засобів біологічного походження, подібних біологічних лікарських засобів (біосимілярів), підлягає предметно-кількісному обліку, відпускається на пільгових умовах чи безоплатно, крім лікарських засобів за переліком міжнародних непатентованих назв лікарських засобів, вартість яких підлягає відшкодуванню, згідно з додатком до постанови Кабінету Міністрів України від 09 листопада 2016 року № 863 «Про запровадження відшкодування вартості лікарських засобів».
Однак, за інформацією Об’єднання організації роботодавців медичної та мікробіологічної промисловості України, на даний час в країні існує тенденція, коли медичні працівники призначають лікарські засоби хворим не на рецептурних бланках, а на папірцях з вказанням торговельних назв препаратів, зазвичай найбільш дороговартісних (що в більшості продиктовано корупційними зв’язками з представниками фармринку). Таким чином, пацієнт позбавлений права вибору аналогічних ліків за найбільш доступною ціною, а лікар офіційно не несе відповідальності за призначення препаратів чи їх надмірної кількості.
Для ілюстрації можна порівняти 2 лікарські засоби, які містять одну й ту саму діючу речовину «desloratadinе» в однаковій пропорції (1 мл сиропу містить 0,5 мг діючої речовини) — «Еріус» (імпортний лікарський засіб) та «Едем» (лікарський засіб вітчизняного виробництва). У цьому випадку «Едем»6 коштує в середньому в 4 рази дешевше за його імпортний аналог «Еріус»5 (55 грн. проти 220 грн. за флакон 60 мл).
З метою реалізації права громадян України на охорону здоров’я держава повинна забезпечити доступність найнеобхідніших лікарських засобів, захист громадян у разі заподіяння шкоди їх здоров’ю внаслідок застосування лікарських засобів за неправильним медичним призначенням лікаря, а також коректність зазначення назв лікарських засобів у рецептах задля забезпечення їх доступності для українців.
5tabletki.ua/%D0%AD%D0%B4%D0%B5%D0%BC/pharmacy/?s=price.
6tabletki.ua/%D0%AD%D1%80%D0%B8%D1%83%D1%81/pharmacy/.
Саме тому законопроектом пропонується створення законодавчої бази для забезпечення раціонального призначення лікарських засобів та підвищення економічної доступності хворих до лікування.
3. Згідно оцінок експертів фармацевтичної галузі, ціни на ліки в Україні інколи на 300% вищі за ціни на аналогічні препарати в сусідніх країнах7.
Експертами, які здійснювали дослідження фармацевтичного ринку України, проведеного в рамках проекту USAID «Лідерство в економічному врядуванні»8, для порівняння цін на лікарські засоби було взято поширені оригінальні препарати (оригінатори) певного виробника, ідентичної форми випуску й упаковки, які вільно продаються в аптечній мережі як в Україні, так і в сусідніх Угорщині та Грузії.
За результатами порівняння встановлено, що ціни на лікарські засоби в сусідніх Угорщині та Грузії подекуди в 2–3, а то й в 4 рази нижчі за ціни в Україні.
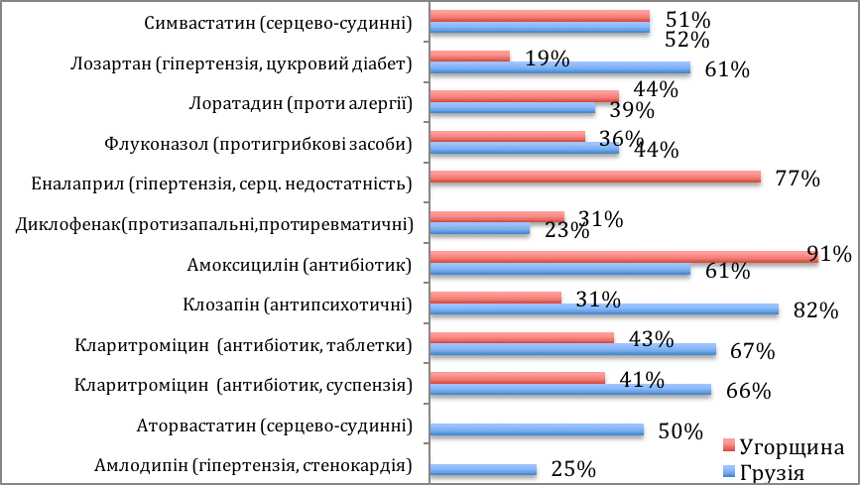
Графік 1. Ціни на оригінатори в Угорщині та Грузії порівняно з Україною (ціна в Україні = 100%)
Окрім того, порівнюючи ціни в аптеках України, Польщі та Білорусії можна дійти наступних вкрай сумних висновків. Наприклад препарат від серцевої недостатності «Мілдронат» в Білорусії коштує 140 грн.9, а в Україні майже вдвічі дорожче — 250 грн.10. Препарат для зниження тиску «Мікардіс» в Польщі коштує 500 грн.11, а в Україні на третину дорожче — 650 грн.12. Кровоспинний засіб «Дицинон» в Білорусії коштує 250 грн.13, а в Україні на 60% дорожче — 400 грн.14. Протиепілептичний препарат «Фінлепсін ретард» в Білорусії коштує 330 грн.15, а в Україні на третину дорожче — 450 грн.16. Препарат для лікування суглобів «Структум» в Польщі коштує 400 грн.17, а в Україні в 2 рази дорожче — 800 грн.18.
При цьому, незважаючи на вищу вартість ліків в Україні, середня заробітна плата українця набагато нижча за заробітні плати робітників в наведених вище країнах. В Україні середня місячна заробітна плата становить в еквіваленті 275 Євро, в Білорусії — 400 Євро, а в Польщі — 1150 Євро.
Крім того, інформація щодо завищених цін на лікарські засоби в Україні також підтверджується й офіційними даними.
Зокрема, Кабінетом Міністрів України з 1 січня 2017 року було запроваджено державне регулювання цін на лікарські засоби, внесені до Національного переліку основних лікарських засобів, які закуповуються або вартість яких відшкодовується (програма «Доступі ліки») за бюджетні кошти.
Міністерству охорони здоров’я України надано повноваження встановлювати референтні ціни на лікарські засоби, в межах яких визначається оптово-відпускна ціна. Крім того, затверджено перелік країн, дані про ціни на лікарські засоби в яких використовуються для встановлення референтних цін — Польща, Словаччина, Чехія, Латвія та Угорщина.
Реєстр ліків, що відшкодовуються державою за урядовою програмою «Доступні ліки», переглядається двічі на рік — у січні та липні. Це робиться задля того, щоб ціни на лікарські засоби були актуальними.
7www.ukrinform.ua/rubric-society/2120433-referentni-cini-na-liki-i-peremoga-nad-maroderami.html.
8https://voxukraine.org/uk/z-dumkoyu-pro-patsienta-zareguliovanist-farmatsevtychnogo-rynku-v-ukraini-ua/#_edn4
9apteka.103.by/mildronat/33252-kapsuly-250-mg-n40/grindeks/minsk/.
10www.add.ua/ua/mildronat-40-kapsuly.html.
11www.doz.pl/apteka/p13874-Micardis_tabletki_80_mg_28_szt.
12www.add.ua/ua/mikardis-80-mg-tabletki-28.html.
13apteka.103.by/ditsinon/38602-tabletki-250-mg-n100/sandoz/minsk/.
14www.add.ua/ua/ditsinon-250mg-100-tabletki.html.
15apteka.103.by/finlepsin-retard/35127-tabletki-400-mg-n50/teva/minsk/.
16www.add.ua/ua/finlepsin-ret-400-mg-50-tabletki.html.
17www.doz.pl/apteka/p21893-Structum_500_mg_kapsulki_60_szt.
18www.add.ua/ua/struktum-500mg-60-kapsuly.html.
В результаті, завдяки референтному ціноутворенню на деякі групи препаратів у програмі «Доступні ліки» ціни знизилися на 60%. В середньому всі виробники знизили ціни на чверть для того, щоб долучитися до програми відшкодування.
Натомість щодо лікарських засобів, які реалізуються через аптечні заклади, регулювання цін не є дієвим. Зокрема, постановою Кабінету Міністрів України № 955 від 17 жовтня 2008 року «Про заходи щодо стабілізації цін на лікарські засоби і медичні вироби» на лікарські засоби, включені до Національного переліку основних лікарських засобів (крім наркотичних, психотропних лікарських засобів, прекурсорів та медичних газів) та обов’язкового мінімального асортименту лікарських засобів для аптечних закладів та фельдшерсько-акушерських пунктів, визначеного Міністерством охорони здоров’я, встановлено граничні постачальницько-збутові надбавки (не вище ніж 10 відсотків, що нараховуються до оптово-відпускної ціни з урахуванням податків та зборів) та граничні торговельні (роздрібні) надбавки (не вище ніж 25 відсотків, що нараховуються до закупівельної ціни з урахуванням податків).
Водночас, у вказаному випадку на відміну від визначення гранчиної вартості ліків за програмою «Доступні ліки» відсутній механізм визначення розрахунку граничних оптово-відпускних цін на основі зовнішніх референтних цін. Це дає можливість постачальникам завищувати вартість ліків ще до нарахування відповідних постачальницько-збутових надбавок та торговельних (роздрібних) надбавок.
Саме тому законопроектом для окремо визначеного урядом переліку лікарських засобів на законодавчому рівні запроваджується механізм визначення граничних оптово-відпускних цін на ліки, що реалізуються через аптечні мережі (за умови, що вони включені до Національного переліку основних лікарських засобів), близький по суті до відповідного механізму визначення цін на ліки в програмі «Доступні ліки».
Наслідками високих цін на ліки для населення є неспроможність більшості українських громадян купувати необхідні для відновлення здоров’я препарати та ефективно долати ті хвороби, які лікуються медикаментозно.
Слід зазначити, що відповідна практика обмеження постачальницьких (Wholesaler mark-up) та роздрібних (Pharmacists mark-up) надбавок на ліки також застосовується в країнах Європейського союзу19.
Наприклад, в Австрії розміри надбавок залежать від цін виробників і можуть становити 7%–15,5% для постачальницьких надбавок та 3,9%–37% для аптечних мереж. У Франції постачальницькі надбавки становлять 6,68% від ціни виробника але не можуть бути меншими за 0,3 євро та більшими за 30 євро. В Німеччині постачальницькі надбавки становлять 3,15% (але максимум 38 євро). В Греції постачальницькі надбавки становлять 4,9% якщо ціна виробника менша за 200 євро та 1,5% якщо більша за 200 євро, для аптек надбавки варіюються від 2% до 30%. В Італії постачальник отримує 3% надбавку, а аптечна мережа — від 11% до 27%.
4. Як зазначалось раніше, у квітні 2017 року за наполяганням Олега Ляшка та фракції Радикальної партії Уряд започаткував роботу програми «Доступні ліки». З цього часу пацієнти з серцево-судинними захворюваннями, бронхіальною астмою чи діабетом ІІ типу мали можливість отримати ліки безоплатно або з незначною доплатою. За перший рік роботи повну або часткову компенсацію лікарських засобів отримали 8 млн людей20, було виписано 15,5 млн рецептів та відшкодовано вартість ліків на суму в майже 708 млн грн.21. На фінансування програми «Доступні ліки» на 2019 рік передбачено виділення 1 млрд грн.
19apps.who.int/medicinedocs/documents/s23163en/s23163en.pdf
20www.kmu.gov.ua/ua/news/programoyu-dostupni-liki-skoristalisya-vzhe-ponad-8-mln-lyudej-volodimir-grojsman
21moz.gov.ua/uploads/0/4379-dl_rik_4_04_18.pdf
Водночас, обсяги бюджетного фінансування програми «Доступні ліки» є нікчемно малими в порівнянні з загальними витратами українців на закупівлю ліків в аптеках. Так, згідно дослідження, проведеного за підтримки Міжнародного фонду «Відродження»22 в 2017 році в українських аптеках було реалізовано ліків на суму, що перевищує 54 млрд грн. Тобто програма «Доступні ліки» перекриває потребу українців в ліках лише на 2%. Крім цього, й недостатньою є кількість нозологій, які включені до вищевказаної програми.
Разом з тим, відповідно до статті 8 Закону України «Основи законодавства про охорону здоров’я» та статті 10 Закону України «Про державні фінансові гарантії медичного обслуговування населення» оплаті за рахунок коштів Державного бюджету України підлягають лікарські засоби, які включені до Національного переліку основних лікарських засобів.
Саме тому з метою зниження рівня захворюваності та гарантованого надання медичної допомоги, забезпечення населення якісними, ефективними, безпечними та доступними лікарськими засобами законопроектом пропонується розширити програму «Доступні ліки» наступними нозологіями:
- противірусні лікарські засоби;
- антибактеріальні лікарські засоби;
- антианемічні лікарські засоби;
- лікарські засоби, що впливають на функцію шлунково-кишкового тракту;
- лікарські засоби, що застосовуються при депресивних розладах.
За розрахунками Об’єднання організації роботодавців медичної та мікробіологічної промисловості України, для реалізації даної пропозиції необхідно передбачати додаткові видатки на урядову програму «Доступні ліки» в сумі близько 1,27 млрд грн.
Розширення програми «Доступні ліки» вищенаведеними нозологіями дозволить охопити додатково близько 20 млн громадян і забезпечити широкий доступ українців до безкоштовних ліків.
Для фінансового забезпечення розширення програми «Доступні ліки» пропонується передбачити щорічний обсяг коштів Державного бюджету України, які спрямовуються на фінансування відшкодування вартості лікарських засобів за програмою «Доступні ліки», на рівні не менше 0,25% від обсягу видатків, що передбачені законом про Державний бюджет України на відповідний рік.
Відповідно до проекту Державного бюджету України на 2019 рік, 0,25% від обсягу видатків становить більше 2,5 млрд грн. Тобто вказана норма дозволить збільшити фінансування програми «Доступні ліки» в 2,5 рази та забезпечити безкоштовними лікарськими засобами 5% попиту населення на ліки.
5. За підсумками розширеного засідання правління Об’єднання організацій роботодавців медичної та мікробіологічної промисловості України, яке відбулось 06 червня 2018 pоку, було прийнято консолідоване рішення стосовно необхідності скасування дискримінаційної норми щодо інтелектуальної власності на лікарські засоби, термін дії патентів яких вийшов. Це обумовлено наступним.
Частиною четвертою статті 6 Закону України «Про охорону прав на винаходи і корисні моделі» дозволено продовжувати термін патентного захисту ще на 5 років на додачу до 20-річного терміну на оригінальний лікарський засіб.
У результаті, перед українськими компаніями виникають серйозні перепони на шляху виведення на ринок перших генериків. Повний цикл розробки і реєстрації генерика тривалий і зазвичай становить 4–5 років.
Тому якщо своєчасно не розпочати їх розробку, цим скористаються закордонні конкуренти, які виведуть на український ринок схожий, але дорожчий за ціною препарат. А кінцевий споживач і держбюджет переплачуватиме за імпортні ліки через недобросовісні умови конкуренції.
22drive.google.com/file/d/1_KM6Odn0aDvbcK9NpRG8j_EtmvbXsF-a/view.
Крім того, у 2012 році статтю 9 Закону України «Про лікарські засоби» було доповнено наступними нормами: «Якщо лікарський засіб, зареєстрований на підставі поданої у повному обсязі (повної) реєстраційної інформації (далі — референтний/оригінальний лікарський засіб), зареєстровано в Україні вперше, державна реєстрація іншого лікарського засобу, що містить ту саму діючу речовину, що й референтний/оригінальний лікарський засіб, можлива не раніше ніж через п’ять років з дня першої реєстрації референтного/оригінального лікарського засобу в Україні».
З цього моменту вітчизняні фармацевтичні виробники втратили право розробляти, реєструвати і виводити на ринок перші генерики впродовж усього п’ятирічного терміну ексклюзивності, який був «подарований» транснаціональним корпораціям.
Відтоді після закінчення 20-річного терміну патентного захисту на оригінальну молекулу згадані компанії могли продовжувати отримувати надприбутки ще 5 років. Цей п’ятирічний термін ексклюзивності є частиною угоди «TRIPS+».
Імплементація дискримінаційного положення «TRIPS+» у національне законодавство дозволило фармацевтичним корпораціям і надалі посідати монопольне становище на ринку, отримуючи надприбутки.
Приклад23 щодо негативних наслідків від такої законодавчої норми наводить заступник Міністра охорони здоров’я України Роман Ілик:
«…на закупівлю життєво необхідного комбінованого препарату Лопінавір/Ритоновір Україна витрачає понад 50% фінансування, яке виділяється на закупівлю антиретровірусних препаратів для лікування ВІЛ/СНІД. Цей лікарський засіб захищають два вторинні патенти: «на похідну речовину» та «метод лікування».
Ці патенти створили штучну монополію на препарат до 2026 року. Натомість дія первинного патенту закінчилась ще у 2016 році, що мало дати можливість вже у 2017-му році закуповувати альтернативні генеричні препарати у 5 разів дешевше.
Фіксована ціна Лопінавіру оригінального у 2017 році становила 60,8 доларів за упаковку. Натомість вартість іноземного генеричного — лише 12 доларів.
Загалом, минулого року на закупівлю цього препарату з державного бюджету було витрачено майже 11 мільйонів 673 тисячі доларів.
Якщо б не дія патенту, на закупівлі такої ж кількості упаковок вдалося б зберегти майже 9 мільйонів 370 тисяч доларів і, таким чином, охопити лікуванням більшу кількість хворих.»
Маючи можливість розробити і зареєструвати вітчизняний генерик, можливо було б забезпечити його нижчу вартість, а зекономлені бюджетні кошти направити на інші потреби програми або на інші програми.
Поправка «TRIPS+», істотно сповільнює виведення на фармацевтичний ринок доступніших за ціною і якісних генериків. Не випадково СОТ радить країнам, що розвиваються, бути обережними стосовно застосування у своєму законодавстві більш жорстких положень, ніж цього вимагає, власне, угода TRIPS.
Саме тому законопроектом пропонується усунути дискримінаційні бар’єри для українських фармацевтичних компаній, значно обмеживши можливість одержання додаткового патентного захисту на ліки, а також ексклюзивного захисту на оригінальні лікарські засоби.
Реалізація вищевказаних положень законопроекту дозволить забезпечити значне зниження вартості основних лікарських засобів в аптечних закладах України (щонайменше на чверть, а подекуди — в рази), залучити до програми «Доступні ліки» додатково 20 млн громадян України, забезпечити населення країни більшою кількістю якісних, безпечних та економічно доступних лікарських засобів вітчизняного виробництва, створити та впровадити у виробництво нову номенклатуру відсутніх у достатній кількості на вітчизняному ринку ліків.
23life.pravda.com.ua/columns/2018/02/6/228825/.
2. Мета і шляхи її досягнення
Метою даного законопроекту є законодавча імплементація комплексного плану, спрямованого на значне зниження вартості основних лікарських засобів в аптечних закладах України, забезпечення широкого кола громадян безкоштовними ліками за програмою «Доступні ліки», забезпечення населення країни якісними, безпечними та економічно доступними лікарськими засобами вітчизняного виробництва, а також розвиток вітчизняної фармацевтичної індустрії.
З цією метою законопроектом пропонується вжиття наступних заходів:
1. Демонополізувати мережі аптечних закладів. Це ліквідує практику вимагання аптеками «агентських платежів» в розмірі 30–40% від вартості лікарського засобу (за експертними оцінками) за потрапляння в мережу, які в кінцевому випадку сплачують споживачі. Крім того, вказаний захід убезпечить аптечні заклади малого та середнього бізнесу від поглинання та знищення.
2. Встановити жорсткий контроль та посилену відповідальність за порушення правил виписування рецептів. Зокрема, штраф 850 грн. лікарю за зазначення в рецепті торговельної назви препарату замість міжнародної непатентованої назви. Це дозволить знищити корупційні схеми, вибудовані фармкомпаніями з лікарями та зробити ліки доступнішими для українців. Адже вартість препаратів, що містять ідентичну діючу речовину (і в ідентичній пропорції) може відрізнятись в рази залежно від виробника. Для прикладу, вартість флакону 60 мл вітчизняного лікарського засобу «Едем» коштує в середньому в 4 рази дешевше за його імпортний аналог лікарський засіб «Еріус».
3. Запровадити дієвий механізм обмеження цін на ліки, що реалізуються через аптечні мережі (згідно переліку, визначеного КМУ), близький по суті до відповідного механізму в програмі «Доступні ліки». Зокрема, пропонується обмежити граничні постачальницько-збутові надбавки на рівні не більшому за 10% (сьогодні так само 10%), та граничні торговельні (роздрібні) надбавки на рівні не більшому за 15% (сьогодні 25%), а також запровадити механізм визначення граничної оптово-відпускної ціни на основі референтного ціноутворення (сьогодні такий механізм присутній лише в програмі «Доступні ліки»). Очікується середнє зниження вартості ліків в аптеках принаймні на чверть. Адже згідно інформації уряду, завдяки референтному ціноутворенню на деякі групи препаратів у програмі «Доступні ліки»у ціни знизилися на 60%. В середньому всі виробники знизили ціни на чверть для того, щоб долучитися до програми відшкодування.
Крім того, пропонується ввести посилену адміністративну відповідальність за порушення правил ціноутворення на лікарські засоби (від 17 тис. грн. до 68 тис. грн.).
4. Розширити програму «Доступні ліки». Забезпечити повне або часткове відшкодування вартості, на додачу до вже передбачених лікарських засобів (від серцево-судинних захворювань, діабету, бронхіальної астми), противірусних лікарських засобів, антибактеріальних лікарських засобів, антианемічних лікарських засобів, лікарських засобів, що впливають на функцію шлунково-кишкового тракту, лікарських засобів, що застосовуються при депресивних розладах.
За оцінками Об’єднання організацій роботодавців медичної та мікробіологічної промисловості України, розширення програми «Доступні ліки» вищенаведеними нозологіями дозволить охопити додатково близько 20 млн громадян і забезпечити широкий доступ українців до безкоштовних ліків.
5. Усунути дискримінаційні бар’єри для українських фармацевтичних компаній, обмеживши можливість одержання додаткового патентного захисту на ліки, а також ексклюзивного захисту на оригінальні лікарські засоби. Це дасть можливість вітчизняним фармкомпаніям розробляти і реєструвати вітчизняні генерики, які були б набагато дешевші (іноді на порядок) за оригінальні іноземні препарати.
Крім того, з метою забезпечення комплексного здешевлення ліків для громадян та забезпечення розвитку повинен розглядатися одночасно із пов’язаними з ним проектом Закону України «Про внесення змін до Бюджетного кодексу України щодо щодо забезпечення безкоштовними лікарськими засобами громадян» та проектом Закону України «Про внесення змін до Податкового кодексу України щодо комплексного здешевлення ліків для громадян та забезпечення розвитку вітчизняної фармацевтичної галузі», якими також пропонується:
1. Зменшити спеціальну ставку податку на додану вартість для операцій з постачання на митній території України та ввезення на митну територію України лікарських засобів з 7% до 0%. Це гарантуватиме зниження вартості лікарських засобів щонайменше на 6,5%.
2. Збільшити фінансування програми «Доступні ліки» до 0,25% від обсягу видатків, що передбачені законом про Державний бюджет України на відповідний рік. Відповідно до проекту Державного бюджету України на 2019 рік, 0,25% від обсягу видатків становить більше 2,5 млрд грн. Тобто вказана норма дозволить збільшити фінансування програми «Доступні ліки» в 2,5 рази та забезпечити 5% попиту населення на ліки безкоштовними лікарськими засобами.
3. Скасувати квотування отримання спирту вітчизняними фармкомпаніями для виробництва лікарських засобів. Вказана норма усуне корупційні ризики та створить передумови для забезпечення населення країни більшою кількістю якісних, безпечних та економічно доступних лікарських засобів вітчизняного виробництва, створення та впровадження у виробництво нової номенклатури відсутніх у достатній кількості на вітчизняному ринку ліків.

Мал. 1. Комплексний план щодо здешевлення лікарських засобів в Україні
3. Загальна характеристика і основні положення законопроекту
Проектом Закону пропонується внести зміни до наступних законодавчих актів.
2. У Законі України «Про лікарські засоби»:
- визначити поняття: аптечна мережа, Національний перелік основних лікарських засобів, оптово-відпускна ціна лікарського засобу, гранична оптово-відпускна ціна лікарського засобу, зовнішнє референтне ціноутворення, мінімальна оптово-відпускна ціна, внутрішнє референтне ціноутворення;
- встановити, що кожна аптечна мережа за кількістю торговельних точок не може займати більше ніж два відсотки від загальної кількості зареєстрованих аптек та їх структурних підрозділів у межах Автономної Республіки Крим, області, міста Києві чи Севастополя;
- усунути дискримінаційні бар’єри для українських фармацевтичних компаній в частині патентного захисту на ліки;
- визначити принципи державного регулювання цін на ліки;
- зобов’язати Кабінет Міністрів України визначити окремий перелік лікарських засобів та встановити для нього граничну постачальницько-збутову надбавку на рівні не більшому за 10% та граничну торговельну (роздрібну) надбавку на рівні не більшому за 15%;
- розширити програму «Доступні ліки» шляхом відшкодування вартості, на додачу до вже передбачених лікарських засобів (від серцево-судинних захворювань, діабету, бронхіальної астми), противірусних лікарських засобів, антибактеріальних лікарських засобів, антианемічних лікарських засобів, лікарських засобів, що впливають на функцію шлунково-кишкового тракту, лікарських засобів, що застосовуються при депресивних розладах;
- збільшити фінансування програми «Доступні ліки» до 0,25% від обсягу видатків, що передбачені законом про Державний бюджет України на відповідний рік.
3. У Законі України «Про захист економічної конкуренції»:
- визначити одним із видів порушенням законодавства про захист економічної конкуренції порушення вимог щодо чисельності торговельних точок аптечної мережі, передбаченої законодавства про лікарські засоби;
- передбачити за вищевказане порушення штраф у розмірі до п’яти відсотків доходу (виручки) суб’єкта господарювання від реалізації продукції (товарів, робіт, послуг) за останній звітний рік, що передував року, в якому накладається штраф.
4. У Кодексі України про адміністративні правопорушення:
- підвищити адміністративну відповідальність за продаж лікарських засобів в аптечних закладах без рецепта у заборонених законодавством випадках;
- запровадити адміністративну відповідальність за порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення, в тому числі зазначення в рецепті торговельної назви лікарського засобу у випадках, заборонених законодавством;
- запровадити адміністративну відповідальність за порушення законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби.
5. У Законі України «Про охорону прав на винаходи і корисні моделі»:
- усунути дискримінаційні бар’єри для українських фармацевтичних компаній;
6. У Законі України «Про ціни і ціноутворення» надати повноваження Кабінету Міністрів України встановлювати граничні оптово-відпускні ціни на лікарські засоби, граничні постачальницько-збутові надбавки на лікарські засоби, а також граничні торговельні (роздрібні) надбавки на лікарські засоби, відповідно до законодавства.
4. Стан нормативно-правової бази у даній сфері правового регулювання
Основними нормативно-правовими актами у даній сфері є Конституція України, Кодекс України про адміністративні правопорушення, Закон України «Основи законодавства про охорону здоров’я», Закон України «Про державні фінансові гарантії медичного обслуговування населення», Закон України «Про лікарські засоби», Закон України «Про захист економічної конкуренції», Закон України «Про охорону прав на винаходи і корисні моделі», Закон України «Про ціни і ціноутворення».
Прийняття даного законопроекту не потребує внесення змін до інших Законів України.
5. Фінансово-економічне обґрунтування
На момент внесення реалізація проекту Закону не потребує додаткових витрат з Державного бюджету.
6. Прогноз соціально-економічних та інших наслідків прийняття законопроекту
Прийняття даного законопроекту дозволить забезпечити значне зниження вартості основних лікарських засобів в аптечних закладах України (щонайменше на чверть, а подекуди в рази), залучити до програми «Доступні ліки» додатково 20 млн громадян України, забезпечити населення країни якісними, безпечними та економічно доступними лікарськими засобами вітчизняного виробництва, створити та впровадити у виробництво нову номенклатуру відсутніх у достатній кількості на вітчизняному ринку ліків.
Народні депутати УкраїниО.В. Ляшко
В.В. Галасюк
В.І. Вовк
О.М. Кириченко
А.В. Кошелєва
М.Ю. Бурбак
В.Л. Заружко
М.В. Довбенко
О.Г. Домбровський
О.В. Кужель
А.М. Гіршфельд
Л.П. Козаченко
Є.Ю. Рибчинський
М.В. Єфімов
А.Ю. Геращенко
О.С. Мусій
В.В. Амельченко
Д.В. Лінько
С.В. Рибалка
Проект
зареєстрований в Парламенті
06.12.2018 р. за № 9372
ЗАКОН УКРАЇНИ
«Зробимо ліки дешевшими!» (про внесення змін до деяких законодавчих актів України щодо комплексного здешевлення ліків для громадян та забезпечення розвитку вітчизняної фармацевтичної галузі)
Верховна Рада України постановляє:
І. Внести зміни до таких законодавчих актів України:
1. В Законі України «Про лікарські засоби» (Відомості Верховної Ради України (ВВР), 1996, № 22, ст. 86):
1) Частину першу статті 2 доповнити новими абзацами такого змісту:
«аптечна мережа — сукупність аптек (їх структурних підрозділів), що мають одного і того ж кінцевого бенефіціарного власника (контролера). Кожна аптечна мережа за кількістю аптек (їх структурних підрозділів) не може займати більше ніж два відсотки від загальної кількості зареєстрованих аптек (їх структурних підрозділів) у межах Автономної Республіки Крим, області, міста Києва чи Севастополя.
Національний перелік основних лікарських засобів — визначений Кабінетом Міністрів України перелік лікарських засобів, що в установленому законом порядку зареєстровані в Україні, та які підлягають закупівлі закладами і установами охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів;
перелік лікарських засобів, на які поширюється зовнішнє референтне ціноутворення — визначений Кабінетом Міністрів України перелік лікарських засобів, для яких з врахуванням вимог цього Закону обов’язково встановлюється (в тому числі при реалізації через аптечну мережу та/або аптеки та їх структурні підрозділи) гранична оптово-відпускна ціна, гранична постачальницько-збутова надбавка та гранична торгівельна (роздрібна) надбавка;
гранична оптово-відпускна ціна лікарського засобу — максимальна оптово-відпускна вартість лікарського засобу в Україні, визначена на основі зовнішнього референтного ціноутворення без урахування постачальницько-збутових та торговельних (роздрібних) надбавок та податку на додану вартість;
зовнішнє референтне ціноутворення — гранична оптово-відпускна ціна лікарського засобу в Україні, встановлена у порядку, визначеному Кабінетом Міністрів України, на основі оптово-відпускних цін аналогічного лікарського засобу, установлених у референтних країнах. Перелік референтних країн визначається Кабінетом Міністрів України.»;
2) Частини дванадцяту і тринадцяту статті 9 замінити трьома частинами такого змісту:
«Якщо лікарський засіб, містить нову активну діючу речовину (активний фармацевтичний інгредієнт) і пройшов повний цикл доклінічних та клінічних досліджень, та зареєстрований в Україні на підставі повної реєстраційної інформації (далі — референтний/оригінальний лікарський засіб), державна реєстрація іншого лікарського засобу, що містить ту саму діючу речовину, що й референтний/оригінальний лікарський засіб, можлива не раніше ніж через п’ять років з дня першої реєстрації референтного/оригінального лікарського засобу в Україні, якщо заява про державну реєстрацію в Україні референтного/оригінального лікарського засобу подана протягом двох років з дня його першої реєстрації в будь-якій країні.
Зазначена вимога не поширюється на випадки, коли заявник відповідно до закону одержав право посилатися та/або використовувати реєстраційну інформацію референтного/оригінального лікарського засобу або подав власну повну реєстраційну інформацію, що відповідає вимогам до реєстраційної інформації референтного/оригінального лікарського засобу, а також у разі видачі Кабінетом Міністрів України дозволу на використання запатентованого винаходу (корисної моделі), що стосується такого лікарського засобу, або у разі необхідності вчинення дій за надзвичайних обставин, які згідно із законодавством України у сфері інтелектуальної власності не визнаються порушенням прав власника патенту на винахід, що стосується такого лікарського засобу, або якщо судом або іншим уповноваженим законом органом встановлено, що власник права інтелектуальної власності зловживав своїми правами, зокрема монопольним (домінуючим) становищем на ринку.
Вимоги цієї статті не виключають права іншого заявника (виробника) здійснювати упродовж строку дії патенту відповідну розробку та випробування, у тому числі проводити дослідження з біо- або терапевтичної еквівалентності між генеричним та референтними лікарським засобом тощо.»
У зв’язку з цим, частини чотирнадцяту — двадцять сьому вважати відповідно частинами п’ятнадцятою — двадцять восьмою;
3) Доповнити новим Розділом VI1 такого змісту:
«Розділ VI1
ЗАБЕЗПЕЧЕННЯ ДОСТУПНОСТІ ЛІКАРСЬКИХ ЗАСОБІВ
Стаття 231. Ціни на лікарські засоби
Державна цінова політика щодо лікарських засобів спрямована на забезпечення соціальних гарантій населенню та необхідних економічних гарантій для виробників лікарських засобів.
Стаття 232. Державне регулювання цін
Граничні оптово-відпускні ціни на лікарські засоби, граничні постачальницько-збутові надбавки на лікарські засоби, а також граничні торговельні (роздрібні) надбавки на лікарські засоби, встановлюються у випадках, визначених законодавством та в порядку, визначеному Кабінетом Міністрів України.
Кабінетом Міністрів України щороку визначається перелік лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, та для яких обов’язково встановлюється (в тому числі при реалізації через аптечну мережу та/або аптеки та їх структурні підрозділи):
гранична оптово-відпускна ціна;
гранична постачальницько-збутова надбавка, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням податків та зборів, та яка не може бути більшою ніж 10 відсотків;
гранична торгівельна (роздрібна) надбавка, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням граничної постачальницько-збутової надбавки, а також з урахуванням податків та зборів, та яка не може бути більшою ніж 15 відсотків.
Оптово-відпускна ціна в Україні для лікарських засобів з переліку лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, не може перевищувати граничну оптово-відпускну ціну.
Центральний орган виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я, веде, розміщує та щоквартально оновлює на своєму офіційному веб-сайті реєстр оптово-відпускних цін на лікарські засоби з переліку лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, в порядку визначеному Кабінетом Міністрів України.
Інформація про оптово-відпускні ціни на лікарські засоби з переліку лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, вноситься на підставі щоквартального подання власником або уповноваженим представником власника реєстраційного посвідчення на лікарський засіб інформації в обсязі, визначеному центральним органом виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я.
Стаття 23–3. Відшкодування вартості лікарських засобів
Держава забезпечує повне або часткове відшкодування вартості лікарських засобів у випадках, визначених цією, статтею суб’єктам господарювання, які провадять господарську діяльність на підставі ліцензії на провадження господарської діяльності з роздрібної торгівлі лікарськими засобами, незалежно від форми власності та підпорядкування, аптечні заклади яких розташовані в межах відповідної адміністративно-територіальної одиниці в порядку, визначеному Кабінетом Міністрів України.
Повне або часткове відшкодування вартості лікарських засобів здійснюється в межах затвердженого центральним органом виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я, розміру відшкодування вартості лікарських засобів, що включені до Реєстру лікарських засобів, вартість яких підлягає відшкодуванню, що затверджується центральним органом виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я.
Відпуск лікарських засобів здійснюється виключно на підставі рецептів, виписаних закладами охорони здоров’я незалежно від форми власності за місцем надання медичної допомоги пацієнту на рецептурних бланках. Рецепт зберігається у суб’єкта господарювання протягом трьох років з моменту відпуску.
Повне або часткове відшкодування вартості лікарських засобів здійснюється під час амбулаторного лікування осіб, що страждають на серцево-судинні захворювання, діабет (цукровий і нецукровий) бронхіальну астму, а також лікарських засобів, що використовуються під час трансплантації у доопераційний та післяопераційний періоди, противірусних лікарських засобів, антибактеріальних лікарських засобів, антианемічних лікарських засобів, лікарських засобів, що впливають на функцію шлунково-кишкового тракту, лікарських засобів, що застосовуються при депресивних розладах, що включені до Національного переліку основних лікарських засобів.
Центральний орган виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я, окрім визначеного цією статтею переліку захворювань та/або лікарських засобів, за якими здійснюється повне або часткове відшкодування вартості лікарських засобів, може затвердити додатковий перелік захворювань та/або лікарських засобів, за якими здійснюється повне або часткове відшкодування вартості лікарських засобів.
Стаття 234. Фінансування відшкодування вартості лікарських засобів
Фінансування відшкодування вартості лікарських засобів, передбачене статтею 23–3 цього Закону, здійснюється за рахунок Державного бюджету України.
Щорічний обсяг коштів Державного бюджету України, які спрямовуються на фінансування відшкодування вартості лікарських засобів, передбачене статтею 23–3 цього Закону, становить не менше 0,25% від обсягу видатків, що передбачені законом про Державний бюджет України на відповідний рік.»;
4) Статтю 24 доповнити новою частиною такого змісту:
«Фінансування відшкодування вартості лікарських засобів, здійснюється у відповідності до статті 23–3 цього Закону.»;
5) Статтю 27 доповнити новою частиною другою такого змісту:
«Порушення вимог щодо чисельності аптек (їх структурних підрозділів) аптечної мережі, передбаченої статтею 2 цього Закону, тягне за собою відповідальність, встановлену законодавством про захист економічної конкуренції.».
2. В Законі України «Про захист економічної конкуренції» (Відомості Верховної Ради України (ВВР), 2001, № 12, ст.64):
1) Статтю 50 доповнити новим пунктом 21 такого змісту:
«21) порушення вимог щодо чисельності аптек (їх структурних підрозділів) аптечної мережі, передбаченої законодавством про лікарські засоби.»;
2) В абзаці третьому частини другої статті 52:
слова та цифри «12 та 19» замінити словами та цифрами «12, 19 та 21».
3. В Кодексі України про адміністративні правопорушення (Відомості Верховної Ради Української РСР (ВВР) 1984, додаток до № 51, ст.1122):
1) В статті 424 :
в абзаці другому слова «від шести до двадцяти п’яти» замінити словами «від п’ятдесяти до ста»
в абзаці четвертому слова «від двадцяти п’яти до сімдесяти» замінити словами «від ста до двохсот»;
2) Доповнити новою статтею 425 наступного змісту:
«Стаття 425. Порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення
Порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення, в тому числі зазначення в рецепті торгівельної назви лікарського засобу, у випадках заборонених законодавством, —
тягне за собою накладення штрафу від п’ятдесяти до ста неоподатковуваних мінімумів доходів громадян.
Повторне протягом року вчинення порушення, передбаченого частиною першою цієї статті, за яке особу вже було піддано адміністративному стягненню, —
тягне за собою накладення штрафу від ста до двохсот неоподатковуваних мінімумів доходів громадян.»;
3) Доповнити новою статтею 1656 наступного змісту:
«Стаття 1656. Порушення законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби
Порушення законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби —
тягне за собою накладення штрафу на посадових осіб від однієї тисячі до двох тисяч неоподатковуваних мінімумів доходів громадян.
Повторне протягом року вчинення порушення, передбаченого частиною першою цієї статті, за яке особу вже було піддано адміністративному стягненню, —
тягне за собою накладення штрафу від двох до чотирьох тисяч неоподатковуваних мінімумів доходів громадян.»;
4) Частину першу статті 2445 викласти у такій редакції:
«Центральний орган виконавчої влади, що реалізує державну політику з контролю за цінами, розглядає справи про адміністративні правопорушення, пов’язані з порушенням порядку формування, встановлення та застосування цін і тарифів, порушенням законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби, а також невиконанням законних вимог посадових осіб зазначеного органу (статті 165–2, 165–6, 188–3).»;
5) У частині першій статті 2448 після слів «з продажем лікарських засобів без рецепта у заборонених законодавством випадках (стаття 42–4),» доповнити словами «з порушенням встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення (стаття 42–5),».
4. В Законі України «Про охорону прав на винаходи і корисні моделі» (Відомості Верховної Ради України (ВВР), 1994, № 7, ст. 32):
1) абзац п’ятий частини четвертої статті 6 виключити;
2) доповнити новою статтею 271 такого змісту:
«Стаття 271. Додаткова охорона прав на винаходи
1. Володілець патенту на винахід, об’єктом якого є активний фармацевтичний інгредієнт лікарського засобу, процес отримання лікарського засобу або застосування лікарського засобу, засіб захисту тварин, засіб захисту рослин, введення в обіг якого в Україні дозволяється відповідним компетентним органом згідно з чинним законодавством України, має право на подовження строку чинності майнових прав інтелектуальної власності на такий винахід (додаткова охорона), яке засвідчується сертифікатом додаткової охорони.
Сертифікат додаткової охорони видається за клопотанням володільця патенту. За подання клопотання сплачується збір.
Права на додаткову охорону обмежені продуктом (активним фармацевтичним інгредієнтом або сукупністю активних фармацевтичних інгредієнтів лікарського засобу), введення в обіг якого в Україні дозволено відповідним компетентним органом згідно з чинним законодавством України, та його застосуванням відповідно, як лікарського засобу, засобу захисту тварин, засобу захисту рослин, у межах прав, що надавалися відповідним патентом на момент подання клопотання про видачу сертифікату додаткової охорони, та є чинними за умови чинності такого дозволу.
2. Строк додаткової охорони дорівнює періоду між датою подання заявки до Установи та датою одержання володільцем патенту першого дозволу компетентного органу, зменшеному на 5 років.
Строк додаткової охорони не може бути більшим ніж 5 років.
Для винаходу, об’єктом якого є активний фармацевтичний інгредієнт лікарського засобу, та стосовно якого були здійснені дослідження у сфері застосування для дітей, результати яких відображені в інформації про лікарський засіб, на який видано дозвіл відповідного компетентного органу, зазначені в абзацах першому та другому цієї частини строки додаткової охорони збільшуються на шість місяців.
3. Клопотання має надійти до Установи протягом 6 місяців від дати публікації відомостей про державну реєстрацію винаходу або від дати видачі першого дозволу відповідного компетентного органу, залежно від того, яка з цих дат є пізнішою. До клопотання мають бути додані документи, що підтверджують право володільця патенту на додаткову охорону.
Клопотання розглядається закладом експертизи в порядку, що визначається центральним органом виконавчої влади, що забезпечує формування державної політики у сфері інтелектуальної власності.
4. У разі, якщо подані документи підтверджують право володільця патенту на додаткову охорону, Установа здійснює державну реєстрацію додаткової охорони шляхом внесення до Реєстру відповідних відомостей. Одночасно з державною реєстрацією додаткової охорони Установа здійснює публікацію в Бюлетені визначених нею відомостей про таку реєстрацію. Видача сертифікату додаткової охорони здійснюється Установою у місячний строк після державної реєстрації додаткової охорони.
5. Права та обов’язки володільця сертифікату додаткової охорони є такими самими, що і права володільця відповідного патенту з урахуванням обмежень, встановлених частиною першою цієї статті.
6. За підтримання чинності сертифікату додаткової охорони сплачується збір за кожен повний чи неповний рік його дії. Порядок сплати зборів за підтримання чинності сертифікату додаткової охорони є таким самим, як визначено в частині другій статті 32 цього Закону.
7. Порядок припинення дії сертифікату додаткової охорони та визнання його недійсним, захисту прав володільця сертифікату додаткової охорони є такими самими, як і щодо відповідного патенту.».
5. Частину першу статті 5 Закону України «Про ціни і ціноутворення» (Відомості Верховної Ради (ВВР), 2013, № 19–20, ст. 190) доповнити новим пунктом четвертим такого змісту:
«4) встановлює граничні оптово-відпускні ціни на лікарські засоби, граничні постачальницько-збутові надбавки на лікарські засоби, а також граничні торговельні (роздрібні) надбавки на лікарські засоби, відповідно до законодавства.».
ІІ. Прикінцеві положення
1.1. Цей Закон набирає чинності з дня, наступного за днем його опублікування, та вводиться в дію з 1 січня 2019 року.
2. Кабінету Міністрів України у місячний строк з дня набрання чинності цим Законом:
привести свої нормативно-правові акти у відповідність із цим Законом;
забезпечити приведення міністерствами, іншими центральними органами виконавчої влади їх нормативно-правових актів у відповідність із цим Законом.
Голова Верховної Ради України А.В. Парубій
ПОРІВНЯЛЬНА ТАБЛИЦЯ
«Зробимо ліки дешевшими!» (про внесення змін до деяких законодавчих актів України щодо комплексного здешевлення ліків для громадян та забезпечення розвитку вітчизняної фармацевтичної галузі)
| Зміст положення (норми) чинного законодавства | Зміст відповідного положення (норми) проекту акта |
|---|---|
| Закон України «Про лікарські засоби» (Відомості Верховної Ради України (ВВР), 1996, № 22, ст. 86) | |
| Стаття 2. Визначення термінівУ законодавстві про лікарські засоби терміни вживаються у такому значенні: |
Стаття 2. Визначення термінівУ законодавстві про лікарські засоби терміни вживаються у такому значенні:… аптечна мережа — сукупність аптек (їх структурних підрозділів), що мають одного і того ж кінцевого бенефіціарного власника (контролера).Кожна аптечна мережа за кількістю аптек (їх структурних підрозділів) не може займати більше ніж два відсотки від загальної кількості зареєстрованих аптек (їх структурних підрозділів) у межах Автономної Республіки Крим, області, міста Києва чи Севастополя. … Національний перелік основних лікарських засобів — визначений Кабінетом Міністрів України перелік лікарських засобів, що в установленому законом порядку зареєстровані в Україні, та які підлягають закупівлі закладами і установами охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів. … перелік лікарських засобів, на які поширюється зовнішнє референтне ціноутворення — визначений Кабінетом Міністрів України перелік лікарських засобів, для яких з врахуванням вимог цього Закону обов’язково встановлюється (в тому числі при реалізації через аптечну мережу та/або аптеки та їх структурні підрозділи) гранична оптово-відпускна ціна, гранична постачальницько-збутова надбавка та гранична торгівельна (роздрібна) надбавка. … гранична оптово-відпускна ціна лікарського засобу — максимальна оптово-відпускна вартість лікарського засобу в Україні, визначена на основі зовнішнього референтного ціноутворення без урахування постачальницько-збутових та торговельних (роздрібних) надбавок та податку на додану вартість; зовнішнє референтне ціноутворення — гранична оптово-відпускна ціна лікарського засобу в Україні, встановлена у порядку, визначеному Кабінетом Міністрів України, на основі оптово-відпускних цін аналогічного лікарського засобу, установлених у референтних країнах. Перелік референтних країн визначається Кабінетом Міністрів України; |
| Стаття 9 Державна реєстрація лікарських засобів | Стаття 9 Державна реєстрація лікарських засобів |
| … Якщо лікарський засіб, зареєстрований на підставі поданої в повному обсязі (повної) реєстраційної інформації (далі — референтний/оригінальний лікарський засіб), зареєстровано в Україні вперше, державна реєстрація іншого лікарського засобу, що містить ту саму діючу речовину, що й референтний/оригінальний лікарський засіб, можлива не раніше ніж через п’ять років з дня першої реєстрації референтного/оригінального лікарського засобу в Україні, якщо інше не передбачено цією статтею. Зазначена вимога не поширюється на випадки, коли заявник відповідно до закону одержав право посилатися та/або використовувати реєстраційну інформацію референтного/оригінального лікарського засобу або подав власну повну реєстраційну інформацію, що відповідає вимогам до реєстраційної інформації референтного/оригінального лікарського засобу.Зазначений у частині дванадцятій цієї статті строк може бути продовжено до шести років, якщо протягом перших трьох років після державної реєстрації референтного/оригінального лікарського засобу центральним органом виконавчої влади, що реалізує державну політику у сфері охорони здоров’я, дозволено його застосування за одним або більше показаннями, які вважаються такими, що мають особливу перевагу над існуючими. Правила та критерії визначення показань, що мають особливу перевагу над існуючими, встановлюються центральним органом виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я. Визначений частиною дванадцятою цієї статті строк встановлюється у разі, якщо заява про державну реєстрацію в Україні референтного/оригінального лікарського засобу подана протягом двох років з дня його першої реєстрації в будь-якій країні. … |
… Якщо лікарський засіб, містить нову активну діючу речовину (активний фармацевтичний інгредієнт) і пройшов повний цикл доклінічних та клінічних досліджень, та зареєстрований в Україні на підставі повної реєстраційної інформації (далі — референтний/ оригінальний лікарський засіб), державна реєстрація іншого лікарського засобу, що містить ту саму діючу речовину, що й референтний/оригінальний лікарський засіб, можлива не раніше ніж через п’ять років з дня першої реєстрації референтного/ оригінального лікарського засобу в Україні, якщо заява про державну реєстрацію в Україні референтного/оригінального лікарського засобу подана протягом двох років з дня його першої реєстрації в будь-якій країні.Зазначена вимога не поширюється на випадки, коли заявник відповідно до закону одержав право посилатися та/або використовувати реєстраційну інформацію референтного/оригінального лікарського засобу або подав власну повну реєстраційну інформацію, що відповідає вимогам до реєстраційної інформації референтного/оригінального лікарського засобу, а також у разі видачі Кабінетом Міністрів України дозволу на використання запатентованого винаходу (корисної моделі), що стосується такого лікарського засобу, або у разі необхідності вчинення дій за надзвичайних обставин, які згідно із законодавством України у сфері інтелектуальної власності не визнаються порушенням прав власника патенту на винахід, що стосується такого лікарського засобу, або якщо судом або іншим уповноваженим законом органом встановлено, що власник права інтелектуальної власності зловживав своїми правами, зокрема монопольним (домінуючим) становищем на ринку.Вимоги цієї статті не виключають права іншого заявника (виробника) здійснювати упродовж строку дії патенту відповідну розробку та випробування, у тому числі проводити дослідження з біо- або терапевтичної еквівалентності між генеричним та референтними лікарським засобом, тощо. |
| Розділ відстуній. | Розділ VI1
ЗАБЕЗПЕЧЕННЯ ДОСТУПНОСТІ ЛІКАРСЬКИХ ЗАСОБІВ Стаття 231. Ціни на лікарські засоби Державна цінова політика щодо лікарських засобів спрямована на забезпечення соціальних гарантій населенню та необхідних економічних гарантій для виробників лікарських засобів. |
| Стаття 232. Державне регулювання цін
Граничні оптово-відпускні ціни на лікарські засоби, граничні постачальницько-збутові надбавки на лікарські засоби, а також граничні торговельні (роздрібні) надбавки на лікарські засоби, встановлюються у випадках, визначених законодавством та в порядку, визначеному Кабінетом Міністрів України. Кабінетом Міністрів України щороку визначається перелік лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, та для яких обов’язково встановлюється (в тому числі при реалізації через аптечну мережу та/або аптеки та їх структурні підрозділи): гранична оптово-відпускна ціна; гранична постачальницько-збутова надбавка, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням податків та зборів, та яка не може бути більшою ніж 10 відсотків;гранична торгівельна (роздрібна) надбавка, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням граничної постачальницько-збутової надбавки, а також з урахуванням податків та зборів, та яка не може бути більшою ніж 15 відсотків. Оптово-відпускна ціна в Україні для лікарських засобів з переліку лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, не може перевищувати граничну оптово-відпускну ціну. Центральний орган виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я, веде, розміщує та щоквартально оновлює на своєму офіційному веб-сайті реєстр оптово-відпускних цін на лікарські засоби з переліку лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, в порядку визначеному Кабінетом Міністрів України. Інформація про оптово-відпускні ціни на лікарські засоби з переліку лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, вноситься на підставі щоквартального подання власником або уповноваженим представником власника реєстраційного посвідчення на лікарський засіб інформації в обсязі, визначеному центральним органом виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я. |
|
| Стаття 23–3. Відшкодування вартості лікарських засобів
Держава забезпечує повне або часткове відшкодування вартості лікарських засобів у випадках, визначених цією, статтею суб’єктам господарювання, які провадять господарську діяльність на підставі ліцензії на провадження господарської діяльності з роздрібної торгівлі лікарськими засобами, незалежно від форми власності та підпорядкування, аптечні заклади яких розташовані в межах відповідної адміністративно-територіальної одиниці в порядку, визначеному Кабінетом Міністрів України. Повне або часткове відшкодування вартості лікарських засобів здійснюється в межах затвердженого центральним органом виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я, розміру відшкодування вартості лікарських засобів, що включені до Реєстру лікарських засобів, вартість яких підлягає відшкодуванню, що затверджується центральним органом виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я. Відпуск лікарських засобів здійснюється виключно на підставі рецептів, виписаних закладами охорони здоров’я незалежно від форми власності за місцем надання медичної допомоги пацієнту на рецептурних бланках. Рецепт зберігається у суб’єкта господарювання протягом трьох років з моменту відпуску. Повне або часткове відшкодування вартості лікарських засобів здійснюється під час амбулаторного лікування осіб, що страждають на серцево-судинні захворювання, діабет (цукровий і нецукровий) бронхіальну астму, а також лікарських засобів, що використовуються під час трансплантації у доопераційний та післяопераційний періоди, противірусних лікарських засобів, антибактеріальних лікарських засобів, антианемічних лікарських засобів, лікарських засобів, що впливають на функцію шлунково-кишкового тракту, лікарських засобів, що застосовуються при депресивних розладах, що включені до Національного переліку основних лікарських засобів. Центральний орган виконавчої влади, що забезпечує формування державної політики у сфері охорони здоров’я, окрім визначеного цією статтею переліку захворювань та/або лікарських засобів, за якими здійснюється повне або часткове відшкодування вартості лікарських засобів, може затвердити додатковий перелік захворювань та/або лікарських засобів, за якими здійснюється повне або часткове відшкодування вартості лікарських засобів. |
|
| Стаття 234. Фінансування відшкодування вартості лікарських засобів Фінансування відшкодування вартості лікарських засобів, передбачене статтею 23–3 цього Закону, здійснюється за рахунок Державного бюджету України. Щорічний обсяг коштів Державного бюджету України, які спрямовуються на фінансування відшкодування вартості лікарських засобів, передбачене статтею 23–3 цього Закону, становить не менше 0,25% від обсягу видатків, що передбачені законом про Державний бюджет України на відповідний рік. |
|
| Стаття 24. Фінансове забезпечення Фінансування створення, доклінічного вивчення, клінічного випробування, виробництва, контролю якості лікарських засобів здійснюється за рахунок Державного бюджету України, місцевих бюджетів, позабюджетних фондів, коштів підприємств, установ, організацій та громадян, а також будь-яких інших джерел, не заборонених законодавством.Витрати на фінансування наукових робіт по створенню нових лікарських засобів відносяться на рахунок собівартості продукції в порядку, визначеному Кабінетом Міністрів України. |
Стаття 24. Фінансове забезпечення Фінансування створення, доклінічного вивчення, клінічного випробування, виробництва, контролю якості лікарських засобів здійснюється за рахунок Державного бюджету України, місцевих бюджетів, позабюджетних фондів, коштів підприємств, установ, організацій та громадян, а також будь-яких інших джерел, не заборонених законодавством.Витрати на фінансування наукових робіт по створенню нових лікарських засобів відносяться на рахунок собівартості продукції в порядку, визначеному Кабінетом Міністрів України. Фінансування відшкодування вартості лікарських засобів, здійснюється у відповідності до статті 23–3 цього Закону. |
| Стаття 27. Відповідальність за порушення законодавства про лікарські засоби
Особи, винні в порушенні законодавства про лікарські засоби, несуть дисциплінарну, адміністративну, цивільно-правову або кримінальну відповідальність згідно із законодавством. |
Стаття 27. Відповідальність за порушення законодавства про лікарські засоби
Особи, винні в порушенні законодавства про лікарські засоби, несуть дисциплінарну, адміністративну, цивільно-правову або кримінальну відповідальність згідно із законодавством. Порушення вимог щодо чисельності аптек (їх структурних підрозділів) аптечної мережі, передбаченої статтею 2 цього Закону, тягне за собою відповідальність, встановлену законодавством про захист економічної конкуренції. |
| Закон України «Про захист економічної конкуренції» (Відомості Верховної Ради України (ВВР), 2001, № 12, ст. 64) | |
| Стаття 50. Порушення законодавства про захист економічної конкуренції Порушеннями законодавства про захист економічної конкуренції є: … пункт відсутній |
Стаття 50. Порушення законодавства про захист економічної конкуренції Порушеннями законодавства про захист економічної конкуренції є: … 21) порушення вимог щодо чисельності аптек (їх структурних підрозділів) аптечної мережі, передбаченої законодавством про лікарські засоби. |
| Стаття 52. Штрафи … 2. За порушення, передбачені:…пунктами 5, 8, 10, 11, 12 та 19 статті 50 цього Закону, накладаються штрафи у розмірі до п’яти відсотків доходу (виручки) суб’єкта господарювання від реалізації продукції (товарів, робіт, послуг) за останній звітний рік, що передував року, в якому накладається штраф; … |
Стаття 52. Штрафи … 2. За порушення, передбачені: … пунктами 5, 8, 10, 11, 12, 19 та 21 статті 50 цього Закону, накладаються штрафи у розмірі до п’яти відсотків доходу (виручки) суб’єкта господарювання від реалізації продукції (товарів, робіт, послуг) за останній звітний рік, що передував року, в якому накладається штраф; … |
| Кодекс України про адміністративні правопорушення (Відомості Верховної Ради Української РСР (ВВР) 1984, додаток до № 51, ст.1122) | |
| Стаття 424. Продаж лікарських засобів без рецепта у заборонених законодавством випадках
Продаж лікарських засобів в аптечних закладах без рецепта у заборонених законодавством випадках – тягне за собою накладення штрафу від шести до двадцяти п’яти неоподатковуваних мінімумів доходів громадян. Повторне протягом року вчинення порушення, передбаченого частиною першою цієї статті, за яке особу вже було піддано адміністративному стягненню, – тягне за собою накладення штрафу від двадцяти п’яти до сімдесяти неоподатковуваних мінімумів доходів громадян. |
Стаття 424. Продаж лікарських засобів без рецепта у заборонених законодавством випадках
Продаж лікарських засобів в аптечних закладах без рецепта у заборонених законодавством випадках – тягне за собою накладення штрафу від п’ятидесяти до ста неоподатковуваних мінімумів доходів громадян. Повторне протягом року вчинення порушення, передбаченого частиною першою цієї статті, за яке особу вже було піддано адміністративному стягненню, – тягне за собою накладення штрафу від ста до двохсот неоподатковуваних мінімумів доходів громадян. |
| Стаття відсутня | Стаття 425. Порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення
Порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення, в тому числі зазначення в рецепті торгівельної назви лікарського засобу, у випадках заборонених законодавством – тягне за собою накладення штрафу від п’ятидесяти до ста неоподатковуваних мінімумів доходів громадян. Повторне протягом року вчинення порушення, передбаченого частиною першою цієї статті, за яке особу вже було піддано адміністративному стягненню, – тягне за собою накладення штрафу від ста до двохсот неоподатковуваних мінімумів доходів громадян. |
| Стаття відсутня | Стаття 1656. Порушення законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби
Порушення законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби – тягне за собою накладення штрафу на посадових осіб від однієї тисячі до двох тисяч неоподатковуваних мінімумів доходів громадян. Повторне протягом року вчинення порушення, передбаченого частиною першою цієї статті, за яке особу вже було піддано адміністративному стягненню, – тягне за собою накладення штрафу від двох до чотирьох тисяч неоподатковуваних мінімумів доходів громадян. |
| Стаття 244-5. Центральний орган виконавчої влади, що реалізує державну політику з контролю за цінами
Центральний орган виконавчої влади, що реалізує державну політику з контролю за цінами, розглядає справи про адміністративні правопорушення, пов’язані з порушенням порядку формування, встановлення та застосування цін і тарифів, а також невиконанням законних вимог посадових осіб зазначеного органу (статті 165–2, 188–3). Від імені центрального органу виконавчої влади, що реалізує державну політику з контролю за цінами, розглядати справи про адміністративні правопорушення та накладати адміністративні стягнення мають право керівник зазначеного органу та уповноважені ним посадові особи. |
Стаття 244-5. Центральний орган виконавчої влади, що реалізує державну політику з контролю за цінами
Центральний орган виконавчої влади, що реалізує державну політику з контролю за цінами, розглядає справи про адміністративні правопорушення, пов’язані з порушенням порядку формування, встановлення та застосування цін і тарифів, порушенням законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби, а також невиконанням законних вимог посадових осіб зазначеного органу (статті 165–2, 165–6, 188–3). Від імені центрального органу виконавчої влади, що реалізує державну політику з контролю за цінами, розглядати справи про адміністративні правопорушення та накладати адміністративні стягнення мають право керівник зазначеного органу та уповноважені ним посадові особи. |
| Стаття 244-8. Центральний орган виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів
Центральний орган виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів, розглядає справи про адміністративні правопорушення, пов’язані з порушенням обмежень, встановлених для медичних і фармацевтичних працівників під час здійснення ними професійної діяльності (стаття 44–2), з порушенням встановленого порядку взяття, переробки, зберігання, реалізації і застосування донорської крові та (або) її компонентів і препаратів (стаття 45–1), з продажем лікарських засобів без рецепта у заборонених законодавством випадках (стаття 42–4), з недодержанням вимог стандартів, норм, правил і технічних умов під час виробництва, зберігання, транспортування, реалізації чи використання лікарських засобів (статті 167, 168–1, 170), а також з невиконанням законних вимог посадових осіб центрального органу виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів (стаття 188–10). Від імені центрального органу виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів, розглядати справи про адміністративні правопорушення і накладати адміністративні стягнення мають право: Головний державний інспектор України з контролю якості лікарських засобів та його заступники, головні державні інспектори з контролю якості лікарських засобів в Автономній Республіці Крим, областях, містах Києві, Севастополі та їх заступники, державні інспектори з контролю якості лікарських засобів. |
Стаття 244-8. Центральний орган виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів
Центральний орган виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів, розглядає справи про адміністративні правопорушення, пов’язані з порушенням обмежень, встановлених для медичних і фармацевтичних працівників під час здійснення ними професійної діяльності (стаття 44–2), з порушенням встановленого порядку взяття, переробки, зберігання, реалізації і застосування донорської крові та (або) її компонентів і препаратів (стаття 45–1), з продажем лікарських засобів без рецепта у заборонених законодавством випадках (стаття 42–4), з порушенням встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення (стаття 42–5), з недодержанням вимог стандартів, норм, правил і технічних умов під час виробництва, зберігання, транспортування, реалізації чи використання лікарських засобів (статті 167, 168–1, 170), а також з невиконанням законних вимог посадових осіб центрального органу виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів (стаття 188–10). Від імені центрального органу виконавчої влади, що реалізує державну політику у сфері контролю якості та безпеки лікарських засобів, розглядати справи про адміністративні правопорушення і накладати адміністративні стягнення мають право: Головний державний інспектор України з контролю якості лікарських засобів та його заступники, головні державні інспектори з контролю якості лікарських засобів в Автономній Республіці Крим, областях, містах Києві, Севастополі та їх заступники, державні інспектори з контролю якості лікарських засобів. |
| Закон України «Про охорону прав на винаходи і корисні моделі» (Відомості Верховної Ради України (ВВР), 1994, № 7, ст. 32) | |
| Розділ II
ПРАВОВА ОХОРОНА ВИНАХОДІВ (КОРИСНИХ МОДЕЛЕЙ) |
Розділ II
ПРАВОВА ОХОРОНА ВИНАХОДІВ (КОРИСНИХ МОДЕЛЕЙ) |
| Стаття 6. Умови надання правової охорони
…………………………. |
Стаття 6. Умови надання правової охорони
…………………………. |
| Відсутня | Стаття 271. Додаткова охорона прав на винаходи
1. Володілець патенту на винахід, об’єктом якого є активний фармацевтичний інгредієнт лікарського засобу, процес отримання лікарського засобу або застосування лікарського засобу, засіб захисту тварин, засіб захисту рослин, введення в обіг якого в Україні дозволяється відповідним компетентним органом згідно з чинним законодавством України, має право на подовження строку чинності майнових прав інтелектуальної власності на такий винахід (додаткова охорона), яке засвідчується сертифікатом додаткової охорони. Сертифікат додаткової охорони видається за клопотанням володільця патенту. За подання клопотання сплачується збір. Права на додаткову охорону обмежені продуктом (активним фармацевтичним інгредієнтом або сукупністю активних фармацевтичних інгредієнтів лікарського засобу), введення в обіг якого в Україні дозволено відповідним компетентним органом згідно з чинним законодавством України, та його застосуванням відповідно, як лікарського засобу, засобу захисту тварин, засобу захисту рослин, у межах прав, що надавалися відповідним патентом на момент подання клопотання про видачу сертифікату додаткової охорони, та є чинними за умови чинності такого дозволу. |
| 2. Строк додаткової охорони дорівнює періоду між датою подання заявки до Установи та датою одержання володільцем патенту першого дозволу компетентного органу, зменшеному на 5 років.
Строк додаткової охорони не може бути більшим ніж 5 років. Для винаходу, об’єктом якого є активний фармацевтичний інгредієнт лікарського засобу, та стосовно якого були здійснені дослідження у сфері застосування для дітей, результати яких відображені в інформації про лікарський засіб, на який видано дозвіл відповідного компетентного органу, зазначені в абзацах першому та другому цієї частини строки додаткової охорони збільшуються на шість місяців. |
|
| 3. Клопотання має надійти до Установи протягом 6 місяців від дати публікації відомостей про державну реєстрацію винаходу або від дати видачі першого дозволу відповідного компетентного органу, залежно від того, яка з цих дат є пізнішою. До клопотання мають бути додані документи, що підтверджують право володільця патенту на додаткову охорону.
Клопотання розглядається закладом експертизи в порядку, що визначається центральним органом виконавчої влади, що забезпечує формування державної політики у сфері інтелектуальної власності. |
|
| 4. У разі, якщо подані документи підтверджують право володільця патенту на додаткову охорону, Установа здійснює державну реєстрацію додаткової охорони шляхом внесення до Реєстру відповідних відомостей. Одночасно з державною реєстрацією додаткової охорони Установа здійснює публікацію в Бюлетені визначених нею відомостей про таку реєстрацію. Видача сертифікату додаткової охорони здійснюється Установою у місячний строк після державної реєстрації додаткової охорони. | |
| 5. Права та обов’язки володільця сертифікату додаткової охорони є такими самими, що і права володільця відповідного патенту з урахуванням обмежень, встановлених частиною першою цієї статті. | |
| 6. За підтримання чинності сертифікату додаткової охорони сплачується збір за кожен повний чи неповний рік його дії. Порядок сплати зборів за підтримання чинності сертифікату додаткової охорони є таким самим, як визначено в частині другій статті 32 цього Закону. | |
| 7. Порядок припинення дії сертифікату додаткової охорони та визнання його недійсним, захисту прав володільця сертифікату додаткової охорони є такими самими, як і щодо відповідного патенту. | |
| Закон України «Про ціни і ціноутворення»(Відомості Верховної Ради (ВВР), 2013, № 19–20, ст. 190) | |
| Стаття 5. Повноваження Кабінету Міністрів України у сфері ціноутворення
1. Кабінет Міністрів України: 1) забезпечує проведення державної цінової політики; 2) здійснює державне регулювання цін, визначає повноваження органів виконавчої влади щодо формування, встановлення та застосування цін, якщо інше не визначено законом або міжнародним договором України, згода на обов’язковість якого надана Верховною Радою України; 3) визначає перелік товарів, державні регульовані ціни на які затверджуються відповідними органами виконавчої влади, якщо інше не визначено законом. |
Стаття 5. Повноваження Кабінету Міністрів України у сфері ціноутворення
1. Кабінет Міністрів України: 1) забезпечує проведення державної цінової політики; 2) здійснює державне регулювання цін, визначає повноваження органів виконавчої влади щодо формування, встановлення та застосування цін, якщо інше не визначено законом або міжнародним договором України, згода на обов’язковість якого надана Верховною Радою України; 3) визначає перелік товарів, державні регульовані ціни на які затверджуються відповідними органами виконавчої влади, якщо інше не визначено законом; 4) встановлює граничні оптово-відпускні ціни на лікарські засоби, граничні постачальницько-збутові надбавки на лікарські засоби, а також граничні торговельні (роздрібні) надбавки на лікарські засоби, відповідно до законодавства. |
Народні депутати УкраїниО.В. Ляшко
В.В. Галасюк
В.І. Вовк
О.М. Кириченко
А.В. Кошелєва
М.Ю. Бурбак
В.Л. Заружко
М.В. Довбенко
О.Г. Домбровський
О.В. Кужель
А.М. Гіршфельд
Л.П. Козаченко
Є.Ю. Рибчинський
М.В. Єфімов
А.Ю. Геращенко
О.С. Мусій
В.В. Амельченко
Д.В. Лінько
С.В. Рибалка
ВИСНОВОК
Головного науково-експертного управління
від 06.03.2019 р.
на проект Закону України ««Зробимо ліки дешевшими!»
(про внесення змін до деяких законодавчих актів України щодо комплексного здешевлення ліків для громадян та забезпечення
розвитку вітчизняної фармацевтичної галузі)»
(реєстр. № 9372 від 06.12.2018 р.)
У законопроекті вносяться зміни до законів України «Про лікарські засоби», «Про ціни та ціноутворення», «Про захист економічної конкуренції», «Про охорону прав на винаходи і корисні моделі», якими передбачається встановити, зокрема, що:
– граничні оптово-відпускні ціни на лікарські засоби, граничні постачальницько-збутові надбавки на лікарські засоби, а також граничні торговельні (роздрібні) надбавки на лікарські засоби встановлюються у випадках, визначених законодавством та в порядку, визначеному Кабінетом Міністрів України;
– Кабінетом Міністрів України щороку визначається перелік лікарських засобів, на які поширюється зовнішнє референтне ціноутворення та для яких обов’язково встановлюється (в тому числі при реалізації через аптечну мережу та/або аптеки та їх структурні підрозділи): гранична оптово-відпускна ціна; гранична постачальницько-збутова надбавка, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням податків та зборів та яка не може бути більшою ніж 10 відсотків.
Крім цього, змінами до Кодексу України про адміністративні правопорушення передбачається встановити адміністративну відповідальність за порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення, порушення законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби, а також збільшити адміністративний штраф за продаж лікарських засобів без рецепта у заборонених законодавством випадках.
У пояснювальній записці зазначається, що метою законопроекту є «законодавча імплементація комплексного плану, спрямованого на значне зниження вартості основних лікарських засобів в аптечних закладах України» (п. 2).
Головне науково-експертне управління, розглянувши внесену законодавчу пропозицію, вважає за доцільне висловити щодо неї міркування, які можуть бути використані при подальшому доопрацюванні законопроекту.
- Щодо змін до Закону України «Про лікарські засоби».
1.1. У частині першій статті 2 Закону України «Про лікарські засоби» пропонується дати визначення нового терміну «аптечна мережа», як «сукупність аптек (їх структурних підрозділів), що мають одного і того ж кінцевого бенефіціарного власника (контролера)». Тобто передбачається, що мережа аптек здійснюватиме свою господарську діяльність як одна юридична особа через філії та представництва.
Разом з тим, на нашу думку, враховуючи сучасні методи господарювання, які передбачені Господарським кодексом України, мережа аптек може бути утворена як об’єднання підприємств з різними кінцевими бенефіціарними власниками (контролерами) та/або діяти на підставі договору комерційної концесії шляхом використання таких об’єктів права інтелектуальної власності, як торговельні марки, комерційної таємниці тощо, а також комерційного досвіду та ділової репутації. Тому, на нашу думку, запропоноване в проекті визначення аптечної мережі недостатньо узгоджується з вимогами частини 1 статті 70 Господарського кодексу України, згідно з якою підприємства мають право на добровільних засадах об’єднувати свою господарську діяльність (виробничу, комерційну та інші види діяльності) на умовах і в порядку, встановлених цим Кодексом та іншими законами, а також зі статтею 366 цього ж Кодексу щодо використання комерційної концесії.
Крім того, при визначенні «аптечної мережі» в проекті передбачається встановити, що кожна аптечна мережа за кількістю аптек (їх структурних підрозділів) не може займати більше ніж 2% від загальної кількості зареєстрованих аптек (їх структурних підрозділів) у межах АР Крим, області, м. Києва чи Севастополя. Вважаємо, що обмежувальні заходи щодо суб’єктів господарювання, які здійснюють роздрібну торгівлю лікарськими засобами, доцільно застосовувати не «взагалі», а у випадку порушення ними законодавства України про захист економічної конкуренції. Це зауваження також стосується нового пункту 21, яким пропонується доповнити перелік випадків порушення законодавства про захист економічної конкуренції у статті 50 Закону України «Про захист економічної конкуренції».
1.2. У законопроекті пропонується доповнити Закон України «Про лікарські засоби» новою статтею 23-2, в якій визначаються питання державного регулювання цін. Зокрема, цією статтею передбачається зобов’язати Кабінет Міністрів України визначити окремий перелік лікарських засобів, на які поширюється зовнішнє референтне ціноутворення, та для яких обов’язково встановлюється (в тому числі при реалізації через аптечну мережу та/або аптеки та їх структурні підрозділи): гранична оптово-відпускна ціна; гранична постачальницько-збутова надбавка, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням податків та зборів, та яка не може бути більшою ніж 10 відсотків; гранична торгівельна (роздрібна) надбавка, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням граничної постачальницько-збутової надбавки, а також з урахуванням податків та зборів, та яка не може бути більшою ніж 15 відсотків.
Такий підхід, загалом, виглядає можливим з огляду, зокрема, на вимоги п.п. 2 та 3 ч. 1 статті 5 Закону «Про ціни та ціноутворення», за якими Кабінет Міністрів України здійснює державне регулювання цін, визначає повноваження органів виконавчої влади щодо формування, встановлення та застосування цін, якщо інше не визначено законом або міжнародним договором України, згода на обов’язковість якого надана Верховною Радою України; визначає перелік товарів, державні регульовані ціни на які затверджуються відповідними органами виконавчої влади, якщо інше не визначено законом.
У той же час, враховуючи те, що за змістом пропонованих змін та чинних норм Закону України «Про ціни та ціноутворення» компетенція щодо встановлення державних регульованих цін на лікарські засоби та застосування відповідного інструментарію державного цінового регулювання покладається на Кабінет Міністрів України, органи виконавчої влади та органи місцевого самоврядування, у супровідних до проекту документах доцільно було б навести інформацію щодо оцінки поточного стану виконання відповідними органами приписів нормативно-правових актів, що регулюють відповідні відносини, адже вони, згідно з вимогами Конституції України, зобов’язані діяти лише на підставі, в межах повноважень та у спосіб, що передбачені Конституцією та законами України (ст. 19).
З цього приводу слід зазначити, що відповідно до ст. 5 Закону України «Про ціни та ціноутворення» забезпечення проведення державної цінової політики; здійснення державного регулювання цін; визначення повноважень органів виконавчої влади щодо формування, встановлення та застосування цін, якщо інше не визначено законом або міжнародним договором України, згода на обов’язковість якого надана Верховною Радою України; визначення переліку товарів, державні регульовані ціни на які затверджуються відповідними органами виконавчої влади, якщо інше не визначено законом, належить до повноважень Кабінету Міністрів України у сфері ціноутворення.
Відповідно ж до статті 13 цього Закону державне регулювання цін здійснюється Кабінетом Міністрів України, органами виконавчої влади та органами місцевого самоврядування відповідно до їх повноважень шляхом: установлення обов’язкових для застосування суб’єктами господарювання: фіксованих цін; граничних цін; граничних рівнів торговельної надбавки (націнки) та постачальницько-збутової надбавки (постачальницької винагороди); граничних нормативів рентабельності; розміру постачальницької винагороди; розміру доплат, знижок (знижувальних коефіцієнтів); запровадження процедури декларування зміни ціни та/або реєстрації ціни.Прикладом підзаконного регулювання цін може слугувати, зокрема, постанова Кабінету Міністрів України від 09.11.2016 р. № 862 «Про державне регулювання цін на лікарські засоби», якою з 1 квітня 2017 року запроваджується державне регулювання цін на лікарські засоби, які закуповуються та/або вартість яких відшкодовується за бюджетні кошти, шляхом встановлення Міністерством охорони здоров’я граничних оптово-відпускних цін, а також визначається перелік країн, дані про ціни на лікарські засоби в яких використовуються для встановлення референтних цін.Відповідно до постанови Кабінету Міністрів України від 09.11.2016 р. № 863 «Про запровадження відшкодування вартості лікарських засобів» запроваджено відшкодування вартості лікарських засобів під час амбулаторного лікування осіб, що страждають на серцево-судинні захворювання, цукровий діабет II типу, бронхіальну астму, а також лікарських засобів, що використовуються під час трансплантації у доопераційний та післяопераційний періоди, за переліком міжнародних непатентованих назв лікарських засобів згідно з додатком.Слід відзначити, що є чинною постанова Кабінету Міністрів України від 17.10.2008 р. № 955 «Про заходи щодо стабілізації цін на лікарські засоби і медичні вироби», якою встановлено:1) на лікарські засоби, включені до Національного переліку основних лікарських засобів (крім наркотичних, психотропних лікарських засобів, прекурсорів та медичних газів) та обов’язкового мінімального асортименту лікарських засобів для аптечних закладів та фельдшерсько-акушерських пунктів, визначеного Міністерством охорони здоров’я, граничні постачальницько-збутові надбавки не вище ніж 10 відсотків, що нараховуються до оптово-відпускної ціни з урахуванням податків та зборів, а граничні торговельні (роздрібні) надбавки не вище ніж 25 відсотків, що нараховуються до закупівельної ціни з урахуванням податків; 2) на лікарські засоби (крім наркотичних, психотропних лікарських засобів, прекурсорів та медичних газів), оптово-відпускні ціни на які внесені до реєстру оптово-відпускних цін на лікарські засоби, і медичні вироби, які придбаваються повністю або частково за рахунок коштів державного та місцевих бюджетів, граничні постачальницько-збутові надбавки не вище ніж 10 відсотків, що нараховуються для лікарських засобів до задекларованої зміни оптово-відпускної ціни з урахуванням податків та зборів і для медичних виробів до оптово-відпускної ціни з урахуванням податків та зборів, а граничні торговельні (роздрібні) надбавки не вище ніж 10 відсотків, що нараховуються до закупівельної ціни з урахуванням податків. При цьому фактичний розмір оптово-відпускної ціни на кожну лікарську форму, дозування, споживчу упаковку лікарського засобу не повинен перевищувати розміру внесеної до зазначеного реєстру оптово-відпускної ціни у гривні;3) на лікарські засоби, включені до переліку міжнародних непатентованих назв лікарських засобів, зазначеного в пункті 1 постанови Кабінету Міністрів України від 9 листопада 2016 р. № 863 «Про запровадження відшкодування вартості лікарських засобів» (Офіційний вісник України, 2016 р., № 95, ст. 3103), граничні постачальницько-збутові надбавки в розмірі 10 відсотків, що нараховуються до оптово-відпускної ціни з урахуванням податків, та граничні торговельні (роздрібні) надбавки в розмірі 15 відсотків, що нараховуються до закупівельної ціни з урахуванням податків.1.3. Пояснювальна записка до законопроекту не містить економічного обґрунтування щодо пропонованого розміру граничної торгівельної (роздрібної) надбавки, яка нараховується на оптово-відпускну ціну лікарського засобу з урахуванням граничної постачальницько-збутової надбавки, а також з урахуванням податків та зборів, та яка не може бути більшою ніж 15 відсотків.2. Щодо змін до Закону України «Про охорону прав на винаходи і корисні моделі».
У проекті пропонується внести зміни до Закону України «Про охорону прав на винаходи і корисні моделі», а саме: виключити зі статті 6 частину 4, що стосується продовження строку дії патенту на винахід, об’єктом якого є лікарський засіб, засіб захисту тварин, засіб захисту рослин тощо, використання якого потребує дозволу відповідного компетентного органу, на строк, що дорівнює періоду між датою подання заявки та датою одержання такого дозволу, але не більше, ніж на 5 років. Натомість проект пропонується доповнити новою статтею 27 1, у якій запровадити додаткову охорону прав на винаходи, яка має підтверджуватися так званим «сертифікатом додаткової охорони». При цьому, відповідно до частини 5 цієї нової статті, «права та обов’язки володільця сертифікату додаткової охорони є такими самим, що і права володільця відповідного патенту з урахуванням обмежень, встановлених частиною першою цієї статті». Вказані права та обмеження полягають в тому, що «права на додаткову охорону обмежені продуктом (активним фармацевтичним інгредієнтом або сукупністю активних фармацевтичних інгредієнтів лікарського засобу), введення в обіг якого в Україні дозволено відповідним компетентним органом … ». При цьому, як пропонується в частині 2 цієї нової статті, «строк додаткової охорони дорівнює періоду між датою подання заявки до Установи та датою одержання володільцем патенту першого дозволу компетентного органу, зменшеному на 5 років».
Звертаємо увагу, що ця пропозиція дублює пропозиції законопроектів № 9088 від 17.09.2018 р. «Про внесення змін до деяких законодавчих актів України щодо підвищення рівня охорони і захисту прав інтелектуальної (промислової) власності та удосконалення державного управління сферою інтелектуальної власності» та № 9385 від 10.12.2018 р. «Про внесення змін до деяких законодавчих актів України щодо імплементації окремих положень законодавства Європейського союзу у сфері інтелектуальної власності» від 10.12.2018 р. Однак, враховуючи, що законопроект № 9372 має своїм предметом, виходячи з його назви, комплексне здешевлення ліків для громадян та розвиток фармацевтичної галузі, а не безпосередньо охорону прав інтелектуальної власності на винаходи, то питання додаткового охоронного сертифікату, на нашу думку, доцільніше вирішити у проектах, які мають на меті удосконалення регулювання сферою прав інтелектуальної власності.
- Щодо змін до Кодексу України про адміністративні правопорушення (далі – КУпАП).
3.1. У статті 42-5 КУпАП (у редакції проекту) пропонується встановити відповідальність за порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення. Натомість, у Законі України «Про лікарські засоби» (зокрема, у статті 21; далі – Закон) використовується термін «правила приписування» лікарських засобів, тоді як наказ Міністерства охорони здоров’я України від 19 липня 2005 р. № 360 знову ж має назву «Про затвердження Правил виписування рецептів на лікарські засоби і вироби медичного призначення, Порядку відпуску лікарських засобів і виробів медичного призначення з аптек та їх структурних підрозділів, Інструкції про порядок зберігання, обліку та знищення рецептурних бланків» (далі – Правила). З огляду на це вважаємо, що вказані норми потребують відповідної уніфікації.
Крім того, зі змісту статті 42-5 КУпАП (у редакції проекту) незрозуміло, що необхідно розуміти під «порушенням встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення». Адже буквальне тлумачення пропонованої норми свідчить про те, що діяння, передбачене цією статтею, у тому числі, може вчинятися і з необережності, наприклад: заповнення рецепту не чітко або нерозбірливо (пункт перший розділу ІІІ Правил); написання номеру рецепта не друкарським способом (підпункт 1 пункту четвертого розділу ІІІ Правил); у графі «(дата виписування Рецепта)» зазначене помилкове число, місяць та рік виписування рецепта (підпункт 4 пункту четвертого розділу ІІІ Правил) тощо. Відповідальність за такі порушення, на наш погляд, має носити виключно дисциплінарний характер, оскільки вказані діяння не досягають того рівня суспільної шкідливості, щоб визнавати їх адміністративними правопорушеннями.
У інших випадках порушення встановлених правил виписування рецептів на лікарські засоби і вироби медичного призначення загалом можуть містити ознаки кримінально караного діяння. Так, наприклад, якщо рецепт виписаний суб’єктом, що не мав на це права (всупереч приписам пункту першого розділу І Правил), може мати місце або злочин, передбачений статтею 318 «Незаконне виготовлення, підроблення, використання чи збут підроблених документів на отримання наркотичних засобів, психотропних речовин або прекурсорів» Кримінального кодексу України (далі – КК) або статтею 358 «Підроблення документів, печаток, штампів та бланків, збут чи використання підроблених документів, печаток, штампів» КК. Якщо ж рецепт за формою ф-3 виписано особі, яка не мала на це права, то йдеться про злочин, передбачений статтею 319 «Незаконна видача рецепта на право придбання наркотичних засобів або психотропних речовин» КК.
З огляду на зазначене, вважаємо, що вказані положення законопроекту потребують суттєвого концептуального уточнення.
3.2. На нашу думку, введення до КУпАП відповідальності за порушення законодавства про лікарські засоби щодо формування або застосування цін на лікарські засоби (див. пропоновану проектом ст. 165-6) є зайвою, оскільки такі діяння, якщо вони вчинені посадовою особою, повною мірою охоплюються чинною статтею 165-2 «Порушення порядку формування та застосування цін і тарифів» КУпАП.
Що ж стосується суб’єктів господарювання, то у пункті 1 частини першої статті 20 Закону України «Про ціни і ціноутворення» визначено, що до них застосовуються адміністративно-господарські санкції за порушення вимог щодо формування, встановлення та застосування державних регульованих цін – вилучення необґрунтовано одержаної виручки, що становить позитивну різницю між фактичною виручкою від продажу (реалізації) товару та виручкою за цінами, сформованими відповідно до запровадженого способу регулювання та штраф у розмірі 100 відсотків необґрунтовано одержаної виручки.
3.3. Крім того, звертаємо увагу, що у випадку доповнення КУпАП новими статтями, одночасно із визначенням органу, який здійснює розгляд справи про адміністративні правопорушення, необхідно також вносити відповідні зміні до статті 255 «Особи, які мають право складати протоколи про адміністративні правопорушення» КУпАП. В даному випадку такі зміни у проекті Закону відсутні.
- Зауваження техніко-юридичного характеру.
4.1. Назва законопроекту не кореспондується з передбаченими ним змінами, зокрема, які вносяться до Кодексу України про адміністративні правопорушення, змінами до ст. 9 Закону України «Про лікарські засоби»
4.2. У законопроекті не дотримані вимоги законодавчої техніки, згідно з якими закони, до яких вносяться зміни, подаються по тексту законопроекту в хронологічному порядку. При цьому, якщо у переліку актів, до яких вносяться зміни, є кодекси, то вони ставляться на першому місці.
4.3. Окремі зміни вносяться до статей законів (наприклад, зміни до ст. 50 Закону України «Про захист економічної конкуренції»), хоча статті переважно складаються із частин. Тому зміни повинні вноситись до частин статей відповідних законів.
| Перший заступник керівника Головного управління | С. Гудзинський |

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим