9 лютого виповнилося 3 роки з моменту запуску європейської системи верифікації лікарських засобів (European Medicines Verification — EMVS). Ця унікальна система забезпечує безпеку пацієнтів, виявляючи фальсифіковані ліки в легальному ланцюжку поставок. EMVS об’єднує 2500 фармацевтичних компаній, 4000 власників дозволів на оптове розповсюдження, 100 000 аптек, 6000 лікарняних аптек і 500 лікарів, які відпускають ліки в 29 країнах.
Тісна співпраця учасників була продемонстрована безперебійною роботою Європейської ради з контролю змін (European Change Control Board), центрального органу управління в рамках EMVS, що наглядав за управлінням та впровадженням понад 300 змін з моменту свого створення, а також зниженням загального рівня хибнопозитивних сповіщень, який знизився з 0,33% до 0,21% у 2021 р.
У вересні 2021 р. Бельгія, досягнувши цільового рівня сповіщень — 0,05%, розмістила на своєму сайті мапу країн (рисунок). За результатами минулого року Чехія повідомила про себе як одну з трьох найбільш успішних країн із рівнем сповіщень у діапазоні 0,01–0,04%. Угорщина досягла рівня 0,02%, Румунія — 0,03%.
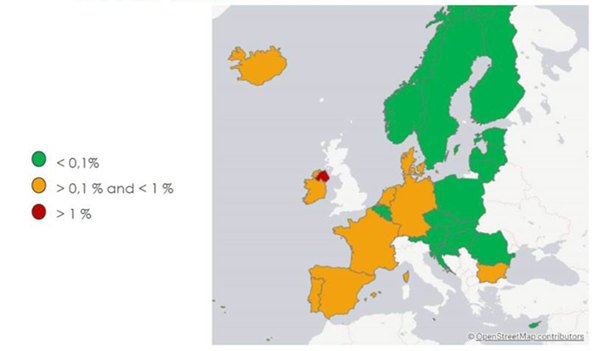
У жовтні до EMVO підключилася Франція. У 2022 р. EMVO зосередиться на досконалості операцій, управлінні сповіщеннями та підтримці повної відповідності законодавству. EMVS також з нетерпінням чекає на встановлення договірних відносин з Грецією й Італією та старанно працює над тим, аби забезпечити їх безперебійне підключення (при цьому згідно з індивідуальною домовленістю сплачується разовий внесок).
Умови використання системи
Репозиторії (EMVS та національні NMVS) фінансуються галуззю, для чого з операторів, які представляють власників реєстраційних посвідчень, стягується щорічний збір для фінансування національних систем, окремо встановлюваний для кожної країни (наприклад, за інформацією з Хорватії на 2022 р., він визначений у розмірі 37 500,00 хорватських кун, тобто близько 160 тис. грн; з Данії — 7800 євро або 250 тис. грн, з можливістю зменшення при обороті менше ніж 500 тис. датських крон (67 тис. євро)).
Для виробника лікарських засобів запровадження системи означає, що він має опанувати новий, надійний і відповідний процес дотримання вимог належної виробничої практики (good manufacturing practice — GMP) для отримання, запису, дослідження та вирішення кожного сповіщення у встановлені терміни. Отримання сповіщення вимагає швидких дій та офіційної відповіді, незважаючи на те, що більшість повідомлень не пов’язані з фальсифікованими лікарськими засобами. На ряді ринків тепер потрібен зворотній зв’язок до кінця наступного робочого дня (за часом ЄС). Аналогічні обов’язки покладаються на іншого «підключеного партнера», наприклад, національного представника. Обробка сповіщень стала юридичним обов’язком і тепер є частиною типового аудиту GMP.
Обов’язок під час відпуску ліків полягає в наступному:
- упаковку, щодо якої при скануванні отримано попередження про підозрювану фальсифікацію, не можна видати пацієнтові, доки не буде повністю досліджено попередження та виключено фальсифікацію ліків;
- попередження автоматично передаються до виробника та національного компетентного органу.
Ключовим пріоритетом EMVS на 2022 р. залишається підвищення активності кінцевих користувачів (аптек, лікарняних аптек та оптовиків) щодо перевірки та виведення з системи упаковок рецептурних ліків під час кожної видачі (у разі розділеної упаковки — під час першого відпуску). Це дозволить повністю досягти основної мети перевірки — захистити споживачів, гарантуючи справжність лікарських засобів.
Активність кінцевих користувачів — це показник, який вимірюється кількістю виведених з експлуатації упаковок по відношенню до загального обсягу ринку. Середньоєвропейський рівень становить 65%. При цьому деякі країни Європи досягли 100% активності в аптеках, а в Болгарії, наприклад, з системи виведено тільки 35–40% упаковок.
За матеріалами emvo-medicines.eu; bemvo.be; www.bgmvo.org;
hopal.hr; www.czmvo.cz; www.dmvo.dk; humvo.hu; osmr.ro

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим