Забезпеченість ліками в усьому світі останніми роками зазнала кількох досить чутливих впливів, пов’язаних із брекситом, COVID-19 (карантин в Китаї, заборона експорту з Індії, значне збільшення потреб), підвищенням захворюваності респіраторними хворобами у постковідний період). Навіть війна в Україні — країні, яка не є провідним постачальником фармацевтичної продукції, натомість є потужним експортером скляної фармацевтичної тари, робить негативний внесок у забезпечення ліками (Plüss J.D., 2023). Зростання цін на енергоносії через війну є одним із факторів, які зумовлюють цей дефіцит.
В умовах наростаючої нестачі ліків країни застосовують національні реєстри проблем з постачанням, фінансові санкції для виробників у разі непоставки та/або невідповідності вимогам щодо звітності чи зберігання, а також спрощені регуляторні процедури. Для визначених лікарських засобів запроваджено обов’язки зі створення запасів, а правові положення дозволяють видавати заборону на експорт (Vogler S., Fischer S., 2020). Реакція на дефіцит ліків з боку операторів ринку включає накопичення, перерозподіл, паралельний імпорт, подекуди — «сірий маркетинг» і закупівлю тимчасових запасів із націнкою 650–1400% від початкової вартості, що призводить до війни між окремими лікарнями та країнами за принципом «переможець отримує все» (Eom G. et al., 2016).
Благословенна складність
Досить тільки зазначити, що кількість «товарних одиниць», якими сьогодні оперують оптові постачальники, подекуди перевищує 100 тис. (рис. 1).
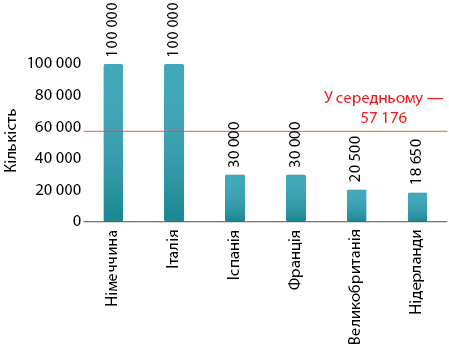
При цьому майже вичерпною номенклатурою лікарських засобів (і не тільки їх) оперують так звані дистриб’ютори широкого асортименту (full-line wholesalers). Ця ознака відмежовує їх від оптових компаній з обмеженим (short-line) асортиментом. Імплементуючи ст. 81 Директиви 2001/83/ЕС у національне законодавство, країни-члени покладають на дистриб’юторів широкого асортименту так звані обов’язки державної служби (Public Service Obligation — PSO) — суспільну відповідальність перед урядами. Відповідно до них ці оператори мають гарантувати постійну доступність адекватного асортименту лікарських засобів, і що вимоги конкретної географічної області (певного регіону чи країни в цілому) можуть бути задоволені у найкоротші терміни. На додаток до цього, PSO запобігають «збиранню вершків» у вигляді вибіркового оперування високомаржинальним товаром (дорогим або дуже масовим). Повну імплементацію відповідних положень забезпечили 23 країни ЄС (з них 15 — навіть суворіші режими PSO), 2 (Фінляндія та Швеція) — часткову та ще 2 (Латвія та Польща) не забезпечили згідно з даними 2022 р. ().
На додаток до PSO 8 країн ЄС (серед яких Чехія, Угорщина, Словаччина) запровадили також зобов’язання виробника або власника реєстраційного посвідчення постачати лікарські засоби дистриб’ютору широкого асортименту ().
Для забезпечення безперебійності дистриб’ютори широкого асортименту мають підтримувати швидку обіговість товару (рис. 2). Згідно з опитуванням, проведеним серед фармацевтів у 6 країнах ЄС, середній час доставки від них становить 4,6 год, а середня кількість доставок на тиждень — 16,02 (рис. 3). При цьому за середньозваженим показником об’єднують продукти від 18,8 різних виробників на поставку.
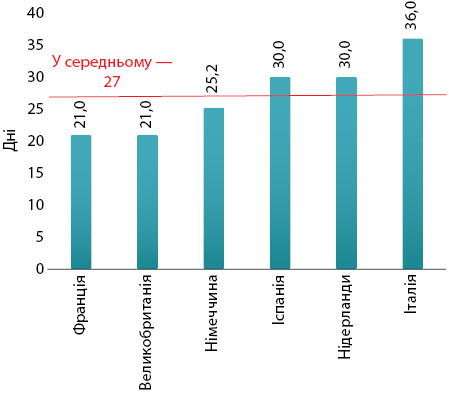
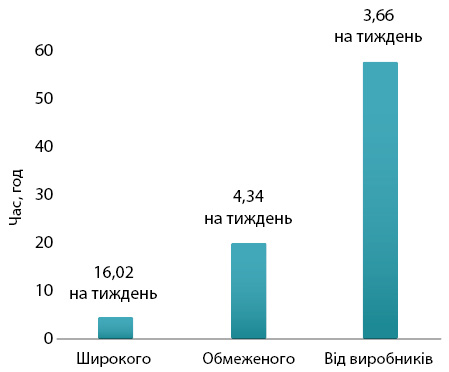
Обов’язки зі створення запасів
У багатьох європейських країнах (12 з 22 у 2020 р.) власники реєстраційних посвідчень та/або оптові оператори зобов’язані зберігати запаси визначених ліків протягом певного періоду (зазвичай щонайменше 3 міс) (Vogler S., Fischer S., 2020). Зокрема, у Нідерландах з 1 січня 2023 р. правило періодично перевірятиметься на предмет здійсненності та застосовності та оновлюватиметься за потреби. Перша оцінка відбудеться через рік після введення в дію (тобто 1 січня 2024 р.) (табл. 1).
| Зобов’язання | Нідерланди | Фінляндія |
| Задіяні оператори | В.Р.П. та дистр. | В.Р.П., імпортери, лікувальні заклади |
| Розрахунок кількості | Обсяги продажу за минулі 52 тиж ділять на 52 та множать на 6 (для В.Р.П.) або 4 (для дистр.) | В.Р.П. та імпортери: обсяги потреби на період від 9 міс (антибіотики, інфузійні розчини) до 3 міс (антинеопластичні та імуномодулюючі) на основі минулорічнихЛікувальні заклади: від 6 міс до 2 тиж |
| Відхилення від методу розрахунку | У разі сильного коливання попиту або після лончу | У разі сильного коливання попиту або відміни дозволу на маркетинг |
| Охоплення | Рецептурні, окрім персоналізованих та із терміном зберігання менше 1 року. Окремо кожна лікарська форма та дозування | Перелічено більше 100 міжнародних непатентованих назв (МНН) та деякі групові назви, наприклад, інсуліни короткої та тривалої дії, гама-глобуліни тощо |
| Компенсація | Немає | Базова державна відсоткова ставка + 2 або 4 процентних пункти від закупівельної ціни |
| Правова база | Staatscourant 2022, 17887 | Laki 19.12.2008/979Valtioneuvoston 1114/2008 |
Зобов’язання аптек
Таким чином, відповідальність за забезпечення сталості поставок у Європі покладають на дистриб’юторів та виробників (власників реєстраційних посвідчень). Фармацевти та їх помічники, що працюють в аптеках, повинні докладати розумних зусиль для забезпечення безперервності догляду за пацієнтом. При цьому можуть виникати певні договірні зобов’язання з підтримки деякого асортименту зі страховими компаніями зокрема. Таких прикладів дуже мало. В якості такого, що розповсюджується на всю країну, можна навести систему якості для аптек (Pharmacy Quality Scheme) в рамках контрактних взаємовідносин із Національною службою охорони здоров’я (National Health Service — NHS) Англії. В якості єдиного критерію якості, що стосується підтримки критичного асортименту, тут застосовують перелік з 16 лікарських засобів для надання паліативної допомоги:
1. Циклізин розчин для ін’єкцій ампули 50 мг/1 мл.
2. Циклізин таблетки 50 мг.
3. Дексаметазон розчин для ін’єкцій ампули 3,3 мг/1 мл.
4. Дексаметазон таблетки 2 мг.
5. Галоперидол таблетки 500 мкг.
6. Гіосцину бутилбромід розчин для ін’єкцій 20 мг/1 мл.
7. Левомепромазин розчин для ін’єкцій ампули 25 мг/1 мл.
8. Метоклопрамід розчин для ін’єкцій ампули 10 мг/2 мл.
9. Мідазолам розчин для ін’єкцій ампули 10 мг/2 мл.
10. Морфіну сульфат пероральний розчин 10 мг/5 мл.
11. Морфіну сульфат розчин для ін’єкцій ампули 10 мг/1 мл.
12. Морфіну сульфат розчин для ін’єкцій ампули 30 мг/1 мл.
13. Оксикодон розчин для ін’єкцій ампули 10 мг/1 мл.
14. Оксикодон пероральний розчин без цукру 5 мг/5 мл.
15. Натрію хлорид 0,9% розчин для ін’єкцій ампули 10 мл.
16. Вода для ін’єкцій 10 мл.
При цьому у 2022 р. аптечні фармацевтичні працівники ЄС щотижня витрачали в середньому 6,4 год на подолання проблем із нестачею лікарських засобів згідно зі згаданим вище опитуванням PGEU. У більшості країн для виходу з ситуації можна застосовувати генеричну заміну (93,10% країн), отримання тих самих ліків з альтернативних авторизованих джерел і аптечне виготовлення (обидва по 62,07%). До речі, за цими ж даними у більшості країн-респондентів (24,14%) на момент завершення опитування повідомлення про дефіцит стосувалися 600 лікарських засобів. Порівняно з попереднім роком (не вистачало 200–300 лікарських засобів) ситуація погіршилася.
Дефіцит від дефіциту відрізняється
Згадані вище національні реєстри проблем з постачанням можуть слугувати для безпосереднього моніторингу масштабів явища, але для оцінки та управління пов’язаними ризиками потрібний більш диференційований підхід. Наприклад, такий, що запропоновано італійськими науковцями та регуляторами (табл. 2). У ньому враховано те, що дефіцит виникне переважно ліків, що давно вийшли з-під патентного захисту. Під впливом закупівельної політики ціни на них постійно знижуються, а зацікавлених постачальників стає все менше. На відміну від них, ланцюги постачання нових ліків здебільшого стабільні, диверсифіковані, ресурси виробничих потужностей великі, розраховані на підвищення попиту. Заради справедливості слід зазначити, що досить дорогі, навіть захищені патентами ліки останнім часом також стають дефіцитними. Наприклад, аналоги глюкагоноподібного пептиду-1 (GLP-1), засоби для інгаляційного застосування при обструктивних захворюваннях дихальних шляхів, ін’єкційні антинеопластичні засоби тощо.
| Рівні (Level) | Бали (Score) |
| I. Мета застосування, у тому числі відповідно до нозології | А. Життєпідтримувальні, життєзабезпечувальні або рідкісні захворювання
В. Серйозні або виснажливі захворювання (гострі або хронічні) C. Інші хвороби |
| II. Наявні терапевтичні альтернативи | А. Не більше двох лікарських засобів із діючими речовинами, що належать до однієї групи III або IV рівнів АТС-класифікації
В. Більше двох лікарських засобів з тієї ж групи ATC III, але жодного — ATC IV С. Більше двох лікарських засобів з тієї ж ATC IV, але жодного генерика з ATC V (тим самим АФІ) D. Більше двох генериків з тієї ж ATC V |
| III. Частка у річному обсязі ринку в конкретній країні | Вище 50%
25–50% Менше 25% |
Одним із способів полегшення ситуації, що склалася, може бути обмеження номенклатури пріоритетних ліків, на яку погоджуються головні учасники процесу. Така ідея лежить в основі створення деяких державних формулярів. Дуже показовим та визначним явищем є поява останніми роками переліків, які призначені для забезпечення стратегічно важливих потреб. Його наявність не обов’язково означає, що уряд чи страховик повинні платити за ці ліки, хоча це може бути. Натомість в обов’язковому порядку забезпечуватиметься доступність критично важливого асортименту, необхідного для вирішення низки важливих проблем зі здоров’ям. Метою підтримки списку за відсутності вимоги забезпечення наявності є попередження дефіциту, оптимізація закупівель та допомога у призначенні (Eom G. et al., 2016).
Шведський «Мудрий список»
 Зазначеній меті більше відповідають невеликі переліки, такі як шведський «Мудрий список» (Kloka listan). У момент свого створення на початку 2000 р. він налічував близько 200 МНН, а у 2023 р. — вже близько 340 МНН. Відбір здійснюють на основі ефективності, безпеки, фармацевтичної придатності (представленість у різних лікарських формах та дозуваннях для різних потреб), економічної ефективності та екологічних аспектів. Наскільки цей перелік рестриктивний, можна проілюструвати таким прикладом: з 2023 р. цетиризин з нього видалили, і з усіх антигістамінних засобів залишився лише дезлоратадин (та очні краплі кетотифену при підвищеній чутливості до консервантів), бо його ефективність така ж сама, а експертна група хоче попередити одночасний прийом різних препаратів цієї групи. До речі, для лікування артеріальної гіпертензії із блокаторів бета-адренорецепторів пропонують тільки метопролол, антагоністів кальцію — амлодипін (klokalistan.se). На цьому ж сайті розміщено діючі прайси для (об’єднаних) закупівель.
Зазначеній меті більше відповідають невеликі переліки, такі як шведський «Мудрий список» (Kloka listan). У момент свого створення на початку 2000 р. він налічував близько 200 МНН, а у 2023 р. — вже близько 340 МНН. Відбір здійснюють на основі ефективності, безпеки, фармацевтичної придатності (представленість у різних лікарських формах та дозуваннях для різних потреб), економічної ефективності та екологічних аспектів. Наскільки цей перелік рестриктивний, можна проілюструвати таким прикладом: з 2023 р. цетиризин з нього видалили, і з усіх антигістамінних засобів залишився лише дезлоратадин (та очні краплі кетотифену при підвищеній чутливості до консервантів), бо його ефективність така ж сама, а експертна група хоче попередити одночасний прийом різних препаратів цієї групи. До речі, для лікування артеріальної гіпертензії із блокаторів бета-адренорецепторів пропонують тільки метопролол, антагоністів кальцію — амлодипін (klokalistan.se). На цьому ж сайті розміщено діючі прайси для (об’єднаних) закупівель.
Спеціалізовані переліки
Дефіцит і нерівний доступ до протипухлинних ліків став реальністю в Європі. У рамках проєкту Європейського товариства дитячої онкології (European Society for Paediatric Oncology — SIOPE) нещодавно створено перелік препаратів для педіатричного напрямку, щоб допомогти забезпечити безперервний доступ до них усім онкохворим дітям і підліткам (Otth M. et. al., 2022).
А яким має бути запас «критичних» ліків у госпітальних аптеках? Відповідь на це запитання надали експерти Європейської асоціації лікарняних фармацевтів (European Association of Hospital Pharmacists), створивши Європейський список лікарських засобів невідкладної допомоги (European List of Emergency Medicines — ELEM) (http://www.eahp.eu). Підготовлено, зокрема, два шаблони Excel. Перший — для оцінки потреби у лікарських засобах на основі кількості пацієнтів, який дозволяє кожній лікарні швидко оцінити свою частку відповідності запропонованому ELEM. Другий — це засіб керування запасами на випадок стихійних лих, що автоматично оновлює кількість наявних запасів.
Державні стратегічні резерви
Більшість держав підтримують необхідні запаси критично важливих ліків. Дієвість цього механізму було перевірено під час пандемії COVID-19. Деякі країни, наприклад, Уельс, скористалися цим досвідом і запровадили створення запасів силами власної NHS. Коли наприкінці 2022 р. різко підвищилася захворюваність на стрептококову інфекцію, NHS Уельсу закупила феноксиметилпеніцилін, термін придатності якого спливав через 6 тиж, — те, чого не могли собі дозволити комерційні оператори (Wickware C., 2023).
Список критичних ліків ЄС
Створення цього списку триває, як і було заплановано, під керівництвом спільної Цільової групи з питань наявності дозволених лікарських засобів для використання людьми та ветеринарами (Task Force on the Availability of Authorised Medicines for Human and Veterinary Use — TF AAM) Європейського агентства з лікарських засобів (European Medicines Agency — EMA) Європейської комісії та керівників медичних агентств (Heads of Medicines Agencies — HMA). Мета списку полягає в тому, щоб допомогти забезпечити постійну доступність ліків, які є найбільш критичними для систем охорони здоров’я в ЄС/Європейській економічній зоні (ЄЕЗ). У цьому переліку будуть каталогізовані лікарські засоби, які чинять значний вплив на громадське здоров’я, щодо яких необхідно вжити заходів для посилення їх постачання, щоб забезпечити безперервність лікування пацієнтів у будь-який час. Очікується, що перша версія списку критично важливих лікарських засобів ЄС буде опублікована до кінця 2023 р.
Паралельно у Європі тривають процеси створення «відкритої стратегічної автономії для конкурентоспроможного та стійкого ЄС» — стратегія під назвою «Resilient EU 2030». Вона передбачає, зокрема, збільшення виробництва найважливіших фармацевтичних продуктів, таких як готові ліки та активні фармацевтичні інгредієнти. На національному рівні також працюють над забезпеченням фармацевтичної безпеки. Списки критично важливих ліків складають спеціально створена урядова комісія у Польщі, Федеральний інститут лікарських засобів та медичних виробів (Bundesinstitut für Arzneimittel und Medizinprodukte — BfArM) Німеччини, Управління з контролю за харчовими продуктами та лікарськими засобами США (Food and Drug Administration — FDA) тощо.
При цьому німецький перелік включає 22 активні фармацевтичні інгредієнти, тоді як американський — 223 основні лікарські засоби, вакцини, компоненти крові, а також 96 медичних виробів та приладів, у тому числі комплекти діагностичних тестів, засоби індивідуального захисту, активного контролю показників життєдіяльності та лікування гострих захворювань, такі як апарати штучної вентиляції легень та ін. У цей перелік увійшли основні лікарські засоби, найбільш необхідні пацієнтам у медичних установах США, що спеціалізуються на наданні допомоги при тяжких травмах та гострих захворюваннях, а також невідкладних медичних станах.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим