НОВІГРА від “Рейнбо-Лтд” вирішення важливої проблеми
Усі, кому відома проблема еректильної дисфункції (ЕД), мають пам'ятати, що лише лікар може встановити точний діагноз (який є лише діагнозом, а не вироком). Останнім часом розроблено принципово нові методи терапії, тому вчасно розпочате лікування допоможе вирішити важливу проблему.
Міністерство охорони здоров’я УкраїниНаказ від 11.02.2004 р. № 79
ПРО ЗАТВЕРДЖЕННЯ ПОРЯДКУ ЗАЛУЧЕННЯ ЕКСПЕРТІВ, ЕКСПЕРТНИХ ОРГАНІЗАЦІЙ ДЛЯ РОЗГЛЯДУ І ВИРІШЕННЯ ПИТАНЬ, ЩО НАЛЕЖАТЬ ДО ПОВНОВАЖЕНЬ ДЕРЖАВНОЇ СЛУЖБИ ЛІКАРСЬКИХ ЗАСОБІВ І ВИРОБІВ МЕДИЧНОГО ПРИЗНАЧЕННЯ
Всеукраинский фармацевтический рейтинг “Еженедельника Аптека” Лучшие при равных условиях. “Фармэксперт”: в поле зрения – производитель-2003
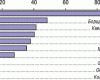
Восьмой с начала года и первый с начала весны номер "Еженедельника АПТЕКА" традиционно - седьмой год подряд - представляет вниманию своих читателей результаты рейтинга "ФармЭксперт". Для наших читателей за этой традицией стоит ежегодная возможность получить четкую, объективную и достоверную "кардиограмму" фармацевтического рынка Украины. Наш рейтинг расширяет охват и получает новые "ответвления": в этом году заработал "ФАРМСТАНДАРТ", который позволяет отобразить картину розничных продаж в украинских аптечных учреждениях. Под именем "ФармЭксперт" объединены три рейтинга: "ВЗГЛЯД ИЗ АПТЕКИ", "ЭКСПЕРТНЫЙ ПРОФИЛЬ" и "ПРОГРАММА ПАРТНЕРСТВА", что важно для соблюдения двух наиболее значимых для любого исследования параметров - достоверности и объективности (при сопоставлении их результаты не только дополняют, но и подтверждают правильность выводов). Все они используют разные подходы и методологии, но в целом позволяют отразить объективную картину фармацевтического рынка. Сегодня мы представляем рейтинги производителей лекарственных средств и изделий медицинского назначения по итогам 2003 г. С рейтингами дистрибьюторов, в том числе "Программа партнерства", вы сможете ознакомиться в следующем номере "Еженедельника АПТЕКА". Если во "ВЗГЛЯДЕ ИЗ АПТЕКИ" отражено мнение наиболее активных украинских провизоров и фармацевтов (читатели "Еженедельника АПТЕКА" самостоятельно заполняли опубликованные анкеты и присылали их в редакцию), то в "ЭКСПЕРТНОМ ПРОФИЛЕ" - объективная картина рынка, полученная методом опроса экспертов - сотрудников аптек, дистрибьюторов и производителей (для этого опроса на основании четких критериев были отобраны специалисты, которые по уровню квалификации и осведомленности могут выступать в качестве экспертов в исследуемом сегменте рынка). Опрос экспертов является наиболее точной формой рейтинга. Во-первых, мало кто знает этот рынок лучше их, во-вторых, имеются необходимые данные для осуществления оценки выборки и структуры рынка, поэтому его результаты представляются наиболее объективными.
Державна інспекція з контролю якості лікарських засобів Міністерства охорони здоров’я УкраїниПрипис від 14.01.2004 р. № 99/07-21
Заборонено реалізацію (торгівлю), зберігання та застосування лікарського засобу Диклопар, таблетки 500 мг/50 мг № 100, серії 108, виробництва "Flamingo Pharmaceuticals Ltd", Індія, до окремого розпорядження Державної інспекції з контролю якості лікарських засобів МОЗ України.
МІОРИТМІЛ-ДАРНИЦЯ: досвід дарує впевненість
Сьогодні арсенал лікаря об'єднує значну кількість лікарських засобів для терапії пацієнтів із порушеннями серцевого ритму. Але досі аритмії залишаються однією з основних нозологій, з якою стикаються у своїй практичній діяльності як кардіологи, так і лікарі загальної практики, через те, що причини їх виникнення надзвичайно різноманітні: ішемічна хвороба серця (ІХС), порушення електролітного балансу, артеріальна гіпертензія, гіперфункція щитоподібної залози тощо. Враховуючи актуальність проблеми, ми продовжуємо цикл публікацій, що ставлять за мету ознайомлення читачів з досвідом застосування ефективних антиаритмічних засобів, зокрема, препарату виробництва "Фармацевтичної фірми "Дарниця" МІОРИТМІЛ-Дарниця ("Щотижневик АПТЕКА", № 47 (418) від 8 грудня та № 48 (419) від 15 грудня 2003 р.) в клінічній практиці. У цій публікації узагальнено досвід застосування препарату МІОРИТМІЛ-Дарниця на основі клінічного дослідження, що проводилося в Кримському республіканському кардіологічному диспансері (керівник дослідження - головний кардіолог МОЗ АР Крим, головний лікар Кримського республіканського кардіологічного диспансеру П.І. Філін).
Державна інспекція з контролю якості лікарських засобів Міністерства охорони здоров’я УкраїниПрипис від 16.01.2004 р. № 124/07-15
Заборонено реалізацію (торгівлю) та застосування:
ДЕКСАМЕТАЗОН НІКОМЕД, розчин для ін'єкцій по 4 мг в ампулах по 1 мл № 5, виробництва "Hafslund Nycomed", Австрія;
ДОКСИЦИКЛІНУ ГІДРОХЛОРИД, порошок для приготування розчину для ін'єкцій по 0,1 г у флаконах № 1, виробництва ЗАТ "Бринцалов-А", Російська Федерація;
РОЗЧИН РІНГЕРА, розчин для інфузій по 500 мл у флаконах № 1, виробництва "Hemofarm DD", Югославія;
СУПОЗИТОРІЇ ГЕМОРЕКТАЛ, супозиторії ректальні № 10, виробництва "GlaxoWellcome S.А.", Польща;
ФЛАГІЛ, таблетки по 250 мг № 20, виробництва "Specia", Франція.
Державна інспекція з контролю якості лікарських засобів Міністерства охорони здоров’я Українивід 30.01.2004 р. № 324/07-15
Лікарський засіб ФЛАГІЛ, таблетки по 250 мг № 20, виробництва "Specia", Франція, за-реєстрований до 12.05.05 за номером реєстраційного посвідчення П.05.00/01740.
Державна інспекція з контролю якості лікарських засобів Міністерства охорони здоров’я УкраїниПрипис від 22.01.2004 р. № 201/07-08
Заборонено реалізацію (торгівлю), зберігання та застосування лікарського засобу Бороментол, мазь по 25 г у банках, серії 101102, виробництва ВАТ "Тернопільська фармацевтична фабрика", м. Тернопіль.
“Зентіва”: енергія двох компаній
На світовому фармацевтичному ринку вже протягом декількох років спостерігається тенденція до укрупнення компаній за рахунок їх злиття. У "Щотижневику АПТЕКА", № 36 (407) від 22 вересня 2003 р. повідомлялося про помітну подію, пов'язану з появою на фармацевтичному ринку нового "сильного гравця" - компанії "Зентіва", що утворилася в результаті злиття компаній "Лечіва" (Чехія) і "Словакофарма" (Словаччина). Які перспективи відкриває об'єднання цих виробників і як буде будуватися робота нової компанії на українському фармацевтичному ринку? На ці та інші запитання відповідає голова представництва компанії "Зентіва" в Україні Костянтин Лебедєв.
Аптечные продажи в Украине. Год 2003
При подготовке публикации использованы данные системы исследований "Фармстандарт" ООО "Морион".