Блокаторы кальциевых каналов способны бороться с ожирением и нарушением сна
Некоторые исследования подтверждают, что диета влияет на сон, другие же — что нарушение сна может провоцировать изменения аппетита, набор веса и общий гормональный дисбаланс.
FDA заявляет, что инспекция завода компании «Mylan» продолжается
Данный комментарий последовал вслед за заявлением, сделанным «Mylan» днем ранее, согласно которому управление пришло к заключению, что обвинения, опубликованные в «Pittsburgh Post-Gazette», необоснованы.
Реакция фармацевтических компаний на ужесточение требований к безопасности препаратов
Результаты опроса, проведенного «ICON Clinical Research» и «IMS Health», показали, что компаниям необходимо позаботиться о повышении своих регуляторных ресурсов, если они собираются успешно выполнять требования к безопасности лекарственных средств, действующие в Европе и США.
Вальпроат приводит к нарушениям когнитивных функций у потомства
ети, подвергшиеся воздействию вальпроата в утробе матери, демонстрировали существенное снижение уровня интеллекта по сравнению с теми, чьи матери во время беременности принимали карбамазепин, ламотригин или фенитоин.
Наименее развитым странам открыт доступ к интеллектуальной собственности
В рамках проекта сотрудничества государственного и частного секторов в этих странах будет открыт доступ к научной литературе, что будет способствовать устранению пробелов в научном развитии.
Открытие фармацевтического сезона в Украине – «Pharmanet Session 2009». 15 сентября 2009 г. Конференц-центр Президент Отеля.
Открытие фармацевтического сезона в Украине – «Pharmanet Session 2009». 15 сентября 2009 г. Конференц-центр Президент Отеля. Уважаемые коллеги, друзья, партнеры! Одной из главных особенностей Первого независимого фармацевтического бизнес портала является инновационность в подходах к любым начинаниям. Примерами таких подходов была организация и проведение Пресс-клубов – мероприятий с новой философией и нового формата: Первый Пресс-клуб : «Финансовый кризис: причины, масштабы и последствия для […]
Проект наказу МОЗ «Про визнання таким, що втратив чинність, наказу МОЗ України від 12.12.2001 р. № 497»
Проект щодо визнання наказу МОЗ "Про затвердження Порядку заборони (зупинення) та вилучення з обігу лікарських засобів на території України" таким, що втратив чинність.
FDA направляет «Shire» завершающее ответное письмо по Intuniv
Компания и регуляторный орган так и не смогли достичь единогласия относительно маркировки к данному препарату.
ЖИЗНЬ — ДЕРЖИСЬ! Мнение врачей и фармацевтов относительно финансового кризиса
Во время кризиса ценна любая информация как о рынке, так и о состоянии экономики в стране. И важнейшим элементом здесь является информация об отношении к кризису различных целевых групп. Особенности восприятия кризиса, резистентность к нему и информация о предполагаемых формах поведения могут рассматриваться как основные элементы, на базе которых может строиться маркетинговая стратегия компаний-производителей в кризисный период.
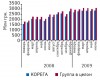
КОРЕГА — популярный брэнд, которому доверяют!
Сегодня многие вынуждены носить съемные зубные протезы, что сопряжено с рядом неудобств, избежать которых поможет фиксирующий крем для зубных протезов КОРЕГА — безусловный лидер в данной категории товаров.