Термин «орфанные болезни» (редкие заболевания) впервые появился в США в 1983 г. при принятии закона о препаратах-сиротах («Orphan Drug Act»), предназначенного для поощрения фармацевтических компаний к разработке лекарственных средств для лечения заболеваний, которые занимают небольшой объем рынка. На тот момент Управлением по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) было одобрено к применению 38 орфанных препаратов. Для сравнения по состоянию на октябрь 2014 г. согласно отчету аналитической компании «Evaluate Pharma» «Orphan Drug Report 2014», в США одобрено 373 орфанных препарата. Дополнительным свидетельством успеха законодательных инициатив США стало принятие аналогичных законов Японией (в 1993 г.) и ЕС (в 2000 г.).
Стоит отметить, что не существует единого широко принимаемого определения редких заболеваний. Некоторые определения основываются на количестве лиц, живущих с заболеванием, другие могут включать иные факторы, например, доступность лечения или возможность облегчения течения заболевания. В США редким заболеванием считается патология, диагностированная менее чем у 200 тыс. человек, что составляет менее 6,4 пациента на 10 тыс. человек (из расчета, что население США составляет 314 млн человек). В странах ЕС под определение «редкое заболевание» подпадают состояния, отмечаемые менее чем у 5 пациентов на 10 тыс. человек или у менее 250 тыс. больных, при том что население стран ЕС составляет 506 млн человек. Для сравнения в Японии заболевание считается орфанным, если от него страдает менее 50 тыс. человек (то есть менее 4 на 10 тыс.), из расчета, что население Японии составляет 128 млн человек.
По данным аналитической компании «Evaluate Pharma», объем продаж орфанных препаратов в США, ЕС и Японии будет уверенно увеличиваться до 2020 г. Причина этому — в снижении затрат на разработку орфанных препаратов по сравнению с инновационными лекарственными средствами, предназначенными для лечения заболеваний в большой популяции, повышении продуктивности таких разработок по сравнению с последними и др. Одной из ключевых законодательных инициатив, призванных стимулировать разработку орфанных лекарственных средств, является продление срока их патентной защиты по сравнению с другими инновационными лекарственными средствами.
Кроме того, фармацевтическим компаниям, которые занимаются разработками таких лекарственных средств в США, предоставляются различные финансовые льготы для осуществления своих проектов. Таким компаниям полагается 50% налоговый кредит на R&D-расходы. Также правительство США дает гранты на проведение I–III фазы клинических исследований продуктов, предназначенных для лечения редких заболеваний, в объеме 30 млн дол. США. Отменены налоговые сборы с потребителей этой продукции, что делает ее более доступной и способствует увеличению объема продаж таковой в натуральном выражении.
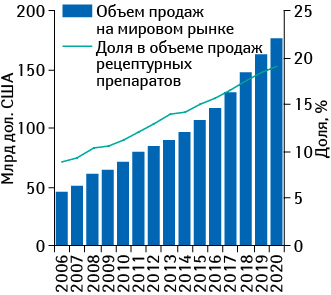
По данным отчета «Orphan Drug Report 2014», доля орфанных препаратов в общем объеме продаж рецептурных лекарственных средств (за исключением генериков) к 2020 г. составит 19,1% (около 176 млрд дол. США), при этом среднегодовой прирост (CAGR) в период 2014–2020 гг. в денежном выражении составит 10,5% (рис. 1). Для сравнения среднегодовой прирост (CAGR) доли лекарственных средств для лечения заболеваний, часто выявляемых в популяции и не относящихся к орфанным, за данный период составит лишь 4,3%, а рецептурных лекарственных средств — 5,3%. Таким образом, можно проследить четкую тенденцию, способствующую увеличению доли орфанных препаратов в общем объеме продаж рецептурных лекарственных средств (за исключением генериков) начиная с 8,9% в 2006 г. до 19,1% в 2020 г. При этом их удельный вес в 2014 г. составил 14,3%.
ОСНОВНЫЕ ИГРОКИ НА МИРОВОМ РЫНКЕ ОРФАННЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
По прогнозам аналитической компании «Evaluate Pharma», в топ-10 фармацевтических компаний по объему продаж орфанных препаратов в денежном выражении на мировом рынке в 2020 г. войдут компании «Bristol-Myers Squibb», «Novartis», «Celgene», «Roche», «Pfizer», «Alexion Pharmaceuticals», «Sanofi», «Vertex Pharmaceuticals», «GlaxoSmithKline», «Merck & Co» (рис. 2). Ожидается, что тройку лидеров по данному показателю возглавит компания «Bristol-Myers Squibb» с объемом продаж орфанных препаратов на мировом рынке в 2020 г. в 11,1 млрд дол., за ней будет следовать компания «Novartis» с показателем в 10,5 млрд дол. и компания «Celgene» с 10,4 млрд дол. Стоит отметить, что в 2013 г. лидирующую позицию в этом рейтинге занимала компания «Novartis» с объемом продаж орфанных препаратов на мировом рынке в 11,3 млрд дол.
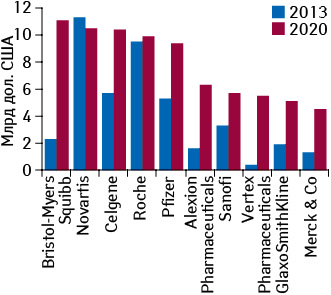
Как ожидается, за период 2013–2020 гг. объем продаж орфанных препаратов на мировом рынке компании «Bristol-Myers Squibb» увеличится с 2,3 млрд дол. в 2013 г. до 11,1 млрд дол. в 2020 г., среднегодовой прирост за данный период составит 26%. Немалых успехов удастся добиться и таким компаниям, как «Vertex Pharmaceuticals» и «Alexion Pharmaceuticals», среднегодовой прирост объема продаж в денежном выражении орфанных препаратов данных компаний на мировом рынке за период 2013–2020 гг., как ожидается, составит 47 и 22% соответственно.
ЗОЛОТЫЕ ПЛОДЫ: ЛИДЕРЫ РЫНКА ОРФАННЫХ ПРЕПАРАТОВ И ПЕРСПЕКТИВНЫЕ R&D-РАЗРАБОТКИ
Какие препараты помогут фармацевтическим компаниям добиться успеха и увеличения объема продаж орфанных лекарственных средств на мировом рынке? Компании «Celgene» поможет в этом иммуномодулятор Revlimid (леналидомид), предназначенный для лечения множественной миеломы, миелодиспластического синдрома, мантийноклеточной лимфомы. Ожидается, что объем продаж данного препарата за период 2013–2020 гг. увеличится практически в 2 раза, с 4,28 млрд дол. в 2013 г. до 8 млрд дол. в 2020 г., что позволит ему занять позицию лидера в рейтинге топ-10 орфанных препаратов по объему продаж на мировом рынке в 2020 г. (рис. 3), при этом среднегодовые темпы увеличения объема продаж данного средства составят 9%.
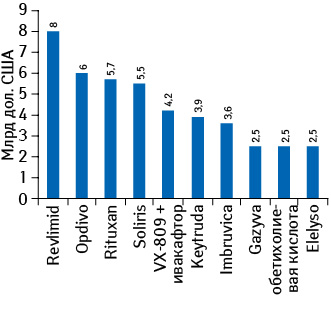
Вторую строчку рейтинга с объемом продаж в 6 млрд дол. на мировом рынке в 2020 г., по прогнозам, займет лекарственное средство Opdivo (ниволумаб) компании «Bristol-Myers Squibb», показанное к применению при нерезектабельной или метастатической меланоме, резистентной к другим лекарственным средствам, одобренное FDA в декабре 2014 г. Замыкает тройку лидеров препарат Rituxan (ритуксимаб) компании «Roche», предназначенный для лечения неходжкинской лимфомы, острого лимфолейкоза, ревматоидного артрита в комбинации с метотрексатом, а также гранулематоза Вегенера и микроскопического полиангиита в комбинации с глюкокортикостероидами.
Среди орфанных препаратов, которые сейчас находятся в стадии разработки, в топ-10 наиболее перспективных попали кандидаты в препараты таких фармацевтических компаний, как «Vertex Pharmaceuticals» (2 продукта), «Intercept Pharmaceuticals», «Northwest Biotherapeutics», «Actelion», «AbbVie» и «Alexion Pharmaceuticals» (2 продукта) и др. (табл. 1).
| Таблица 1 | Топ-10 наиболее перспективных кандидатов в орфанные препараты |
| № п/п | Кандидат в препараты | Компания | Терапевтическая сфера применения | Прогнозируемый объем продаж на мировом рынке в 2020 г., млрд дол. | NPV, млрд дол. |
|---|---|---|---|---|---|
| 1 | VX-809 + ивакафтор | «Vertex Pharmaceuticals» | Муковисцидоз | 4,23 | 13,78 |
| 2 | Обетихолиевая кислота | «Intercept Pharmaceuticals» | Заболевания печени | 2,52 | 7,61 |
| 3 | DCVax-L | «Northwest Biotherapeutics» | Онкопатология | 2,05 | 5,67 |
| 4 | Селексипаг | «Actelion» | Легочная артериальная гипертензия | 1,27 | 2,38 |
| 5 | RG7601/ABT-199 | «AbbVie» | Онкопатология | 0,79 | 2,38 |
| 6 | ENB-0040 | «Alexion Pharmaceuticals» | Гипофосфатазия | 0,82 | 2,16 |
| 7 | Элотузумаб | «Alexion Pharmaceuticals» | Онкопатология | 0,71 | 2,14 |
| 8 | MLN9708 | «Takeda» | Онкопатология | 0,66 | 1,90 |
| 9 | VX-809 | «Vertex Pharmaceuticals» | Муковисцидоз | 0,74 | 1,83 |
| 10 | Себелипаза альфа | «Synageva BioPharma» | Болезнь Вольмана | 0,81 | 1,70 |
Первая позиция в данном рейтинге принадлежит комбинации VX-809 + ивакафтор компании «Vertex Pharmaceuticals», предназначенной для лечения муковисцидоза. Ожидается, что в 2020 г. объем продаж данного продукта на мировом рынке составит 4,23 млрд дол., а чистая приведенная стоимость (Net present value — NPV) этого проекта — более 13,78 млрд дол.
Стоит отметить, что NPV показывает объем средств, которые инвестор ожидает получить от проекта после того, как денежные притоки окупят его первоначальные инвестиционные вложения и периодические денежные оттоки, связанные с осуществлением проекта. В упрощенном виде NPV можно трактовать как стоимость, добавляемую проектом.
В 2013 г. из 35 новых препаратов, одобренных FDA, 16 были классифицированы как орфанные. Таким образом, доля орфанных лекарственных средств в структуре одобренных FDA в 2013 г. составила 46%. В свою очередь, в 2014 г. FDA выдало разрешение на маркетирование 41 инновационного лекарственного средства, благодаря чему этот год стал рекордным за последние 18 лет по количеству одобренных FDA инновационных препаратов (с 1996 г., когда было утверждено 53 инновационных препарата). По данным информационного агентства «Reuters», орфанные препараты составляют почти 40% утвержденных FDA в 2014 г. новых лекарственных средств.
Рейтинг топ-10 орфанных препаратов по объему продаж в денежном выражении в США в 2014 г. возглавил препарат Rituxan (ритуксимаб) компании «Roche» с показателем 3,71 млрд дол. (табл. 2) За ним следует препарат Revlimid (леналидомид) компании «Celgene» с показателем 2,87 млрд дол. и Copaxone (глатирамера ацетат) компании «Teva Pharmaceutical Industries», предназначенный для лечения рассеянного склероза, с объемом продаж в США в 2014 г. в 2,7 млрд дол.
| Таблица 2 | Топ-10 орфанных препаратов по объему продаж в денежном выражении в США в 2014 г. |
| № п/п | Препарат | Действующее вещество | Компания | Объем продаж в США в 2014 г., млрд дол. |
|---|---|---|---|---|
| 1 | Rituxan | Ритуксимаб | «Roche» | 3,71 |
| 2 | Revlimid | Леналидомид | «Celgene» | 2,87 |
| 3 | Copaxone | Глатирамера ацетат | «Teva Pharmaceutical Industries» | 2,70 |
| 4 | Gleevec | Иматиниба месилат | «Novartis» | 2,02 |
| 5 | Avonex | Интерферон бета-1 альфа | «Biogen Idec» | 1,91 |
| 6 | Alimta | Пеметрексид дисодиум | «Eli Lilly» | 1,25 |
| 7 | Rebif | Интерферон бета-1 альфа | «Merck KGaA» | 1,24 |
| 8 | Velcade | Бортезомиб | «Takeda» | 0,98 |
| 9 | NovoSeven/NovoSeven RT | Эптаког альфа | «Novo Nordisk» | 0,83 |
| 10 | Advate | Фактор VIII (прокоагулянт) | «Baxter International» | 0,82 |
Стоит отметить, что в 2014 г. Европейское агентство по лекарственным средствам (European Medicines Agency — EMA) рекомендовало к одобрению наибольшее количество орфанных препаратов. Из 82 лекарственных средств для применения у человека, рекомендованных к одобрению в 2014 г., 17 предназначены для терапии больных с редкими заболеваниями, среди них препарат Translarna (аталурен) компании «PTC Therapeutics, Inc», предназначенный для лечения пациентов с мышечной дистрофией Дюшенна, Scenesse (афамеланотид) компании «Clinuvel Pharmaceuticals» — первый препарат для терапии эритропоэтической протопорфирии, а также первый препарат стволовых клеток, одобренный EMA, Holoclar компаний «Chiesi Farmaceutici S.p.A» и «Holostem Terapie Avanzate», предназначенный для лечения дефицита лимбальных стволовых клеток, обусловливающего развитие корнеальной слепоты. Активный компонент этого средства — собственные лимбальные стволовые клетки пациента, взятые из неповрежденного участка роговицы, а затем культивированные в лабораторных условиях и вновь пересаженные в пораженную часть глаза.
Таким образом, благодаря законодательным инициативам США и стран ЕС по стимулированию R&D-разработок орфанных препаратов, удается постепенно повысить доступность и эффективность таких препаратов для пациентов с редкими заболеваниями.
По материалам http://www.evaluategroup.com, http://www.fda.gov, http://www.reuters.com, http://www.ema.europa.eu, http://www.pharmexec.com

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим