АНТИМОНОПОЛЬНИЙ КОМІТЕТ УКРАЇНИ
РЕКОМЕНДАЦІЙНІ РОЗ’ЯСНЕННЯ
від 21.02.2019 р. № 5-рр
щодо застосування законодавства про захист економічної конкуренції учасниками ринків лікарських засобів у вертикальних відносинах щодо постачання та просування лікарських засобів
І. Правове регулювання
1. Під узгодженими діями Закон України «Про захист економічної конкуренції» (далі — Закон) розуміє укладення суб’єктами господарювання угод у будь-якій формі, прийняття об’єднаннями рішень у будь-якій формі, а також будь-яку іншу погоджену конкурентну поведінку (діяльність, бездіяльність) суб’єктів господарювання (стаття 5).
Вертикальні узгоджені дії суб’єктів господарювання стосовно постачання та використання товарів — це узгоджені дії, в яких беруть участь два або більше суб’єктів господарювання, що в межах таких узгоджених дій діють на різних рівнях ланцюга виробництва або постачання, та учасники яких можуть купувати, продавати або перепродавати окремі товари.
2. За загальною нормою статті 6 Закону, узгоджені дії, що призвели чи можуть призвести до недопущення, усунення чи обмеження конкуренції, є антиконкурентними узгодженими діями (частина 1), вчинення яких забороняється (частина 4).
3. Частина перша статті 8 Закону, як виняток, допускає вертикальні узгоджені дії щодо постачання чи використання товарів, навіть якщо один учасник таких дій (постачальник) стосовно іншого учасника (покупця) встановлює обмеження на:
- використання поставлених ним товарів чи товарів інших постачальників;
- придбання в інших суб’єктів господарювання або продаж іншим суб’єктам господарювання чи споживачам інших товарів;
- придбання товарів, які за своєю природою або згідно з торговими та іншими чесними звичаями у підприємницькій діяльності не належать до предмета угоди;
- формування цін або інших умов договору про продаж поставленого товару іншим суб’єктам господарювання чи споживачам.
Але такі вертикальні узгоджені дії не допускаються, якщо вони призводять до істотного антиконкурентного впливу на ринок, а саме:
- призводять до суттєвого обмеження конкуренції на всьому ринку чи у значній його частині, у тому числі монополізації відповідних ринків;
- обмежують доступ на ринок інших суб’єктів господарювання;
- призводять до економічно необгрунтованого підвищення цін або дефіциту товарів (частина друга статті 8 Закону).
4. Дозволяються і не потребують отримання дозволу органів Комітету вертикальні узгоджені дії суб’єктів господарювання, які відповідають положенням Типових вимог до вертикальних узгоджених дій суб’єктів господарювання стосовно постачання та використання товарів, затверджених розпорядженням Антимонопольного комітету України від 12.10.2017 № 10-рп, зареєстрованих у Міністерстві юстиції України 09.11.2017 за № 1364/31232 (із змінами) (далі — Типові вимоги)1.
Зокрема, є дозволеними вертикальні узгоджені дії, якщо частка кожного з їх учасників (як постачальника, так і покупця) на відповідному ринку контрактного товару не перевищує 30% (пункт 1 частини першої розділу 2 Типових вимог).
5. Водночас, незалежно від розміру часток учасників, загальний дозвіл Типових вимог не поширюється на вертикальні узгоджені дії, що містять жорсткі (англ. hardcore) вертикальні обмеження, до яких належать положення, що, зокрема:
1) прямо або непрямо встановлюють фіксовану чи мінімальну ціну перепродажу покупцем контрактного товару;
Як виняток, не вважається «жорстким» обмеженням встановлення постачальником максимальної або рекомендованої ціни перепродажу, а також рекомендації постачальника щодо цінової політики покупця, що не передбачають жодних зобов’язань з боку покупця. Але якщо різниця між встановленою максимальною ціною перепродажу і ціною постачання товару покупцеві-дистриб’юторові є настільки малою, що не дозволить покупцеві встановлювати ціну перепродажу, нижчу за максимальну, без понесення збитків, таке встановлення максимальної ціни розглядається як форма встановлення фіксованої ціни;
2) обмежують територію або коло замовників, у межах якої або яким покупець-дистриб’ютор може перепродавати контрактний товар, або обмежують перехресні поставки між покупцями — учасниками вибіркової системи постачання, або обмежують активні та пасивні продажі товару кінцевим споживачам учасниками вибіркової системи постачання, які діють на ринку роздрібної торгівлі;
Як винятки, не вважаються «жорсткими» і допускаються встановлення постачальником:
- обмеження активних продажів покупцем контрактного товару виключній групі замовників або на виключній території, щодо яких постачальник залишив за собою право виключного продажу товару або надав це право іншому суб’єктові господарювання, за умови, що таке обмеження не призводить до скорочення обсягів продажу відповідного товару замовниками цього покупця;
- обмеження на продаж товару кінцевим споживачам покупцем, який здійснює діяльність на рівні оптової торгівлі;
- обмеження продажів товару учасниками вибіркової системи постачання суб’єктам господарювання, яким постачальник не надавав права перепродажу товару на території, яка закріплена постачальником, для функціонування цієї системи постачання;
- обмеження щодо місцезнаходження покупця, а також заборони учасникові вибіркової системи постачання здійснювати діяльність із певного місця, не дозволеного для цього.
6. Якщо на певному ринку паралельні (не пов’язані між собою) мережі схожих вертикальних обмежень охоплюють понад 50 відсотків ринку, органи Антимонопольного комітету України можуть прийняти розпорядження про незастосування дозволу, передбаченого Типовими вимогами, до таких узгоджених дій, за винятком узгоджених дій, що фактично мали місце на час прийняття такого розпорядження.
7. Якщо вертикальні узгоджені дії не є дозволеними відповідно до Типових вимог, суб’єкти господарювання мають право звернутися до органів Комітету за одержанням дозволу на такі дії у порядку статті 10 Закону, довівши, що такі вертикальні узгоджені дії сприяють:
- вдосконаленню виробництва, придбанню або реалізації товару;
- техніко-технологічному, економічному розвитку;
- розвитку малих або середніх підприємців;
- оптимізації експорту чи імпорту товарів;
- розробленню та застосуванню уніфікованих технічних умов або стандартів на товари;
- раціоналізації виробництва.
8. Водночас, навіть якщо вертикальні узгоджені дії відповідають зазначеним вище вимогам, вони не можуть бути дозволені Антимонопольним комітетом України, якщо буде встановлено, що ці узгоджені дії суттєво обмежують (обмежать) конкуренцію на всьому ринку чи в значній його частині.
9. Узгоджені дії, на які не було надано дозволу Антимонопольним комітетом України, можуть бути дозволені Кабінетом Міністрів України, якщо учасники узгоджених дій доведуть, що позитивний ефект для суспільних інтересів переважає негативні наслідки обмеження конкуренції, за винятком випадків, коли учасники узгоджених дій застосовують обмеження, які не є необхідними для реалізації узгоджених дій, або обмеження конкуренції становить загрозу системі ринкової економіки. Порядок надання Кабінетом Міністрів України дозволу на узгоджені дії суб’єктів господарювання затверджено постановою Кабінету Міністрів України від 28 лютого 2002 р. № 219.
ІІ. Особливості функціонування ринків лікарських засобів
10. У процесі руху лікарських засобів від виробника до споживача беруть участь такі суб’єкти:
а) виробники лікарських засобів та їх представництва;
б) представники (дистриб’ютори) виробників лікарських засобів;
в) оптові продавці лікарських засобів, у тому числі асортиментні компанії;
г) суб’єкти господарювання, які здійснюють роздрібну торгівлю лікарськими засобами;
д) органи влади, зокрема Міністерство охорони здоров’я України;
е) заклади охорони здоров’я та науково-дослідні установи тощо;
є) споживачі лікарських засобів (фізичні особи).
Схема функціонування фармацевтичних ринків в Україні
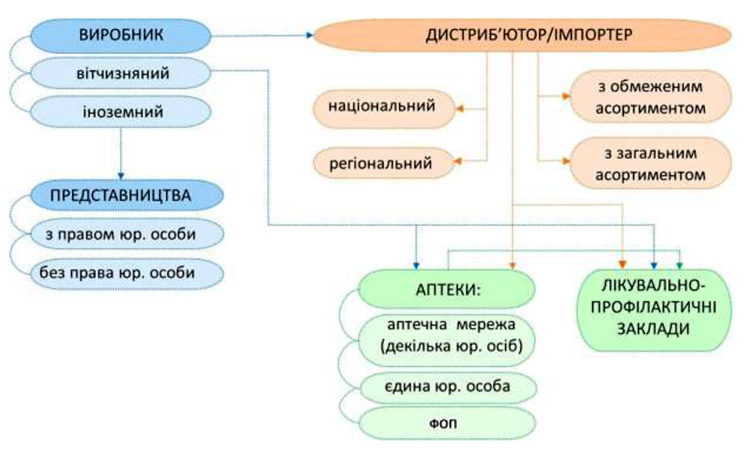
11. На рівні виробництва/імпорту лікарських засобів основними учасниками ринків є виробники лікарських засобів, у т.ч. їх представництва, імпортери.
Сфера виробництва/імпорту лікарських засобів відзначається великою кількістю учасників, при цьому рівень конкуренції на відповідних ринках є різним залежно від товарних меж ринків.
Виробник виробляє не лише один товар, а принаймні декілька, а іноді — сотні лікарських засобів.
Тому відносини продажу лікарських засобів від виробника/імпортера до оптового дистриб’ютора — це відносини щодо умов реалізації асортименту лікарських засобів із різними споживчими властивостями, різними умовами зберігання, терміном придатності, наявністю замінників тощо.
Протягом останніх років на рівні дистрибуції/оптової торгівлі два найбільших вітчизняних дистриб’ютори мають суттєву ринкову владу на ринку постачання оптових партій лікарських засобів та медичних виробів у широкоасортиментному наборі та не зазнають значної конкуренції на цьому ринку внаслідок відносно невеликого розміру часток, які належать конкурентам.
Ринки на рівні оптової торгівлі лікарськими засобами мають обмежені можливості доступу до них для нових учасників, зокрема, внаслідок існування бар’єрів вступу на ринок:
- адміністративних, встановлених ліцензійними умовами провадження господарської діяльності;
- економічних, що пов’язані із суттєвими витратами та обсягами інвестицій;
- організаційних, що пов’язані із стратегіями поведінки значущих суб’єктів господарювання, що діють на ринках.
12. Виробники, імпортери, дистриб’ютори здійснюють господарську діяльність з оптової торгівлі лікарськими засобами на загальнодержавному ринку.
13. Ринки, на яких діють учасники роздрібної торгівлі лікарськими засобами, є регіональними.
14. Фармацевтичні ринки на рівні роздрібної реалізації лікарських засобів є висококонкурентними на загальнодержавному рівні, але мають структурні ознаки монопольного (домінуючого) становища / колективної монополії окремих суб’єктів господарювання на регіональних рівнях.
ІІІ. Визначення меж ринку
15. Визначення товарних меж ринків лікарських засобів для оцінки впливу вертикальних відносин між виробником / імпортером та дистриб’юторами на стан конкуренції на ринках здійснюється відповідно до положень Методики визначення монопольного (домінуючого) становища суб’єктів господарювання на ринку, затвердженої розпорядженням Антимонопольного комітету України від 5 березня 2002 року № 49-р (далі — Методика).
Відповідно до Методики товарні межі ринку визначаються шляхом формування групи взаємозамінних товарів (товарних груп), у межах якої споживач за звичайних умов може легко перейти від споживання одного товару до споживання іншого.
16. Під час визначення товарних меж ринків лікарських засобів, беручи до уваги положення Методики, слід враховувати подібність та умови призначення лікарських засобів (рецептурні / безрецептурні), споживчі властивості, подібність хімічних та фізичних показників (генеричні, біоеквівалентні, терапевтично взаємозамінні), умови реалізації (публічні закупівлі, вільна торгівля) тощо з обов’язковим врахуванням законодавства, що регулює обіг лікарських засобів на території України.
17. Ґрунтуючись на умовах реалізації лікарських засобів (публічні закупівлі, вільна торгівля), умовах призначення лікарських засобів (рецептурні / безрецептурні), визначаються товарні межі певного ринку та формуються групи взаємозамінних товарів (генеричні, біоеквівалентні, терапевтично взаємозамінні).
18. За походженням усі лікарські засоби2 поділяються на хімічно синтезовані й отримані з біологічної сировини.
Хімічно синтезовані лікарські засоби — це органічні речовини синтезовані на фармакологічних заводах (хімічний синтез — це процес отримання хімічних сполук заданої структури, складу й властивостей з інших хімічних сполук за допомогою послідовності хімічних реакцій).
Біологічні лікарські засоби — лікарські засоби, що містять діючі речовини біологічного походження, отримані шляхом виробництва з біологічного джерела (тваринного, людського, рослинного, мікробного або біотехнологічного).
Біологічні лікарські засоби отримують із живих клітин або організмів, тому вони складаються з відносно великих і дуже складних молекулярних субстанцій, які складно повністю охарактеризувати за допомогою доступних на сьогодні аналітичних методів. Відмінності хімічних і біологічних лікарських засобів пов’язані з багатьма чинниками. Серед них основними є особливості структури молекули та процесу виробництва.
Біологічні лікарські засоби відрізняються від хімічно синтезованих лікарських засобів характеристикою молекули (розмір, структура, стабільність, структурно-функціональні взаємини), виробничим процесом та його впливом на якість і безпеку біологічних лікарських засобів. Якість біологічних лікарських засобів визначається обраною технологією та процесом виробництва. Незначні зміни у виробничому процесі можуть мати значний вплив на якість біологічного лікарського засобу, тому розробка виробничого процесу має першочергове значення для біологічних лікарських засобів.
19. Підходи щодо встановлення групи взаємозамінних товарів хімічно синтезованих лікарських засобів та біологічних лікарських засобів є різними.
До лікарського засобу хімічного походження зазвичай застосовується стандартний генеричний підхід — на підставі доведення біоеквівалентності до референтного лікарського засобу.
На відміну від генеричних лікарських засобів, біосиміляри не є точним віддзеркаленням оригінальних біологічних лікарських засобів, оскільки розмір і складність структури молекули діючої речовини, а також характер виробничого процесу (використання різних екстракційних систем, процесів ферментації та очистки, допоміжних речовин тощо) не дають можливості відтворити точну копію, а тільки лікарський засіб, подібний до біологічного.
З причин складності біологічних, отриманих за допомогою біотехнологій, лікарських засобів генеричний підхід з наукової точки зору для них не прийнятний. У таких випадках необхідно застосовувати підхід «подібні біологічні лікарські засоби», що базується на дослідженнях порівнянності3.
20. За способом призначення лікарські засоби поділяються на рецептурні та безрецептурні.
Рецепт на лікарський препарат — це медичний документ у вигляді припису чи вимоги лікувально-профілактичного закладу до аптеки, виписаний уповноваженим на це фахівцем відповідно до чинного законодавства, на підставі якого здійснюється виготовлення та/або відпуск лікарського засобу. Відповідно:
рецептурний лікарський засіб — це препарат, який відпускають в аптечній установі тільки за рецептом;
безрецептурний лікарський засіб — це препарат, що офіційно дозволено відпускати в аптечній установі без рецепта лікаря.
Перелік лікарських засобів, дозволених до відпускання з аптеки без рецепта, затверджується наказом МОЗ України4.
21. Нормативно-правовими актами у сфері обігу лікарських засобів встановлено критерії, які визначають можливість взаємозаміщення різних лікарських засобів5.
22. Найбільш конкурентними є ринки генеричних лікарських засобів.
Генерик — лікарський засіб, який має такий самий кількісний та якісний склад діючих речовин і таку саму лікарську форму, що й референтний препарат, та чия взаємозамінність з референтним препаратом доведена відповідними дослідженнями.
Вихід генериків на ринок суттєво знижує вартість лікарських засобів, стимулює конкуренцію та знижує ринкову владу суб’єктів господарювання — виробників оригінальних лікарських засобів.
Результати секторального дослідження Європейської Комісії у сфері фармацевтики6 свідчать, що при виході на ринок генерика його ціна є в середньому на 25 відсотків нижчою, ніж ціна на оригінальний лікарський засіб, а після виходу генерика на ринок протягом двох років його ціна стає на 40 відсотків нижчою за первісні ціни оригінального лікарського засобу. Також зниження на майже 20 відсотків зазнає ціна оригінального препарату.
Активний фармацевтичний інгредієнт (лікарська речовина, діюча речовина, субстанція) (далі — АФІ або діюча речовина) — будь-яка речовина чи суміш речовин, що призначена для використання у виробництві лікарського засобу і під час цього використання стає його активним інгредієнтом. Такі речовини мають фармакологічну чи іншу безпосередню дію на організм людини, у складі готових форм лікарських засобів їх застосовують для лікування, діагностики чи профілактики захворювання, для зміни стану, структур або фізіологічних функцій організму, для догляду, обробки та полегшення симптомів (Закон України «Про лікарські засоби»).
3Передбачено Порядком проведення експертизи реєстраційних матеріалів на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію), а також експертизи матеріалів про внесення змін до реєстраційних матеріалів протягом дії реєстраційного посвідчення. Наказ МОЗ від 26.08.2005 № 426.
Крім впливу на ціну, відбувається значний вплив на обсяг ринку та ринкові частки учасників. Так, компанії, що випускають генерики, отримують наприкінці першого року своєї роботи на ринку препарату близько 30 відсотків обсягу ринку, а наприкінці другого року — 45 відсотків обсягу ринку.
23. Під час розслідувань Комітет отримав від медичних установ висновки, що у зв’язку із прийняттям рішення про вибір та призначення певного лікарського засобу враховується цілий комплекс факторів, зокрема, вік та загальний стан пацієнта, стадія захворювання, наявність супутньої патології (захворювання нирок, ока, серця та інші), наявність у пацієнта вихідних протипоказань до призначення окремого лікарського засобу тощо, дотримуючись індивідуального підходу для кожного конкретного пацієнта.
Відповідно до клінічних протоколів лікування різних захворювань, лікар, під час призначення певного лікарського засобу, має враховувати попередній досвід застосування в пацієнта препарату цього класу, наявність інших захворювань, можливість взаємодії з препаратами, які використовують для лікування супутньої патології у пацієнта, протипоказання та побічну дію лікарських засобів, їх вартість тощо.
24. Отже, підхід Комітету щодо визначення товарних меж ринку лікарського засобу для аналізу вертикальних відносин між виробниками/імпортерами та дистриб’юторами, де як товар визначається лікарський засіб або група лікарських засобів, що реалізується великим оптом, є комплексним та залежить від ряду факторів.
25. Відповідно до підходів формування замовлення лікарських засобів за кошти державного / місцевого бюджетів, що застосовуються державними/комунальними установами, враховуються такі критерії щодо взаємозамінності лікарських засобів:
- містять ту саму кількість тієї самої діючої речовини (тих самих діючих речовин) у тих самих дозованих формах;
- мають однакову лікарську форму;
- вводяться тим самим шляхом;
- мають однакові показники безпеки, якості та ефективності;
- відповідають вимогам тих самих або порівнюваних стандартів;
- мають однакові показники біодоступності.
При цьому базовими показниками взаємозамінності для лікарських засобів є сукупність таких характеристик:
- міжнародна непатентована назва (тобто діюча речовина або комбінація діючих речовин);
- дозування;
- лікарська форма.
Такий підхід до визначення товарних меж ринку підтверджується висновками провідних медичних установ, що застосовують його під час призначення лікарських засобів для лікування відповідних захворювань у пацієнтів та під час закупівлі лікарських засобів за бюджетні кошти та/або кошти місцевих бюджетів.
26. Враховуючи наведене, підхід взаємозамінності лікарських засобів та до визначення товарних меж ринків лікарських засобів, описаний у п. 25, застосовується Комітетом, зокрема:
- під час дослідження ринків, проведення розслідування у справах про порушення, під час аналізу/встановлення відповідності законодавству про захист економічної конкуренції вертикальних відносин між виробниками/імпортерами та дистриб’юторами щодо реалізації лікарських засобів за процедурами публічних закупівель та впливу таких дій на ціни на лікарські засоби, що реалізуються через процедури публічних закупівель;
- під час дослідження ринків, проведення розслідування у справах про порушення, під час аналізу/встановлення відповідності законодавству про захист економічної конкуренції вертикальних відносин між виробниками/імпортерами та дистриб’юторами щодо реалізації рецептурних лікарських засобів, де вплив кінцевого споживача на ринок не є вирішальним.
27. В інших випадках під час проведення досліджень та розслідувань стосовно вертикальних відносин між виробниками/імпортерами та дистриб’юторами, а також з метою оцінки відносин між учасниками концентрації, що відбуваються на ринках лікарських засобів, визначення товарних меж ринків починається виходячи з більш широкого розуміння взаємозамінності лікарських засобів, наприклад, їх терапевтичної взаємозамінності (за АТХ-3).
Зокрема, це можливо в тих випадках, коли йдеться про безрецептурні лікарські засоби поза сферою публічних закупівель, призначені для усунення/полегшення симптомів певних нескладних захворювань, і де рішення про вибір товару приймає споживач (без участі лікаря) та за власний кошт. При цьому до уваги береться попит кваліфікованого (обізнаного) споживача та пропозиція добросовісного продавця (провізора, фармацевта тощо).
При застосуванні широкого підходу необхідно аналізувати угоди на предмет пов’язаності продажу вищеописаних (безрецептурних) лікарських засобів із продажем унікальних препаратів, які не мають взаємозамінних аналогів. Разом із цим, оскільки відносини між виробником/імпортером та дистриб’юторами — це вертикальні відносини між суб’єктами господарювання, слід враховувати, що дистриб’ютор:
- не є кінцевим споживачем;
- придбає товари не лише виходячи з їх споживчих властивостей;
- має попит на широкий асортимент лікарських засобів.
IV. Вертикальні узгоджені дії на ринках лікарських засобів, що містять ризик порушення вимог законодавства про захист економічної конкуренції
4.1. Застосування знижок та маркетингових програм у вертикальних угодах учасниками ринків лікарських засобів
28. Застосування знижок є поширеною торговельною практикою та може мати багато проконкурентних наслідків. Проте знижки також можуть мати антиконкурентні ефекти.
29. Знижки можна характеризувати за такими вимірами:
- часовий вимір — ретроспективні та проспективні;
- вимір цільових рівнів — за досягнення частки ринку чи частки загальної потреби покупця, за досягнення вартісного чи кількісного обсягу закупівель тощо;
- вимір покупця — індивідуальні для окремих покупців чи загальнодоступні для всіх покупців за виконання ними певних умов;
- товарний вимір — знижки на один товар чи на певні групи товарів (або переліки);
- вимір рівня ланцюга поставок — знижки дистриб’юторам першої ланки, оптовим покупцям, роздрібним точкам продажу, кінцевим споживачам.
30. Антиконкурентними ефектами знижок є:
- знижки як частина механізму витіснення з ринку конкурентів шляхом встановлення цін, нижчих за витрати на виробництво та реалізацію товару;
- знижки як інструмент уникнення цінового регулювання та завищення цін на публічних закупівлях;
- знижки як інструмент дилерства (обмеження доступу до покупців) та підвищення витрат конкурентів;
- знижки як засіб обмеження доступу до ключових ресурсів, якими можуть бути сировина чи доступ до основних ланок поставки, зокрема, доступ до потужних дистриб’юторів. Так, в умовах асиметрії в інформованості учасників ринку лікарських засобів про товар, який знаходиться в обігу, а також враховуючи, що пацієнти (фізичні особи) як найменш поінформовані учасники ринку самостійно за власні кошти придбають лікарські засоби для профілактики та лікування, наслідком для товару-замінника ускладненого доступу до кінцевого споживача в каналі продажів через широкоасортиментного дистриб’ютора може стати його відсутність або наявність у незначних обсягах на ринку, що особливо важливо для продажу генериків та виходу на ринок нових товарів;
- знижки на переліки товарів можуть мати ефект посилення ринкової влади постачальника на конкурентних ринках, за рахунок включення в один перелік для отримання знижок як унікальних препаратів, так і препаратів, що мають багато замінників. Застосування таких переліків для знижок одночасно з умовами досягнення певних рівнів продажу переліків, додатково має ефект ексклюзивності;
- знижки на переліки товарів можуть мати ефект нав’язування ширшого асортименту товарів порівняно із ситуацією, коли знижка встановлюється на кожний препарат окремо.
31. Угоди між виробником/постачальником (імпортером) та дистриб’юторами, які містять положення про: надання переваг для окремих дистриб’юторів (якщо такі умови прямо не дозволяються згідно з Типовими вимогами); запровадження непрозорих механізмів ціноутворення (знижки, бонуси, кредит-ноти), метою або наслідком яких є: обмеження, усунення, недопущення конкуренції з боку генериків, розподіл ринків (крім випадків, що дозволяються згідно з Типовими вимогами); фіксування певного завищеного рівня цін на ринку, завищення цін на лікарські засоби, які реалізуються через процедури публічних закупівель, можуть кваліфікуватися як антиконкурентні узгоджені дії.
32. Враховуючи місцезнаходження роздрібних точок продажу на всій території України, важливим фактором доступу до кінцевого споживача для товарів-замінників є доступ до каналу продажів через широкоасортиментного дистриб’ютора. Результатом ускладненого доступу до дистриб’ютора може стати відсутність або наявність товарів-замінників у незначних обсягах на ринку, що особливо важливо для продажу генериків та виходу на ринок нових товарів.
33. Якщо частка постачальника та/або покупця на ринку дорівнює чи перевищує 30%, вертикальні узгоджені дії, що передбачають стимулювання постачальником покупця до збільшення обсягів реалізації продукції постачальника замовникам шляхом надання покупцеві знижок, спрямованих на заохочення покупців-дистриб’юторів до збільшення обсягів реалізації лікарських засобів, можуть бути дозволені в порядку статті 10 Закону за умови, що це не призводить до витіснення та/або недопущення продукції інших виробників з/до портфеля покупців-дистриб’юторів.
34. Мотивування продажів у відносинах із дистриб’юторами може містити ознаки порушення законодавства про захист економічної конкуренції у випадках:
- застосування різних підходів до різних дистриб’юторів без об’єктивно виправданих причин, зокрема, незалежно від обсягів перепродажу, що впливають на витрати постачальника, пов’язані з реалізацією товарів;
- розподілу ринків за територією, колом покупців (крім випадків, що дозволяються згідно з Типовими вимогами), асортиментом товарів тощо;
- стимулювання виконання планів закупівлі/збуту (у вартісних показниках), підтримання рівня складських запасів, що призводить до створення бар’єрів входу на ринок генериків (замінників) або витіснення з ринку лікарських засобів-конкурентів, коли ринкова частка хоча б одного з учасників узгоджених дій дорівнює чи перевищує 30%.
35. Як правило, не призводять до негативних наслідків, передбачених частиною першою статті 6, частиною другою статті 8 Закону, вертикальні узгоджені дії, що стосуються оригінальних препаратів, які знаходяться під дією патентного захисту, якщо вони призводять до підвищення доступності (в тому числі цінової) для кінцевого споживача.
36. Підвищеним ризиком порушення законодавства про захист економічної конкуренції є змішування в одному переліку для надання знижок унікальних препаратів (лікарських засобів) та препаратів, що мають замінники.
37. Порушенням може бути визнано застосування знижок під час закупівлі одних препаратів, що надаються за умови закупівлі інших препаратів (тобто створення покупцем таких умов, за яких знижка від закупівлі одного препарату фактично надається постачальнику на закупівлю іншого).
Зокрема, якщо на ринках лікарських засобів, на які надаються знижки, постачальник зазнає конкуренції, а на ринках лікарських засобів, придбанням яких ця знижка обумовлена, постачальник займає монопольне (домінуюче) становище, надання знижки має наслідки обмеження конкуренції на ринках, де постачальник її зазнає.
При цьому, у разі настання негативних наслідків для конкуренції на фармацевтичних ринках та наявності відчутного ефекту, за певних обставин знижками може бути визнано маркетингові послуги чи навіть безповоротну фінансову допомогу, що надається як відсоток від обсягу продажу.
38. При застосуванні знижок для запобігання вчиненню порушення законодавства про захист економічної конкуренції, учасникам ринків лікарських засобів доцільно:
- для встановлення цільових рівнів застосовувати кількісні, а не вартісні, обсяги продажу в натуральному виразі — з метою уникнення виконання таких рівнів за рахунок підвищення цін;
- не надавати ретроспективних знижок за реалізацію лікарських засобів через процедури публічних закупівель, які по факту не зменшують ціни реалізації лікарських засобів, створюючи різницю між їх номінальною та реальною ціною;
- окремо формувати маркетингові політики щодо унікальних препаратів за МНН та щодо препаратів, які мають замінники;
- не допускати змішування унікальних та неунікальних препаратів в одному переліку для надання знижки;
- не ставити отримання знижки від закупівлі одних препаратів у залежність від закупівлі інших препаратів (тобто уникати умов, за яких знижка від закупівлі одного препарату надається на закупівлю іншого).
39. Залежно від виміру знижки, можна оцінити ризики негативного впливу на конкуренцію:
| «Вимір покупця» — індивідуальні знижки окремим покупцям більш ризикові, ніж стандартні знижки, доступні для всіх покупців за виконання певних умов« Товарний вимір» — змішування в переліку для знижки унікальних та неунікальних препаратів має високий ступінь ризику |
Часовий вимір знижки | ||
| Ретроспективний (надається на весь уже куплений товар) | Проспективний (знижка надається на покупки понад досягнутий рівень) | ||
| Вимір цільових рівнів для досягнення знижки | Ринкова частка або частка закупівель покупця | Високий ризик | Середній ризик |
| Обсяг продажу у вартісному вимірі | Високий ризик | Низький ризик | |
| Обсяг продажу у кількісному вимірі | Середній ризик | Низький ризик | |
40. Посилюють ризик імовірності антиконкурентного ефекту під час встановлення знижок положення вертикальних угод, що передбачають:
- змішування декількох типів знижок одночасно;
- застосування значних часових періодів для досягнення знижок.
41. Впливають на визначення ступеня ризику ймовірності антиконкурентного ефекту:
- відсоток знижки;
- частка ринку або потреби покупця, що становить цільовий рівень для досягнення знижки.
4.2. Положення вертикальних угод у частині звітності
42. Під час встановлення умов звітування дистриб’юторів перед постачальниками, з метою запобігання вчиненням порушення законодавства про захист економічної конкуренції слід керуватися таким:
- розумністю та адекватністю обсягу інформації та частоти її надання, що є об’єктом звітування, з метою недопущення встановлення контролю над ринками;
- уникати положень про обмін порадами стосовно цінової політики;
- уникати надання знижки просто за факт звітування.
4.3. Положення вертикальних угод про дистрибуцію лікарських засобів щодо програми підтримки пацієнтів
43. Програми підтримки пацієнтів та будь-які дії суб’єктів господарювання, спрямовані на забезпечення хворих доступними ліками, як правило, не містять ознак порушення законодавства про захист економічної конкуренції.
Проте під час їх реалізації необхідно дотримуватися таких принципів:
- загальнодоступність інформації про можливість участі у відповідній програмі як для всіх хворих, так і для всіх задіяних суб’єктів господарювання (аптеки, дистриб’ютори), а також про період тривалості такої програми; при цьому має бути недискримінаційний підхід;
- недопущення встановлення мінімального рівня ціни на лікарські засоби на всіх рівнях дистрибуції або фіксування конкретного рівня цін;
- недопущення нав’язування супутніх товарів та послуг як умови участі в акції (для всіх учасників ланцюга продажів);
- надання переваги free packs (безкоштовні пакети) над фінансовими стимулами участі у програмі, а за умови застосування таких фінансових стимулів, як, наприклад, знижки або бонуси, — зазначення таких знижок безпосередньо у інвойсі.
44. Водночас програми підтримки пацієнтів:
- особливо доцільні в разі унікальності препарату (дія патентного захисту) та його високої вартості, а не в разі, коли такою програмою суб’єкт господарювання намагається витіснити з ринку генерик або не допустити його входження на ринок;
- з особливою уважністю потрібно ставитися до умов таких програм у випадку їх проведення стосовно лікарських засобів, що приймаються пожиттєво (до прикладу, інсуліни), оскільки в подальшому пацієнт не зможе відмовитися від цього лікарського засобу, а ціна на нього після закінчення програми зросте; при цьому перехід на інший, навіть генеричний препарат іншого виробника, з огляду на терапевтичний ефект може бути ускладненим.
V. Застосування рекомендаційних роз’яснень
45. Наведені в цих рекомендаційних роз’ясненнях підходи можуть братися до уваги під час розслідування інших, крім антиконкурентних узгоджених дій, порушень законодавства про захист економічної конкуренції, а також у зв’язку з виконанням органами Комітету інших завдань, передбачених законодавством про захист економічної конкуренції.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим