 Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) 20 декабря выдало разрешение на маркетинг по ускоренной процедуре препарата Enhertu (фам-трастузумаб дерукстекан- nxki) для лечение взрослых с неоперабельным или метастатическим HER2-положительным раком молочной железы, получивших лечение двумя или более предшествующими схемами терапии на основе направленных на HER2 препаратов.
Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) 20 декабря выдало разрешение на маркетинг по ускоренной процедуре препарата Enhertu (фам-трастузумаб дерукстекан- nxki) для лечение взрослых с неоперабельным или метастатическим HER2-положительным раком молочной железы, получивших лечение двумя или более предшествующими схемами терапии на основе направленных на HER2 препаратов.
Новый препарат – это конъюгат антитела, нацеленного на рецепторы эпидермального фактора роста человека (HER-2) и ингибитора топоизомеразы. То есть фам-трастузумаб дерукстекан избирательно связывается с рецепторами HER2, обусловливающими рост и распространение злокачественного новообразования, и доставляет раковым клеткам токсичный для них ингибитор топоизомеразы.
Общий уровень ответа в клиническом исследовании с участием 184 пациенток с HER2-положительным раком молочной железы составил 60,3% при средней продолжительности ответа 14,8 мес.
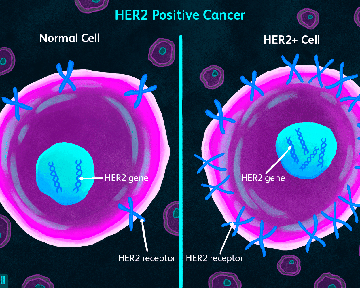
Избыток белка HER2 в раковых клетках наблюдают примерно в пятой части злокачественных новообразований молочной железы. HER2-положительный тип опухоли считается агрессивной разновидностью рака, поясняет FDA. Разрешение на маркетинг препарата Enhertu, получившего статус прорывной терапии, предоставлено «Daiichi Sankyo».
По материалам www.fda.gov; фото: Verywell/Brianna Gilmartin

Коментарі