 Після дозволу застосування двох вакцин на основі мРНК у пацієнтів, починаючи з 16- («Pfizer/BioNTech») і 18-річного віку («Moderna»), європейський регулятор видав умовний дозвіл на маркетинг першої векторної вакцини ChAdOx1 nCoV19 (AZD1222). Однак тільки невелика кількість учасників її клінічних випробувань були віком 55 років і старше, тому висновок про те, як дана вакцина працює в цій віковій групі, до отримання додаткової інформації зробити неможливо. Проте Європейське агентство з лікарських засобів (European Medicines Agency — ЕМА) вирішило схвалити застосування вакцини в осіб з 18-річного віку, посилаючись на сприятливі дані про безпеку. З огляду на актуальність цього питання, ми зібрали дані про ефективність схвалених вакцин в осіб старшої вікової групи на основі результатів клінічних досліджень, якими регулятори обґрунтовують свої висновки.
Після дозволу застосування двох вакцин на основі мРНК у пацієнтів, починаючи з 16- («Pfizer/BioNTech») і 18-річного віку («Moderna»), європейський регулятор видав умовний дозвіл на маркетинг першої векторної вакцини ChAdOx1 nCoV19 (AZD1222). Однак тільки невелика кількість учасників її клінічних випробувань були віком 55 років і старше, тому висновок про те, як дана вакцина працює в цій віковій групі, до отримання додаткової інформації зробити неможливо. Проте Європейське агентство з лікарських засобів (European Medicines Agency — ЕМА) вирішило схвалити застосування вакцини в осіб з 18-річного віку, посилаючись на сприятливі дані про безпеку. З огляду на актуальність цього питання, ми зібрали дані про ефективність схвалених вакцин в осіб старшої вікової групи на основі результатів клінічних досліджень, якими регулятори обґрунтовують свої висновки.Comirnaty від «Pfizer/BioNTech»
В аналіз ефективності вакцини від «Pfizer/BioNTech» (BNT162b2 або Comirnaty) включали пацієнтів, 42% яких були віком ≥55 років (21% — старше 65 і 4% — старше 75 років), при цьому приблизно у половини учасників виявлені супутні захворювання (Polack F.P. et al., 2020). Результати в різних підгрупах, у тому числі вікових, можна порівняти з оцінкою загальної ефективності — 95,0% (90,3–97,6) (табл. 1).
| Підгрупа | Кількість випадків у групах | Ефективність (efficacy), (95% довірчий інтервал — ДІ), % | |
| BNT162b2 (N = 19 965) | Плацебо (N = 20 172) | ||
| Старша вікова група | |||
| Вік 65–74 роки | 1/3434 | 14/3467 | 92,9 (53,2–99,8) |
| Вік ≥75 років | 0/860 | 5/852 | 100,0 (–12,1–100,0) |
| Вік ≥65 років з факторами ризику* | 1/1533 | 12/455 | 91,7 (44,2–99,8) |
| Вік ≥65 з ожирінням | 0/1327 | 7/1382 | 100,0 (27,4–100,0) |
| Із супутніми захворюваннями* | |||
| Ожиріння | 3/6934 | 67/7093 | 95,4 (86,0–99,1) |
| Артеріальна гіпертензія | 2/4585 | 44/4623 | 95,4 (82,6–99,5) |
| Онкопатологія | 1 | 4 | 75,7 (–145,8–99,5) |
| Серцево-судинні захворювання | 0 | 5 | 100,0 (–0,8–100,0) |
| Захворювання органів дихання | 1 | 14 | 93,0 (54,1–99,8) |
| Цукровий діабет | 1 | 19 | 94,7 (66,8–99,9) |
mRNA-1273 від «Moderna»
У дослідженні вакцини «Moderna» 25,3% учасників були віком ≥65 років (Baden L.R. et al., 2020). Більшість пацієнтів (82%) вважалися групою професійного ризику впливу SARS-CoV-2, у тому числі 25,4% медичних працівників. У близько 22,3% учасників відзначали хоча б один з факторів високого ризику розвитку тяжкої форми COVID-19, а у 4% — 2 або більше, в тому числі хронічні захворювання дихальної (хронічний бронхіт, бронхіальна астма середнього та тяжкого ступеня), серцево-судинної (серцева недостатність, ішемічна хвороба серця, кардіоміопатія, легенева гіпертензія) систем, тяжке ожиріння (індекс маси тіла (ІМТ) ≥40 кг/м2), цукровий діабет, захворювання печінки, ВІЛ-інфекція.
У учасників віком ≥18 років виявлено 5 випадків COVID-19 у групі вакцинованих і 90 — в групі плацебо, так що розрахункова ефективність вакцинації становила 94,5% (95% ДІ 86,5–97,8%) (табл. 2). В учасників віком ≥65 років у групі вакцинованих зареєстровано 4 випадки COVID-19, а в групі плацебо — 29 випадків.
| Підгрупа | Кількість випадків у групах | Ефективність (efficacy), (95% ДІ), % | |
| mRNA-1273 (N = 13934) | Плацебо (N = 13883) | ||
| Усі учасники | 11 | 185 | 94,1 (89,3–96,8) |
| Вік ≥65 років | 4/3583 | 29/3552 | 86,4 (61,4–95,5) |
| Ожиріння (ІМТ ≥40 кг/м2) | 2/5269 | 46/5207 | 95,8 (82,6–99,0) |
| З факторами ризику | |||
| Будь-які, незалежно від віку | 1/3116 | 24/3075 | 95,9 (69,7–99,4) |
| Хронічні захворювання легень | 0/661 | 6/673 | 100 |
| Серцево-судинні захворювання | 0/686 | 3/678 | 100 |
| Тяжке ожиріння (ІМТ ≥40 кг/м2) | 1/901 | 11/884 | 91,2 (32,0–98,9) |
| Цукровий діабет | 0/1338 | 7/1309 | 100 |
| ВІЛ-інфекція | 0/80 | 1/76 | 100 |
Слід також особливо підкреслити, що термін спостереження учасників поки невеликий, особливо в дослідженні «Moderna»: 26,3% вакцинованих і 25,7% із тих, що отримали плацебо, спостерігали 2 міс, інші — менше). Аналогічний показник у дослідженні вакцини від «Pfizer/BioNTech» – 43,9%.
AZD1222 від «AstraZeneca»/ Оксфордського університету
У первинному аналізі ефективності оксфордської вакцини задіяно 12,2% осіб віком ≥56 років, 4% — ≥70 років (Voysey M. et al., 2020). Розрахункова величина цього показника щодо симптоматичних підтверджених випадків становила 70,4% (54,8–80,6). Тільки 5 випадків COVID-19, включених в первинний аналіз, виявлено в учасників віком старше 55 років. Тому ефективність оксфордської вакцини у старших вікових групах оцінити неможливо, але її буде визначено після виявлення більшої кількості випадків.
CoronaVac від «Sinovac»
У проведеному в Бразилії дослідженні ІІІ фази інактивованої вакцини CoronaVac від «Sinovac» всі учасники були медичними працівниками, а ефективність становила 50,39% (35,26–61,98). Кількість випадків COVID-19 у пацієнтів віком ≥60 років (3 — в групі плацебо і 2 — в групі вакцинації) не дозволяє зробити висновок про її ефективність у даній віковій групі. До такого ж висновку дійшли експерти Національного агентства з санітарного нагляду (Agência Nacional de Vigilância Sanitária — Anvisa) Бразилії і щодо осіб із супутніми захворюваннями, ослабленим імунітетом, а також дітей, підлітків і вагітних: «Не представлено даних, які могли б гарантувати ефективність ні щодо даного режиму, ні цих груп».
Тільки подальші дослідження, у тому числі збереження «осліплення» та продовження спостереження учасників дадуть відповіді на запитання, що залишаються.
Список використаної літератури
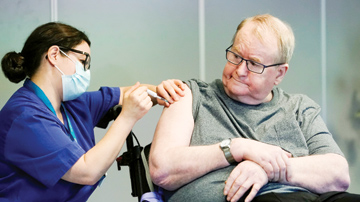
27 грудня 2020 р. (Fredrik Hagen/NTB)

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим