Обмежені повноваження і прогалини в інформації
 Держави — члени ЄС самостійно відповідають за організацію національних систем охорони здоров’я та надання медичної допомоги населенню. Проте на рівні ЄС передбачена підтримка в цій сфері. У 2022 р. Європейське агентство з лікарських засобів (European Medicines Agency — EMA) отримало офіційний мандат на координацію дій держав-членів у випадку криз у сфері громадського здоров’я («великих подій» або «надзвичайних ситуацій»), однак не для повсякденного дефіциту. Проблемою є те, що EMA не отримує своєчасної, повної та порівнянної інформації про дефіцит, що перешкоджає обізнаності агентства про це та його здатності підтримувати держави-члени у своєчасному запобіганні критичній нестачі ліків.
Держави — члени ЄС самостійно відповідають за організацію національних систем охорони здоров’я та надання медичної допомоги населенню. Проте на рівні ЄС передбачена підтримка в цій сфері. У 2022 р. Європейське агентство з лікарських засобів (European Medicines Agency — EMA) отримало офіційний мандат на координацію дій держав-членів у випадку криз у сфері громадського здоров’я («великих подій» або «надзвичайних ситуацій»), однак не для повсякденного дефіциту. Проблемою є те, що EMA не отримує своєчасної, повної та порівнянної інформації про дефіцит, що перешкоджає обізнаності агентства про це та його здатності підтримувати держави-члени у своєчасному запобіганні критичній нестачі ліків.
Законодавство ЄС вимагає від промисловості та національних компетентних органів надавати EMA дані про можливі альтернативні лікарські засоби та їх наявність (дані про запаси, попит, пропозицію або виробничі потужності) під час оголошеної кризи в галузі охорони здоров’я. Однак EMA стикається з певними труднощами, пов’язаними з отриманням цих даних. Частина гравців надали неповну або не надали інформацію. При цьому EMA не має повноважень запитувати цю інформацію, і вона не є легкодоступною. EMA вже розпочато створення центральної бази даних лікарських засобів. Вона має містити інформацію про всі дозволені ліки та їхній ринковий статус. Проте база не охоплює дані про альтернативи чи їхню доступність.
З листопада 2024 р. EMA розміщує Європейську платформу моніторингу дефіциту, яка призначена для виконання функцій гармонізованого порталу звітності про дефіцит у рамках підготовки до та під час кризи у сфері охорони здоров’я. Платформа має потенціал для значного спрощення звітності та аналізу даних. Станом на початок 2025 р. платформа діє, але все ще потрібно додати багато функцій, щоб повною мірою використовувати її потенціал.
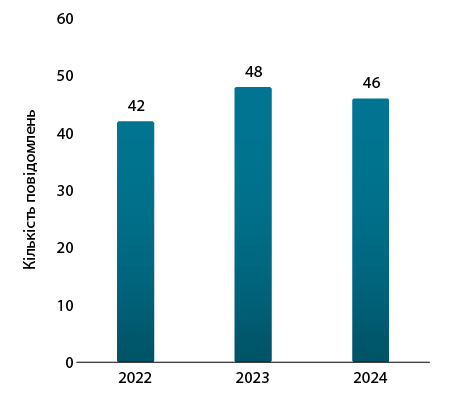
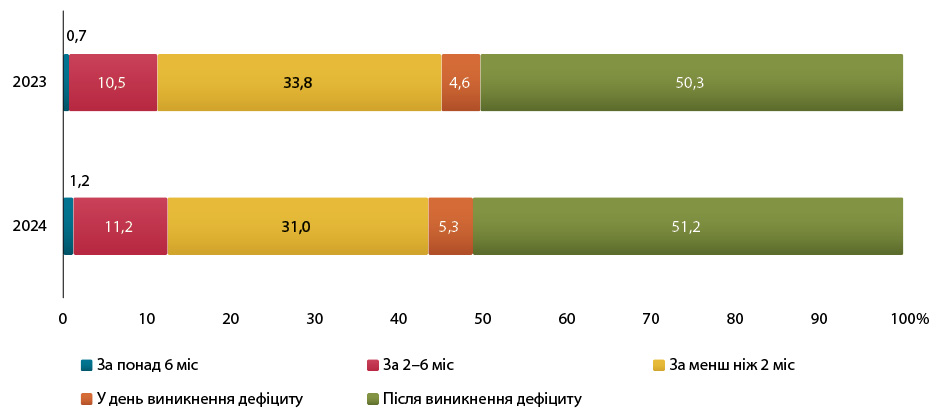
У період 2022–жовтень 2024 р. компетентні органи ЄС повідомили EMA про 136 критичних дефіцитів (рис. 1). У більшості випадків інформація надходила вже після виникнення проблеми, а не превентивно (рис. 2). Також були випадки, коли про дефіцит взагалі не повідомлялося.
EMA підтримувала держави-члени в запобіганні критичному дефіциту. Однак ця робота була зосереджена на видачі рекомендацій, наприклад, щодо використання планів запобігання дефіциту та готовності до криз. EMA також підтримувало держави-члени в пом’якшенні критичного дефіциту шляхом обміну інформацією щодо існуючих альтернативних препаратів в інших державах-членах або за межами Європейської економічної зони (ЄЕЗ), координації дій для усунення критичного дефіциту та комунікації з медичними працівниками. За оцінкою Європейського суду аудиторів, загалом підтримка EMA держав-членів у пом’якшенні критичного дефіциту мала для них значну додаткову цінність. Однак її внесок у запобігання дефіциту був зосереджений на рекомендаціях, а в її комунікації з громадськістю бракувало важливої інформації.
У квітні 2023 р. Європейська комісія запропонувала зміни до правової бази EMA. Пропозиції включали, зокрема, розширення Європейської платформи моніторингу дефіциту за межі криз охорони здоров’я. Європейський суд аудиторів вважає, що запропоновані зміни не розв’язують усіх проблем. Пропозиції не містять механізму для забезпечення дотримання зобов’язання промисловості своєчасно повідомляти EMA про дефіцит, пов’язаний з централізовано зареєстрованими лікарськими засобами, а це означає, що все ще існує ризик запізнення або неподання звітності. Пропозиції також не містять юридично обов’язкових інструментів для EMA, щоб впливати на дії промисловості під час критичного дефіциту. Аудитори вважають це серйозною прогалиною.
Одними з перших рекомендацій Європейського суду аудиторів є подальше вдосконалення системи для вирішення критичної нестачі та комплексних скоординованих дій для усунення першопричин дефіциту лікарських засобів. Європейська Комісія має вжити заходів для покращення послідовного застосування та забезпечення виконання державами-членами зобов’язання галузі забезпечувати безперервне постачання; та оцінити необхідність і доцільність координації національних вимог до накопичення запасів. Відсутність узгодженого підходу до формування стратегічних запасів призводить до того, що країни діють хаотично і нерівномірно.
Єдиний ринок під тиском: бар’єри і фрагментація
Добре функціонуючий єдиний ринок лікарських засобів є передумовою для їхньої доступності. Це потребує гармонізованого регуляторного середовища (щодо регуляторних процедур, стандартів та упаковок), прозорого ринку та відсутності внутрішніх бар’єрів для торгівлі.
Головним досягненням у гармонізації регуляторних процедур стало створення схеми ЄС для лікарських засобів, яка дозволяє централізовано авторизувати деякі препарати. Однак більшість лікарських засобів досі авторизуються на національному рівні, а ті, що авторизовані для всього ЄС, фактично не продаються в усіх державах-членах, що зумовлює нерівний доступ до них та труднощі у їхній торгівлі.
Держави-члени намагалися обмежити дефіцит, спричинений паралельною торгівлею та квотами на постачання, встановлюючи різні торговельні бар’єри. Однак ці заходи, своєю чергою, можуть створювати дефіцит у країнах-імпортерах. Держави-члени не завжди повідомляли Європейську комісію про односторонні заходи, які можуть обмежувати торгівлю, що знижувало обізнаність про такі заходи на рівні ЄС.
Тому ще одна рекомендація передбачає покращення функціонування єдиного ринку лікарських засобів шляхом усунення бар’єрів. Зокрема, Європейська комісія має краще виявляти бар’єри для торгівлі, створені державами-членами, та прагнути їх усунення.
Глибинні причини дефіциту
Робота з усунення першопричин дефіциту лікарських засобів знаходиться на початковому етапі і стикається з багатьма труднощами. Зокрема, останніми роками виробництво багатьох лікарських засобів та активних фармацевтичних інгредієнтів (АФІ) перемістилося за межі ЄС. Крім того, у галузі відзначалася значна концентрація. Наприклад, АФІ часто виробляються кількома або лише однією компанією. Водночас ланцюги постачання ліків стали складнішими, довшими та ширше розповсюджуються по всьому світу. Хоча ці події мають економічне обґрунтування, вони також стали джерелом вразливості ланцюга поставок на ринку лікарських засобів.
Єдиний ринок лікарських засобів ЄС фрагментований, що призводить до багатьох проблем з їх доступністю. Лікарські засоби, дозволені на рівні ЄС, часто недоступні у всіх державах-членах. Також упаковки лікарських засобів (зокрема їх розміри та маркування) відрізняються в межах ЄС, що перешкоджає економічно ефективній торгівлі. Різні упаковки для різних ринків ускладнюють та роблять торгівлю лікарськими засобами в ЄС більш дорогою. Одним з основних способів зниження дефіциту ліків є переміщення ліків з однієї держави-члена в іншу. Це має бути гарантовано вільним рухом товарів на єдиному ринку.
Доступність лікарських засобів є спільною відповідальністю держав-членів та органів ЄС. Європейська комісія відповідає за створення та забезпечення функціонування єдиного ринку, зокрема ринку лікарських засобів. Крім того, вона має заохочувати співпрацю між державами-членами у сфері охорони здоров’я та підтримувати держави-члени в цій галузі. Комісію у виконанні її завдань підтримує EMA.
Звіт Європейського суду аудиторів показує, що дефіцит лікарських засобів у ЄС є наслідком глибоких структурних вразливостей. Розв’язання проблеми потребує узгодженої політики, посилення повноважень регуляторів і більшої відповідальності з боку фармацевтичної індустрії.
за матеріалами www.eca.europa.eu

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим