Аутофагия — эволюционно консервативный процесс, характерный для всего надцарства эукариот (организмов, содержащих ядро в клетках). Эукариотические клетки имеют возможность рециклировать части собственных составляющих путем отделения (секвестрования) части цитоплазмы двухмембранной органеллой, которая сливается с лизосомой для дальнейшего переваривания (рис. 1).
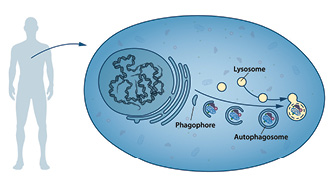
Формирование аутофагосомы. Фагофора растягивается для формирования двойной мембраны аутофагосомы, которая поглощает цитоплазматический материал. Аутофагосома сливается с лизосомой, в которой содержимое подвергается деградации.
©Нобелевский комитет по физиологии или медицине (The Nobel Committee for Physiology or Medicine). Иллюстратор: Маттиас Карлен (Mattias Karlén)
В отличие от других процессов клеточной деградации, аутофагия удаляет долгоживущие белки (long-lived proteins), макромолекулярные комплексы и устаревшие или поврежденные органеллы.
Аутофагия является посредником процессов переваривания и рециклирования второстепенных (не являющихся необходимыми для выживания) частей клетки во время голодания, а также присутствует в огромном количестве физиологических процессов, в рамках которых клеточные компоненты должны быть изъяты из клетки, дабы предоставить место новым частям.
Кроме этого, аутофагия является ключевым процессом по удалению чужеродных микроорганизмов и токсических белковых агрегатов, и таким образом принимает непосредственное участие в развитии иммунного ответа и инфекционного процесса, старения и патогенеза многих заболеваний.
Несмотря на то что сам процесс аутофагии был открыт в начале 1960-х годов, механизмы и физиологическое значение оставались серым пятном клеточной биологии на протяжении нескольких десятилетий.
Что такое аутофагия
Термин «аутофагия» происходит от древнегреческого αὐτός — ауто (сам) и φαγεῖν (есть). Это процесс, при котором внутренние компоненты клетки доставляются в лизосомы или вакуоли для последующей деградации (переваривания).
В настоящее время различают три вида аутофагии.
1. Макроаутофагия. При данном процессе участок цитоплазмы, нередко содержащий органеллы, окружается мембраной, которая похожа на цистерну эндоплазматического ретикулума. Таким образом содержимое отделяется от цитоплазмы двухмембранной оболочкой. Такие двухмембранные пузырьки, внутри которых находятся органеллы и цитоплазма, называются аутофагосомами. Они соединяются с лизосомами с образованием аутофаголизосом. В них и происходит переваривание захваченного содержимого клетки. Такой процесс является как неспецифическим, так и избирательным, поскольку клетка может прибегать к этому процессу в случае необходимости избавиться от устаревших органелл (рибосом, митохондрий и прочих). Именно за открытие этого процесса присуждена Нобелевская премия в 2016 г. Далее в статье под термином «аутофагия» будет подразумеваться макроаутофагия.
2. Микроаутофагия. При этом процессе макромолекулы и частицы клеточных мембран захватываются лизосомой. Таким способом происходит переваривание белков при нехватке в клетке энергии или субстрата для синтеза новых белков. Этот процесс в целом характерен для голодания.
3. Шапероновая аутофагия. При этом процессе осуществляется целенаправленный транспорт белков (частично денатурированных) из цитоплазмы в полость лизосомы, где они подвергаются деградации. Этот тип аутофагии, насколько известно, характерен только для млекопитающих. Как правило, шапероновая аутофагия индуцируется стресс-факторами, в частности, активируется при голодании, физических нагрузках и пр. Процесс осуществляется при участии белков-шаперонов (семейства hsc-70), LAMP-2 (мембранный рецептор комплекса шаперона и транспортируемого белка) и некоторых вспомогательных белков.
Аутофагия и клеточная смерть
На сегодня ряд ученых относят аутофагию к процессам клеточной гибели. Современная классификация выделяет несколько таких процессов: апоптоз, аутофагия, некроз, аноикис (смерть клетки, вызванная ее отделением от окружающего внеклеточного матрикса), некроптоз (программируемый некроз).
С тем, что аутофагия является одним из видов клеточной смерти, согласны далеко не все. Есть множество научных исследований, подтверждающих, что аутофагия является защитным механизмом клетки, поскольку позволяет спасти ее от гибели при неблагоприятных условиях. В случае интенсификации аутофагии клетка все же погибает. Ученые выделили несколько критериев, которые позволяют говорить о том, что аутофагия является видом клеточной смерти. Так, должны отсутствовать признаки апоптоза, не должны быть активированы каспазы, конденсироваться хроматин. В клетке должно увеличиваться число аутофагосом и аутолизосом. Кроме того, ингибирование белков аутофагии должно предотвращать смерть клетки.
Процессы, связанные с клеточной гибелью, происходят постоянно и поддерживаются в строгом равновесии, сдвиг которого в одну или другую сторону неминуемо приводит к развитию нарушений и, в конечном счете, — к смерти организма. Какую роль все-таки играет в этом процессе аутофагия — ученым еще предстоит узнать.
Загадка аутофагии или предыстория открытия
Открытию Е. Осуми, за которое он получил наиболее престижную научную награду, предшествовали ранние исследования.
В 1950-е годы Кристиан Рене де Дюв (Christian Renе de Duve) изучал действие инсулина в клетках печени крыс. В рамках своей исследовательской работы он изучал локализацию фермента глюкозо-6-фосфатазы. Этот фермент играет важнейшую роль в гликогенолизе — процессе расщепления гликогена до глюкозы. В печени фермент глюкозо-6-фосфатаза расщепляет промежуточный метаболит на фосфат и глюкозу, которая затем поступает в кровь. При исследовании глюкозо-6-фосфатазы был использован метод фракционирования, разработанный Альбером Клодом (Albert Claude). Однако выявить ферментную активность в свежевыделенных печеночных фракциях не удавалось. В то же время ферментная активность сохранялась и усиливалась после того, как фракции хранились 5 сут в холодильнике.
Таким образом, Кристиан де Дюв и его студенты выявили различия в активности кислой фосфатазы в зависимости от способа выделения. Первоначально команда решила, что причина в какой-либо технической ошибке. Однако в последующих экспериментах результаты получались точно такими же.
Довольно скоро стало понятно, что ферменты каким-то образом отделены от всего содержимого клетки мембранной органеллой. На протяжении 3 лет были выявлены еще несколько кислых ферментов, связанных с этой микросомальной фракцией. Далее последовали опыты, показавшие, что фракция является самостоятельной органеллой.
В 1955 г. на основании полученных данных Кристиан де Дюв предложил название «лизосома» для органеллы, окружающей мембраной клеточные частицы, внутри которой поддерживается низкий рН (кислотный) и в которой функционируют кислые ферменты.
В том же 1955 г. Алекс Новиков (Alex B. Novikoff, американский ученый украинского происхождения) посетил лабораторию Кристиана де Дюва. Там он сделал электронные фотографии открытых органелл. Далее А. Новиков провел эксперименты и подтвердил, что в лизосомах содержится кислая фосфатаза.
За эти и другие открытия Кристиану де Дюву, Альберу Клоду и Джорджу Паладу (George E. Palade) была присуждена Нобелевская премия в 1974 г.
Интересный факт, что А. Новиков также внес большой вклад в открытие лизосом и понимание их функционирования. Однако ученый подвергался социальному и политическому преследованию. Так, в 1953 г. он был уволен из медицинского колледжа Университета штата Вермонт за отказ в сотрудничестве по раскрытию его друзей-коммунистов. Он также дважды получил отказ по поводу службы в американской армии. Спустя 20 лет после начала расследования его связей с коммунистами дело против ученого было закрыто по причине отсутствия существенных доказательств. Спустя 30 лет после начала преследований Университет принес ему официальные извинения и предоставил почетную степень доктора. В официальном заявлении Университета Миннесоты значится, что А. Новиков является одним из наиболее недооцененных ученых в контексте получения Нобелевской премии.
Вскоре после открытия лизосом ученые стали все больше узнавать об этих органеллах. Так, было показано, что определенные «порции» цитоплазмы отделяются (секвестрируются) мембранными структурами во время нормального развития почек у мышей. Выявлено, что аналогичные структуры, содержащие небольшой объем цитоплазмы и митохондрий, находятся в клетках проксимальных канальцев при гидронефрозе.
Ученые установили, что вакуоли группируются вместе с гранулами, содержащими кислые фосфатазы. Также стало известно, что количество таких структур увеличивается по мере интенсификации дегенеративных процессов.
Мембранные структуры, содержащие дегенеративную цитоплазму, находились и в нормальной печени (исследовалось на крысах), но их количество существенно возрастало при воздействии на животное глюкагоном (перфузией) или токсическими агентами.
Понимая, что эти структуры обладают свойством переваривать части внутриклеточного содержимого, Кристиан де Дюв ввел термин «аутофагия» в 1963 г. и широко описал эту концепцию в публикации, сделанной несколькими годами позже.
На протяжении следующих десятилетий достижения в этой области были весьма ограниченными. Установлено, что питательная среда и гормоны оказывают влияние на аутофагию, в частности, стимулирование инсулином супрессирует аутофагию в тканях млекопитающих.
Одно из исследований продемонстрировало, что на ранних этапах процесса происходит формирование двухмембранной структуры — фагофоры, которая образуется вокруг участка цитоплазмы и замыкается в пузырек, не содержащий гидролитических ферментов, — аутофагосому (см. рис. 1).
Открытие Осуми — поворотный этап в понимании аутофагии
Несмотря на понимание того, что аутофагия — чрезвычайно важный клеточный процесс, механизмы его функционирования и регуляции не были известны. Исследования этого процесса были довольно непростыми, поскольку период жизни фаговор и аутофагосом очень короткий. Аутофагосома существует только 10–20 мин перед слиянием с лизосомой, поэтому морфологические и биохимические исследования проводить крайне сложно. Работой в этом направлении занимались неохотно. Всего лишь несколько исследовательских лабораторий по всему миру изучали этот процесс, в основном используя сравнительные и описательные подходы и фокусируясь на поздних стадиях аутофагии, то есть непосредственно перед слиянием с лизосомой.
В начале 1990-х годов, почти через 30 лет после введения Кристианом де Дювом термина «аутофагия», еще не были выделены молекулярные маркеры и не были описаны компоненты (этапы) механизма аутофагии. Множество фундаментальных вопросов оставались открытыми: инициация процесса, формирование аутофагосом, роль аутофагии в клеточном и организменном выживании, влияние на патогенез заболеваний.
В это время Е. Осуми, тогда ассистент профессора в Токийском университете, принял решение изучать аутофагию, используя дрожжи Saccharomyces cerevisae в качестве модельной системы.
Первое, что решил узнать ученый, — существует ли аутофагия в этих одноклеточных организмах. Вакуоли дрожжей являются эквивалентом лизосом млекопитающих. Е. Осуми предположил, что если аутофагия существует у дрожжей, ингибирование вакуольных ферментов приведет к накоплению поглощенных цитоплазматических компонентов в вакуоли. Для того чтобы проверить выдвинутую гипотезу, он создал штамм дрожжей, у которых отсутствовали вакуольные протеазы: протеаза А, протеаза В и карбоксипептидаза.
Он выявил, что аутофагические тела накапливаются в вакуоле при росте дрожжей в обедненной питательной среде. Такие вакуоли становились очень большими, и их можно было исследовать под световым микроскопом.
Е. Осуми идентифицировал уникальный фенотип, который стал использовать для открытия генов, регулирующих индукцию аутофагии. Ученый индуцировал случайные мутации. И одна из них оказалась первой удачей: он смог найти первый ген, при мутации которого не отмечено накопления аутофагических телец, то есть не происходят начальные этапы процесса аутофагии. Этот ген он назвал — ген аутофагии 1 (autophagy gene 1 — APG-1). Продолжая работу в том направлении, ученому удалось выявить 75 мутаций.
В 1993 г. он опубликовал статью, в которой сообщил об открытии 15 генов, играющих ключевую роль в активации аутофагии в эукариотических клетках. Они получили название APG-1–15. После открытия этих генов у других организмов всей группе было присвоено название ATG-гены. Эта номенклатура используется вплоть до настоящего времени.
На протяжении последующих лет Е. Осуми клонировал некоторые ATG-гены и охарактеризовал их функции. Клонирование гена ATG-1 позволило узнать, что он кодирует серин/треониновую киназу. Таким образом, было доказано, что в процессе аутофагии происходит фосфорилирование белков (присоединение фосфатного остатка, что является одним из самых распространенных механизмов посттрансляционной модификации белка, приводящей к изменению его активности).
Дополнительные исследования показали, что ATG-1 формирует комплекс с белком, кодируемым геном ATG-13, и что это взаимодействие регулируется TOR-киназой (рис. 2).
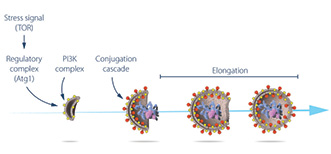
Регуляция формирования аутофагосомы
© Нобелевский комитет по физиологии или медицине (The Nobel Committee for Physiology or Medicine). Иллюстратор: Маттиас Карлен (Mattias Karlén)
TOR-киназа регулирует клеточный рост и выживание. Она активна в клетках, растущих в среде, богатой питательными веществами. Она фосфорилирует ATG-13 и препятствует формированию комплекса ATG-13:ATG-1. Так, при голодании TOR-киназа инактивируется и дефосфорилированный ATG-13 соединяется с ATG-1.
ATG-13:ATG-1 соединяется с ATG-17, ATG-29 и ATG-31. Образование этого пентамерного комплекса является первым этапом в каскаде реакций, необходимых для формирования аутофагосомы.
Формирование аутофагосомы также требует наличия интегрального белка (пронизывающего мембрану) — ATG-9, фермента фосфатидилинозитола-3-киназы (PI3K) и ряда других протеинов (Vps-34, Vps-15, ATG-6 и ATG-14).
Для формирования мембраны требуются дополнительные белки и молекула фосфатидилинозитол-3 фосфата. Расширение мембраны с образованием зрелой аутофагосомы происходит при активности двух каскадов убиквитинсопряженных реакций.
В вопросах клеточного функционирования большое значение имеет локализация белков. Е. Осуми сделал интереснейшее открытие: в нормально растущих клетках дрожжей белок ATG-8 распределяется равномерно по всей цитоплазме. А в случае голодания этот же белок формирует крупные агрегаты, которые скапливаются в аутофагосомах и аутофаготических тельцах.
Ученому принадлежит еще одно удивительное открытие. Оказалось, что мембранная локализация гена ATG-8 зависит от двух увиквитинсопряженных реакций, которые работают последовательно. Они приводят к ковалентному (наиболее крепкому) присоединению ATG-8 к липидной мембране, а именно — к молекуле фосфатидилэтаноламина. Обе системы активируются одним и тем же ферментом — ATG-7.
Во время первого этапа ATG-12 активируется путем формирования тиоэфирной связи с остатком серосодержащей аминокислоты — цистеином, которая входит в состав ATG-7. Затем он переносится на сопряженный фермент ATG-10, катализирующий образование ковалентной связи с белком ATG-5.
Комплекс ATG-12:ATG-5 вовлекает ATG-16, и вместе белки формируют тримолекулярную структуру. Она также критически важна в аутофагии, поскольку приобретает функцию фермента — лигазы, который задействован во второй убиквитинсопряженной реакции. В этой второй уникальной реакции аргинин, расположенный на С-конце белка ATG-8, убирается белком ATG-4. Теперь уже подготовленный белок ATG-8 активируется ATG-7 для последующего переноса. Наконец две сопряженные системы пересекаются. ATG-12:ATG-5:ATG-16-лигаза способствует присоединению ATG-8 к фосфатидилэтаноламину (к мембране).
Соединенный с липидами ATG-8 является ключевым драйвером удлинения (элонгации) и слияния аутофагосом. Обе сопряженные системы являются высококонсервативными процессами.
У млекопитающих аналог белка ATG-8 называется LC3, и он используется в качестве маркера формирования аутофагосом.
 Есинори Осуми
Есинори Осуми
Японский клеточный биолог, специализация — изучение аутофагии. Работает профессором в Институте инновационных исследований Технологического университета Токио. Образование получил в Университете Токио. В 1974–1977 гг. работал в Университете Рокфеллера, затем вернулся в Японию и получил ставку научного сотрудника. В 1996 г. перешел в Национальный институт фундаментальной биологии (National Institute for Basic Biology), где со временем ему было присуждено звание профессора. С 1998 г. является руководителем исследовательской группы.
Аутофагия и патологические процессы
Изучение молекулярных принципов аутофагии позволило понять патогенез многих заболеваний (рис. 3). В то же время в этой теме еще очень многое остается не изученным.
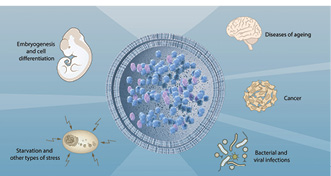
Аутофагия в норме и при патологии
© Нобелевский комитет по физиологии или медицине (The Nobel Committee for Physiology or Medicine). Иллюстратор: Маттиас Карлен (Mattias Karlén)
Как известно, аутофагия первоначально открыта в виде клеточного ответа на стресс, но сейчас известно, что этот процесс активен и на ранних стадиях дифференциации клеток. В отличие от убиквитин-протеосомной системы, которая в основном деградирует белки с коротким сроком жизни, аутофагия позволяет клетке избавиться от долгоживущих белков. Кроме того, это единственный известный процесс, позволяющий уничтожать целые органеллы, такие как митохондрии, пероксисомы, эндоплазматический ретикулум и прочие. Таким образом, аутофагия играет важнейшую роль в поддержании клеточного гомеостаза. Более того, этот процесс задействован во множестве нормальных процессов, в частности — эмбриогенезе, клеточной дифференциации, которые требуют удаления тех или иных частей цитоплазмы.
Аутофагия прямо или косвенно связана с развитием множества заболеваний.
Онкологические заболевания развиваются несколькими путями и связаны с дифференцировкой клеток. Аутофагия в некоторых случаях защищает организм от развития онкопатологии (онкосупрессор), а в некоторых — способствует развитию злокачественных новообразований. Поскольку аутофагия — это в первую очередь механизм выживания клетки, она помогает выживанию раковых клеток. Это связано с тем, что при изменении фенотипа нормальных клеток, когда они становятся злокачественными, существенно ускоряется скорость их деления и клетки испытывают голодание, гипоксию и пр. В этот момент запускается механизм аутофагии, помогающий клеткам переваривать некоторые участки и выживать в неблагоприятной среде.
Также с помощью аутофагии могут уничтожаться апоптические медиаторы. В таких случаях перспективным терапевтическим направлением представляется ингибирование поздних стадий аутофагии.
Интерес представляет белок Beclin-1 — продукт гена BECN-1 (гомолог дрожжевого гена ATG-6, регулирующего этапы инициации аутофагии). Экспрессия мутированного белка Beclin-1 характерна для ряда онкологических заболеваний, в частности группы рака молочной железы и яичника. В экспериментах на моделях мышей показано, что гиперэкспрессия нормального Beclin-1 приводит к подавлению опухолевого процесса.
Таким образом, влияние на аутофагию может стать эффективным способом борьбы с онкологическими заболеваниями.
Поскольку интенсивность аутофагии снижается с возрастом, существуют гипотезы, что этот процесс играет ключевую роль в развитии болезней, ассоциированных со старением. По некоторым данным, снижение активности аутофагии связано с развитием остеоартроза.
Одна из наиболее популярных теорий развития нейродегенеративных заболеваний (в настоящее время) также отводит аутофагии значимую роль в этом процессе. Как известно, неправильно упакованные белки имеют тенденцию к формированию нерастворимых агрегатов, являющихся токсичными для клеток. Способность клетки противостоять этому процессу целиком и полностью зависит от активности аутофагии. В исследованиях, проведенных на животных моделях, показано, что активация аутофагии путем ингибирования TOR-киназы приводит к снижению токсичности белковых агрегатов. Кроме того, выключение генов ATG-5 и ATG-7 в нейронах головного мозга мышей приводит к развитию нейродегенеративных заболеваний.
Существует ряд аутосомно-рецессивных нарушений, при которых у человека изменяются процессы аутофагии. Среди них — порок развития мозга, задержки в развитии, умственная отсталость, нарушения двигательных функций, нейродегенерация и другие.
Е. Осуми и его коллеги стали первыми учеными, которые смогли идентифицировать гомологи ATG у млекопитающих. Это позволило проводить исследования аутофагии у высших эукариот.
Со временем были представлены убедительные доказательства того, что аутофагия существует и в клетках всех млекопитающих. Это было подтверждено рядом исследований с использованием электронной микроскопии. Стало известно, что аутофагия присутствует на различных стадиях клеточной дифференциации — от наименее дифференцированных клеток до узкоспециализированных. Тогда было высказано предположение, что аутофагия может быть ответом организма на метаболический стресс, и что процесс может играть роль в патогенезе ряда заболеваний. Со временем было выявлено, что аутофагия существует и в одноклеточных организмах — простейших, что указывало на консервативный характер этого механизма.
Новаторские открытия Е. Осуми существенно повысили интерес к процессу аутофагии. Этот сегмент стал одним из наиболее изучаемых в сфере биомедицинских исследований. Так, в начале 2000-х годов ученые делали не более 150 публикаций в год на эту тему, а в 2015 г. их было более 4 тыс.
На основании фундаментальных открытий Е. Осуми были выделены различные типы аутофагии. Критерием к их разделению послужил объем вещества, который они деградируют. Наиболее изучен процесс макроаутофагии, при котором деградации подвергаются большие объемы цитоплазмы и клеточные органеллы.
Ученые также выяснили, что существует селективная и неселективная аутофагия. Неселективная аутофагия происходит постоянно, в основном она индуцируется стрессом, в частности — голодом. Селективная аутофагия специфических классов субстрата — протеиновых агрегатов, цитоплазматических органелл, вирусов и бактерий, включает специфические адапторы, распознающие субстрат и присоединяющие его к ATG-8/LC3, расположенному на мембране аутофагосомы.
Таким образом, открытие молекулярных основ механизма аутофагии позволило ученым понять очень важный клеточный процесс, характерный для всех эукариот. В настоящее время в этой сфере все еще остается много неизвестного современной науке.
Евгения Бочерикова
© The Nobel Committee for Physiology
or Medicine; фото и иллюстрации
© The Nobel Committee for Physiology or Medicine

Коментарі