|
|
Аспекты проведения инспекции и анализ выявленных нарушений представила Людмила Ковтун, руководитель отдела аттестации и инспекции клинических баз Государственного фармакологического центра (ГФЦ) МЗ Украины.
В Украине с 1999 г. инспекционные проверки (ИП) проводятся сотрудниками ГФЦ на основании действующей нормативно-правовой базы: Закона Украины «О лекарственных средствах» (1996), Руководства по клиническим исследованиям. Надлежащая клиническая практика (приказ МЗ Украины от 22.06.2005 г. № 373), Порядка проведения клинических испытаний лекарственных средств и экспертизы материалов клинических испытаний (приказ МЗ Украины от 13.02.2006 г. № 66), Инструкции по проведению инспекционных проверок клинических испытаний лекарственных средств (приказ ГФЦ от 01.11.2001 г.), Стандартных операционных процедур по проведению инспекции (приказ ГФЦ МЗ Украины от 14.12.2004 г. № 84).
Инспекция КИ — процедура официальной проверки представителем регуляторного органа документов, помещений, оборудования и технического оснащения, записей, системы гарантии качества и других ресурсов, которые имеют отношение к проведению КИ и могут находиться на клинической базе (КБ), в офисе спонсора или контрактной исследовательской организации (КИО).
Инспекции подлежат все КИ (отечественные и международные многоцентровые), при этом инспекторы могут привлекаться из состава экспертных комиссий ГФЦ и Государственной службы лекарственных средств и изделий медицинского назначения.
 |
В ходе инспекции проверяются: возможность проведения КИ на данной КБ (квалификация исследователей и персонала, место проведения, оборудование, лаборатория, документы); соответствие КИ протоколу и нормативным требованиям; защита прав пациентов (в том числе наличие подписанного информированного согласия); соответствие и достоверность записей в индивидуальной регистрационной форме (ИРФ) данным первичной документации; документация о получении, хранении, выдаче, распределении и возврате ЛС; учет побочных реакций на ЛС.
ГФЦ проводит рутинные инспекции текущих КИ (в том числе ретроспективные инспекции по данным архива) и целенаправленные, проводимые в случаях: одновременного проведения двух и более КИ в одном клиническом центре; при включении в КИ здоровых добровольцев, детей, ВИЧ-инфицированных, пациентов с психическими расстройствами, беременных и кормящих грудью; при возникновении серьезных побочных реакций.
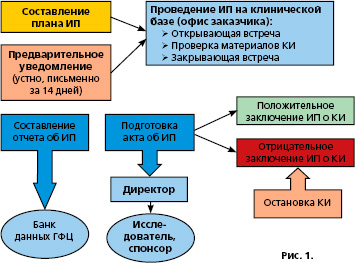
На рис. 1 показаны этапы проведения ИП.
Инспекторы проверяют файл исследователя, формы информированного согласия испытуемых (которые должны быть подписанными и датированными); записи в ИРФ на соответствие первичным данным (истории болезни, амбулаторные карты, лабораторные записи, дневники испытуемых, журналы выдачи медикаментов); документацию о ЛС (получение, распределение, возврат исследуемого препарата, его маркировка); сообщения о побочных реакциях.
|
В ходе проверок, проводимых ГФЦ, основные замечания, возникавшие у инспекторов, касались плохого знания исследователями своих обязанностей и протокола, неполной комплектации файла исследователя (недостаточно документации, отсутствие или утрата документа, отсутствие подписи и даты); нарушений маркировки и условий хранения (отсутствует контроль получения, учета и выдачи ЛС, нарушение инструкций спонсора по условиям хранения — температурному режиму, сроку хранения), нарушений в распределении исследуемого препарата (доступ к препарату не только субъектов исследования, назначение не по протоколу с нарушением дозы, кратности, правил приема). Случается, что замечания, возникающие у инспекторов, касаются нарушений процедуры получения информированного согласия: отсутствие информированного согласия, подписи исследователя, пациента, независимого свидетеля, законного представителя; расхождение в датах подписания информированного согласия и включения в КИ, дата поставлена рукой исследователя, отсутствует запись в первичной документации о подписании информированного согласия и даче согласия на участие в КИ; непредоставление пациенту второго экземпляра информированного согласия; версия информированного согласия не одобрена этическим комитетом). Также инспекторы выявляют нарушения по ведению ИРФ — некорректные исправления, несоответствие данным первичной документации, неполное внесение данных, отсутствие подписи исследователя, нарушения выполнения лабораторной диагностики (отсутствие у лаборатории сертификата аккредитации, стандартных операционных процедур (СОП), нет документального подтверждения метрологического контроля оборудования, нарушение условий хранения биоматериалов). В ходе проверок инспекторы ГФЦ определяли нарушения процедуры информирования спонсора, ГФЦ и этического комитета о побочных реакциях (сроки предоставления отчетов или сокрытие информации). Также к исследователям иногда возникают замечания по ведению первичной документации (отсутствие записей о назначении исследуемого ЛС, результатах анализов и инструментальных методах обследования) и пропаже документов (дневников и вопросников пациентов, ИРФ, историй болезни, амбулаторных карт, журналов, распечаток приборов и др.).
|
Основанием для дисквалификации исследователей или КБ может стать факт фальсификации данных КИ, систематические нарушения при проведении КИ, нарушение этических норм, сокрытие информации о побочных реакциях или отказ от ИП.
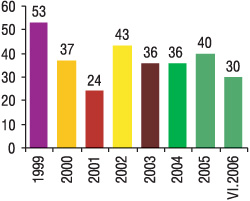
С начала 1999 до средины 2006 г.отделением инспекции ГФЦ МЗ Украины были проведены 299 ИП (рис. 2), среди них — 272 инспекции КИ препаратов отечественного производства и 27 — международных многоцентровых КИ (22 КБ и 5 офисов спонсоров). За весь период работы были приостановлены 15, остановлены полносью 2 КИ.
В конце доклада Л. Ковтун подчеркнула важность прозрачного проведения инспекции и обсуждения результатов проверки с каждым из исследователей.
Кондруца Трандафир (Condruta Trandafir), директор компании «Verum.edu» (Бухарест, Румыния), поделилась опытом проведения инспекций в роли GCP-инспектора в Румынии, а также в качестве наблюдателя рабочей группы инспекторов Европейского медицинского агентства по лекарственным средствам (European Medicines Agency — EMEA). Она участвовала в тренингах, проводимых Европейской комиссией, EMEA, и была наблюдателем в совместных инспекциях, проводимых в разных странах, — Великобритании, Италии, Венгрии, Болгарии.
|
В Румынии компетентным регуляторным органом, занимающимся вопросами КИ, является Национальное агентство по контролю за лекарственными средствами Румынии (NMA). В 1998 г. министерство здравоохранения Румынии одобрило руководство по надлежащей клинической практике в соответствии с ICH GCP. К 2007 г., когда Румыния станет членом ЕС, законодательная база страны будет полностью соответствовать ICH GCP (с 1998 г.), Директиве 2001/20/EC и Директиве 2005/28/EC (с 2006 г.).
Начиная с 2000 г. в Румынии были проведены более 1000 КИ, заказчиками которых стали представительства фармацевтических компаний или КИО, 40% спонсоров КИ являлись резидентами Евросоюза либо США. За это время NMA провело около 160 GCP-инспекций на КБ и в офисах спонсоров КИ. Параллельно были проведены GCP-инспекции, инициированные Управлением по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) и EMEA, в которых были получены положительные результаты.
Согласно ст. 15 Директивы 2001/20/EC страны — члены ЕС должны назначать инспекторов для проверок КБ, офисов спонсоров, мест производства исследуемых ЛС и лабораторий, осуществляющих анализ образцов биоматериалов, полученных от участников КИ. Кроме того, согласно ст. 15.4 Директивы 2001/20/EC Европейская комиссия или страна — член ЕС может подать запрос о проведении ИП на территории страны, не являющейся членом ЕС. Мероприятия по верификации соответствия GCP и осуществлению фармаконадзора координирует ЕМЕА.
Рутинная инспекция осуществляется:
- при проверке текущего КИ национальным регуляторным органом страны — члена Евросоюза;
- перед выдачей национальным регуляторным органом страны-члена разрешения на маркетинг, в том числе может проводиться аудит КИ в третьих странах (страны, не являющиеся членами Евросоюза);
- при проверке оконченных КИ, материалы которых поданы на рассмотрение Консультативного научного комитета (Committee for Medicinal Products for Human Use — CHMP) EMEA для получения разрешения на маркетинг (в рамках получения разрешения на маркетинг по централизованной процедуре).
Целенаправленная инспекция осуществляется по запросу чиновников CHMP в ответ на сообщения о возможных нарушениях, полученных от других государственных чиновников, инспекторов, пациентов, средств массовой информации. В ходе рутинных инспекций КИ проверяется то, как соблюдаются права участников, их конфиденциальность, благополучие и безопасность; надежность данных. При целенаправленных инспекциях КИ прежде всего проверяют аспекты, названные в запросе чиновников после изучения материалов КИ. Целенаправленные инспекции осуществляются с целью проверить, как исследователь, спонсор, КИО, лаборатория отреагировали на замечания, возникшие в ходе предыдущей инспекции. Кроме того, такая инспекция может осуществляться, если имеются подозрения о подлоге результатов.
Соответственно с классификацией рутинных инспекций (см. выше), инспекторы назначаются:
- регуляторным органом страны — члена Евросоюза. В состав группы инспекторов входят эксперты и врачи, фармакологи, чиновники, имеющие статус GCP-инспектора;
- регуляторным органом страны — члена Евросоюза. Инспектор осуществляет проверку КИ, проводимых в третьих странах, совместно с национальным инспектором, назначенным EMEA в качестве наблюдателя;
- регуляторным органом страны — члена Евросоюза из числа своих инспекторов по требованию EMEA (в рамках процедуры центральной авторизации).
Перед проведением проверки инспектор должен составить подробный план. При необходимости план может быть изменен во время инспекции, если это поможет легче достичь поставленных целей. Как правило, в ходе инспекции осматривают все места, имеющие отношение к проведению КИ: КБ, офис спонсора, офис КИО, лабораторию, компьютерные системы, комплексы для проведения I фазы КИ и исследований по биоэквивалентности. При проверке КБ инспектор обращает внимание на правовые и административные вопросы, связанные с проведением КИ, в том числе на: наличие для каждого из участников подписанного информированного согласия, соответствие первичных данных и данных, внесенных в ИРФ, обращение с исследуемыми препаратами. При проверке КИО инспектор прежде всего обращает внимание на систему обеспечения качества работы организации: вопросы управления персоналом, технического оснащения, наличие и содержание СОП. В ходе плановой ИП спонсора КИ прежде всего обращают внимание на соблюдение всех предписаний, связанных с выполнением и окончанием КИ, мониторингом, обращение с исследуемыми препаратами, правильностью и своевременностью оформления отчетов о побочных реакциях, ИРФ, обращение с данными и отчетами о КИ, а также о своевременном проведении внутреннего аудита.
|
Доклад Ольги Голубевой, директора по контролю качества компании «PSI Co Ltd» (Санкт-Петербург, Россия), был посвящен опыту проведения инспекций FDA в России. Основной целью таких инспекций является проверка самого факта существования пациентов, изучение их первичной документации, проверка соответствия пациента критериям включения/невключения, наличия информированного согласия для каждого пациента, соблюдения этических принципов, правильности лечения исследуемым препаратом, понимания исследователем своих обязанностей. Порядок проведения инспекции и ее продолжительность (от 5 рабочих дней и более в зависимости от целей и задач) регламентируются руководствами FDA. Предварительные результаты инспекции оглашаются инспектором на заключительном совещании с участием исследователя и спонсора исследования. Окончательные результаты предоставляются исследователю в письме, которое направляется в исследовательский центр после изучения внутреннего отчета инспектора сотрудниками главного управления FDA. Результаты работы исследователя оцениваются FDA по следующей шкале:
- NAI — no action indicated. Требования к проведению исследования соблюдены полностью;
- VAI — voluntary action indicated. Неточное соблюдение требований к проведению исследования. Исследователю даются рекомендации на будущее. Данные, полученные исследователем, принимаются FDA для изучения и принятия решения о регистрации препарата;
- OAI — official action indicated. Исследование проводилось с серьезным нарушением международных и/или местных требований, выявлена необходимость регуляторных или административных санкций в отношении исследователя и/или медицинского учреждения вплоть до дисквалификации исследователя и/или предъявления ему судебного иска, либо вплоть до аннулирования полученных результатов.
Ирина Борзенко, доцент кафедры фармакологии с курсом клинической фармакологии Национального медицинского университета имени А.А. Богомольца, говорила о значении личности монитора для успешного проведения КИ. Докладчица отметила недостаток внимания, уделяемого подготовке таких специалистов в нашей стране. Тем не менее, работа монитора является одним из факторов успешного проведения КИ наряду с корректно составленным протоколом исследования, хорошей подготовкой и опытом врача-исследователя, достаточным бюджетом проекта.
Монитор (Clinical Research Associate, Clinical Monitor, Trial Monitor, Medical Monitor) — лицо, назначаемое спонсором или КИО, контролирующее проведение КИ в соответствии с протоколом. Обязанности монитора прописаны в ICH GCP, инструкциях, СОП спонсора и КИО. В обязанности монитора входит: контроль хода КИ; регистрация данных; составление отчетов в соответствии с протоколом, GCP, СОП и требованиями официальных инстанций.
|
Монитор организовывает подачу документов по КИ в регуляторные органы (что требует знания законодательной базы), подготавливает и подписывает договора с руководителями медицинских учреждений и подразделений (необходимо знать юридические нормы и правила оформления документов). На плечи монитора ложатся обязанности по заключению договоров с торгово-промышленной палатой и таможней (при процедуре разового ввоза исследуемых препаратов); органами санитарного контроля (при проведении процедуры уничтожения препаратов); с курьерскими службами (при отправке препаратов, документов, биологических проб и образцов); со складами ЛС (в случае их хранения на специализованных складах); представительствами фармацевтических фирм (по поиску и закупке препаратов, реактивов, тест-систем, что требует знаний по фармакологии и менеджменту). Весь этот перечень обязанностей свидетельствует о том, что монитор является основным связующим звеном между исследователем и спонсором КИ. Несмотря на широкий круг обязанностей, основным показателем работы монитора является верификация данных КИ. Монитор, находящий и устраняющий единичные ошибки в работе центра, экономит время для исправления их в будущем, когда они перерастут в систематические нарушения. Общаясь с исследователями, монитор помогает им улучшить качество работы. Качество работы монитора можно оценить по тому, насколько успешными были результаты аудитов и инспекций КИ, за проведение которых он отвечает.
По собственному опыту докладчицы, у 44 из 48 опрошенных ею мониторов с опытом работы от 2 до 5 лет было высшее медицинское образование, остальные 4 имели высшее фармацевтическое, биологическое, техническое и филологическое образование соответственно. Проведя опрос среди мониторов, И. Борзенко выявила те личные и профессиональные качества, которые наиболее важны для успешной работы в этой должности. Обязательным для монитора являются знание английского, украинского и русского языков, навыки работы на ПК на уровне уверенного пользователя, наличие водительского удостоверения. Среди наиболее важных личных качеств называли такие: коммуникабельность, интеллигентность, дипломатичность, порядочность, аналитический склад ума, самокритичность, быстрая обучаемость, пунктуальность и готовность к частым командировкам. Ежедневно монитору приходится работать с большим количеством документов одновременно, поэтому он непременно должен уметь определять приоритеты и проявлять здоровую долю педантизма. Непременным качеством для монитора является умение ясно излагать мысли, ставить задачи и анализировать результаты. В своей работе он должен ориентироваться на спонсора КИ и быть готовым к работе под давлением (спонсора и руководства). Эта профессия требует не только специальных знаний и умений, но и приверженности мобильному образу жизни.
Франсуа Гилен (Francois Geelen «How to select the right monitor», 1997), главный управляющий кадрового агентства «Geelen&Geelen», специализирующегося на КИ, для определения опыта монитора предлагает следующий прием для приблизительной оценки зрелости монитора: нужно умножить количество лет, которые отработал монитор, на количество компаний-спонсоров, с которыми он имел дело, или на количество медицинских показаний, в области которых он мониторировал исследования.
Если полученный результат не меньше 9, то монитора можно считать достаточно опытным.
Завершая доклад, И. Борзенко заметила, что сотни КИ в Украине были успешно проведены не только благодаря качественной работе врачей, но также и хорошей работе мониторов.
|
Алексей Михеев, генеральный директор компании «Верум Украина», выступил с докладом «Ошибки при проведении мониторинга клинических исследований». Основываясь на солидном опыте в подготовке клинических мониторов, А. Михеев дал много полезных практических рекомендаций для тех, кто только начинает свою карьеру в этой области, а также для тех, кто занимается подготовкой таких специалистов.
По словам докладчика, мониторинг КИ является ведущим видом услуг, предоставляемых КИО в Украине. Поэтому наряду с квалификацией медицинского персонала и оснащенностью лечебных заведений качество мониторинга играет ведущую роль при оценке Украины как места качественного проведения КИ. Главной целью мониторинга КИ является:
- обеспечение защиты прав и благополучия людей — субъектов испытания;
- обеспечение уверенности в том, что данные, содержащиеся в отчетах, являются полными и подтверждаются первичными документами (протоколом и поправками к нему), соответствует правилам GCP и регуляторным требованиям.
Мониторинговые визиты и их периодичность регламентированы протоколом КИ. Согласно Руководству по надлежащей клинической практике (CPMP/ICH/135/95 (E6), 1997) монитор в ходе своего визита на КБ:
- получает представление о ходе КИ в исследовательском центре, о выполнении требований протокола и нормативных документов;
- обозначает круг проблем и вопросов, связанных с ходом КИ;
- убеждается в соблюдении прав и безопасности испытуемых, в частности проверяет наличие подписанных информированных согласий, наличие скрининговых списков, идентификационных списков пациентов, наличие записей в первичной документации, подтверждений интерактивной системы и т.п.;
- проверяет выполнение требований протокола КИ;
- сверяет (верифицирует) полученные данные;
- исправляет ошибки и пропуски, выявленные при верификации;
- собирает полученные данные;
- убеждается в правильности использования испытуемого продукта и действий, связанных с ним;
- подготавливает и передает собранные данные в статистические отделы.
«Продуктом» работы монитора являются собранные данные в виде заполненных ИРФ (на электронных или бумажных носителях), а также отчет о мониторинге.
Специальность монитора КИ отсутствует в государственных образовательных программах, поэтому профессиональную подготовку мониторов проводят КИО и спонсоры КИ. Основные профессиональные требования, предъявляемые к клиническому монитору, это знание украинского и международного законодательства в области КИ, владение медицинской терминологией, научный/клинический багаж, хорошее знание английского языка. Среди персональных требований, предъявляемых к клиническому монитору, — общительность и дипломатичность, способность к планированию своих действий (в том числе следование СОП), дисциплинированность, способность к работе в стрессовых ситуациях, в команде, гибкость, а также хорошие коммуникативные навыки. Важнейшими качествами монитора, необходимыми для общения с любыми лицами, задействованными в организации и проведении КИ, является вежливость в сочетании с настойчивостью.
|
Наиболее частыми причинами ошибок, допускаемых при мониторинге КИ, бывают неправильное планирование или отсутствие планирования монитором своих действий, недопонимание приоритетности выполняемых заданий, недостаточные знания в области локального и международного законодательства в области КИ. Случается, что неопытные мониторы недостаточно времени уделяют изучению протокола КИ, поправок к нему, сведений о безопасности испытуемого продукта и СОП. Результатом неправильного планирования может стать несоблюдение установленной периодичности визитов, невыполнение всех задач мониторинга, перерасход установленного контрактом рабочего времени на проведение мониторингового визита, задержка отчетности о мониторинге.
Основываясь на длительном опыте подготовки мониторов, А. Михеев дал рекомендации по планированию:
- знать установленную спонсором периодичность мониторинговых визитов;
- в начале исследования обсудить с исследователем планируемую периодичность визитов;
- составлять план подготовки к мониторинговому визиту с указанием задач и длительности их выполнения;
- накануне визита предупредить исследователя, чтобы он заполнил все ИРФ, запланированные для проверки, и подготовил всю необходимую для верификации первичную документацию.
Монитор должен помнить, что первоочередной задачей является обеспечение защиты прав и благополучия людей — субъектов исследования. Далее идут задачи по проверке первичной документации и ИРФ, проверке обращения с испытуемым ЛС, обсуждению результатов мониторингового визита и составлению плана действий для устранения выявленных нарушений и недостатков.
Типичной ошибкой монитора является допущение использования не установленных нормативными актами форм и вставок в карты пациентов. Такие ошибки допускают мониторы, имеющие недостаточные знания в области медицинского делопроизводства и медицинской статистики. Поэтому монитор обязан знать все существующие виды учетных статистических форм, особенности их заполнения, порядок их регистрации и архивирования.
В завершение доклада А. Михеев отметил, что успех мониторинга зависит от того, насколько налаженным является взаимодействие между монитором, администрацией лечебно-профилактического учреждения и исследователем. n
|
Пресс-служба «Еженедельника АПТЕКА»







Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим