Потрібно розробити нову редакцію законопроєкту «Про медичні вироби» — Торгово-промислова палата
17 листопада відбулося засідання комітету з питань охорони здоров’я та фармації при Торгово-промисловій палаті України
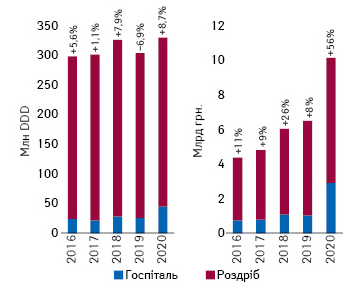
Споживання антибіотиків в Україні за класифікацією ВООЗ
Нещодавно у журналі «The Lancet» було опубліковано* результати дослідження із залученням методів геостатистичного моделювання для оцінки споживання антибіотиків у 204 країнах. Крім іншого, у дослідженні було проаналізовано споживання антибіотиків у розрізі класифікації антибіотиків «AWaRe», розробленої Всесвітньою організацією охорони здоров’я (ВООЗ), втім, на жаль, відповідні дані щодо України не були доступні авторам, а тому ми вирішили заповнити цю прогалину та провести відповідне дослідження споживання […]
Допуск до державних закупівель — ООРММП України звернулося до міністра охорони здоров’я
Об’єднання організацій роботодавців медичної та мікробіологічної промисловості України (далі — ООРММП України) направило листа Віктору Ляшку, міністру охорони здоров’я, з проханням посприяти допуску українських фармвиробників до участі в тендерах із закупівлі протитуберкульозних препаратів та ліків для попередження розвитку СНІД-асоційованих захворювань та передачі ВІЛ у зв’язку з тим, що Глобальний фонд у рамках програми протидії туберкульозу та ВІЛ-інфекції/СНІДу закуповує для України лише препарати, […]
Позиція Асоціації AMOMD® щодо законопроєкту «Про медичні вироби»: сумнівна користь та нові бар’єри для операторів
Асоціація «Оператори ринку медичних виробів»® AMOMD® (далі — Асоціація) як перше та єдине в Україні професійне соціально відповідальне об’єднання близько 80 національних виробників, імпортерів, дистриб’юторів та інших учасників ринку медичних виробів, у тому числі й операторів дезінфекційних засобів, засобів індивідуального захисту та косметичної продукції, є розвиненою професійною організацією з міжнародним членством у Global Medical Technology Alliance (GMTA), цим пресповідомленням доводить до […]
Критерії визначення ліків, які заборонені до рекламування: на повторне обговорення винесено проєкт змін
23 листопада на сайті МОЗ для повторного громадського обговорення оприлюднено проєкт наказу Міністерства, яким вносять зміни до Критеріїв, що застосовуються при визначенні лікарських засобів, рекламування яких заборонено, затверджених наказом МОЗ від 06.06.2012 р. № 422. Як зазначається в супровідній документації, його повторне оприлюднення для громадського обговорення пов’язане з оновленням Аналізу регуляторного впливу проєкту. Зокрема, у ньому уточнено цілі державного регулювання. Так, […]
Регулювання клінічних випробувань в Україні наближається до європейського — ЄБА
Європейська Бізнес Асоціація (ЄБА) звертає увагу, що 18 листопада Парламент прийняв в цілому проєкт закону «Про страхування», зареєстрований 29 березня 2021 р. за № 5315, у якому враховано зміни до регулювання страхування в клінічних випробуваннях, які були запропоновані експертами Підкомітету з клінічних досліджень асоціації. Завдяки цим змінам Україна перейде до повністю європейської моделі страхування відповідальності у клінічних дослідженнях. Законом вносяться відповідні зміни у чинний […]
У ДЕЦ обговорили поточні питання галузі
23 листопада під головуванням директора ДЕЦ Михайла Бабенка відбулася чергова робоча нарада з керівниками структурних підрозділів
Перші пілотні проєкти щодо фармацевтичного страхування вже розпочалися — Михайло Радуцький
Михайло Радуцький, голова Комітету Верховної Ради України з питань здоров’я нації, медичної допомоги та медичного страхування (далі — Комітет) на своїй сторінці у Facebook опублікував допис, у якому зазначив, що після низки публікацій щодо запровадження фармацевтичного страхування до Комітету звернувся керівник однієї з українських страхових компаній. Він розповів, що спільно з державними установами вже реалізує пілотний […]
НСЗУ розпочинає прийом звернень від медичних закладів для підготовки до контрактування на 2022 р.
Йдеться про перевірку наявності медичного обладнання, персоналу, ліцензій, дозвільних документів, необхідних для надання медичних послуг, а також можливості залучення підрядників за відповідними напрямами
Проєкт наказу МОЗ України «Про внесення змін до Критеріїв, що застосовуються при визначенні лікарських засобів, рекламування яких заборонено»
Оприлюднений на сайті МОЗ України 23.11.2021 р.