Рідкісні, незвичні, генетичні — що ми знаємо про орфанні захворювання?
Рідкісні, або орфанні захворювання — часто хронічні та прогресуючі небезпечні для життя хвороби, які уражують невелику частку населення порівняно з іншими видами патології. База даних Orphanet налічує інформацію про понад 6 тис. рідкісних захворювань, більшість з яких є генетично зумовленими. Загальна поширеність рідкісних захворювань серед населення світу оцінюється на рівні 3,5–5,9% (Вакап С. та ін.., 2020). Особи з рідкісними хворобами можуть стикатися […]
Надання пацієнтам ліків зі співчуття: Парламентом урегульовано систему оподаткування
Європейська Бізнес Асоціація (далі — Асоціація) повідомляє, що 23 лютого Парламентом ухвалено проєкт закону України «Про внесення змін до Податкового кодексу України щодо вдосконалення онлайн комунікації з платниками податків та уточнення окремих положень законодавства» (реєстр. № 9662), який наразі очікує підписання Президентом України. В Асоціації відмічають, що врегулювання вимог щодо проведення програм зі співчуття є надзвичайно […]
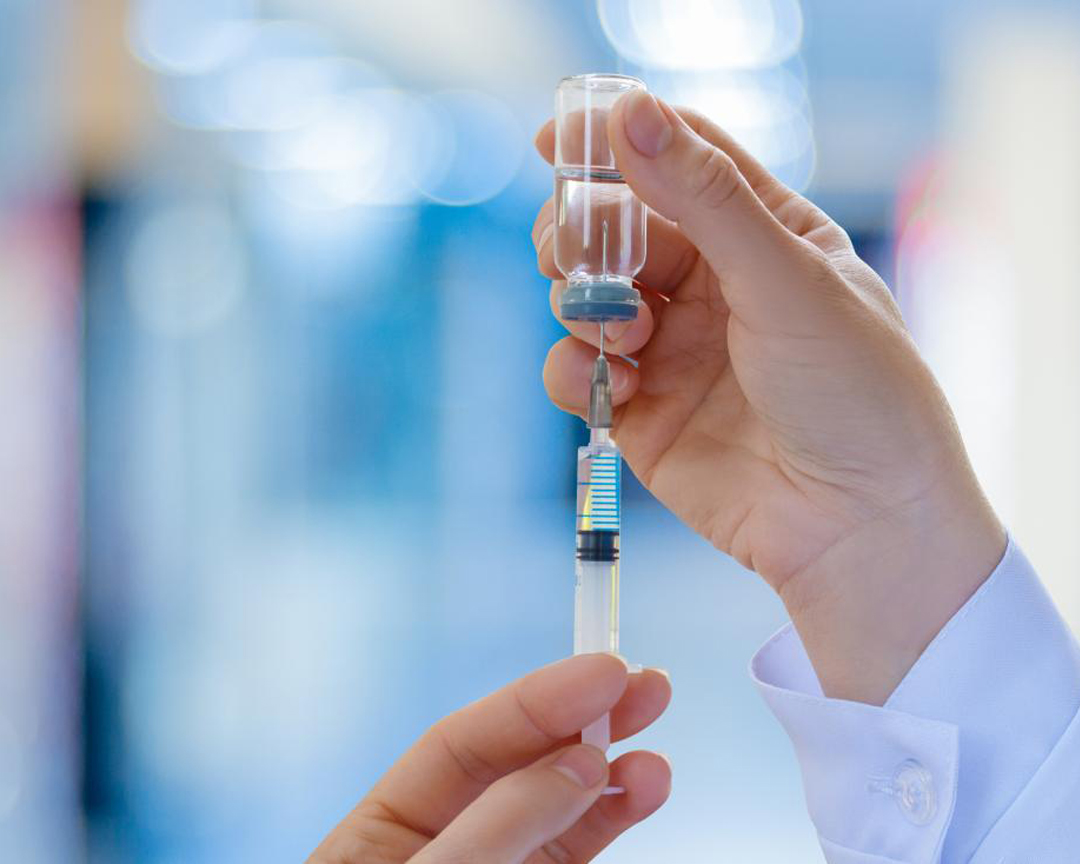
Уряд надав можливість фармацевтам робити щеплення в приміщеннях аптек
27 лютого Уряд ухвалив зміни до Ліцензійних умов провадження господарської діяльності з медичної практики, які стосуються проведення щеплень в аптечних закладах. Відповідна постанова КМУ від 27.02.2024 р. № 213 набуде чинності через 3 міс з дня її опублікування. Так, змінами надається можливість проведення профілактичних щеплень в аптечних закладах фармацевтичними працівниками (фармацевтами, фармацевтами клінічними), які пройшли спеціальні щорічні […]
Наказ МОЗ України від 23.02.2024 р. № 320
Про декларування зміни оптово-відпускних цін на лікарські засоби станом на 21 лютого 2024 року
Додаток 2 до наказу Міністерства охорони здоров’я України «Про декларування зміни оптово-відпускних цін на лікарські засоби станом 21 лютого 2024 року»
Додаток 2 до наказу Міністерства охорони здоров’я України «Про декларування зміни оптово-відпускних цін на лікарські засоби станом 21 лютого 2024 року» Позиції, які виключаються з реєстру оптово-відпускних цін на лікарські засоби Міжнародна непатентована або загальноприйнята назва лікарського засобу Торговельна назва лікарського засобу Форма випуску Дозування Кількість одиниць лікарського засобу у споживчій упаковці Найменування виробника, країна Код АТХ […]
Додаток 1 до наказу Міністерства охорони здоров’я України «Про декларування зміни оптово-відпускних цін на лікарські засоби станом 21 лютого 2024 року»
Додаток 1 до наказу Міністерства охорони здоров’я України «Про декларування зміни оптово-відпускних цін на лікарські засоби станом 21 лютого 2024 року» Задекларовані зміни оптово-відпускних цін на лікарські засоби станом на 21 лютого 2024 року, що вносяться до реєстру оптово-відпускних цін на лікарські засоби Міжнародна непатентована або загальноприйнята назва лікарського засобу Торговельна назва лікарського засобу Форма випуску Дозування Кількість одиниць […]
Особливості відпуску за новим переліком медичних виробів, що реімбурсуються
Національна служба здоров’я України (НСЗУ) звертає увагу на зміни при відпуску медичних виробів за Переліком медичних виробів, які підлягають реімбурсації за програмою державних гарантій медичного обслуговування населення (далі — Перелік), станом на 12 лютого 2024 р., що затверджений наказом Міністерства охорони здоров’я (МОЗ) України від 20.02.2024 р. № 279. Цей наказ набуде чинності 29 лютого 2024 р. […]
З квітня у Франції забороняють рекламу ібупрофену 400 мг для споживачів
Французьке національне агентство з безпеки лікарських засобів і товарів медичного призначення (Agence national de securité du médicament et des produits de santé — ANSM) повідомило 8 лютого, що реклама лікарських засобів, що містять ібупрофен у дозуванні 400 мг, буде заборонена з 2 квітня 2024 р. Таким чином, більше не буде реклами цих ліків у газетах, […]
Витяг із постанови КМУ від 29.03.2024 р. № 344
Про внесення змін до постанов Кабінету Міністрів України щодо використання печаток та визнання такими, що втратили чинність, деяких постанов Ради Міністрів Української РСР та Кабінету Міністрів України
Витяг з постанови КМУ від 27.02.2024 р. № 212
Деякі питання реалізації пілотного проекту щодо зубопротезування окремих категорій осіб, які захищали незалежність, суверенітет та територіальну цілісність України