Ірину Суворову призначено виконуючою обов’язки Голови Державної служби України з лікарських засобів та контролю за наркотиками
Виконувати обов’язки Голови цього органу І. Суворова буде до призначення очільника Державної служби України з лікарських засобів та контролю за наркотиками
Уряд схвалив доопрацьований законопроект щодо спрощеної реєстрації ліків, зареєстрованих в країнах з жорсткою регуляторною системою (оновлено)
Планується, що законопроект буде розглянуто Верховною Радою України на наступному пленарному тижні
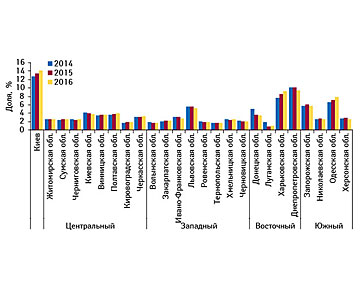
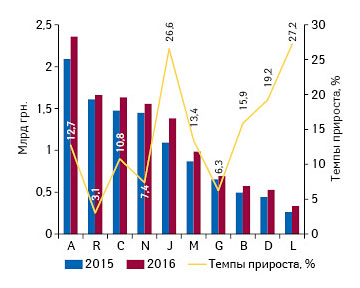
Аптечные продажи в регионах Украины по итогам I кв. 2016 г. Helicopter view
В данной публикации мы рассмотрим аптечные продажи в региональном разрезе
Частная медицина в Украине: поиск новых возможностей во время перемен
В рамках данной публикации рассмотрены доклады, прозвучавшие во время 1 и 2 сессий 6-го Специализированного бизнес-форума «Частная медицина в Украине–2016» в Днепропетровске
Профільний комітет рекомендує Парламенту відправити на доопрацювання законопроект щодо спрощеної реєстрації
На думку членів комітету, він містить неточності та корупційні ризики
Частная медицина в Украине-2016. Конкуренция как необходимость
6-й Специализированный бизнес-форум «Частная медицина в Украине–2016» объединил более 100 ведущих экспертов отрасли, топ-менеджеров и владельцев частных учреждений здравоохранения, страховых, исследовательских, консалтинговых, сервисных и юридических компаний
ЄБРР планує інвестувати в розвиток фармацевтичної галузі України близько 1 млрд євро
Окрім фінансування компаній або виробництв, банк може також надати й іншу допомогу, в тому числі і консультативну за участю міжнародних експертів
Аптечный рынок Украины по итогам I кв. 2016 г.: Helicopter View
Традиционно мы продолжаем аналитические обзоры деятельности операторов фармрынка Украины. О том, как стартовали аптечные продажи в I кв. 2016 г., пойдет речь в данной публикации
Питання сплати ПДВ під час закупівель ліків через міжнародні організації потребує врегулювання — профільний парламентський Комітет
Члени Комітету прийняли рішення звернутися до Прем’єр-міністра України з вимогою терміново створити міжвідомчу робочу групу з врегулювання питання сплати ПДВ під час здійснення закупівель ліків через міжнародні організації
Через неузгодженості зі сплатою ПДВ заблоковано поставку ліків, закуплених через міжнародні організації, на суму понад 500 млн грн.
Впродовж півроку народні депутати не можуть витребувати у заступника міністра охорони здоров’я Ігоря Перегінця вичерпну інформацію щодо закупівель і поставки ліків