Первый глобальный саммит фармакопей
В работе саммита приняли участие и украинские специалисты во главе с Александром Гризодубом, директором Украинского научного фармакопейного центра качества лекарственных средств
Пациенты без границ!
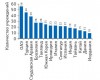
Медицинский туризм за последние годы получил значительное развитие и продолжает представлять перспективное направление для ведения бизнеса. В данной публикации будут рассмотрены основные игроки, присутствующие на этом рынке
Назустріч VIII Національному з’їзду фармацевтів України Упорядкування та значення термінології у фармацевтичній діяльності
Враховуючи те, що фармацевтична термінологія виконує роль понятійно-термінологічного засобу інформації та є правовою основою для прийняття рішень і організаційно-виконавчих дій, а базові терміни мають соціальне значення при наданні фармацевтичної (медичної) допомоги, пропонована до уваги читачів стаття була схвалена на робочій нараді провідних фахівців Національного фармацевтичного університету
Асоціація виробників інноваційних ліків «АПРАД»: світовий досвід та українські реалії
Цілі, завдання, досягнення та стратегічні напрямки подальшої діяльності Асоціації висвітлили Жан-Поль Шоєр, голова правління, та Юрій Савко, виконавчий директор Асоціації
Плательщики vs фармкомпании: искусство коммуникации
В последнее время во многих странах отмечается повышение влияния плательщиков на процессы ценообразования и выведения новых препаратов на рынок, что не могло не отобразиться на маркетинговой стратегии фармацевтических компаний
Набула чинності постанова КМУ від 14 листопада 2011 р. № 1165
Опублікована в бюлетені «Офіційний вісник України» № 88.
Грипп и перечни
В настоящее время МЗ Украины разрабатывается проект приказа «Об утверждении обязательного минимального ассортимента лекарственных средств и изделий медицинского назначения для аптечных учреждений». Проанализируем возможные последствия его имплементации
ЗАО «Фармацевтическая фирма «Дарница»: готовность к импортозамещению № 1
Сегодня для страны существует уникальный шанс — стать относительно независимым государством в сфере медикаментозного обеспечения. Помочь ей в этом готова отечественная компания
На розширеному засіданні в КМУ вирішувалася доля фармацевтичного ринку
17 листопада поточного року в КМУ під головуванням Прем’єр-міністра Миколи Азарова відбулася нарада, присвячена ситуації на вітчизняному ринку лікарських засобів
Микола Азаров про цінове регулювання, ПДВ на лікарські засоби та реформування системи охорони здоров’я
Прем’єр-міністр України констатував, що лікарські засоби сьогодні не по кишені двом третинам пацієнтів, а фармацевтичні компанії опираються контролю за обґрунтованістю цін. З метою пошуку рішень проблемних питань у сфері ціноутворення на лікарські засоби 17 листопада в КМУ відбудеться розширена нарада за участю представників МОЗ, НАМН України, фармацевтичних компаній, громадських організацій.