Новий Національний перелік базується на 19-му виданні Базового переліку основних лікарських засобів, рекомендованих ВООЗ. Ліки, що в установленому законом порядку зареєстровані в Україні та включені до Національного переліку основних лікарських засобів, підлягають закупівлі закладами й установами охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів. За умови задоволення в повному обсязі потреби в ліках, включених до Національного переліку, замовники зможуть закуповувати препарати, що не включені до зазначеного Національного переліку. При цьому перевага надаватиметься препаратам, включеним до галузевих стандартів у сфері охорони здоров’я. Відповідно до вимог постанови КМУ від 17 жовтня 2008 р. № 955 (зі змінами, внесеними постановою КМУ від 17.03.2017 р. № 152) на препарати, включені до Національного переліку, розповсюджується вимога щодо встановлення граничних постачальницько-збутових та роздрібних надбавок у розмірі 10 та 25% відповідно.
Порівняння з попередньою редакцією документа
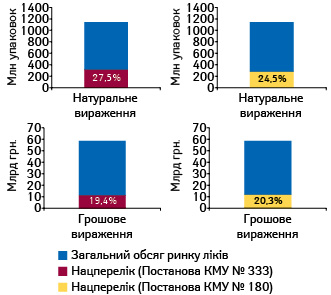
Новий Національний перелік включає 377 МНН лікарських засобів. Попередня редакція Національного переліку налічувала 215 МНН. За підсумками 2016 р. загальні обсяги аптечного продажу та госпітальних закупівель лікарських засобів становлять 58,7 млрд грн. за 1,14 млрд упаковок. У досліджуваний період сумарна частка лікарських засобів, включених до нового Національного переліку, охоплює 20,3% ринку в грошовому і 24,5% в натуральному вираженні (рис. 1). Попередня редакція Національного переліку охоплювала 19,4 та 27,5% ринку відповідно.
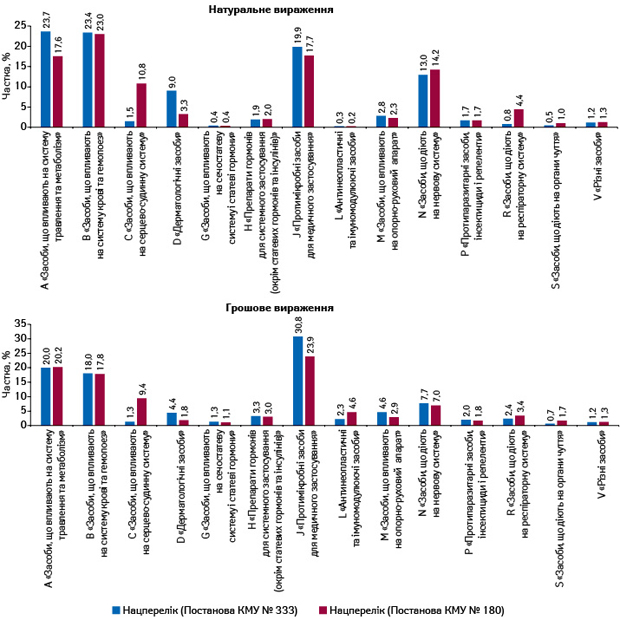
Щодо препаратів, включених до нового Національного переліку, у розрізі груп АТС-класифікації слід зазначити, що в загальному обсязі аптечного продажу та госпітальних закупівель за підсумками 2016 р. в натуральному вираженні фіксується суттєве зниження частки препаратів АТС-груп A «Засоби, що впливають на травну систему і метаболізм» та D «Дерматологічні засоби» у порівнянні з попередньою редакцією Національного переліку. У той же час значно збільшився обсяг препаратів АТС-груп C «Засоби, що впливають на серцево-судинну систему» та R «Засоби, що діють на респіраторну систему». При цьому в грошовому вираженні для АТС-групи А частка майже не змінилася (рис. 2).
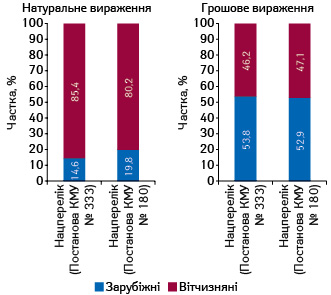
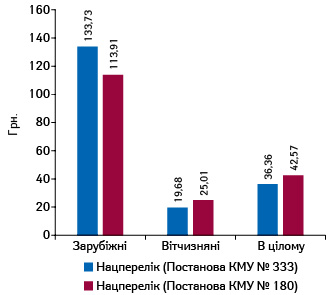
За підсумками 2016 р., частка препаратів зарубіжного виробництва (за власником ліцензії), включених до нового Національного переліку, збільшилася з 14,6 до 19,8% порівняно з попередньою редакцією Національного переліку. При цьому у грошовому вираженні їх частка майже не змінилася (рис. 3). У звя’зку зі зміною структури препаратів, включених до нового Національного переліку, у порівнянні з попередньою редакцією змінилася і середньозважена вартість 1 упаковки. При цьому для вітчизняних препаратів вона стала вищою, а для зарубіжних — нижчою (рис. 4). Загалом середньозважена вартість 1 упаковки препаратів, включених до нового Національного переліку, підвищилася з 36,4 до 42,6 грн. за 1 упаковку.
Порівняння з переліком ВООЗ
У новий Національний перелік не включено більше 50 МНН лікарських засобів у порівнянні з 19-м виданням Базового переліку основних лікарських засобів, рекомендованих ВООЗ (табл. 1). При цьому до Національного переліку включено деякі МНН, які відсутні в переліку ВООЗ (табл. 2). Більшість із цих препаратів пропонується використовувати як альтернативу препаратам з переліку ВООЗ. Також на близько 70 МНН, включених до Національного переліку, розширено вимоги щодо дозувань та упаковки лікарських засобів порівняно з Базовим переліком ВООЗ.
| Таблиця 1 | Перелік МНН, які включені до 19-го видання Базового переліку ВООЗ, але не включені до Національного переліку основних лікарських засобів в Україні |
| № з/п | МНН |
| 1 | Hyoscine hydrobromide |
| 2 | Trimethoprim |
| 3 | Bedaquiline |
| 4 | Stavudine |
| 5 | Darunavir |
| 6 | Lopinavir + ritonavir |
| 7 | Lamivudine + nevirapine + stavudine |
| 8 | Lamivudine + nevirapine + zidovudine |
| 9 | Valganciclovir |
| 10 | Simeprevir |
| 11 | Daclatasvir |
| 12 | Dasabuvir |
| 13 | Ledipasvir + sofosbuvir |
| 14 | Ombitasvir + paritaprevir + ritonavir |
| 15 | Suramin sodium |
| 16 | Eflornithine |
| 17 | Melarsoprol |
| 18 | Nifurtimox |
| 19 | Benznidazole |
| 20 | Asparaginase |
| 21 | Mesna |
| 22 | Leuprorelin |
| 23 | Whole blood |
| 24 | Coal tar |
| 25 | Podophyllum resin |
| 26 | Copper-containing device |
| 27 | Condoms |
| 28 | Diaphragms |
| 29 | Hpv vaccine |
| 30 | Pneumococcal vaccine |
| 31 | Rotavirus vaccine |
| 32 | Japanese encephalitis vaccine |
| 33 | Yellow fever vaccine |
| 34 | Tick-borne encephalitis vaccine |
| 35 | Cholera vaccine |
| 36 | Hepatitis a vaccine |
| 37 | Meningococcal meningitis vaccine |
| 38 | Typhoid vaccine |
| 39 | Influenza vaccine (seasonal) |
| 40 | Varicella vaccine |
| 41 | Bevacizumab |
| 42 | Nicotine replacement therapy (nrt) |
| 43 | Glucose with sodium chloride |
| 44 | Ascorbic acid |
| 45 | Calcium |
| 46 | Cholecalciferol |
| 47 | Ergocalciferol |
| 48 | Iodine |
| 49 | Nicotinamide |
| 50 | Pyridoxine |
| 51 | Retinol |
| 52 | Riboflavin |
| 53 | Sodium fluoride |
| 54 | Thiamine |
| Таблиця 2 | Перелік МНН, які включені до Національного переліку основних лікарських засобів в Україні, але не включені до 19-го видання Базового переліку ВООЗ |
| № з/п | МНН |
| 1 | Гідроморфон (Hydromorphone) (може бути використаний як альтернатива морфіну) |
| 2 | Оксикодон (Oxycodone) (може бути використаний як альтернатива морфіну) |
| 3 | Теризидон (Terizidone) (може бути використаний як альтернатива циклосерину) |
| 4 | Протіонамід (Protionamide) (може бути використаний як альтернатива етіонаміду) |
| 5 | Офлоксацин (Ofloxacin)(може бути використаний як альтернатива левофлоксацину) |
| 6 | Моксифлоксацин (Moxifloxacin) (може бути використаний як альтернатива левофлоксацину) |
| 7 | Надропарин (Nadroparin) (може бути використаний як альтернатива еноксапарину) |
| 8 | Далтепарин (Dalteparin)(може бути використаний як альтернатива еноксапарину) |
| 9 | Деферасірокс (Deferasirox) (може бути використаний як альтернатива дефероксаміну) |
| 10 | Декстран 1 (Dextran 1) (може бути використаний як альтернатива декстрану 70) |
| 11 | Декстран 40 (Dextran 40) (може бути використаний як альтернатива декстрану 70) |
| 12 | Атенолол (Atenolol) |
| 13 | Глібенкламід (Glibenclamide) (може бути використаний як альтернатива гліклазиду) |
| 14 | Гоматропін (гідробромід) (Homatropine hydrobromide) (може бути використаний як альтернатива атропіну) |
| 15 | Циклопентолат (гідрохлорид) (Cyclopentolate) (може бути використаний як альтернатива атропіну) |
| 16 | Бупренорфін (Buprenorphine) |
Подвійна регуляція
Як вже повідомлялося, з 25 березня 2017 р. на препарати, включені до Національного переліку, розповсюджується вимога щодо встановлення граничних постачальницько-збутових та роздрібних надбавок у розмірі 10 та 25% відповідно. Однак слід звернути увагу операторів ринку на те, що до Національного переліку включено деякі лікарські форми препаратів, які також входять до переліку МНН лікарських засобів, затвердженого постановою КМУ від 9 листопада 2016 р. № 863 «Про запровадження відшкодування вартості лікарських засобів». На ці препарати, відповідно до постанови КМУ від 17 жовтня 2008 р. № 955 (із змінами, внесеними постановою КМУ від 17.03.2017 р. № 152), з 1 квітня 2017 р. встановлюється гранична постачальницько-збутова та роздрібна надбавка на рівні 10 та 15% відповідно. При цьому для госпітальних закупок граничні надбавки встановлено на рівні 10 та 10% відповідно.
Роз’яснення МОЗ України
31 березня 2017 р. на офіційному сайті МОЗ України розміщено роз’яснення щодо реалізації залишків лікарських засобів, у якому зазначається, що:
- лікарські засоби, закуплені операторами ринку фармацевтичної діяльності, у тому числі аптечними мережами, до 25 березня 2017 р., регулюються нормативно-правовими актами, чинними на момент закупівлі таких препаратів;
- лікарські засоби, включені до Національного переліку, закуплені операторами ринку фармацевтичної діяльності, у тому числі аптечними мережами, після 25 березня 2017 р., необхідно реалізовувати з дотриманням вимог державного регулювання цін шляхом встановлення на них граничних постачальницько-збутових та торговельних (роздрібних) надбавок згідно з постановою Кабінету Міністрів України від 17.10.2008 р. № 955 «Про заходи щодо стабілізації цін на лікарські засоби і вироби медичного призначення» (зі змінами). А саме: встановлення граничних постачальницько-збутових та роздрібних надбавок 10 та 25% відповідно на препарати, включені до Національного переліку, та 10 і 15% — на препарати, вартість яких підлягає відшкодуванню.
P.S. Зазначимо, що ідеологічно Базовий перелік основних лікарських засобів, рекомендованих ВООЗ, має рекомендаційну функцію і не застосовується для цілей цінового регулювання ліків. Натомість в Україні Національний перелік є регуляторним у контексті державного регулювання цін на лікарські засоби. Запровадження нових вимог цінового регулювання прийнято без надання операторам ринку перехідного періоду для адаптації своїх облікових систем до нових вимог цінового регулювання. Зважаючи на те, що оновлений Національний перелік сформований за МНН препаратів з урахуванням дозувань та кількості в упаковці, суб’єктам господарювання необхідний час для того, щоб визначити торгові назви препаратів, на які розповсюджується вимога щодо встановлення граничних постачальницько-збутових та роздрібних надбавок у розмірі 10 та 25% відповідно. Наше видання опублікувало перелік торгових назв лікарських засобів, що включені до Національного переліку. Також на нашому сайті наданий сервіс пошуку лікарських засобів, які включені до нового Національного переліку. Для того щоб отримати перелік торгових назв лікарських засобів, що включені до Національного переліку, в електронному вигляді з унікальними кодами/кодами Моріон, можна звертатися за тел.: (044) 585-97-12 або e-mail:

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим