НАЦІОНАЛЬНИЙ ПЕРЕЛІК ТА СТАТИСТИКА
Згідно з Положенням про Національний перелік, затвердженим наказом МОЗ від 11.02.2016 р. № 84 «Про затвердження Положення про Національний перелік основних лікарських засобів та Положення про експертний комітет з відбору та використання основних лікарських засобів», структура та зміст Національного переліку базуються на останньому виданні Базового переліку основних лікарських засобів, рекомендованих ВООЗ. При складанні Національного переліку збережено структуру Базового переліку ВООЗ — його поділено на розділи, до яких включено міжнародні непатентовані назви (МНН) лікарських засобів та лікарські форми. При цьому одна й та сама МНН може міститися у різних розділах.
Як і Базовий перелік ВООЗ, український Національний перелік не містить кодів АТС-класифікації та кодів Міжнародної класифікації хвороб (МКХ). Це суттєво ускладнює його використання для статистичних розрахунків.
Зауважимо, що розвинені країни та ВООЗ для статистичних розрахунків використовують статистичні класифікації, а саме АТС-класифікацію лікарських засобів та Міжнародну класифікацію хвороб (на сьогодні у світі використовується Міжнародна статистична класифікація хвороб та споріднених проблем охорони здоров’я, відома як МКХ-10). Для прикладу можна взяти позитивний перелік будь якої країни, де застосовується механізм реімбурсації, й побачити, що він являє собою перелік торгових назв лікарських засобів із зазначенням лікарської форми та коду АТС-класифікації.
ОБСЯГИ РЕГУЛЯЦІЇ
З ухваленням Національного переліку скасовано постанову КМУ від 5 вересня 1996 р. № 1071 «Про порядок закупівлі лікарських засобів закладами та установами охорони здоров’я, що фінансуються з бюджету», якою визначався перелік лікарських засобів, які заклади охорони здоров’я могли закуповувати за бюджеті кошти, а аптечні заклади — реалізовувати в межах безоплатного або пільгового забезпечення певних категорій населення відповідно до постанови КМУ № 1303.
Скасування постанови КМУ від 5 вересня 1996 р. № 1071 викликало резонанс у суспільстві, адже перелік лікарських засобів, включених до нового Національного переліку, значно менший у порівнянні з переліком, затвердженим постановою КМУ № 1071. Тому 23.08.2017 р. Уряд ухвалив рішення щодо відтермінування до 1 січня 2018 р. обов’язкового застосування Національного переліку під час державних закупівель та безоплатного або пільгового відпуску ліків відповідно до постанови КМУ № 1303. Таким чином, до 1 січня 2018 р. заклади охорони здоров’я можуть закуповувати, а аптечні заклади — відпускати безоплатно або на пільгових умовах лікарські засоби, які зареєстровані в Україні.
Нагадаємо, що постановою КМУ від 4 липня 2017 р. № 547 «Про внесення змін до постанови Кабінету Міністрів України від 25 березня 2009 р. № 333» до нового Національного переліку внесені зміни з метою включення МНН, які регулюються у рамках урядової програми «Доступні ліки».
Але, крім програми «Доступні ліки», в Україні реалізуються заходи щодо забезпечення лікування пацієнтів з окремими захворюванням, наприклад, цукровим діабетом. Для вимірювання рівня глюкози в крові пацієнти із цукровим діабетом потребують тест-смужок. Проте медичні вироби взагалі не включені до Національного переліку, хоча Базовий перелік ВООЗ, який був взятий за основу українськими експертами, все ж таки містить окремі медичні вироби.
У зв’язку із цим зауважимо наступне. Якщо держава реалізує програму боротьби з ВІЛ/СНІД, то наркозалежних необхідно забезпечувати одноразовими шприцами. Якщо у пріоритеті програма безпечної контрацепції — то громадянам необхідно забезпечити доступ до засобів контрацепції. Тобто не лише лікарські засоби, а й медичні вироби мають соціальне значення.
Розглянемо власне регуляторний вплив Національного переліку та порівняємо його з постановою КМУ № 1071.
За підсумками 2016 р., на українському фармринку в роздрібному та госпітальному сегментах реалізовувалося більше 1 тис. МНН, фіксованих комбінацій та загальноприйнятих назв лікарських засобів з переліку, затвердженого постановою КМУ № 1071. Натомість кількість МНН, включених до Національного переліку, становить близько 250. Значно менші й обсяги споживання препаратів, включених до Національного переліку, у порівнянні з переліком, затвердженим постановою КМУ № 1071.
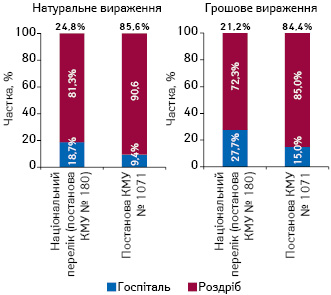
За підсумками 2016 р., частка лікарських засобів, включених до Національного переліку, у загальному обсязі ринку лікарських засобів становила 21,2% ринку лікарських засобів в грошовому і 24,8% — в натуральному вираженні. При цьому левова частка цих препаратів постачається через аптечну мережу, тобто в амбулаторному сегменті. Обсяг госпітальних закупівель становив 3,4 млрд грн. за 52,9 млн упаковок. Для порівняння постанова КМУ № 1071, за підсумками 2016 р., охопила 84,4% в грошовому та 85,6% в натуральному вираженні від загального обсягу ринку лікарських засобів у аптечному та госпітальному споживанні (рис. 1).
ДЕРЖАВНІ ЗАКУПІВЛІ
Постанова КМУ № 1071 майже повністю охоплює госпітальний сегмент. За підсумками 2016 р., частка лікарських засобів, включених до постанови КМУ № 1071, у загальному обсязі госпітального сегменту становила 96,8% в натуральному та 92,1% — у грошовому вираженні.
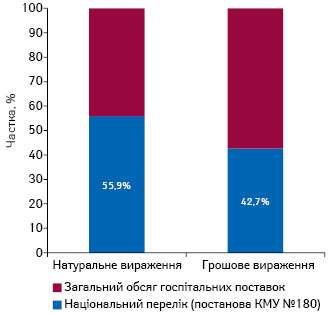
Натомість новий Національний перелік охоплює суттєво меншу частку госпітального споживання. За підсумками 2016 р., обсяг державних закупівель препаратів, включених до Національного переліку, становив 52,9 млн упаковок та 3,4 млрд грн., що становить 55,9% в натуральному та 42,7% в грошовому вираженні від загального обсягу державних закупівель (рис. 2).
Близько 760 МНН, фіксованих комбінацій, та загальноприйнятих назв лікарських засобів, які закуповувалися в 2016 р. відповідно до переліку, затвердженого постановою КМУ № 1071, не включені до Національного переліку. 85 з цих МНН покриваються за рахунок закупівель через міжнародні організації. Таким чином, близько 675 МНН заклади охорони здоров’я зможуть закуповувати лише за умови задоволення у повному обсязі потреби в лікарських засобах, що входять до Національного переліку.
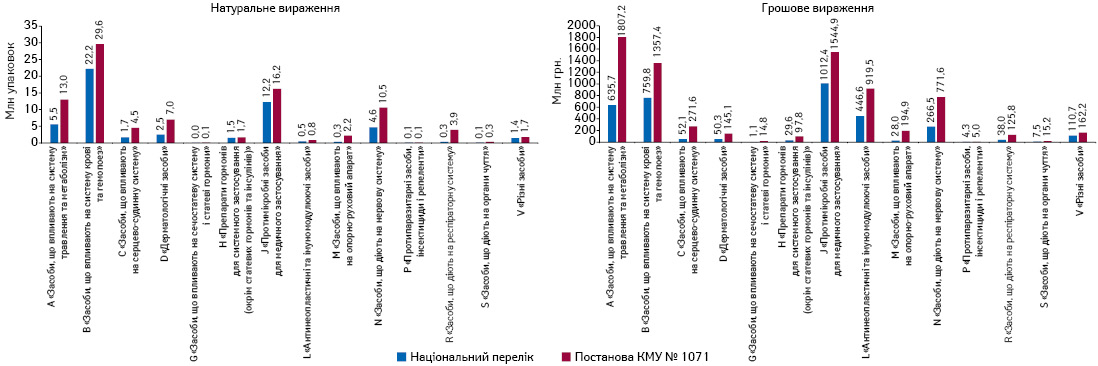
Дані щодо обсягів госпітальних поставок лікарських засобів, включених до Національного переліку, у порівнянні з постановою КМУ № 1071 представлені на рис. 3. За всіма групами АТС-класифікації обсяги госпітального споживання препаратів, включених до Національного переліку, менші порівняно з такими відповідно до постанови КМУ № 1071.
Щодо проблем, які можуть виникнути у лікувально-профілактичних закладах з 1 січня 2018 р., зазначимо наступне. Оскільки Національний перелік не містить кодів МКХ-10 та АТС-класифікації, лікарям буде незрозуміло, на терапію яких нозологій поширюється державне фінансування. А відтак постане питання ефективності використання бюджетних коштів.
БЕЗОПЛАТНИЙ ТА ПІЛЬГОВИЙ ВІДПУСК ЛІКАРСЬКИХ ЗАСОБІВ
Окрім закупівель за бюджетні кошти, перелік препаратів, включених до Національного переліку, також використовуватиметься для безоплатного або пільгового відпуску ліків відповідно до постанови КМУ № 1303, а також урядової програми «Доступні ліки».
Щодо постанови КМУ № 1303, то у цьому документі зазначені категорії населення та перелік нозологій, на які розповсюджується дія постанови. При цьому перелік нозологій не відповідає МКХ-10 та розділам Національного переліку.
Раніше відпуск таких препаратів здійснювався в рамках переліку, затвердженого постановою КМУ № 1071. При цьому лікар виписував рецепт на відповідний лікарський засіб, а при зверненні пацієнта з рецептом в аптеку провізор перевіряв, чи включений цей препарат у перелік лікарських засобів, які підлягають безоплатному або пільговому відпуску. Провізор міг легко здійснити таку перевірку, оскільки перелік, затверджений постановою КМУ № 1071, містив коди АТС-класифікації.
У разі якщо аптечні заклади не отримають чіткого списку торгових назв лікарських засобів, які підпадають під дію Національного переліку, з 1 січня 2018 р. виникне проблема — працівник аптеки повинен буде самостійно визначити, чи розповсюджуються на препарат, виписаний лікарем у рецепті, пільгові умови відпуску.
Натомість з урядовою програмою «Доступні ліки» таких проблем не виникатиме, тому що наказом МОЗ України затверджено перелік торгових назв лікарських засобів, які включені до програми реімбурсації, їх гранична оптово-відпускна й роздрібна ціна та рівень відшкодування. Тобто це по суті «позитивний перелік».
ПОЗИТИВНИЙ ПЕРЕЛІК ТА РЕГУЛЮВАННЯ ЦІН
У розвинених країнах для цілей державного регулювання застосовуються «позитивні переліки». «Позитивний перелік» — це перелік препаратів, вартість яких підлягає відшкодуванню з боку держави або які можуть закуповуватися за бюджетні кошти.
Кожна країна висуває чіткі критерії щодо включення лікарського засобу до «Позитивного переліку». Наприклад, якщо мова йде про генерики, то для включення у «Позитивний перелік» заявник повинен надати відомості щодо результатів порівняльних досліджень біоеквівалентності цього генерика референтному/оригінальному препарату.
Крім того, заявник обов’язково повинен надати дані щодо вартості лікарського засобу.
На сьогодні в Україні заявники, які мають бажання постачати лікарські засоби за бюджетні кошти, проходять процедуру декларування оптово-відпускних цін відповідно до постанови КМУ від 2 липня 2014 р. № 240. Дія цієї постанови поширюється на лікарські засоби які закуповуються та/або вартість яких відшкодовується за бюджетні кошти. Участь у програмі відшкодування та бюджетних закупівлях здійснюється на добровільних засадах. Принцип добровільності необхідно застосовувати й у контексті Національного переліку.
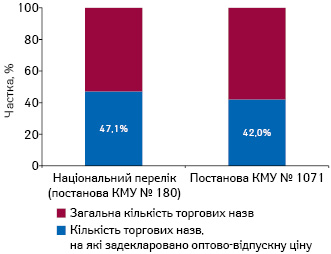
Зауважимо, що на сьогодні в Україні зареєстровано 4953 торгових назви препаратів, які включені до Національного переліку. Оптово-відпускна ціна, відповідно до постанови КМУ № 240, задекларована на 2333 препарати, що становить 47% від загальної кількості (рис. 4). Для порівняння — перелік лікарських засобів, затверджений постановою КМУ № 1071, налічує 19 778 торгових назв, з яких на 8306 торгових назв задекларовано оптово-відпускну ціну, а їх частка становить 42%. Але, як ми зауважили раніше, постанова КМУ № 1071 містила суттєво більшу кількість торгових назв лікарських засобів порівняно з Національним переліком.
ВИЗНАЧЕННЯ ПОТРЕБИ У ФІНАНСУВАННІ
На сьогодні Порядок визначення обсягів потреби в закупівлі лікарських засобів закладами й установами охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів, затверджено наказом МОЗ України від 11.07.2017 р. № 782 «Про затвердження Порядку визначення обсягів потреби в закупівлі лікарських засобів закладами й установами охорони здоров’я, що повністю або частково фінансуються з державного та місцевих бюджетів». Цей порядок передбачає два методи кількісної оцінки потреби в лікарських засобах, зокрема метод, що базується на показниках захворюваності, та метод, що базується на показниках споживання. Потреба в лікарських засобах може визначатися за допомогою одного або комбінації двох методів кількісної оцінки.
Оцінити обсяги фінансування за показниками захворюваності неможливо, оскільки на сьогодні в Україні відсутні реєстри пацієнтів.
Наразі ми можемо оцінити обсяги фінансування, необхідного для задоволення потреби в лікарських засобах, включених до Національного переліку, на основі даних щодо їх споживання.
Як вже повідомлялося, у 2016 р. загальний обсяг споживання лікарських засобів, включених до Національного переліку, у роздрібному та госпітальному сегментах становить 12,4 млрд грн. Зростання споживання в середньому становить +20% на рік. Таким чином, якщо держава планує забезпечити на 100% потребу системи охорони здоров’я в лікарських засобах, включених до Національного переліку, загальний обсяг фінансування на 2017 р. може становити 14,9 млрд грн. А на 2018 р. — 17,9 млрд грн. Також необхідно врахувати рівень можливих втрат, який відповідно до методики може становити до 3% на рік. Тобто додаємо ці 3% до загального обсягу фінансування та отримуємо необхідний рівень фінансування на 2018 р. — 18,4 млрд грн.
У разі ж якщо держава планує забезпечити фінансування лише госпітального сегменту, то обсяги фінансування будуть дещо меншими. За підсумками 2016 р., обсяги споживання лікарських засобів, включених до Національного переліку, в госпітальному сегменті становлять 3,4 млрд грн. Враховуючи середній приріст споживання на рівні +20%, отримуємо необхідний обсяг фінансування на 2017 р. на рівні 4,1 млрд грн., а на 2018 р. — 5 млрд грн. З урахуванням рівня можливих втрат в 3% необхідний обсяг фінансування на 2018 р. становитиме 5,1 млрд грн.
Однак під час розрахунку обсягів фінансування слід мати на увазі, що, за підсумками 2016 р., препарати, включені до Національного переліку, забезпечували потребу госпітального сегменту лише на 40%. Крім того, професійна спільнота вважає за доцільне необхідність його розширення. Тому слід передбачити додаткове фінансування для забезпечення потреби в препаратах, які не включені до Національного переліку, в розмірі близько 7,7 млрд грн.
ВИСНОВКИ
На сьогодні у сегменті державних закупівель лікарських засобів використовуються два різних переліки — Національний перелік та номенклатура для закупівель через міжнародні організації. Для уникнення подвійних стандартів Уряд має затвердити єдиний перелік лікарських засобів, які закуповуватимуться за державні кошти.
Це має бути перелік, складений за торговими назвами, із зазначенням вартості лікарського засобу, яка має застосовуватися як під час бюджетних закупівель, так і при амбулаторному споживанні лікарських засобів, вартість яких відшкодовується з боку держави. Регульований перелік повинен базуватися на статистичних класифікаціях — АТС-класифікації та МКХ-10. Крім того, державне регулювання має розповсюджуватися й на медичні вироби з урахуванням пріоритетних станів та хвороб.
Для включення до переліку лікарських засобів, які закуповуватимуться або відшкодовуватимуться за бюджетні кошти, МОЗ України має визначити чіткі критерії, наприклад — дослідження біоеквівалентності для генериків. Головний принцип, який повинно врахувати профільне міністерство, — це добровільна участь заявників. Також важливо не припуститися помилки та уникнути запровадження прямого цінового регулювання на всі лікарські засоби, що підпадають під дію Національного переліку.

Коментарі