Вакцини до пандемії коронавірусу
 Вакцинація стимулює формування імунної відповіді на певний патоген, що дає організму перевагу в боротьбі з хворобою в разі можливого зараження в майбутньому. Вакцини на основі ослаблених або інактивованих цільних вірусів існують вже давно (прикладами є вакцини проти поліомієліту, кору та жовтої лихоманки).
Вакцинація стимулює формування імунної відповіді на певний патоген, що дає організму перевагу в боротьбі з хворобою в разі можливого зараження в майбутньому. Вакцини на основі ослаблених або інактивованих цільних вірусів існують вже давно (прикладами є вакцини проти поліомієліту, кору та жовтої лихоманки).
Завдяки прогресу в молекулярній біології в останні десятиліття розроблено вакцини на основі окремих вірусних компонентів, а не цілих вірусів. Частини вірусного генетичного коду, які зазвичай кодують білки, що знаходяться на поверхні вірусу, використовуються для створення білків, які стимулюють утворення антитіл, що блокують вірус. Прикладами є вакцини проти вірусу гепатиту В і вірусу папіломи людини. Крім того, частини вірусного генетичного коду можна перенести на нешкідливий вірус-носій, «вектор». При введенні векторної вакцини в клітинах виробляється антиген, який стимулює імунну відповідь проти цільового вірусу.
Виробництво вакцин, в основі яких лежать цільні інактивовані віруси, та вакцин, створених на основі вірусних векторів, вимагає використання великомасштабних клітинних культур. Цей ресурсоємний процес може обмежувати можливості швидкого виробництва вакцин у відповідь на спалахи та пандемії. Тому дослідники вже давно намагаються розробити технології виробництва вакцин, які не залежать від клітинних культур, але це виявилося складним завданням.
Вакцини на основі мРНК
У 1980-х роках з’явилися методи отримання мРНК без використання клітинних культур (безклітинні системи), які отримали назву «транскрипція in vitro». Це прискорило розвиток застосування молекулярної біології в кількох галузях. Зокрема, набули розвитку ідеї щодо використання мРНК-технологій для створення вакцин і терапевтичних цілей, але попереду були перешкоди. Транскрибована in vitro мРНК вважалася нестабільною і складною для доставки, що потребувало розробки складних ліпідних систем-носіїв для інкапсуляції мРНК. Крім того, мРНК, отримана in vitro, спричиняла запальні реакції. Тому ентузіазм щодо розробки технології мРНК для клінічних цілей спочатку був обмеженим.
Відкриття лауреатів
К. Каріко та Д. Вайсман, які працювали разом в Університеті Пенсільванії, займалися розробкою методів використання мРНК у терапевтичних цілях. Їх дослідження зосередилося на тому, як різні типи РНК взаємодіють з імунною системою.
Вчені помітили, що дендритні клітини розпізнають транскрибовану in vitro мРНК як чужорідну речовину, що призводить до їх активації та вивільнення сигнальних молекул запалення. Постало питання, чому транскрибована in vitro мРНК розпізнається як чужорідна, в той час як мРНК з клітин ссавців не викликає такої ж реакції. Зрештою вони зрозуміли, що різні типи мРНК можуть мати певні критичні властивості, які відрізняють їх одну від одної.
Будова РНК містить 4 азотисті основи: аденін (A), цитозин (C), гуанін (G) і урацил (U). Вчені знали, що основи в РНК з клітин ссавців часто піддаються хімічним модифікаціям, тоді як у мРНК, транскрибованій in vitro, таких змін не відбувається. Їм стало цікаво, чи може відсутність модифікації основ у транскрибованій in vitro РНК пояснити небажану запальну реакцію. Щоб дослідити це, вони створили різні варіанти мРНК, кожен з яких мав унікальні хімічні зміни в основах. Вони виявили, що запальна реакція майже зникла, коли в мРНК були включені модифікації основ. Результати подальших досліджень, опублікованих у 2008 і 2010 р., показали, що модифікована мРНК підвищує експресію білка порівняно з немодифікованою мРНК. Це зумовлено зниженням активації ферменту, який регулює вироблення білка.
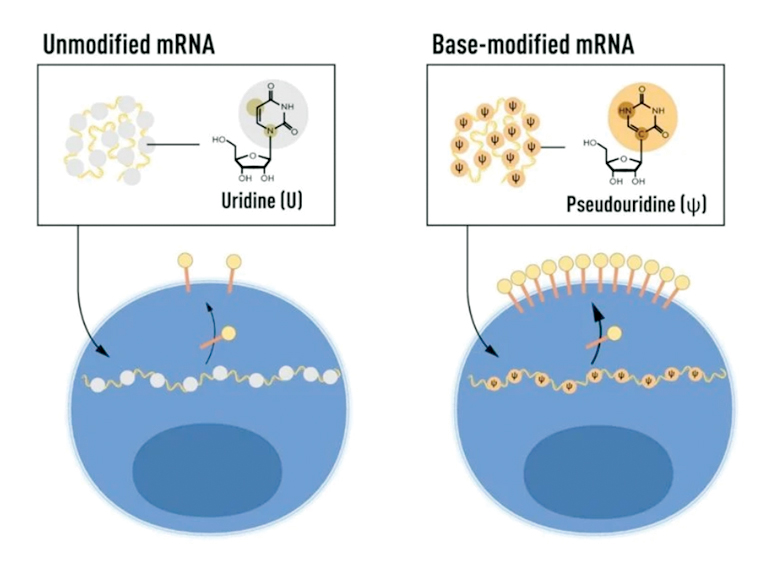
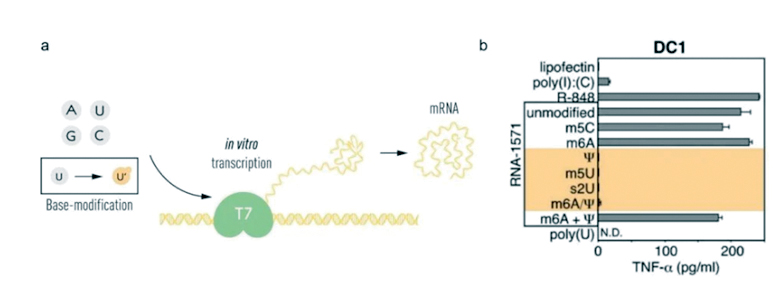
Інтерес до технології мРНК почав зростати, і в 2010 р. вже декілька компаній працювали над розробкою цього методу.
Так, біофармацевтична компанія CureVac (Німеччина), заснована у 2000 р., спеціалізується на розробці вакцин проти інфекційних захворювань, ліків проти раку і орфанних захворювань; біотехнологічна компанія BioNTech (Німеччина), заснована у 2008 р., розробляє препарати на основі матричної РНК для індивідуалізованої терапії онкопатології; біотехноогічна компанія Moderna (США), заснована у 2010 р., використовує платформу мРНК для перепрограмування соматичних клітин у плюрипотентний стан та доставки терапевтичних білків, наприклад, для відновлення пошкоджених тканин.
Після спалаху пандемії COVID-19 дві вакцини для профілактики коронавірусної інфекції на основі мРНК були розроблені та схвалені з рекордною швидкістю — завдяки попереднім відкриттям, безпрецедентному рівню співпраці, фінансуванню з боку індустрії та матеріально-технічній підтримці урядів. І Pfizer/BioNTech, і Moderna використовували технологію К. Каріко та Д. Вайссмана для створення своїх вакцин.
У сучасному глобально взаємопов’язаному суспільстві ризик виникнення нових пандемій є вищим, ніж будь-коли раніше. Пандемії зазвичай спричиняються зоонозними вірусами, які перетинають видовий бар’єр, потрапляють до людини та поширюються повітряно-крапельним або аерозольним шляхом, викликаючи інфекції дихальних шляхів. Розробка та впровадження вакцин достатньо швидко, щоб пом’якшити пандемію у розпалі, є величезним викликом, з яким під час пандемії COVID-19 стикнулися вперше.
У майбутньому технологія РНК також може бути використана у сфері лікування деяких видів онкологічних захворювань.
На сьогодні дослідники виявили понад 100 різних посттранскрипційних модифікацій РНК і показали, що модифікації більш поширені в РНК еукаріотів, ніж прокаріотів.
Клітини модифікують РНК за допомогою ферментативних реакцій, наприклад, псевдоуридин каталізується ферментами псевдоуридинсинтетазами або за допомогою малих рибонуклеопротеїнових комплексів (snoRNPs). Модифікації РНК впливають на її стабільність, специфічність сполучення основ, згортання та інші функціональні властивості. Для більшості з понад 100 відомих модифікацій РНК існує обмежена кількість функціональних даних. Тому розуміння фізіологічних наслідків цих модифікацій залишається актуальним напрямком досліджень.
Про лауреатів
 Каталін Каріко народилася в 1955 р. в місті Сольнок, Угорщина. Отримала ступінь доктора філософії в Сегедському університеті, Угорщина. У 1989 р. стала доцентом кафедри нейрохірургії Школи медицини Парельмана Університету Пенсільванії (США), де працювала до 2013 р. Після цього стала віцепрезидентом, а згодом старшим віцепрезидентом компанії BioNTech RNA Pharmaceuticals. З 2021 р. є професором Сегедського університету та ад’юнкт-професором Школи медицини Перельмана при Університеті Пенсільванії.
Каталін Каріко народилася в 1955 р. в місті Сольнок, Угорщина. Отримала ступінь доктора філософії в Сегедському університеті, Угорщина. У 1989 р. стала доцентом кафедри нейрохірургії Школи медицини Парельмана Університету Пенсільванії (США), де працювала до 2013 р. Після цього стала віцепрезидентом, а згодом старшим віцепрезидентом компанії BioNTech RNA Pharmaceuticals. З 2021 р. є професором Сегедського університету та ад’юнкт-професором Школи медицини Перельмана при Університеті Пенсільванії.
Дрю Вайссман народився 1959 р. в Лексингтоні, штат Массачусетс, США. Здобув ступінь доктора медицини та доктора філософії в Бостонському університеті. У 1997 р. заснував свою дослідницьку групу в Школі медицини Перельмана при Університеті Пенсільванії. Є директором Інституту РНК-інновацій.
«Ви повинні навчитися справлятися з невдачами. Адже найчастіше експерименти не показують той результат, на який ви сподівалися. Але на невдачах можна вчитися», — зазначила К. Каріко під час урочистої пресконференції в Університеті Пенсільванії. Наука не обов’язково дає негайні результати чи похвалу. Вчені продовжували працювати, незважаючи на те, що не отримували фінансування і не змогли переконати інших у тому, що мРНК є цікавою і життєздатною. Довгий час їх відкриття залишалося недооціненим. Вчена стала 13-ю жінкою, яка отримала Нобелівську премію з фізіології та медицини.
«Якщо вам подобається бути в центрі уваги, тоді вам варто стати актором чи актрисою. Якщо вам подобається слідувати інструкціям, можливо, військова справа — це ваше. Якщо ви хочете бути багатим, я не знаю відповіді на це запитання. Але якщо вам подобається вирішувати проблеми, то наука — для вас», — сказала вона.
Відповідаючи на запитання, чому молодь повинна йти в науку, Д. Вайссман зазначив, що молодих людей, які хочуть іти в цю сферу, не вистачає, що багато хто хоче піти в ІТ, розбагатіти і піти на пенсію.
«Для того щоб наше суспільство розвивалося, нам потрібна наука. Все, що рухало наше суспільство вперед протягом останніх тисяч років, базувалося на науці: винахід круглого колеса, транспортних засобів, антибіотиків тощо, — зазначив нобелівський лауреат. — Ми повинні заохочувати наших дітей, наших онуків, усіх, що наука — це те, що рухає світ уперед».
Інші переможці
Нобелівську премію з хімії 2023 р. присуджено трьом вченим — Мунгі Бавенді (Массачусетський технологічний університет, США), Луїсу Брусу (Колумбійський університет, США), Олексію Єкімову (Nanocrystals Technology Inc., США) — за відкриття та розробку квантових точок — наночастинок, які настільки малі, що їх розмір визначає їхні властивості. Хімічні властивості елемента залежать від числа електронів. Однак коли речовина стискається до нанорозмірів, виникають квантові явища, які залежать від розміру речовини.
Нобелівським лауреатам з хімії 2023 р. вдалося створити частинки настільки малі, що їх властивості визначаються квантовими явищами. Частинки, які називають квантовими точками, зараз мають велике значення в нанотехнологіях. Ці найдрібніші компоненти нанотехнологій, серед іншого, поширюють своє світло від телевізорів та світлодіодних ламп, а також можуть направляти хірургів, коли вони видаляють пухлинні тканини. Премія з хімії присуджується Шведською королівською академією наук у Стокгольмі, Швеція.
Лауреами премії у галузі фізики стали науковці П’єр Агостіні (Університет штату Огайо, США), Ференц Крауш (Інститут квантової оптики Макса Планка, Німеччина) і Анн Л’Ульє (Лундський університет, Швеція) за експериментальні методи генерації аттосекундних імпульсів світла для вивчення динаміки електронів у речовині. У світі електронів зміни відбуваються за кілька десятих аттосекунди. Аттосекунда (дорівнює 1·10¹⁸ секунди) настільки коротка, що за одну секунду їх відбувається стільки, скільки було секунд з моменту народження Всесвіту.
Експерименти вчених дали нові інструменти для дослідження світу електронів всередині атомів і молекул. Вони продемонстрували спосіб створення надзвичайно коротких імпульсів світла, які можна використовувати для вимірювання швидких процесів, у яких електрони рухаються або змінюють енергію.
за матеріалами http://www.nobelprize.org, penntoday.upenn.edu
Ілюстрації: The Nobel Committee for Physiology or Medicine. Ill. Mattias Karlén

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим