ВОЗ опубликовала новое руководство по лечению пациентов с туберкулезом
Накануне Всемирного дня борьбы с туберкулезом Всемирная организация здравоохранения (ВОЗ) опубликовала новое сводное руководство по лечению и уходу за пациентами с лекарственно-устойчивым туберкулезом, основанное на новейших данных. Сводное руководство включает рекомендации по схемам лечения туберкулеза со множественной лекарственной устойчивостью, а также рекомендации относительно мониторинга пациентов, моделей поддержки и контроля за пациентом и многое другое. Так, ВОЗ рекомендует перейти на полностью пероральный режим лечения. Такой курс […]
Pfizer покупает долю у Vivet, французского разработчика в области генной терапии
Pfizer Inc (США) объявила о приобретении 15% акций Vivet Therapeutics (Франция) с исключительным правом на приобретение всей компании в дальнейшем. Pfizer уже перечислил 51 млн дол. США, а в случае использования права на покупку компании может выплатить до 636 млн дол. По условиям соглашения Pfizer может воспользоваться этим правом в случае получения определенных показателей в ходе ранних стадий клинических исследований экспериментального препарата для […]
Zentiva приобретает румынскую фармкомпанию Solacium
Zentiva Group (Чехия) собирается приобрести румынскую фармацевтическую компанию Solacium. В настоящее время Solacium входит в состав Dr. Max Group и принадлежит Siyiara Enterprises. 13 марта 2019 г. Zentiva сообщила о подписании соглашения с Siyiara Enterprises о приобретении Solacium, включая дочернюю компанию Be Well Pharma. «Это приобретение позволит дополнить наш существующий бизнес по производству генериков, увеличить потенциал ОТС-подразделения, а также расширить […]
Объем мировых продаж кардиостимуляторов к 2028 г. может достичь 4,1 млрд дол. США
Аналитическая компания «GlobalData» прогнозирует увеличение объема мирового рынка кардиостимуляторов в среднем на 2% ежегодно. К 2028 г. объем продаж этой категории товаров может достичь 4,1 млрд дол. США. Как считают аналитики «GlobalData», росту рынка в значительной степени способствует увеличение распространенности такого состояния, как дисфункция синусового узла в популяции стареющего населения. Шерил Танг (Sheryl Tang), аналитик «GlobalData», отмечает, что именно […]
Реклама фармбрендов в различных медиа по итогам 2018 г. Helicopter view
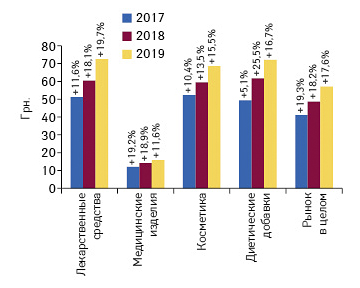
Медианосители многогранны и способны предложить различные способы контакта с целевой аудиторией. В данной публикации вниманию читателей представлены основные тенденции рынка рекламы фармацевтических товаров в различных медиа — на телевидении, в неспециализированной прессе, на радио и в интернете
Промоция лекарственных средств по итогам 2018 г. Helicopter View
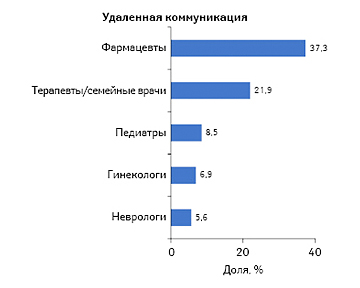
Сегодня доступен целый арсенал инструментов для коммуникации с различными целевыми аудиториями. Какие тенденции преобладают в сфере промоционной активности фармкомпаний, направленной на профессиональную аудиторию, и какие виды промоции развиваются наиболее активно, читатели смогут узнать из данной публикации.
Управление изменениями в эпоху цифровых технологий: новые вызовы в маркетинге
Тенденции в мультиканальном маркетинге, новые вызовы и тренды в коммуникации с конечным потребителем — об этом и не только речь шла во время третьей сессии 14-го Ежегодного аналитического форума «Фармавзгляд–2019», который состоялся 14–15 февраля в столичном «Mercure Kyiv Congress Centre»
Пішов з життя видатний український вчений Олександр Тихонов
11 вересня 1938 р. — 25 лютого 2019 р. Пішов із життя Олександр Іванович Тихонов – видатний учений, лауреат Державної премії України в галузі науки і техніки, заслужений діяч науки і техніки України, заслужений винахідник СРСР, академік Української академії наук (УАН), доктор фармацевтичних наук, заслужений професор Національного фармацевтичного університету (НФаУ). За 55 років науково-педагогічної роботи О.І. Тихонов створив науково-педагогічну школу та […]
Бриф-анализ фармрынка: итоги января 2019 г.
В данной публикации вниманию читателей представлены ключевые показатели фармацевтического рынка Украины (территории, подконтрольной украинскому Правительству) в январе 2019 г.
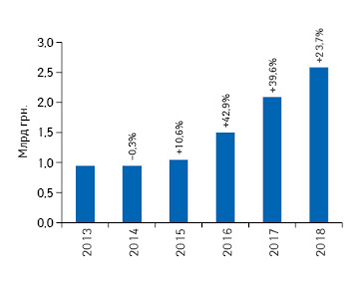
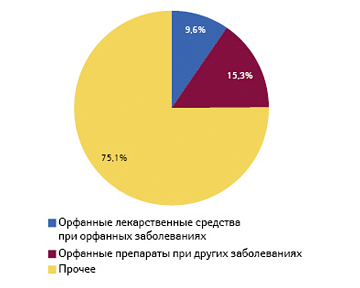
Мировой рынок орфанных препаратов: активная фаза роста
Сейчас благодаря развитию технологий, индивидуализированной медицины (Precision Medicine), а также достижениям в науке и медицине, на рынке появляется все больше лекарственных средств, предназначенных для лечения редких (орфанных) заболеваний