 Конференцию открыл Валентин Черных, ректор Национального фармацевтического университета (НФаУ), член-корреспондент НАН Украины, доктор химических наук, доктор фармацевтических наук, профессор, заслуженный деятель науки и техники Украины, лауреат Государственной премии Украины, заведующий кафедрой органической химии. Он отметил, что путь, по которому сегодня идет Украина, а именно ориентация на генерические, а не брэндовые лекарственные средства, в значительной степени оправдан. Однако отечественная фармация требует и развития. По мнению ректора НФаУ, будущее науки — за биотехнологиями, которым в нашей стране пока уделяется недостаточно внимания.
Конференцию открыл Валентин Черных, ректор Национального фармацевтического университета (НФаУ), член-корреспондент НАН Украины, доктор химических наук, доктор фармацевтических наук, профессор, заслуженный деятель науки и техники Украины, лауреат Государственной премии Украины, заведующий кафедрой органической химии. Он отметил, что путь, по которому сегодня идет Украина, а именно ориентация на генерические, а не брэндовые лекарственные средства, в значительной степени оправдан. Однако отечественная фармация требует и развития. По мнению ректора НФаУ, будущее науки — за биотехнологиями, которым в нашей стране пока уделяется недостаточно внимания.
Открытым остается и вопрос экстемпоральной рецептуры. В. Черных обратил внимание на то, что увеличить спрос населения на изготовленные в аптечных условиях лекарственные средства достаточно сложно, поэтому государству следует направить усилия на межбольничные аптеки. Но для реализации такой системы следует разработать нормативно-правовую базу, обеспечить аптечные учреждения необходимой аппаратурой, средствами малой механизации.
В завершение приветственной речи ректор заметил, что украинская система здравоохранения вслед за западными странами будет делать упор на профилактику и индивидуальный подход в лечении. В фармации акцент сместится в сторону повышения эффективности препаратов. В частности, на технологические приемы адресации лекарственного средства больному органу.
 Далее выступил Александр Дудка, научный консультант главы Харьковской облгосадминистрации, директор КП «Индустриальный парк «Рогань» (Харьков). В своем докладе он рассказал о практических шагах, способных повысить конкурентоспособность региона, на примере формирования харьковского биофармацевтического кластера.
Далее выступил Александр Дудка, научный консультант главы Харьковской облгосадминистрации, директор КП «Индустриальный парк «Рогань» (Харьков). В своем докладе он рассказал о практических шагах, способных повысить конкурентоспособность региона, на примере формирования харьковского биофармацевтического кластера.
Докладчик пояснил, что согласно теории Майкла Портера, профессора Гарвардского университета, кластер (англ. cluster — скопление) — это группа географически соседствующих взаимосвязанных компаний (производителей, поставщиков) и имеющих к ним отношение организаций (образовательных учреждений, органов власти и др.), действующих в определенной сфере и взаимодополняющих друг друга.
Первопричина географической концентрации компаний — в конкуренции. Актуальность кластеров объясняется тем, что в глобализованной экономике существенные преимущества чаще всего определяются местными условиями: знаниями, системой отношений и мотивацией. Кластеры эффективно способствуют повышению конкурентоспособности благодаря эффекту синергии, когда значимость целого превышает сумму составных частей.
По словам А. Дудки, популярность кластерной теории объясняется тем, что именно она отражает реальное состояние экономики. По модели кластерного развития сейчас идут Япония, где активно развивается проект «Фармацевтическая долина Фудзи», Финляндия, Венгрия и другие страны.
А. Дудка отметил, что биофармацевтический кластер включает:
- фармацевтические заводы;
- поставщиков сырья и вспомогательных веществ;
- дистрибьюторов лекарственных средств;
- производителей тары и упаковки;
- специализированные СМИ, информационно-маркетинговые компании;
- управления областной государственной администрации;
- вузы, готовящие специалистов в сфере биологии и фармации;
- центры трансфера технологий, бизнес-инкубаторы, патентных поверенных;
- центры сертификации и валидации;
- лаборатории токсикологических и биофармацевтических исследований
- научные лаборатории вузов, инновационные фирмы.
Докладчик напомнил: для того чтобы успешно конкурировать на рынке, фармацевтический производитель должен создавать новые лекарственные формы, привлекая дополнительные инвестиции. Именно с целью упрощения пути новых идей к рынку открываются центры инновационных технологий, научные и технологические парки.

А. Дудка сообщил о том, что на данный момент в Украине готовится ряд законодательных актов, в которых будет введено понятие «кластер», и это поднимет направление на новый уровень.
В ожидании утверждения нормативно-правовой основы руководство Харьковской области уже выделило главный вектор своей активности — инфраструктуру трансфера технологий, которая позволит коммерциализировать разработки отечественных ученых. Планируется создание IT-парка, технополиса «Пятихатки», украинско-российского парка «Слобожанщина». По словам докладчика, биофармация занимает одно из ведущих мест среди направлений, которые будут реализованы в рамках всех перечисленных проектов.
В планах у авторов биофармацевтического кластера — создание инновационного центра, направленного на привлечение зарубежных партнеров, а также строительство завода по производству субстанций, которые поставлялись бы на отечественный рынок и позволяли минимизировать затраты на закупку сырья для отечественных производителей фармацевтической продукции.
А. Дудка выразил уверенность в том, что формирование харьковского биофармацевтического кластера станет мощным элементом взращивания инновационных бизнесов и привлечения инвестиций.
 Доклад «Актуальность методических рекомендаций по организации валидационной деятельности на отечественных фармацевтических предприятиях» представила Наталья Тахтаулова, начальник Управления лицензирования и сертификации производства Государственной службы Украины по лекарственным средствам (далее — Гослекслужба Украины).
Доклад «Актуальность методических рекомендаций по организации валидационной деятельности на отечественных фармацевтических предприятиях» представила Наталья Тахтаулова, начальник Управления лицензирования и сертификации производства Государственной службы Украины по лекарственным средствам (далее — Гослекслужба Украины).
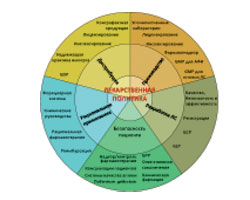
Н. Тахтаулова отметила, что контроль качества лекарственных средств играет важную роль в многоуровневой системе лекарственной политики государства (рисунок).
Докладчица проинформировала участников конференции о результатах работы Гослекслужбы Украины относительно производителей фармацевтической продукции. Так, за 9 мес 2011 г. не допущено на рынок 70 серий некачественных лекарственных средств зарубежного производства. Выдано 299 предписаний о запрете оборота, в частности 96 серий 102 наименований некачественных препаратов, 19 серий 9 наименований фальсифицированных и 196 наименований незарегистрированных лекарственных средств.
Как подчеркнула докладчик, проектом приказа МЗ Украины «Об утверждении Лицензионных условий осуществления хозяйственной деятельности по производству, оптовой и розничной торговле лекарственными средствами» планируется внести изменения в квалификационные требования к уполномоченному лицу и к лабораториям лицензиатов.
Н. Тахтаулова также продемонстрировала распределение производства лекарственных средств в нашей стране по состоянию на 1 ноября 2011 г. (таблица).
| Таблица | Распределение производства лекарственных средств в Украине |
| Производители лекарственных средств | Количество |
|---|---|
| Нестерильные лекарственные средства | 82 |
| Стерильные лекарственные средства, в том числе асептика | 30 |
| Лекарственные средства растительного происхождения, гомеопатические средства | 35 |
| Радиофармацевтические препараты | 0 |
| Биологические (иммунобиологические)средства, препараты, полученные из донорской крови и плазмы | 6 |
| Медицинские газы | 20 |
| Активные фармацевтические ингредиенты | 28 |
Отдельно начальник Управления лицензирования и сертификации производства остановилась на замечаниях, которые зачастую возникают у регуляторных органов при проверке производства лекарственных средств. Так, предприятия предоставляют недостаточную документацию по системе качества. Нередко в таких документах выявляют исправления, сделанные не в соответствии с требованиями Надлежащей практики (используется карандаш, внесена информация, которая может быть стерта, отсутствуют подписи сделавшего исправления, дата внесения правки).
Грубым нарушением считается проведение не в полном объеме квалификации помещений, которые квалифицируются по классам чистоты.
Существуют проблемы и с архивными образцами: часто предприятия отбирают их в количестве, недостаточном для проведения двух полных анализов по всем показателям качества.
Подводя итоги инспектирования фармацевтических производств, докладчица отметила, что наибольшую обеспокоенность регуляторного органа вызывает ситуация с организацией деятельности по валидации. У многих производителей нет понимания сути данного процесса и необходимости проведения валидационных работ. По мнению Н. Тахтауловой, это серьезная проблема, которая требует решения.
 Тему валидации в своем выступлении продолжил Роман Гуржий, менеджер по обеспечению качества и организации процесса валидации корпорации «Артериум» (Киев). Р. Гуржий напомнил, что согласно определению Управления по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration) валидация — сбор и анализ данных, которые начинаются на стадии разработки процесса и продолжаются на стадии промышленного производства для получения научно обоснованного доказательства того, что процесс способен стабильно производить качественную продукцию.
Тему валидации в своем выступлении продолжил Роман Гуржий, менеджер по обеспечению качества и организации процесса валидации корпорации «Артериум» (Киев). Р. Гуржий напомнил, что согласно определению Управления по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration) валидация — сбор и анализ данных, которые начинаются на стадии разработки процесса и продолжаются на стадии промышленного производства для получения научно обоснованного доказательства того, что процесс способен стабильно производить качественную продукцию.
Практическая роль валидации в жизненном цикле лекарственного средства включает три стадии:
- Разработка процесса (фармацевтическая разработка). Процесс промышленного производства оценивается на этой стадии, основываясь на знании процесса, полученном при его разработке и масштабировании.
- Квалификация процесса (пилотное производство). Производственный процесс проверяется на способность устойчиво производить качественную продукцию при промышленном производстве.
- Продолжающаяся верификация процесса (сопутствующая валидация). Включает регулярные проверки, проводимые в процессе текущего производства для подтверждения того, что процесс находится под контролем.
Как объяснил Р. Гуржий, необходимо проводить анализ всех рисков, от этапа фармацевтической разработки до сопутствующей валидации. При этом первым шагом должна стать идентификация риска. Следует определить риск для пациента в связи с выходом нормативных показателей препарата в течение срока годности за пределы спецификации.
Вторым шагом является анализ риска. При разработке препарата он включает исследование субстанций, в том числе технологии, профиля примесей, вариабельности параметров. Также следует изучить влияние первичной упаковки, определить фотостабильность препарата, совместимость компонентов. Затем проводится мониторинг ситуации и все данные, полученные при анализе рисков, вносятся в протокол сопутствующей валидации.
 Интерес аудитории вызвал доклад Елены Гриценко, доктора фармацевтических наук, профессора, посвященный особенностям создания твердых лекарственных форм фитоконцентратов на ООО «Экомед» (Киев).
Интерес аудитории вызвал доклад Елены Гриценко, доктора фармацевтических наук, профессора, посвященный особенностям создания твердых лекарственных форм фитоконцентратов на ООО «Экомед» (Киев).
В своем выступлении Е. Гриценко осветила процесс создания гранул на основе сахарной пудры. Прецедентом для разработки такой лекарственной формы стало желание компании импортировать фитоконцентраты в арабские страны. Однако зарубежные партнеры предприятия по религиозным соображениям не могли согласиться на закупку спиртосодержащих средств. Тогда было принято решение использовать в качестве основы сахарную пудру, создать на ее базе три лекарственные формы: гранулы «нонпарель», таблетки на основе таких гранул, а также таблетки на основе сахарной пудры.
Докладчица пояснила, что технология создания гранул довольно простая. Единственная сложность возникает при определении дозы фитоконцентрата в гранулах. На 10 капель приходится 1 г пудры, это примерно 30 гранул. Изготовление таблеток на основе гранул также несложный процесс. Измельчается пудра, фракционируются частицы, наносится фитоконцентрат, подсушивается масса. На завершающей стадии происходит опудривание кальция стеаратом таблетирования. Однако стоимость данной лекарственной формы достаточно высока, что потребовало поиска других вариантов.
При выпуске таблеток на сахарной пудре в качестве увлажнителя компанией применяется крахмальный клейстер. Фитоконцентрат добавляется не сразу, а уже после получения готовой таблеточной массы, ее гранулирования, подсушивания гранулята.
По словам Е. Гриценко, в клинических исследованиях доказано, что нанесение фитоконцентрата на сахарную пудру позволяет значительно снизить дозировку препарата, сохранив при этом его эффективность.
 Александр Щиковский, кандидат медицинских наук, представитель ЗАО НПЦ «Борщаговский химико-фармацевтический завод» (Киев), представил обзор современных тенденций и достижений в создании твердых лекарственных форм из труднорастворимых лекарственных субстанций.
Александр Щиковский, кандидат медицинских наук, представитель ЗАО НПЦ «Борщаговский химико-фармацевтический завод» (Киев), представил обзор современных тенденций и достижений в создании твердых лекарственных форм из труднорастворимых лекарственных субстанций.
А. Щиковский сообщил, что, по данным мировой фармацевтической литературы, на протяжении последних десятилетий при разработке новых лекарственных средств более 41% неудач были связаны с тем, что новая активная субстанция имела несоответствующие биофармацевтические свойства, прежде всего, плохую растворимость в воде. Как свидетельствуют ведущие фармакопеи мира (EP, USP, JP и др.), одна из трех лекарственных субстанций, как правило, является труднорастворимой или совсем не растворимой. Поэтому постоянно повышается важность технологических методов, улучшающих растворимость препаратов.
Для оценки степени растворимости субстанции из твердых лекарственных форм, таких как таблетки и капсулы, используют тест растворения, приведенный в Государственной Фармакопее Украины. Тест позволяет улучшить регулярный контроль качества лекарственных средств от серии к серии, гарантирует качество препарата после внесения изменений и т.д.
Большое значение при разработке лекарственных средств имеет также Биофармацевтическая система классификации, выступающая руководством для прогнозирования всасывания препарата в желудочно-кишечном тракте. Система базируется на растворимости и проницаемости лекарственных субстанций и может применяться как основа для теста растворимости in vivo-in vitro при разработке новых лекарственных средств.
Основываясь на результатах проведенных исследований, А. Щиковский предположил, что для изготовления твердых лекарственных форм существует закономерность: если растворимость субстанции составляет более 50 мг/л, большое значение для ее улучшения имеют вспомогательные вещества, такие как наполнители и солюбилизаторы. При растворимости менее 50 мг/л ее можно увеличить, используя физическую модификацию лекарственной субстанции. В некоторых случаях имеет смысл применять комбинирование технологических методов.
Одним из популярных современных подходов для повышения растворимости лекарственных средств в водной среде являются нанотехнологии. Выступающий напомнил, что наночастицы представляют собой твердые коллоидные частицы размером от 1 до 1000 нм.
Однако, заметил А. Щиковский, следует учитывать, что утверждение «чем меньше частицы лекарственного средства, тем лучше его биодоступность и в целом фармакологическое действие» по большей мере является ошибочным.

Размер частиц должен быть специально подобран с учетом достижения необходимого терапевтического эффекта. То есть в случае, когда необходимо быстрое всасывание субстанции, как правило, размер частиц должен быть порядка 100–200 нм. Когда же необходимо медленное растворение, средний размер частиц находится в более высоком нанометровом диапазоне — 800–1000 нм.
Для получения наносуспензий из лекарственных препаратов используются технологии, базирующиеся на ультразвуковом диспергировании кристаллических микрочастиц до наночастиц. С этой же целью ультразвук может быть применен в процессе образования наносуспензий при их кристаллизации.
В завершение выступления А. Щиковский сообщил, что физическая модификация лекарственных субстанций, например, уменьшение размера частиц, изменение формы субстанции в наше время применяется довольно широко. Однако уже появились новые варианты (наносуспензии, наноэмульсии), которые дают многообещающие результаты в повышении растворимости и биодоступности труднорастворимых лекарственных препаратов.
По мнению докладчика, любой метод, используемый учеными в этих целях, должен быть направлен как на удешевление процесса, так и на повышение эффективности препарата.
В ходе конференции также выступил Владимир Пашко, директор компании «Донау Лаб», рассказавший о современном оборудовании для фармацевтического анализа.
В докладе Ольги Пантелеевой, представителя немецкой компании «Инноджет Хербер Хютлин» в странах СНГ, речь шла об инновационном оборудовании кипящего слоя для грануляции и нанесения покрытия, внедряемом на предприятиях, производящих фармацевтическую продукцию.
На секционных заседаниях звучали доклады Аэлиты Кричковской, доцента Национального университета «Львовская политехника», представившей ретроспективный анализ сроков годности некоторых лекарственных средств; Татьяны Жидковой, представителя ОАО «Фармак», рассмотревшей трансфер технологии производства таблеток комплекса витаминной группы В, покрытых оболочкой; Елены Покотило, сотрудника фармацевтического факультета Тернопольского государственного медицинского университета им. И.Я. Горбачевского, посвятившей свое выступление обработке состава и технологии комбинированного препарата «Альфа+Омега», а также ряд других интересных докладов.
Большинство выступлений находили живой отклик у аудитории и становились поводом для дискуссий. В целом по итогам мероприятия можно отметить, что невзирая ни на что отечественная наука продолжает активно развиваться, и это обеспечивает движение вперед всего фармацевтического сектора.
«Еженедельника АПТЕКА»

Коментарі