
4 березня проблеми, які наразі призвели до драматичної ситуації у сфері медикаментозного забезпечення населення, обговорювалися під час розширеного спільного засідання Об’єднання організацій роботодавців медичної та мікробіологічної промисловості України (ООРММПУ) та Асоціації виробників ліків України (АВЛУ). У заході також взяли участь представники аптечних мереж, міжнародних фармацевтичних асоціацій та пацієнтських організацій.
Вітчизняну фармацевтичну промисловість представляли потужні підприємства: ПАТ «Фармак», ПАТ НВЦ «Борщагівський ХФЗ», Корпорація «Артеріум», ТОВ «Фармацевтична компанія «Здоров’я», ПрАТ «Біофарма», ПАТ «Київський вітамінний завод», АТ «Лекхім», ТДВ «Інтерхім», ТОВ «Юрія-Фарм», ТОВ «Кусум Фарм», ПрАТ «Технолог», ТОВ «Сперко Україна», ПАТ «Фітофарм» та ін.
До заходу долучилися асоціації міжнародних виробників, а саме Асоціація виробників інноваційних ліків «АПРАД», громадська організація «Асоціація представників міжнародних фармацевтичних виробників» (AIPM Ukraine), Американська торговельна палата в Україні.
Крім того, на запрошення ООРММПУ та АВЛУ відгукнулися пацієнтські організації — Всеукраїнська Рада захисту прав та безпеки пацієнтів, громадська організація «Медичний контроль», Спілка захисту прав пацієнтів «Здоров’я нації», ВГО «Асоціація хворих хронічним мієлолейкозом», Союз споживачів медичних послуг, лікарських засобів, виробів медичного призначення. На засіданні були присутні представники ЗМІ.
Під час засідання його учасники наголошували на необхідності дерегуляції фармацевтичного ринку, важливості створення прозорих та зрозумілих правил гри тощо. Шукаючи шляхи подолання кризи, головне зрозуміти її ключові причини.
Валерій Печаєв, президент ООРММПУ, привітавши присутніх, повідомив, що на сайті МОЗ України для громадського обговорення опубліковано проект закону «Про внесення змін до Закону України «Про лікарські засоби» (щодо державної реєстрації лікарських засобів)» стосовно передання функцій державної реєстрації лікарських засобів від одного центрального органу влади до іншого. «Ми маємо відреагувати на цю ініціативу та надати оцінку її обґрунтованості», — зазначив доповідач.
Окремо президент ООРММП запропонував розглянути нагальні проблеми у сфері забезпечення населення ліками. Він зауважив, що на сьогодні на фармацевтичному ринку України склалася критична ситуація у зв’язку з неможливістю закладів охорони здоров’я закуповувати лікарські засоби за державні кошти. Це обумовлено дією постанови КМУ від 2 липня 2014 р. № 240 «Про референтне ціноутворення на лікарські засоби та вироби медичного призначення, що закуповуються за кошти державного та місцевих бюджетів».
Нагадаємо, що відповідно до постанови КМУ № 240 з 1 березня поточного року заклади охорони здоров’я мають право закуповувати ліки за бюджетні кошти лише за наявності задекларованої оптово-відпускної ціни. Але станом на 6 березня 2015 р. оптово-відпускні ціни відповідно до вимог постанови КМУ від 02.07.2014 р. № 240 задекларовано лише для 1964 торгових назв лікарських засобів. Для порівняння у минулому році кількість торгових назв препаратів у номенклатурі державних закупівель становила 7873. Таким чином, на сьогодні лікувальні заклади мають право закуповувати близько 25% минулорічного асортименту. Наше видання вже повідомляло, що до державних закупівель не допущено цілу низку терапевтичних груп життєво необхідних препаратів, без яких неможливо забезпечити безперервність терапії для українських пацієнтів (див. «Щотижневик АПТЕКА» № 8 (979) від 02.03.2015 р.)
Причиною неможливості декларування оптово-відпускних цін заявниками і, як наслідок, участі в державних закупівлях є складна й непрозора процедура декларування на тлі девальвації гривні та запровадження додаткового оподаткування лікарських засобів, що значно впливає на їх вартість.
На сьогодні ситуація із забезпеченням лікарень уже дійшла до колапсу й стала предметом прокурорських розслідувань, а в окремих регіонах України органи місцевої влади вимушені вживати крайніх заходів. Бюджетні кошти, спрямовані на забезпечення лікарськими засобами, зокрема пільгових категорій населення, перераховуються до департаментів соціальної політики для надання адресної допомоги населенню, щоб хворі потім самостійно придбавали ліки в аптеці, якщо, звичайно, необхідні препарати взагалі будуть там у наявності.
Криза, що виникла у сфері забезпечення препаратами населення, обумовлена бездіяльністю МОЗ України у той час, коли слід оперативно вирішувати проблеми фармацевтичного сектору. Необхідність дерегуляції фармацевтичного ринку лише декларується керівництвом профільного міністерства, але жодних кроків у цьому напрямку донині не зроблено.
Петро Багрій, президент Асоціації «Виробники ліків України», нагадав, що на початку 2014 р. за ініціативою Державної служби України з лікарських засобів (далі — Держлікслужба України) та за підтримки МОЗ України було створено 5 робочих груп, які займалися розробкою проектів нормативно-правових актів, спрямованих на поліпшення бізнес-середовища та інвестиційної привабливості фармацевтичного ринку України шляхом його дерегуляції. Звичайно, ці ініціативи у разі їх реалізації мають сприяти забезпеченню безперервного лікування українських пацієнтів якісними, ефективними та доступними препаратами. Зокрема, йдеться про зміни до постанови КМУ від 26.05.2005 р. № 376, які передбачають удосконалення порядку державної реєстрації (перереєстрації) лікарських засобів, наказу МОЗ України від 26.08.2005 р. № 426 «Про затвердження Порядку проведення експертизи реєстраційних матеріалів на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію), а також експертизи матеріалів про внесення змін до реєстраційних матеріалів протягом дії реєстраційного посвідчення», постанови КМУ від 14.09.2005 р. № 902 «Про затвердження Порядку здійснення державного контролю якості лікарських засобів, що ввозяться в Україну, та інших документів, які впливають на господарську діяльність суб’єктів фармацевтичного ринку». Загалом, фармацевтична спільнота разом із фахівцями регуляторних органів розробила понад 40 проектів регуляторних актів, які направлені в профільне міністерство.
Замість вирішення проблем, які існують у сфері забезпечення населення ліками, МОЗ України виступило з несподіваною ініціативою передати функцію державної реєстрації/перереєстрації лікарських засобів Держлікслужбі України. При цьому удосконалення процедури допуску препаратів на український ринок не передбачено. «Фактично МОЗ України пропонує передати процес реєстрації/перереєстрації препаратів з усіма проблемами, які існують на теперішній час у цій сфері, від одного регуляторного органу іншому», — зазначив П. Багрій. За його словами, це лише ускладнить існуючі проблеми, адже передача функції здійснення експертизи матеріалів реєстраційного досьє Держлікслужбі України потребуватиме суттєвих змін до нормативно-правової бази, що забере багато часу. «На сьогодні МОЗ має працювати над удосконаленням процедури державної реєстрації/перереєстрації лікарських засобів, а не займатися перерозподілом функцій у цій сфері», — підкреслив президент АВЛУ.
З огляду на це ініціатива МОЗ України сколихнула фармацевтичну спільноту. Законопроект щодо передачі функцій реєстрації ліків від міністерства до Держлікслужби України викликав негативну реакцію з боку як вітчизняних, так і зарубіжних виробників ліків. Навіть пацієнтські організації розуміють його недолугість. Не дивлячись на це, МОЗ не знімає законопроект з обговорення й загроза щодо його розгляду та ухвалення залишається.
Щодо ситуації навколо Держлікслужби України П. Багрій нагадав, що в минулому році вперше за часи незалежності України фармацевтична промисловість домоглася призначення на посаду голови відомства особи, яка має професійні знання, відрізняється європейським підходом до прийняття регуляторних рішень, довела свою управлінську ефективність та реально сприяє розвитку фармацевтичного сектору галузі охорони здоров’я і є заслуженим авторитетом серед операторів ринку. Мова йде про Михайла Пасічника. Його кандидатуру підтримали вітчизняні та зарубіжні виробники, дистриб’юторські компанії, оператори роздрібної ланки та навіть пацієнтські організації. Саме завдяки зусиллям М. Пасічника було створено вищезгадані робочі групи. Очоливши Держлікслужбу України у складний для країни час, він брав особисту участь у роботі цих робочих груп, заглиблювався у проблеми галузі та намагався їх вирішувати. Не дивлячись на це, на сьогодні постало питання про заміну очільника Держлікслужби України ( Прим. ред. — 4 березня Уряд прийняв рішення звільнити за угодою сторін М. Пасічника з посади голови Державної служби України з лікарських засобів. Відповідне розпорядження підписано Прем’єр-міністром України Арсенієм Яценюком за № 149-р). «Це нагадує звичайну рокіровку на користь певних бізнес-груп, які намагаються дестабілізувати й без того складну ситуацію на фармацевтичному ринку України на користь власних інтересів», — підкреслив доповідач.
П. Багрій зауважив, що непрозорі кадрові ротації відбуваються без жодного контролю з боку громадськості. Тому представники фармацевтичної спільноти наполягають на обов’язковому проведенні відкритих та прозорих конкурсів за участю представників професійних кіл під час призначення керівництва МОЗ, Держлікслужби України, а також державних підприємств, що працюють у системі цих відомств.
Влада та суспільство мають розуміти, у якому напрямку надалі розвиватиметься фармацевтичний сектор галузі охорони здоров’я, адже успішність реформ залежить від системної цілеспрямованої роботи. Це можливо за наявності Концепції нової національної системи охорони здоров’я, тобто системи поглядів на те, якою ми її бачимо, стратегії розвитку як шляху до цілі та конкретного плану дій з чітким визначенням відповідальних, виконавців та критеріїв моніторингу результативності.
Ще одна кричуща проблема, з якою останнім часом зіткнулися фармацевтичні виробники, — це блокування на рівні МОЗ процедури державної реєстрації/перереєстрації лікарських засобів. Профільне міністерство з незрозумілих причин гальмує підписання наказів щодо реєстрації/перереєстрації понад 650 препаратів. Це може призвести до штучного створення дефіциту ліків на вітчизняному ринку в умовах економічної нестабільності.
АВЛУ пропонує звернутися до керівництва держави з проханням долучитися до вирішення проблем фармацевтичного ринку, адже мова йде про забезпечення населення лікарськими засобами, а відтак й про національну безпеку держави.
Щодо проблем у сфері державної реєстрації/перереєстрації ліків, то редакція «Щотижневика АПТЕКА» провела відповідний аналіз на основі інформації бази даних «Лікарські засоби» компанії «Софтінформ».
Так, за результатами моніторингу було встановлено, що у 2013 та 2014 р. на ринок допущено приблизно однакову кількість препаратів (рис. 1).
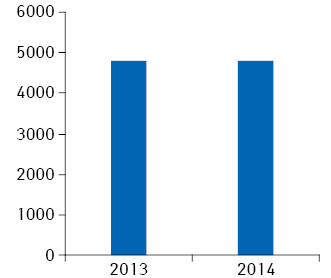
Якщо ж помісячно розглянути процес державної реєстрації/перереєстрації ліків у 2013–2014 рр. та січні–лютому 2015 р. виявляється, що за останні 2 зимових місяці поточного року зареєстровано/перереєстровано у 2–3 рази менше препаратів, ніж за аналогічні періоди 2013–2014 рр.
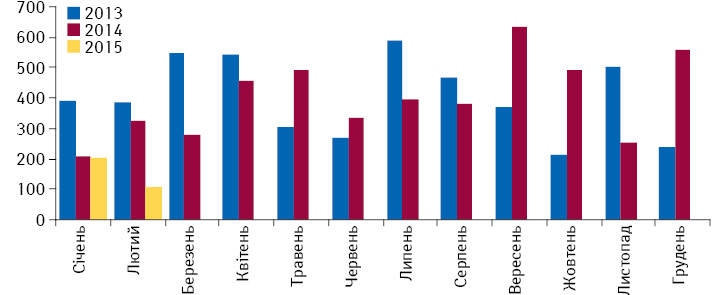
Як можна побачити на рис. 2, у січні 2014 р. кількість зареєстрованих лікарських засобів була вдвічі меншою, ніж у січні 2013 р. Це може бути пов’язано з впровадженням обов’язкової наявності сертифікату належної виробничої практики (Good Manufacturing Practice — GMP). Нагадаємо, що у 2013 р. набули чинності законодавчі вимоги щодо обов’язкової наявності сертифіката GMP, який має супроводжувати заяву на державну реєстрацію/перереєстрацію лікарських засобів. У лютому 2014 р. процес допуску препаратів на ринок активізувався й у подальшому тривав без перебоїв.
Але ж у січні 2015 р. без об’єктивних причин кількість зареєстрованих ліків є навіть меншою, ніж у 2014 р., не кажучи вже про 2013 р., коли реєструвалося вдвічі більше препаратів. А у лютому 2015 р. відмічається безпрецедентно мала кількість зареєстрованих/перереєстрованих лікарських засобів.
Зазначимо, що затягування держаної реєстрації/перереєстрації ліків ставить під загрозу безперервне лікування українських пацієнтів. І все це відбувається в умовах, коли внаслідок запровадження нових податків та суттєвої девальвації гривні економічна доступність препаратів для українців відчутно знизилася. З 1 квітня за ініціативою попереднього Уряду Верховна Рада України запровадила 7% ставку ПДВ на лікарські засоби та медичні вироби. А нинішній Уряд з 1 березня 2015 р. ініціював запровадження в Україні додаткового 5% податку на імпорт ліків.
Розглянувши нагальні проблеми у сфері медикаментозного забезпечення населення України, учасники заходу прийшли до спільної думки, що з метою розблокування процесу закупівель ліків закладами охорони здоров’я Уряд має терміново скасувати або принаймні зупинити дію постанови КМУ № 240.
Для забезпечення безперебійного доступу хворих до якісних, ефективних та безпечних ліків Уряд має усунути бар’єри в процесі реєстрації/перереєстрації лікарських засобів. Зі свого боку зазначимо, що системне вирішення цього питання лежить у площині законодавчого врегулювання процесу допуску препаратів на український ринок шляхом ухвалення нової редакції Закону України «Про лікарські засоби», гармонізованої з положеннями Директиви 2001/83/ЕС Європейського Парламенту та Ради ЄС від 6 листопада 2001 р. про звід законів Співтовариства щодо лікарських препаратів для людини.
За результатами засідання його учасники підготували лист Президенту України Петру Порошенку та спільний прес-реліз від АВЛУ та ООРММПУ.
фото автора

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим