Головне — дорога до мети: ООРММП України визначило вектор діяльності на наступні 3 роки
28 вересня 2018 р. за сприяння компанії «Фіто-Лек» Слобожанщина гостинно прийняла учасників VIІ З’їзду Об’єднання організацій роботодавців медичної та мікробіологічної промисловості України. Про те, чим займалося об’єднання впродовж останніх років, які отримало здобутки, та про план діяльності на наступні 3 роки ми дізналися безпосередньо під час з’їзду
На засіданні Комітету прийнято ряд важливих рішень
Під час засідання депутати розглянули низку важливих питань, у тому числі й щодо звільнення із займаних посад першого заступника міністра охорони здоров’я України Уляни Супрун та заступника міністра охорони здоров’я України Олександра Лінчевського.
Иммунотерапия рака — Нобелевский Эверест 2018
Открытия американца Джеймса П. Эллисона и японца Тасуку Хондзё коренным образом меняют как парадигму лечения рака, так и в целом взгляд на его излечимость
НФаУ — SAFEMed: перспективи досліджень біоеквівалентності в Україні
Робочий візит до НФаУ міжнародного експерта в галузі біоеквівалентності д-ра В. Гілсдорфа та представників проекту SAFEMed — почесний етап співпраці університету в царині вдосконалення інституту досліджень біоеквівалентності в Україні
Вакцина аКДП — ацелюлярна або цільноклітинна?
Починаючи з 2015 р. вакцини проти дифтерії, правця та кашлюку з ацелюлярним компонентом централізовано не закуповують. Чому так відбулося та які ризики несе стратегія відмови від закупівель ацелюлярних вакцин проти дифтерії, правця та кашлюку (далі — ааКДП)?
Вакцинировать или нет: открытое письмо от международных организаций к ВОЗ о проблеме безопасности вакцин
Недоверие к вакцинации — проблема, известная глобальному сообществу с момента появления вакцин. Недавно было опубликовано открытое письмо ряда мировых профессиональных и общественных организаций, которые выразили свою обеспокоенность настоящим положением дел относительно качества и безопасности вакцин.
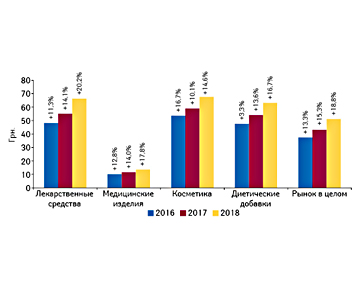
Бриф-анализ фармрынка: итоги сентября* 2018 г.
В данной публикации вниманию читателей представлены ключевые показатели фармацевтического рынка Украины (территории, подконтрольной украинскому правительству) в сентябре* 2018 г.
Закон щодо відкриття доступу до результатів клінічних досліджень ліків набув чинності
4 жовтня 2018 р. набув чинності та 4 листопада 2018 р. вводиться в дію прийнятий Парламентом 4 вересня Закон України № 2519-VIII «Про внесення зміни до статті 9 Закону України «Про лікарські засоби» щодо доступу до результатів доклінічного вивчення та клінічних випробувань лікарських засобів». Новий закон встановив зобов’язання для МОЗ України забезпечувати на своєму офіційному веб-сайті вільний доступ до всіх результатів доклінічного вивчення та клінічних випробувань лікарських засобів (звітів […]
Народні депутати ініціюють скасування ПДВ на операції з постачання ліків та окремих медичних виробів
Автори законодавчої ініціативи сподіваються, що прийняття законопроекту матиме наслідком здешевлення ліків для українців