Затверджено десятий випуск Державного формуляра лікарських засобів
Наказом МОЗ України від 10.05.2018 р. № 868 затверджено десятий випуск Державного формуляра лікарських засобів (далі — Державний формуляр), який визначає перелік зареєстрованих в Україні лікарських засобів, що включає ліки з доведеною ефективністю, допустимим рівнем безпеки, використання яких є економічно прийнятним, як складової системи галузевих стандартів у сфері охорони здоров’я. Державний формуляр розроблений з метою створення на державному рівні та впровадження якісної формулярної системи […]
Розпочато прийом заяв щодо включення лікарських засобів до Національного переліку
Експертний комітет з відбору та використання основних лікарських засобів (далі — експертний комітет) повідомляє про прийом листів і заяв про внесення змін до Національного переліку основних лікарських засобів (далі — Національний перелік) та документів, що додаються до заяви. Відповідно до Положення про здійснення відбору лікарських засобів для внесення до Національного переліку, затвердженого наказом МОЗ України від 07.10.2016 р. № 1050 (далі — Положення), до заяви додаються документи, що підтверджують порівняльну ефективність […]
Набули чинності зміни до Порядку проведення експертизи реєстраційних матеріалів на лікарські засоби, подані на реєстрацію
15 травня у зв’язку з опублікуванням у газеті «Офіційний вісник» № 37 набув чинності наказ МОЗ України від 13.04.2018 р. № 711, яким вносяться зміни зміни до Порядку проведення експертизи реєстраційних матеріалів на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію), а також експертизи матеріалів про внесення змін до реєстраційних матеріалів протягом дії реєстраційного посвідчення (далі — Порядок), затвердженого наказом МОЗ України від 26.08.2005 р. № 426. Нагадаємо, що даними змінами виключено […]
Движение ко всеобщему охвату услугами здравоохранения, или Здоровье для всех!
Движение ко всеобщему охвату услугами здравоохранения (universal health coverage — UHC) сегодня является одним из важнейших направлений в развитии систем здравоохранения
Оприлюднено Порядок проведення єдиного кваліфікаційного іспиту для здобувачів ступеня «магістр» у галузі охорони здоров’я
На Урядовому порталі оприлюднено постанову КМУ від 28.03.2018 р. № 334, відповідно до якої атестація здобувачів ступеня вищої освіти «магістр» за спеціальностями галузі знань «22 Охорона здоров’я» здійснюватиметься у формі єдиного державного кваліфікаційного іспиту (далі — кваліфікаційний іспит). Також цією постановою затверджено Порядок проведення такого іспиту. Кваліфікаційний іспит складатиметься в залежності від спеціальності з: інтегрованого тестового іспиту «КРОК»; об’єктивного структурованого практичного (клінічного) іспиту, під […]
Державний контроль при ввезенні ліків в Україну: про що мають пам’ятати оператори ринку
13 квітня 2018 р. ДП «Український фармацевтичний інститут якості» за підтримки та участі Держлікслужби провело семінар «Особливості здійснення відомчого та державного контролю при ввезенні лікарських засобів в Україну», у якому взяли участь більше 30 слухачів, у тому числі уповноважені особи імпортерів та виробників лікарських засобів
Медичний канабіс в Україні: бути чи ні?
Для того щоб обговорити результати досліджень медичного канабісу в зарубіжних країнах, сфери його застосування та досвід використання в лікарняній практиці, проблеми легалізації та перспективи використання медичного канабісу в Україні, у Харкові 20 квітня близько 500 осіб — представники регуляторних органів, освіти, пацієнтських та громадських організацій, лікарі, зацікавлені особи — зібралися на першій Міжнародній медичній канабіс-конференції (International medical cannabis conference — IMCC).
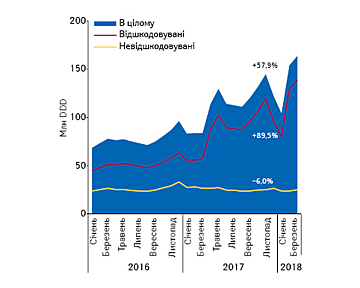
Програма «Доступні ліки»: підсумки першого року реалізації
У даній публікації розглянуто динаміку споживання та вартості препаратів, які включені до програми реімбурсації. Аналіз проведено для чинного на сьогодні Реєстру. Показники динаміки представлені за показником МАТ (квітень 2017 — березень 2018 р. до квітня 2016 — березня 2017 р.) Під час підготовки матеріалу використано дані аналітичної системи дослідження ринку «PharmXplorer»/«Фармстандарт» компанії «Proxima Research»
Медичний форум 2018: ключові події і подробиці заходу
Медичний форум — це платформа для комунікації вчених, лікарів, інвесторів та виробників продукції медичного призначення. Завдяки його проведенню розробники новітніх технологій мають можливість репрезентувати медикам нові досягнення і тенденції світової та вітчизняної медицини.
Ринковий нагляд за медичними виробами. Законодавство та практики країн — членів ЄС
26 квітня 2018 р. Комітет з охорони здоров’я Європейської Бізнес Асоціації (ЄБА) провів освітній семінар «Ринковий нагляд за медичними виробами. Законодавство та практики країн — членів ЄС». Європейські спікери — експерти з багаторічним досвідом, які працюють на ринках країн ЄС, — поділилися зі слухачами досвідом щодо системи ринкового нагляду за медичними виробами в цих державах, звітування про інциденти, вимог до документації та маркування медичних виробів та важливих аспектів з оцінки та управління ризиками