Хворі, які звертаються до лікаря, дуже часто скаржаться на біль. Міжнародна Асоціація вивчення болю визначає біль як «неприємне відчуття та емоційне переживання, що виникає у зв’язку із наявною або потенційною загрозою пошкодження тканин». Таке визначення постулює взаємозалежність між об’єктивними аспектами болю та його суб’єктивними емоційними компонентами [1].
Розрізняють біль гострий та хронічний. Гострий біль — це біль, що виникає раптово, швидко наростає до максимальної інтенсивності. Як правило, він є симптомом якогось захворювання чи травми. Хронічний біль набуває статусу хвороби, триває довго, досить часто з невстановлених причин [2].
Виділяють біль ноцигенний, нейрогенний і психогенний [1]. Ноцигенний біль виникає при подразненні ноцицепторів (рецепторів, чутливих до патологічних подразників, або до подразників, які стають патологічними при тривалій дії) і може бути соматичним і вісцеральним. Соматичний біль виникає у м’язах, зв’язках, суглобах, кістках, вісцеральний — при пошкодженні внутрішніх органів. До ноцигенного відносять біль при травмах, запаленні, ішемії, післяопераційний біль, біль у хворих онкологічного профілю.
Нейрогенний біль пов’язують з пошкодженням периферичних і центральних структур нервової системи. Зокрема, це невралгія, фантомний, таламічний біль, каузалгія та ін.
Психогенний біль може виникати за відсутності або у разі незначного пошкодження тканин, коли вирішальним фактором є психоемоційний стан (депресія, психоз, істерія). Такий біль не позв’язаний зі ступенем тяжкості пошкодження.
Біль — не тільки симптом більшості гострих і хронічних захворювань, але й складний психоемоційний феномен, що формується за участю емоційних, гуморальних та гемодинамічних реакцій.
В організмі існують дві системи модулювання болю — ноцицептивна і антиноцицептивна. Ноцицептивна система починається з нервових закінчень, які ідентифікуються з больовими рецепторами, або ноцицепторами (noci — пошкодження, втрата). Останні у великій кількості знаходяться в різних органах, тканинах, з них починається формування соматичного та вісцерального болю. Подальше проведення больових імпульсів відбувається трьома нейронами, закінчення яких розташовані в задніх рогах спинного мозку і далі в таламусі. Звідси третій нейрон передає імпульси через синапси в постцентральну звивину мозку. Ці вихідні шляхи та ділянки головного мозку є основними субстанціями не тільки для ноцицептивної інформації, але й для інших видів взаємопов’язаної функціональної активності. В процесі такої інтеграції формуються ендогенні протибольові системи головного мозку. На сьогодні досить детально встановлена ієрархія різних рівнів формування болю, роль антиноцицептивних систем мозку. Передача ноцицептивних сигналів зазнає первинних змін вже на рівні спинного мозку, а субстратом складної початкової взаємодії ноцицептивної і антиноцицептивної систем виявляються задні роги спинного мозку. Подальша інтеграція вищих відділів мозку значно змінює больові сигнали, формуються антибольові впливи. Одночасно з анальгезією розвивається артеріальна гіпертензія, тахікардія, збільшується кровотік у м’язах, виникають емоційні реакції, зміни поведінки, що розцінюються як адаптаційні реакції організму на вплив ноцицептивних факторів [3].
В останні роки досить активно застосовують так звану ад’ювантну або додаткову протибольову фармакотерапію, що передбачає використання непрямих шляхів інгібування окремих ланок ноцицепції. До ад’ювантних засобів належать антидепресанти, нейролептики, кортикостероїди, протисудомні засоби, a2-адреноміметики, антигістамінні препарати та ін.
Найяскравішою ілюстрацією можливостей такого підходу є застосування для усунення болю нестероїдних протизапальних засобів (НПЗЗ), в основі механізму дії яких лежить зворотний інгібуючий вплив на периферичний та центральний синтез простагландинів (див. рисунок) [4].
НПЗЗ пригнічують відповідь на ноцицептивну стимуляцію на таламічному рівні, запобігають накопиченню простагландинів у спинномозковій рідині. Ефективність НПЗЗ вище у разі їх внутрішньовенного введення. Вони швидко проникають через гематоенцефалічний бар’єр, реалізуючи свої центральні механізми дії, сприяючи швидкій та надійній анестезії [3].
І все ж основними знеболювальними засобами є опіати та опіоїди, адже важливим компонентом антиноцицептивної системи є опіоїдна система, до складу якої входять опіоїдні рецептори та ендогенні опіоїдні речовини — ендорфіни та енкефаліни.
Існує декілька видів опіатних рецепторів: m (мю), d (дельта), k (капа), e (епсілон), s (сигма), збудження яких зумовлює певні ефекти [1] (див. таблицю).
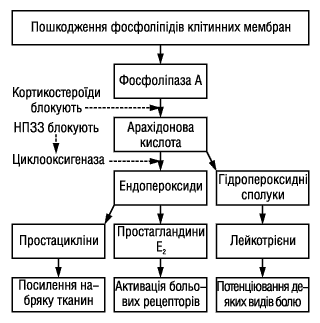 |
Рисунок. Механізм дії НПЗЗ і кортикостероїдів
Таблиця
Ефекти, що виникають у разі збудження
різних підтипів опіатних рецепторів
|
Підтип |
Ефекти |
|
m |
Анальгезія, пригнічення дихання, ейфорія, формування залежності, седативний ефект, пригнічення перистальтики травного тракту |
|
d |
Анальгезія, седативний ефект, таламічна дія |
|
d |
Анальгезія, ейфорія, зміна поведінки |
|
s |
Галюцинації, манія, мідріаз, тахіпное |
Збудження опіатних рецепторів супроводжується гемодинамічними змінами: активація m-рецепторів сприяє гальмуванню ноцицептивної гіпертензивної реакції, d-рецептори забезпечують формування пресорних реакцій при болю, їх посилення при опіатній залежності. Опіоїдні нейропептиди також регулюють вегетативні функції: енкефаліни спричиняють пресорні реакції судин, ендорфіни — депресорні. Це означає, що опіоїдні системи організму забезпечують гальмування негативних реакцій в ноцицептивних системах і мобілізують вегетативні функції у відповідь на пошкодження.
Опіати (речовини, що містяться в соку опійного маку з анальгезивною дією) та опіоїди (речовини іншої хімічної будови, але з фармакологічними ефектами, аналогічними таким опіатів) взаємодіють з опіатними рецепторами і подібно до опіоїдних нейропептидів впливають на міжнейронну передачу больових (ноцицептивних) імпульсів. Така взаємодія відбувається у первинних пресинаптичних аферентних нейронах спинного мозку (c — волокнах) і реалізується відкриванням калієвих каналів (в?m– та d-рецепторах) або блокуванням кальцієвих каналів (в k-рецепторах). Як наслідок зменшується виділення біологічно активних речовин — медіаторів ноцицептивних сигналів [1].
Класичним представником наркотичних анальгетиків є морфін, який виявляє сильний знеболювальний ефект. Збудження морфіном, іншими опіатами та опіоїдами опіоїдних рецепторів постсинаптичної мембрани викликає її гіперполяризацію та відповідно гальмування активності нейронів задніх рогів спинного мозку і ряду структур середнього і довгастого мозку, змінюючи емоційний фон больового відчуття. Ключове значення для виявлення центральної дії морфіну має серотонінова медіація, оскільки її зміни суттєво впливають на анальгезивний, гіпотермічний, локомоторний, ейфоригенний ефекти.
За вибірковістю та характером впливу на опіатні рецептори наркотичні анальгезивні засоби можна поділити на такі групи [3]:
1. Морфіноподібні агоністи: морфін, тримеперидин, фентаніл, метадон, леворфанол, еторфін, кодеїн, героїн.
2. Змішані агоністи-антагоністи: пентазоцин, буторфанол, налорфін, корфанол та ін.
3. Часткові агоністи — бупренорфін.
4. Препарати зі змішаним опіоїдним та неоопіоїдним компонентами механізму дії — трамадол.
Особливого значення знеболювальні засоби набувають в онкологічній практиці. Онкологія є унікальною галуззю медицини, яку не можна уявити без анальгетиків через наявність у хворих онкологічного профілю всіх варіантів гострого та хронічного больового синдрому будь-якої інтенсивності.
Неусунений біль ускладнюється емоційним стресом, депресією, безсонням, дестабілізацією функцій внутрішніх органів, що значно погіршує стан хворого, а значить, потребує фармакологічної корекції — комплексної протибольової терапії симптоматичними ад’ювантними засобами [1].
Існує так званий 4-ступеневий підхід до вибору анальгетиків за принципом наростаючої інтенсивності анальгезії на основі рекомендацій ВООЗ про поступову заміну препаратів з низькою активністю на препарати з високим знеболювальним потенціалом: НПЗЗ -> кодеїн -> тримепиридин -> морфін [5]. Поява нових синтетичних опіоїдів дозволяє удосконалити схему: НПЗЗ -> трамадол -> бупренорфін -> морфін. Особливо вдалою є заміна у схемі кодеїну на трамадол з його високим знеболювальним потенціалом, безпекою, простотою застосування через наявність різних форм випуску (таблетки, капсули, краплі, свічки, ін’єкційний розчин) [6]. Застосування трамадолу в комбінації із засобами ад’ювантної терапії сприяє зниженню інтенсивності болю та дозволяє віддалити необхідність переходу на використання тримеперидину чи морфіну. Лікування трамадолом не потребує спеціального медичного контролю, тому його можна використовувати в домашніх умовах. Враховуючи мінімальний наркогенний потенціал трамадолу, тобто наркологічну безпеку, препарат широко використовують і для знеболювання в хірургії оперованих хворих.
Одним із препаратів трамадолу, що представлений на фармацевтичному ринку України, є ТРАМАДОЛ СТАДА® виробництва німецької фірми «Стада Арнайміттель АГ». ТРАМАДОЛ СТАДА® — це синтетичний опіоїдний анальгетик з високою біодоступністю (60–70% при різних шляхах введення). Виділяють два механізми дії трамадолу. Перший пов’язаний з його спорідненістю до опіоїдних m-, d– та k-рецепторів, в основному до m-рецепторів. Тобто трамадол має властивості неселективного чистого агоністу опіоїдних рецепторів. Другий механізм зумовлений здатністю трамадолу активувати центральні норадренергічні та серотонінергічні механізми, які моделюють потік больових імпульсів. Гальмуючи зворотний захват ендогенного норадреналіну та посилюючи вивільнення серотоніну, трамадол пригнічує передачу больових імпульсів на спінальному рівні. Це підтверджується тим, що опіоїдний антагоніст налоксон лише послаблює знеболювальну дію трамадолу [3].
Трамадол поступається морфіну вираженістю знеболювального ефекту в 5–10 разів. Після введення трамадолу у вену анальгезія розвивається через 5–10 хв. Період напіввиведення становить близько 6 год при хворобах печінки, нирок, у людей похилого віку — триває дещо довше. При внутрішньому прийомі знеболювання наступає через 30–40 хв і зберігається протягом 9 год. В обох випадках трамадол застосовують у дозі 100–200 мг на 70 кг маси тіла, що забезпечує анальгезивну концентрацію в сироватці крові (100 нг/мл і вище). У терапевтичних дозах трамадол майже не пригнічує дихання, не впливає на моторику травного тракту. На фоні використання трамадолу не відбувається змін параметрів кровообігу. У разі застосування згідно з рекомендаціями фізичної або психічної залежності до препарату не розвивається. Встановлено, що в осіб з опіатною залежністю на фоні абстинентного синдрому трамадол, як і плацебо, не поліпшує їх субактивний стан та настрій (на відміну від опіатів), що свідчить про відсутність суттєвого наркогенного потенціалу. Протягом 20 років застосування трамадолу майже у 30 млн хворих розвиток психічної залежності було зафіксовано лише у 152 пацієнтів, що складає 0,0005% [3].
Трамадол у незначній кількості проникає через гематоенцефалічний бар’єр та плаценту (у грудному молоці виявляється до 0,1% введеної дози). Біотрансформується в печінці, виділяється нирками. В сечі виявляють 11 метаболітів, фармакологічно активним з яких є О-дисметилтрамадол, який перевищує активність вихідної сполуки в 2–4 рази.
Основними показаннями для застосування трамадолу є соматичний та вісцеральний помірної вираженості та сильний біль різної локалізації та етіології.
Дозування трамадолу повинно бути адекватним до інтенсивності болю та індивідуальної чутливості до препарату. Якщо біль не минає протягом 30–60 хв, призначають повторно ту саму дозу. Добова доза препарату не повинна перевищувати 400 мг, разова — становить 50–100 мг.
Побічні ефекти трамадолу можуть проявлятися нудотою, блюванням, відчуттям дискомфорту в епігастральній ділянці, а також запором, відчуттям сухості в роті, пітливістю. Деколи виникає серцебиття, кволість, рідко — колапс, зміна настрою, дратівливість, неадекватність поведінки. Не виключені епілептиформні напади, алергічні реакції (як правило, на початку лікування). Пригнічення дихання спостерігається лише при застосуванні препарату у дуже високих дозах.
Трамадол протипоказаний при нирковій та печінковій недостатності, підвищеній чутливості до препарату, в період годування груддю, дітям до 12 років, при гострих отруєннях алкоголем, снодійними, анальгезивними та психотропними засобами, антидепресантами, інгібітором МАО, деякими транквілізаторами.
Передозування трамадолу може проявлятися коматозним станом, нападами судом, гіпотензією, тахікардією, пригніченням дихання. У разі пригнічення дихання вводять налоксон, повторно у низьких дозах, при судомах — бензодіазепіни. Необхідні підтримка функцій серцево-судинної системи, промивання шлунка.
Наркологічна безпека ТРАМАДОЛУ СТАДА®, його виражена знеболювальна дія, добра переносимість навіть при тривалому застосуванні, наявність різних лікарських форм (розчин для інфузій, капсули, краплі) дозволяє розглядати його як надійний та ефективний засіб для лікування больового синдрому, в тому числі хронічного, особливо у хворих, що знаходяться в домашніх умовах.
А.М. Олійник, професор Тернопільської медичної державної академії ім. І. Горбачевського
ЛІТЕРАТУРА
|
Новый НПВП с выраженным обезболивающим эффектом уже в Украине

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим