Документ набув чинності 08.01.2013 р.
у зв’язку з опублікуванням в
«Офіційному віснику України»
від 08.02.2013 р. № 8
МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ
НАКАЗ
від 27.12.2012 р. № 1130
Зареєстровано в Міністерстві юстиції України
21 січня 2013 р. за № 133/22665
Про затвердження Порядку проведення підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики
Відповідно до статті 9 Закону України «Про лікарські засоби», пункту 3 Порядку державної реєстрації (перереєстрації) лікарських засобів, затвердженого постановою Кабінету Міністрів України від 26 травня 2005 року № 376, Порядку здійснення державного контролю якості лікарських засобів, що ввозяться в Україну, затвердженого постановою Кабінету Міністрів України від 14 вересня 2005 року № 902 (у редакції постанови Кабінету Міністрів України від 8 серпня 2012 року № 793), НАКАЗУЮ:
1. Затвердити Порядок проведення підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики, що додається.
2. Визнати таким, що втратив чинність, наказ Міністерства охорони здоров’я України від 30 жовтня 2002 року № 391 «Про затвердження Порядку проведення сертифікації виробництва лікарських засобів», зареєстрований у Міністерстві юстиції України 22 листопада 2002 року за № 908/7196.
3. Управлінню лікарських засобів та медичної продукції Міністерства охорони здоров’я України в установленому порядку забезпечити подання цього наказу на державну реєстрацію до Міністерства юстиції України.
4. Контроль за виконанням цього наказу покласти на заступника Міністра – керівника апарату Р. Богачева.
5. Цей наказ набирає чинності з дня його офіційного опублікування.
МіністрР. Богатирьова
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони
здоров’я України
від 27.12.2012 № 1130
Зареєстровано в Міністерстві
юстиції України
21 січня 2013 р. за № 133/22665
ПОРЯДОК
ПРОВЕДЕННЯ ПІДТВЕРДЖЕННЯ ВІДПОВІДНОСТІ УМОВ ВИРОБНИЦТВА ЛІКАРСЬКИХ ЗАСОБІВ ВИМОГАМ НАЛЕЖНОЇ ВИРОБНИЧОЇ ПРАКТИКИ (GMP)
I. Загальні положення
1. Цей Порядок розроблено відповідно до Закону України «Про лікарські засоби», з урахуванням вимог Директиви 2001/83/ЄС Європейського Парламенту та Ради від 06 листопада 2001 року щодо Кодексу Співтовариства стосовно лікарських засобів, призначених для застосування людиною, Директиви Комісії 2003/94/ЄС від 08 листопада 2003 року, яка встановлює принципи і правила належної виробничої практики щодо лікарських засобів, призначених для застосування людиною, та досліджуваних лікарських засобів, призначених для застосування людиною, Збірника процедур Співтовариства з питань інспекцій та обміну інформацією (EMA/572454/2014, 17 редакція) та рекомендацій документівдокумента міжнародної Системи співробітництва фармацевтичних інспекцій (PIC/S) РІ 002-3 Вимоги до системи якості фармацевтичних інспекторатів. , PIC/S РІ 008-3 Настанова по інспектуванню установ з отримання плазми та місць зберігання плазми, РІ 019-3 Досьє виробничої дільниці для установ з отримання плазми, РІ 020-3 Досьє виробничої дільниці для місць зберігання плазми, PI 040-1 Настанови PIC/S з класифікації невідповідностей GMP.
2. У цьому Порядку терміни вживаються у таких значеннях:
активний фармацевтичний інгредієнт (лікарська речовина, діюча речовина, субстанція) (далі — АФІ або діюча речовина) — будь-яка речовина чи суміш речовин, що призначена для використання у виробництві лікарського засобу і під час цього використання стає його активним інгредієнтом. Такі речовини мають фармакологічну чи іншу безпосередню дію на організм людини, у складі готових форм лікарських засобів їх застосовують для лікування, діагностики чи профілактики захворювання, для зміни стану, структур або фізіологічних функцій організму, для догляду, обробки та полегшення симптомів;
атестована лабораторія — лабораторія з контролю якості лікарських засобів, яка атестована відповідно до Порядку проведення галузевої атестації лабораторій з контролю якості та безпеки лікарських засобів, затвердженого наказом Міністерства охорони здоров’я України від 14 січня 2004 року № 10, зареєстрованим у Міністерстві юстиції України 30 січня 2004 року за № 130/8729;та безпеки лікарських засобів, яка пройшла галузеву атестацію Держлікслужбою України;
виробник лікарських засобів — суб’єкт господарювання, який здійснює хоча б один із етапів виробництва лікарських засобів та має ліцензію (дозвіл) на виробництво лікарських засобів (якщо останнє передбачено національним законодавством країни, на території якої знаходяться виробничі потужності виробника);
виробництво лікарських засобів — діяльність, пов’язана із серійним випуском лікарських засобів, яка включає всі або хоча б одну з операцій щодо технологічного процесу, контролю якості, видачі дозволу на випуск (сертифікації) серії, а також закупівлі матеріалів і продукції, зберігання, оптової торгівлі (дистрибуції) лікарських засобів власного виробництва;
висновок щодо підтвердження відповідності умов виробництва лікарського засобу вимогам належної виробничої практики (далі — Висновок) — документ, виданий ДержлікслужбоюДержавною службою України з лікарських засобів (далі — Держлікслужба України), який засвідчує, що за результатами проведеної спеціалізованої експертизи поданих документів офіційний документ щодо відповідності виробництва лікарських засобів вимогам належної виробничої практики (Good Manufacturing Practice, GMP)GMP, виданий уповноваженим органом країни-члена ЄС, Великої Британії або країни, що має угоду про взаємне визнання з ЄС або з УкраїноюPIC/S, вважається таким, що підтверджує відповідність умов виробництва лікарських засобів чинним в Україні вимогам належної виробничої практики;
Заявник — суб’єкт господарювання — власник реєстраційного посвідчення (торгової ліцензії) та/або ліцензії на виробництво лікарських засобів, який подає до Держлікслужби України особисто або через уповноважену особу (представника), що знаходиться в Україні, заяву на видачу сертифіката відповідності умов виробництва лікарських засобів вимогам належної виробничої практики або заяву на видачу висновку щодо підтвердження відповідності умов виробництва лікарського засобу вимогам належної виробничої практики (далі — Заява) та який відповідає за достовірність наданої інформації та документів;
зразок (проба) від серії — частина від серії, відібрана таким чином і в такій кількості, що є репрезентативною для всієї серії;
інспектор — посадова особа Держлікслужби України та/або фахівець, який залучається нею, має вищу освіту за однією з таких спеціальностей: фармація, технологія фармацевтичних препаратів, хімія, хімічна технологія, біологія, біотехнологія, має досвід роботи у виробництві лікарських засобів, контролі якості, управлінні (забезпеченні) якістю або створенні лікарських засобів та має підтвердження компетентності з питань належної виробничої практики;
інспектування — процедура оцінки відповідності фармацевтичної системи якості суб’єкта господарювання йта фактичного стану наявних умов виробництва лікарських засобів та умов контролю якості чинним в Україні вимогам належної виробничої практики за місцем провадження діяльності (місцезнаходженням виробничих потужностей, у тому числі зон контролю якості та зон зберігання за контрактом (договором));
країна — член PIC/S — країна, що має уповноважений орган у сфері контролю якості лікарських засобів, який є членом міжнародної Системи співробітництва фармацевтичних інспекцій (Pharmaceutical Inspection Cooperation Scheme, PIC/S);
критичне порушення — порушення вимог належної виробничої практики, що призводить до виробництва лікарського засобу, небезпечного для життя людини, або до високого ризику виробництва такого лікарського засобу;
лабораторнийого аналіз — аналіз зразків лікарських засобів на відповідність показників якості лікарських засобів вимогам специфікації якості методів контролю якості лікарських засобів або загальним вимогам до лікарських засобів, встановленим Державною фармакопеєю України, в атестованих лабораторіях;
лікарський засіб критичного рівня ризику — лікарський засіб, для якого виконується будь-яка з таких умов: вузький терапевтичний індекс; висока токсичність; стерильний продукт; біологічний лікарський препарат або складний виробничий процес, проте лікарські засоби низького рівня ризику не можуть розглядатися як критичні, навіть якщо для їх виробництва застосовуються складні виробничі процеси;
лікарський засіб високого рівня ризику — лікарський засіб, що може становити ризик для здоров’я людини навіть при малих кількостях внаслідок перехресної контамінації продуктами, які включають, але не обмежуються пеніцилінами, певними цитотоксинами та біологічними лікарськими засобами;
лікарські засоби низького рівня ризику — лікарські засоби, такі як: місцевого застосування для терапії проти акне; лікарські засоби проти лупи; антисептичні очищувачі шкіри; протигрибкові лікарські засоби для ніг; продукція по догляду за шкірою, яка містить лікарські засоби; засоби захисту від сонячних опіків; льодяники від болю в горлі або кашлю, лікарські засоби, аналогічні їм, а також які не відносяться до стерильних або рецептурних лікарських засобів;
належна виробнича практика (Good Manufacturing Practice, GMP) — частина управління якістю, яка гарантує, що лікарські засоби постійно виробляються і контролюються відповідно до стандартів якості, які відповідають їх призначенню, а також відповідно до вимог реєстраційного досьє, досьє досліджуваного лікарського засобу для клінічних випробувань або специфікації на цю продукцію;
несуттєве порушення — порушення вимог GMP, яке не належить до критичних або суттєвих порушень (така класифікація присвоюється, якщо невідповідність оцінена як така або якщо не вистачає інформації для оцінки невідповідності як критичної чи суттєвої);
офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP — сертифікат відповідності умов виробництва лікарських засобів вимогам GMP, виданий уповноваженим органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною (відомості з офіційного електронного реєстру — для FDA США)PIC/S, або ліцензія на виробництво лікарських засобів (якщо уповноваженим органом країни — члена ЄС, Великої Британії або країни, що має угоду про взаємне визнання з ЄС або з УкраїноюPIC/S не передбачена видача сертифіката відповідності умов виробництва лікарських засобів вимогам GMP);
первинна експертиза — перевірка комплектності поданих документів та відповідності таких документів законодавству, у тому числі вимогам цього Порядку, яка проводиться працівниками Держлікслужби України;
підтвердження відповідності умов виробництва лікарських засобів вимогам GMP — процедура підтвердження Держлікслужбою України відповідності умов виробництва лікарських засобів вимогам GMP шляхом видачі сертифіката відповідності умов виробництва лікарських засобів вимогам GMP або висновку щодо підтвердження відповідності виробництва лікарського засобу вимогам GMP;
представник Заявника (уповноважена особа, що знаходиться в Україні та виступає від імені Заявника) — юридична або фізична особа, яка діє на підставі відповідного доручення (довіреності), у якому Заявником надано право представляти його інтереси в Україні при проведенні процедур підтвердження відповідності умов виробництва лікарських засобів вимогам GMP;
прекваліфікація лікарського засобу — стандартизована процедура/програма Всесвітньої організації охорони здоров’я (ВООЗ),ВООЗ, яка проводиться з метою оцінки якості, безпечності та ефективності лікарського засобу;
препарат обмеженого застосування (препарат-сирота) — лікарський засіб, що призначений для діагностики, профілактики чи лікування рідкісного захворювання, тобто захворювання, що загрожує життю чи призводить до втрати працездатності (зазвичай не більше 5 осіб з кожних 10000 жителів на дату подання заяви про державну реєстрацію);
продукція «in bulk» — будь-який лікарський засіб, призначений для виробництва готового лікарського засобу, який пройшов усі стадії технологічного процесу, крім стадії фасування та/або кінцевого пакування і маркування;
сертифікат відповідності умов виробництва лікарських засобів вимогам GMP (далі — Сертифікат) — документ, виданий Держлікслужбою України за результатами інспектування, який засвідчує відповідність умов виробництва лікарських засобів чинним в Україні вимогам GMP;
складний виробничий процес — процес, для якого навіть незначні відхилення в контрольних параметрах можуть призвести до отримання неоднорідного продукту або продукту, який не відповідає вимогам специфікації (наприклад, процеси гомогенізації або грануляції для твердих лікарських форм з низькою дозою, препарати пролонгованої або відкладеної дії, стерильні продукти);
спеціалізована експертиза — експертиза поданих документів на відповідність вимогам GMP, аналіз їх повноти і достовірності наданої інформації;
суттєве порушення — порушення, яке не є критичним, але призвело або може призвести до виробництва лікарського засобу, який не відповідає вимогам реєстраційного досьє на цей лікарський засіб, або при виробництві лікарського засобу не додержуються вимоги належної виробничої практики, гармонізованої із законодавством ЄС, або полягає в невідповідній процедурі випуску серій чи неналежному виконанні уповноваженою особою суб`єкта господарюванняє суттєвим порушенням вимог GMP, або є суттєвим порушенням ліцензійних умов, або полягає в невідповідній процедурі випуску серій чи неналежному виконанні Уповноваженою особою своїх обов’язків, або є комбінацією декількох несуттєвих порушень, кожне з яких власне не може класифікуватися як суттєве порушення, але разом вони мають бути класифіковані та відображені ув звіті як суттєве порушення;
угода про взаємне визнання — угода про взаємне визнання результатів інспектування на відповідність умов виробництва лікарських засобів вимогам GMP;
фармацевтична система якості — система управління, що спрямовує та контролює діяльність суб’єкта господарювання щодо якості.
3. Підтвердження відповідності умов виробництва лікарських засобів чинним в Україні вимогам GMP запроваджено з метою доведення, що лікарські засоби постійно виробляються і контролюються згідно зі стандартами якості, які відповідають їх призначенню, а також відповідно до вимог реєстраційного досьє, досьє досліджуваного лікарського засобу для клінічних випробувань або специфікації на цю продукцію. Підтвердження відповідності умов виробництва лікарських засобів, у тому числі активних фармацевтичних інгредієнтів (субстанцій), вимогам GMP здійснюється на добровільних засадах за бажанням заявника.
4. Підтвердження відповідності умов виробництва лікарських засобів вимогам GMP для резидентів та нерезидентів здійснюється Держлікслужбою України шляхом проведення експертизи документів, поданих відповідно до цього Порядку, та інспектування виробництва у випадках, передбачених цим Порядком.
Електронний портал Держлікслужби повинен бути доступним для осіб з інвалідністю та відповідати вимогам ДСТУ EN 301 549:2022 (EN 301 549 V3.2.1 (2021-03), IDT) «Інформаційні технології. Вимоги щодо доступності продуктів та послуг ІКТ», прийнятого наказом державного підприємства «Український науково-дослідний і навчальний центр проблем стандартизації, сертифікації та якості» від 05 травня 2022 року № 68.
За наявності запровадженого електронного порталу Держлікслужби для подання документів для підтвердження відповідності умов виробництва лікарських засобів вимогам GMP документообіг здійснюється з дотриманням вимог законодавства про електронні документи та електронний документообіг.
5. Відповідно до цього Порядку проводиться підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики на виробничих дільницях згідно із відповідною заявою:
на видачу сертифіката відповідності умов виробництва лікарських засобів вимогам належної виробничої практики згідно з додатком 1 до цього Порядку (далі — Заява на видачу Сертифіката);
на видачу висновку щодо підтвердження відповідності умов виробництва лікарських засобів вимогам GMP згідно з додатком 2 до цього Порядку (далі — Заява на видачу Висновку).
6. Згідно з цим Порядком Держлікслужба України видає документи, що підтверджують відповідність умов виробництва лікарських засобів вимогам GMP:
сертифікат відповідності умов виробництва лікарських засобів вимогам належної виробничої практики за формою згідно з додатком 3 (Форма 1) до цього Порядку;
висновок щодо підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики за формою згідно з додатком 4 до цього Порядку.
ІІ. Етапи підтвердження відповідності умов виробництва лікарських засобів вимогам GMP
1. Процедура підтвердження відповідності умов виробництва лікарських засобів вимогам GMP включає такі етапи:
- подання до Держлікслужби України Заяви на видачу Сертифіката або Заяви на видачу Висновку та комплекту документів, передбаченого пунктами 2, 3, 8 цього розділу;
- перевірку та опрацювання поданої Заяви на видачу Сертифіката або Заяви на видачу Висновку та комплекту документів (спеціалізована експертиза);(включаючи первинну експертизу та спеціалізовану експертизу);
- інспектування виробництва лікарських засобів за місцем провадження діяльності, в тому числі лабораторій, що здійснюють контроль якості за контрактом (договором), складських зон за контрактом (договором), у випадках, передбачених цим Порядком;
- прийняття рішення щодо видачі документа про відповідність умов виробництва лікарських засобів вимогам GMP або вмотивованого висновку про відмову у його видачі;
- внесення змін до виданого документа про відповідність виробництва лікарських засобів вимогам GMP у випадках, передбачених пунктом 12 розділу V цього Порядку.
2. Для підтвердження відповідності умов виробництва лікарських засобів вимогам GMP Заявник (представник Заявника) подає до Держлікслужби України Заяву на видачу Сертифіката або Заяву на видачу Висновку, до яких додаються такі документи:
1) копія заяви про державну реєстрацію (перереєстрацію) лікарського засобу, що була подана до МОЗ України, засвідчена підписом і печаткою (за наявності) Заявника або його представника, — для лікарських засобів, що подаються на державну реєстрацію (перереєстрацію), або при внесенні відповідних змін, що стосуються зміни виробника або його виробничих потужностей або внесення додаткового виробника до реєстраційних матеріалів зареєстрованих в Україні лікарських засобів, або зміни назви лікарського засобу, або зміни Заявника;(за наявності);
2) засвідчена в установленому порядку копія офіційного документа, який дає право на здійснення господарської діяльності з виробництва лікарських засобів та виданий відповідним державним органом країни, де розташоване виробництво, на виробничу дільницю, що вказана в Заяві на видачу Сертифіката (Заяві на видачу Висновку), та засвідчений в установленому порядку переклад українською та англійською мовами (для нерезидентів). Якщо згідно із законодавством країни-виробника ліцензія на виробництво існує лише в електронному вигляді, мають бути надані роздруківка із посиланням на відповідний офіційний сайт, засвідчена підписом та/або (за наявності) печаткою Заявника (представника Заявника), та переклад українською мовою.
Якщо внесено до бази даних EudraGMP або електронного реєстру FDA США, Заявник (представник Заявника) надає засвідчену Заявником/представником Заявника роздруківку з бази даних EudraGMP або електронного реєстру FDA США із засвідченим перекладом на українську мову;
3) засвідчена в установленому порядку копія офіційного документа, виданого державним органом країни, де розташовано виробництво, про відповідність вимогам GMP виробничої дільниці, що вказана в Заяві (за наявності); засвідчені в установленому порядку копії додатків до цього документа з переліком лікарських засобів (за наявності) та засвідчені в установленому порядку переклади цих документів українською та англійською мовами.
Якщо внесено до бази даних EudraGMP, Заявник (представник Заявника) надає засвідчену Заявником/представником Заявника роздруківку з бази даних EudraGMP із засвідченим перекладом на українську мову;
4) засвідчена в установленому порядку копія офіційного документа щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданого уповноваженим органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною.PIC/S, засвідчені в установленому порядку копії додатків до такого документа з переліком лікарських засобів (за наявності) та засвідчені в установленому порядку переклади цих документів українською та англійською мовами.
Якщо внесено до бази даних EudraGMP або електронного реєстру FDA США, Заявник (представник Заявника) надає роздруківку з цієї бази даних та переклад українською мовою, у тому числі із додатками (за наявності). Ці документи повинні бути засвідчені Заявником (представником Заявника);
5) копія досьє виробничої дільниці (Site Master File) та його переклад на українську та/або англійську мову, засвідчені Заявником (представником Заявника) (для резидентів та нерезидентів, за винятком виробників, виробничі потужності яких знаходяться на території країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною);країн-членів PIC/S);
6) засвідчена Заявником (представником Заявника) копія звіту, складеного за результатами останньої перевірки, проведеної уповноваженим органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною (для нерезидентів, за винятком виробників, виробничі потужності яких знаходяться на території країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або Україною). При цьому перевірка повинна бути проведена не раніше ніж за 3 роки до подання Заяви;
6) засвідчена Заявником (представником Заявника) копія звіту, складеного за результатами останньої перевірки, проведеної уповноваженим органом країни – члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною (для нерезидентів, за винятком виробників, виробничі потужності яких знаходяться на території країни – члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або Україною). При цьому перевірка повинна бути проведена не раніше ніж за 5 років до подання Заяви.
У разі відмови виробника у наданні копії звіту, Заявник може звернутися до Держлікслужби із клопотанням про здійснення запиту щодо надання такого звіту уповноваженим органом країни-члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною, що здійснював зазначену перевірку. Після отримання звіту, Держлікслужба долучає його до комплекту документів відповідної Заяви. Про отримання звіту або відмови у його наданні Держлікслужба повідомляє Заявника в паперовій або електронній формі;
6) засвідчена Заявником (представником Заявника) копія звіту, складеного за результатами останньої перевірки, проведеної уповноваженим органом країни-члена PIC/S (для нерезидентів, виробничі потужності яких розташовані за межами території країн-членів PIC/S). При цьому перевірка повинна бути проведена не раніше ніж за 3 роки до подання Заяви. У разі відмови виробника у наданні копії звіту Заявник може звернутися до Держлікслужби України із клопотанням про здійснення запиту щодо надання такого звіту уповноваженим органом країни-члена PIC/S, що здійснював зазначену перевірку. Після отримання звіт долучається Держлікслужбою України до комплекту документів відповідної Заяви. Про отримання звіту або відмови у його наданні Держлікслужба України повідомляє Заявника в письмовій формі;
7) інформація щодо останньої перевірки, проведеної за процедурою прекваліфікації ВООЗ (за наявності). При цьому перевірка повинна бути проведена не раніше ніж за 3 роки до подання Заяви на видачу Сертифіката або Висновку (якщо немає інших поданих Заявником або представником Заявника відповідним чином оформлених копій офіційних документів ВООЗ);
8) довідка про якість продукції, що виробляється, згідно з додатком 5 до цього Порядку;
9) довідка про результати перевірок виробничої дільниці, проведених органами державного контролю, за формою згідно з додатком 6 до цього Порядку, що зазначена в Заяві на видачу Сертифіката (Заяві на видачу Висновку);
10) Загальний перелік номенклатури продукції за формою згідно з додатком 7 до цього Порядку (за формою 1 — у разі подання Заяви на видачу Висновку; за формою 2 — у разі подання Заяви на видачу Сертифіката), в якому наводиться перелік лікарських засобів, які зареєстровані в Україні та/або знаходяться в процесі реєстрації/внесення змін і виробництво яких вже здійснюється або планується здійснювати на виробничій дільниці, що вказана в Заяві на видачу Висновку (Заяві на видачу Сертифіката). Такий перелік подається в письмовій формі та на електронному носії інформації (файл Excel). У разі коли Заявником є власник ліцензії на виробництво для виробничої дільниці, зазначеної у Заяві на видачу Висновку (Заяві на видачу Сертифіката), перелік може містити лікарські засоби одного або декількох власників реєстраційних посвідчень.
10) Загальний перелік номенклатури продукції за формою згідно з додатком 7 до цього Порядку (за формою 1 — у разі подання Заяви на видачу Висновку; за формою 2 — у разі подання Заяви на видачу Сертифіката), в якому наводиться перелік лікарських засобів, які зареєстровані в Україні та/або плануються до реєстрації і виробництво яких вже здійснюється (за наявності) або планується здійснювати на виробничій дільниці, що вказана в Заяві на видачу Висновку (Заяві на видачу Сертифіката). Такий перелік подається в письмовій формі та на електронному носії інформації (файл Excel). Перелік може містити лікарські засоби, що виробляються на відповідній виробничій дільниці для одного та/або декількох Заявників;
11) засвідчені Заявником (представником Заявника) копія сертифіката лікарського засобу для міжнародної торгівлі (certificate of a pharmaceutical product) або копія реєстраційного посвідчення (marketing authorization), виданого компетентним органом країни виробника лікарського засобу або власника реєстраційного посвідчення (заявника) або іншим регуляторним органом країни з суворою регуляторною системою, на ринку якої розміщено лікарський засіб, із зазначенням назви документа та найменування компетентного органу, що його видав, дати видачі (для незареєстрованих лікарських засобів, які плануються до реєстрації або перереєстрації в Україні);
11) засвідчені Заявником (представником Заявника) копія сертифіката лікарського засобу для міжнародної торгівлі (certificate of a pharmaceutical product), виданого компетентним органом країни виробника лікарського засобу або власника реєстраційного посвідчення (заявника), або іншим регуляторним органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною, на ринку якої розміщено лікарський засіб, із зазначенням назви документа та найменування компетентного органу, що його видав, дати видачі (для незареєстрованих лікарських засобів, які знаходяться в процесі реєстрації/внесенні змін в Україні), назви та адрес виробничих дільниць;
12) гарантійний лист згідно з додатком 8 до цього Порядку;
13) засвідчені Заявником (представником Заявника) копії реєстраційних посвідчень (marketing authorization), виданих компетентним органом країни ЄС, уповноважений орган якої видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, або виданих компетентними органами інших країн — членів ЄС, Великої Британії або країн, які мають угоду про взаємне визнання з ЄС або з Україною (подається для лікарських засобів, виробництво хоча б однієї стадії яких здійснюється не в країні — члені ЄС, Великої Британії або в країні, яка не має угоди про взаємне визнання з ЄС або з Україною, включаючи контрактні виробничі дільниці);
14) засвідчені Заявником (представником Заявника) та викладені українською та/або англійською мовами Досьє виробничої дільниці для установ з отримання плазми та/або Досьє виробничої дільниці для місць зберігання плазми.
12) гарантійні листи згідно з додатком 8 (за формою 1 — про суттєві зміни, які стосуються виробничої дільниці, що пройшла підтвердження відповідності умов виробництва лікарських засобів вимогам GMP; за формою 2 — про завершення процедури підтвердження або надання звіту останньої перевірки, проведеної уповноваженим органом країни-члена PIC/S).
У випадку, якщо будь-які документи із зазначеного вище переліку, які подано до Держлікслужби України з метою отримання Сертифіката або Висновку, містять конфіденційну інформацію, яку виробник не може розкрити Заявнику (представнику Заявника) в Україні, виробник може надіслати такі документи безпосередньо до Держлікслужби України. Після отримання таких документів Держлікслужба України своїм листом невідкладно інформує Заявника (представника Заявника) про їх надходження та розгляд Заяви на видачу Сертифіката або Заяви на видачу Висновку та документів, які додаються.
3. Для виробників-резидентів підтвердження відповідності умов виробництва лікарських засобів вимогам GMP може здійснюватися Держлікслужбою за результатами планової перевірки додержання відповідних ліцензійних умов. За відсутності критичних порушень та/або численних (не менше 6 у сукупності, по конкретних лікарських засобах або процесам) суттєвих порушень відповідності вимогам GMP виробничих дільниць або окремих лікарських засобів в акті планової перевірки додержання ліцензійних умов Держлікслужба відповідно до розділу V цього Порядку, у разі прийнятного плану коригувальних та запобіжних дій за результатами інспектування, видає ліцензіату Сертифікат протягом 30 робочих днів з дня отримання від нього листа щодо видачі Сертифіката із загальним переліком номенклатури продукції у паперовому вигляді та на електронному носії. Лист подається ліцензіатом до Держлікслужби протягом 15 робочих днів після проведення планової перевірки додержання ліцензійних умов.
У разі наявності критичних порушень та/або численних (не менше 6 у сукупності, по конкретних лікарських засобах або процесам) суттєвих порушень відповідності вимогам GMP виробничих дільниць або окремих лікарських засобів, виявлених під час останньої планової перевірки додержання ліцензійних умов, Держлікслужба приймає рішення про відмову у видачі Сертифіката згідно з розділом V цього Порядку. За наявності документальних підтверджень про усунення критичних порушень та/або численних (не менше 6 у сукупності, по конкретних лікарських засобах або процесам) суттєвих порушень відповідності вимогам GMP виробничих дільниць або окремих лікарських засобів, виявлених під час останньої планової перевірки додержання ліцензійних умов, проводиться інспектування за місцем провадження виробництва (виробничої дільниці) на підставі поданої ліцензіатом Заяви на видачу Сертифіката.
3. Для виробників-резидентів підтвердження відповідності умов виробництва лікарських засобів вимогам GMP здійснюється Держлікслужбою України за результатами планової перевірки додержання відповідних ліцензійних умов. За відсутності критичних порушень в акті планової перевірки додержання ліцензійних умов Держлікслужба України відповідно до розділу V цього Порядку видає ліцензіату Сертифікат протягом 30 робочих днів з дня отримання від нього листа із загальним переліком номенклатури продукції у паперовому вигляді та на електронному носії щодо видачі Сертифіката. Лист подається ліцензіатом до Держлікслужби України протягом 15 робочих днів після проведення планової перевірки додержання ліцензійних умов.
У разі наявності критичних порушень, виявлених під час останньої планової перевірки додержання ліцензійних умов, Держлікслужба України приймає рішення про відмову у видачі Сертифіката згідно з розділом V цього Порядку. За наявності документальних підтверджень про усунення критичних порушень, виявлених під час останньої планової перевірки додержання ліцензійних умов, проводиться інспектування за місцем провадження виробництва (виробничої дільниці) відповідно до поданої ліцензіатом Заяви на видачу Сертифіката.
4. Заява та документи, що додаються до неї, приймаються за описом документів згідно з додатком 9 до цього Порядку, копія якого видається Заявнику (представнику Заявника) з відміткою про дату прийняття документів Держлікслужбою та підписом відповідальної особи.
4. Заява та документи, що додаються до неї, приймаються за описом документів, що додаються до заяви на видачу сертифіката відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (до заяви на видачу висновку щодо підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики), згідно з додатком 9 до цього Порядку, копія якого видається Заявнику (представнику Заявника) з відміткою про дату прийняття документів Держлікслужбою України та підписом відповідальної особи.
5. Держлікслужба України здійснює первинну експертизу поданих документів з метою перевірки їх комплектності та відповідності форми таких документів законодавству, у тому числі вимогам цього Порядку.
5. Відповідна заява та комплект документів для підтвердження відповідності умов виробництва лікарських засобів вимогам GMP, листи Заявників та/або представників Заявників можуть подаватися в електронному вигляді за наявності запровадженого електронного порталу Держлікслужби для подання таких документів.
У разі подання відповідних документів через електронний портал Держлікслужби на електронні документи накладається електронний підпис Заявника (представника Заявника), що базується на кваліфікованому сертифікаті електронного підпису, відповідно до вимог Закону України «Про електронні довірчі послуги».
6. Для проведення лабораторного аналізу якості зразків лікарських засобів, експертиз, інспектування, виконання окремих видів робіт тощо Держлікслужбою України можуть залучатися підприємства, установи, організації, окремі вчені та фахівці (за їх згодою).
7. Для нерезидентів, які не мають офіційних документів щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданих уповноваженим органом країни-члена ЄС, Великої БританіїPIC/S, або країни, яка має угоду про взаємне визнання з ЄС або з Україною,якщо виробництво лікарських засобів здійснюється у країні, з якою Україна не має міжнародного договору про взаємне визнання результатів інспектування щодо відповідності виробництва лікарських засобів вимогам GMP, додатково до проведення експертизи документів здійснюється інспектування виробництва (виробничої дільниці) відповідно до розділу ІV цього Порядку.
8. При проведенні підтвердження відповідності умов виробництва лікарських засобів вимогам GMP мають бути зазначені усі проміжні виробничі дільниці (включно з контрактними дільницями), що задіяні у процесі виробництва готового лікарського засобу. Всі стадії виробництва лікарських засобів (нерозфасована продукція, первинне та вторинне пакування, сертифікація серії) повинні відповідати вимогам GMP та мати відповідні Сертифікати, видані згідно з цим Порядком, крім випадків коли в комплекті документів надані:
Для проведення підтвердження відповідності умов виробництва лікарських засобів вимогам GMP, у процесі якого здійснюється випуск готових лікарських засобів із форми «in bulk», виробництво всієї продукції у формі «in bulk», яка використовується в процесі випуску цих лікарських засобів, повинно мати Сертифікати або Висновки, видані згідно з цим Порядком, крім таких випадків:
1) у разі якщо сертифікація серій готового лікарського засобу та видача дозволу на їх випуск здійснюються виробником на території країни-члена Європейського Союзу (далі — ЄС), яка є членом PIC/S, Заявник (представник Заявника) разом із Заявою на видачу Висновку подає:
перелік документів відповідно до пункту 2 цього розділу — для виробника, що здійснює видачу дозволу на випуск серій;
засвідчені підписом та печаткою (за наявності) Заявника або представника Заявника копії документів та їх переклади українською мовою, зазначені у підпунктах 2 та 4 пункту 2 цього розділу, — для проміжних виробничих дільниць, у тому числі контрактних, що задіяні у виробництві лікарського засобу та розташовані на території країни-члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною;члена ЄС, а також мають офіційні документи щодо відповідності умов виробництва лікарських засобів вимогам GMP, видані уповноваженим органом країни-члена PIC/S;
засвідчені підписом та печаткою (за наявності) Заявника або представника Заявника копії документів та їх переклади українською мовою, зазначені у підпунктах 2, 4, 6 пункту 2 цього розділу, — для проміжних виробничих дільниць, включно із контрактними виробничими дільницями, що задіяні у виробництві лікарського засобу та розташовані поза територією країни-члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною.члена ЄС, які мають офіційні документи щодо відповідності умов виробництва лікарських засобів вимогам GMP, видані уповноваженим органом країни-члена PIC/S. Копія документа, зазначеного у підпункті 6 пункту 2 цього розділу, для проміжної стадії виробництва (уключаючи контрактну виробничу ділянку), подається не пізніше шести місяців після отримання Висновку під гарантійні зобов’язання Заявника. У разі ненадання Заявником (представником Заявника) копії документа, зазначеного у підпункті 6 пункту 2 цього розділу, у шестимісячний строк Держлікслужба України приймає рішення про анулювання виданого Висновку або його переоформлення шляхом вилучення цього лікарського засобу із переліку лікарських засобів, який є невід’ємною частиною Висновку.
При цьому видача Держлікслужбою України окремих Висновків для проміжних виробничих дільниць (уключаючи контрактні виробничі дільниці) не здійснюється;
2) у разі якщо сертифікація серій готового лікарського засобу та видача дозволу на їх випуск здійснюються виробником, який має офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданий уповноваженим органом країни-члена PIC/S, Заявник (представник Заявника) разом із Заявою на видачу Висновку подає:
перелік документів, визначений пунктом 2 цього розділу, — для виробника, що здійснює видачу дозволу на випуск серій;
документи, зазначені в підпунктах 2, 4, 6 пункту 2 цього розділу, — для проміжних виробничих дільниць, уключаючи контрактні виробничі дільниці, що задіяні у виробництві лікарського засобу, які мають офіційні документи щодо відповідності умов виробництва лікарських засобів вимогам GMP, видані уповноваженим органом країни-члена PIC/S.
При цьому видача Держлікслужбою України окремих Висновків для проміжних виробничих дільниць (включаючи контрактні виробничі дільниці), що мають офіційні документи щодо відповідності умов виробництва лікарських засобів вимогам GMP, видані уповноваженим органом країни-члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною, не здійснюється.PIC/S, не здійснюється.
Для лікарського засобу, проміжні стадії виробництва (включаючи контрактні виробничі дільниці) якого здійснюються на виробничих дільницях, що не мають офіційних документів щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданих уповноваженим органом країни-члена PIC/S, на підставі гарантійних зобов’язань Заявника щодо завершення в строк не більше шести місяців з дати подання Заяви на видачу Висновку процедури підтвердження відповідності вимогам GMP Держлікслужбою України видається Висновок. У разі невиконання Заявником гарантійних зобов’язань Держлікслужба України приймає рішення про анулювання виданого Висновку або його переоформлення шляхом вилучення такого лікарського засобу із переліку лікарських засобів, який є невід’ємною частиною Висновку.
9. При проведенні підтвердження відповідності умов виробництва лікарських засобів вимогам GMP для резидентів та нерезидентів з метою отримання Сертифіката або Висновку для установ з отримання плазми та/або місць зберігання плазми, включно, якщо установи з отримання плазми та/або місця зберігання плазми є проміжними виробничими дільницями або контактними, в комплекті документів до відповідної Заяви повинні бути надані зазначені у підпункті 14 пункту 2 цього розділу Досьє виробничої дільниці для установ з отримання плазми та/або Досьє виробничої дільниці для місць зберігання плазми, які складені не пізніше, ніж за шість місяців від дати подання відповідної Заяви на видачу Сертифіката або Висновку.
10. У разі оголошення Україною чи іншою країною — виробником надзвичайного стану, надзвичайної ситуації, воєнного стану, в разі стихійного лиха, визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, в тому числі враховуючи санітарно-епідеміологічну ситуацію, Заяви на видачу Сертифіката або Висновку з відповідними комплектами документів (без опису згідно з додатком 9 до цього Порядку) можуть бути направлені до Держлікслужби поштовим відправленням. Після реєстрації відповідальною особою Держлікслужби Заяви на видачу Сертифіката або Висновку та оформлення опису згідно з додатком 9 до цього Порядку представнику заявника електронною поштою повідомляється номер та дата їх реєстрації.
11. При здійсненні закупівель, що проводяться особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я виробництво лікарського засобу, який не зареєстрований в Україні на час проведення процедури закупівлі, але зареєстрований компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстрований компетентним органом Європейського Союзу за централізованою процедурою повинно відповідати вимогам GMP. При проведенні підтвердження відповідності умов виробництва лікарських засобів вимогам GMP мають бути зазначені усі проміжні виробничі дільниці (включно з контрактними дільницями), що задіяні у процесі виробництва готового лікарського засобу.
Для підтвердження відповідності умов виробництва лікарського засобу вимогам GMP Заявник (представник Заявника) подає до Держлікслужби Заяву на видачу Сертифіката або Заяву на видачу Висновку та документи, визначені пунктом 2 розділу II цього Порядку.
ІІІ. Строки підтвердження відповідності умов виробництва лікарських засобів вимогам GMP
1. Строк проведення первинної експертизи поданих документів, що проводиться Держлікслужбою України з метою перевірки їх комплектності, відповідності форми таких документів законодавству, у тому числі вимогам цього Порядку, становить не більше 5 робочих днів після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), крім випадків:
1) для лікарських засобів, призначених для лікування туберкульозу, ВІЛ/СНІД, вірусних гепатитів, онкологічних та рідкісних (орфанних) захворювань, які зареєстровані як лікарський засіб компетентним органом Сполучених Штатів Америки, Швейцарії, Японії, Австралії, Канади або Європейського Союзу, — не більше ніж 2 робочих дні після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), у разі звернення Заявника (представника Заявника);
2) для лікарських засобів, що зареєстровані за централізованою процедурою Європейським агентством з медичних продуктів (EMA), та для лікарських засобів, що пройшли процедуру прекваліфікації ВООЗ та включені до переліку ВООЗ прекваліфікованих лікарських засобів, — не більше ніж 2 робочих дні після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), у разі звернення Заявника (представника Заявника).
1.2. Спеціалізована експертиза, до якої можуть залучатися фахівці або уповноважені Держлікслужбою України організації, проводиться з метою складання вмотивованого висновку щодо підтвердження відповідності умов виробництва лікарських засобів вимогам GMP.
Спеціалізована експертиза за умови надання офіційного документа щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданого уповноваженим органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною, проводиться не більше, ніж 15 робочих днів з дати реєстрації заяви на видачу Сертифікату або Висновку, крім випадків:
1) для лікарських засобів, призначених для профілактики, діагностики та лікування туберкульозу, ВІЛ/СНІД, вірусних гепатитів, онкологічних та рідкісних (орфанних) захворювань, для лікарських засобів, які реєструються в Україні за спрощеною процедурою реєстрації згідно Закону України « Про лікарські засоби» , для лікарських засобів, які включені до протоколів лікування України у випадку офіційного визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, — не більше ніж 5 робочих днів після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), у разі зазначення цієї інформації у поданій Заяві на видачу Сертифіката (Заяві на видачу Висновку);
2) для лікарських засобів, що зареєстровані за централізованою процедурою Європейським агентством з лікарських засобів (European Medicines Agency, EMA), та для лікарських засобів, що пройшли процедуру прекваліфікації ВООЗ та включені до переліку ВООЗ прекваліфікованих лікарських засобів, — не більше ніж 5 робочих днів після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), у разі зазначення цієї інформації у поданій Заяві на видачу Сертифіката (Заяві на видачу Висновку);
3) для лікарських засобів, незареєстрованих в Україні, але зареєстрованих компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстрованих компетентним органом Європейського Союзу за централізованою процедурою, які закуповуються особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я — не більше ніж 5 робочих днів після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), у разі зазначення цієї інформації у поданій Заяві на видачу Сертифіката (Заяві на видачу Висновку) та надання належним чином засвідченої копії документа, що підтверджує визначення переможця процедури закупівлі.
Спеціалізована експертиза за умови надання офіційного документа щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданого уповноваженим органом країни-члена PIC/S, проводиться не більше ніж 10 робочих днів після проведення первинної експертизи, крім випадків:
1) для лікарських засобів, призначених для лікування туберкульозу, ВІЛ/СНІД, вірусних гепатитів, онкологічних та рідкісних (орфанних) захворювань, які зареєстровані як лікарський засіб компетентним органом Сполучених Штатів Америки, Швейцарії, Японії, Австралії, Канади або Європейського Союзу, — не більше ніж 3 робочих дні після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), у разі звернення Заявника (представника Заявника);
2) для лікарських засобів, що зареєстровані за централізованою процедурою Європейським агентством з медичних продуктів (EMA), та для лікарських засобів, що пройшли процедуру прекваліфікації ВООЗ та включені до переліку ВООЗ прекваліфікованих лікарських засобів, — не більше ніж 3 робочих дні після реєстрації Заяви на видачу Сертифіката (Заяви на видачу Висновку), у разі звернення Заявника (представника Заявника).
В усіх інших випадках спеціалізована експертиза проводиться не більше ніж 20 робочих днів.15 робочих днів після проведення первинної експертизи.
Для лікарських засобів, призначених для профілактики, діагностики та лікування туберкульозу, ВІЛ/СНІД, вірусних гепатитів, онкологічних та рідкісних (орфанних) захворювань, для лікарських засобів, що зареєстровані за централізованою процедурою EMA, для лікарських засобів, що пройшли процедуру прекваліфікації ВООЗ та включені до переліку ВООЗ прекваліфікованих лікарських засобів, а також для лікарських засобів, які реєструються в Україні за спрощеною процедурою реєстрації згідно Закону України « Про лікарські засоби» , для лікарських засобів, які включені до протоколів лікування України у випадку офіційного визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, для лікарських засобів, незареєстрованих в Україні, але зареєстрованих компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстрованих компетентним органом Європейського Союзу за централізованою процедурою, які закуповуються особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я, у разі зазначення цієї інформації у відповідній Заяві спеціалізована експертиза здійснюється позачергово.
2. Під час проведення спеціалізованої експертизи береться до уваги інформація щодо результатів проведення інспектувань з боку Держлікслужби даної виробничої дільниці за попередні роки, крім випадків, якщо ця інформація вже була предметом перевірки з боку Держлікслужби, а також наявність документальних підтверджень усунення критичних, суттєвих та несуттєвих порушень, встановлених Держлікслужбою під час цих інспектувань та/або планової та/або позапланової перевірок додержання ліцензійних умов (для резидентів), інформація щодо вилучення з обігу в установленому порядку серій лікарського засобу, які вироблялись на даній дільниці, що пов’язані з якістю лікарського засобу.
3. Під час проведення спеціалізованої експертизи враховується інформація щодо результатів проведення інспектувань з боку Держлікслужби України даної виробничої дільниці за попередні роки та наявність документальних підтверджень усунення критичних, суттєвих та несуттєвих порушень, встановлених Держлікслужбою України під час цих інспектувань, крім випадків, якщо ця інформація вже була предметом перевірки з боку Держлікслужби України.
За необхідності під час проведення експертизи Держлікслужбою України може бути направлений відповідний запит до компетентного органу країни-члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з УкраїноюPIC/S для з’ясування питань, що виникли під час проведення експертизи, про що повідомляється Заявник (представникЗаявника (представника Заявника) протягом 10 робочих днів від дати направлення запиту. Час, потрібний для отримання відповіді на запит, не включається до строків проведення спеціалізованої експертизи.
3.4. У разі некомплектності документів, виявленої під час проведення первинної експертизи, та/або невідповідностей, виявлених під час проведення спеціалізованої експертизи, вимогам цього Порядку доданих до Заяви на видачу Сертифіката (Заяви на видачу Висновку) документів Заявнику (представнику Заявника) надається про це письмове повідомлення. Час, необхідний для усунення Заявником (представником Заявника) виявлених порушень та/або для надання необхідних документів, не включається до строків проведення первинної або спеціалізованої експертизи.
Строк розгляду наданих Заявником (представником Заявника) додаткових документів або відповідей щодо виявлених невідповідностей складає не більше 15 календарних днів.
4.5. Якщо Заявник (представник Заявника) протягом 30 робочих днів після отримання повідомлення не усуває виявлені порушення або не надає необхідного комплекту документів відповідно до вимог цього Порядку, Заява на видачу Сертифіката (Заява на видачу Висновку) за рішенням, яке оформляється наказом Держлікслужби України, залишається без розгляду (із зазначенням причин), про що Держлікслужба України повідомляє Заявника (представника Заявника). У разі необхідності продовжити строк надання необхідної інформації Заявник (представник Заявника) повинен надати відповідне обґрунтування причини і необхідного йому додаткового строку.
5.6. У випадку, якщо умови виробництва лікарських засобів та контролю їх якості були предметом інспектування з боку Держлікслужби України за попередні роки, наступне інспектування здійснюється у разі, якщо є документальні підтвердження усунення критичних, суттєвих та несуттєвих порушень, встановлених під час попереднього(іх) інспектування(нь).
6.7. Під час складання плану та програми інспектування враховується необхідність перевірки усунення критичних та суттєвих та несуттєвих порушень, встановлених під час попереднього(іх) інспектування(нь) з боку Держлікслужби України за попередні роки умов виробництва лікарських засобів та контролю їх якості, крім випадків, якщо ця інформація вже була предметом перевірки з боку Держлікслужби України.
Копії плану та програми інспектування, які погоджуються Держлікслужбою України, надсилаються за місцезнаходженням Заявника або представника Заявника у строк не пізніше ніж за 10 робочих днів до дати початку інспектування, у тому числі у разі повторного інспектування за зверненням Заявника з метою перевірки усунення порушень, виявлених під час попереднього інспектування.
У разі наявності обґрунтованих зауважень з боку Заявника щодо участі в інспектуванні окремих інспекторів ці зауваження повинні бути надіслані до Держлікслужби України не пізніше ніж за 5 днів до проведення інспектування з метою їх урахування.
7.8. Строк проведення інспектування за місцем провадження діяльності має становити не більше 15 робочих днів.
8.9. Строк складання звіту за результатами інспектування виробництва становить не більше 10 робочих днів з дати закінчення інспектування.
Строк складання звіту за результатами інспектування виробництва лікарських засобів, незареєстрованих в Україні, але зареєстрованих компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстрованих компетентним органом Європейського Союзу за централізованою процедурою, які закуповуються особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я, становить не більше 5 робочих днів з дати закінчення інспектування.
9.10. Лабораторний аналіз якості зразків лікарських засобів, що були відібрані при проведенні інспектування, проводиться в строк не більше ніж 21 робочий день з дня надходження відібраних зразків до атестованої лабораторії за направленням Держлікслужбиз контролю якості та безпеки лікарських засобів або в строк, передбачений відповідними методами контролю якості лікарських засобів виробника. При цьому наявність необхідних стандартних зразків забезпечує Заявник. Час, потрібний Заявнику для забезпечення стандартними зразками, не включається до строків виконання лабораторного аналізу.
Відбір зразків лікарських засобів, що плануються до промислового випуску та знаходяться на стадії державної реєстрації, не здійснюється.
10.11. Розгляд Держлікслужбою України на робочому засіданні звіту, складеного за результатами інспектування, з метою його оцінки та обґрунтованості викладених у ньому порушень здійснюється не пізніше 10 робочих днів від дати його складання. У разі наявності наданого до Держлікслужби України письмового звернення з обґрунтованими зауваженнями з боку Заявника та/або виробника щодо проведеного інспектування, час, необхідний для розгляду результатів інспектування, може бути продовжено до закінчення розгляду цих зауважень, що становить не більше 15 робочих днів з дати їх надходження до Держлікслужби України, якщо не потребується додатковий час Заявнику/виробнику для надання необхідних письмових відповідей.
11. Письмове12. Оформлення та видача Сертифіката або Висновку або письмового повідомлення щодо неможливості видачі Сертифіката або Висновку становлять не більше 10 робочих днів після прийняття відповідного рішення Держлікслужбою України. Час, потрібний Заявнику для усунення зауважень за результатами спеціалізованої експертизи, розгляду Держлікслужбою України письмового звернення Заявника та/або виробника з обґрунтованими зауваженнями щодо проведеного інспектування (у разі його надходження після розгляду результатів інспектування), не включається до строків оформлення та видачі Сертифіката або Висновку.
12. Проєкт13. Проект Сертифіката або Висновку з відповідним переліком лікарських засобів надсилається електронною поштою або факсом Заявнику (представнику Заявника) з метою його погодження. Заявник (представник Заявника) засвідчує підписом проєктпроект Сертифіката або Висновку з відповідним переліком лікарських засобів та надає його до Держлікслужби України. Час, потрібний Заявнику для погодження проєктупроекту Сертифіката або Висновку з відповідним переліком лікарських засобів, не включається до строків оформлення та видачі Сертифіката або Висновку.
13.14. Оформлення внесення змін до Висновку, Сертифіката або переліку лікарських засобів до Висновку чи Сертифіката або їх переоформлення здійснюються у порядку, визначеному пунктом 1211 розділу V цього Порядку, у строк не більше ніж 15 робочих днів. Час, потрібний Заявнику (представнику Заявника) для погодження проєктупроекту змін до Сертифіката, Висновку або переліку лікарських засобів, не включається до строків їх оформлення та видачі.
14. У разі наявності запровадженого електронного порталу Держлікслужби інформування з боку Держлікслужби Заявника (представника Заявника) або виробника, надання відповідних відповідей на зауваження з боку Заявника (представника Заявника) або виробника, надання плану та програми інспектування, звіту за результатами інспектування, видача або відмова у видачі Сертифікату або Висновку тощо здійснюється в електронному вигляді.
15. У період визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, що унеможливлює проведення інспектування за місцем провадження діяльності, в тому числі враховуючи санітарно-епідеміологічну ситуацію, Заявники (представники Заявників) можуть подати до Держлікслужби лист щодо проведення оцінки ризиків з метою перенесення строку наступної інспекції виробництва лікарського засобу на відповідність вимогам GMP та видачі Сертифіката з врахуванням інформації про останнє інспектування на відповідність виробництва вимогам GMP або останнє планове інспектування на відповідність ліцензійним умовам (для виробників-резидентів, якщо підтвердження відповідності умов виробництва лікарських засобів вимогам GMP здійснювалося Держлікслужбою за результатами планової перевірки додержання ліцензійних умов).
Заявник не може подавати заяву, передбачену абзацом першим цього пункту, якщо строк проведення останнього інспектування становить більше, ніж три роки. Звіти за результатами інспектування або акти за результатами планової перевірки додержання відповідних ліцензійних умов, строк проведення яких становить більше, ніж три роки, не можуть бути враховані під час проведення оцінки ризиків з метою перенесення строку наступної інспекції виробництва лікарського засобу на відповідність вимогам GMP.
У разі наявності в Держлікслужбі прийнятних документальних підтверджень усунення суттєвих та несуттєвих порушень, встановлених Держлікслужбою під час останнього інспектування на відповідність виробництва вимогам GMP або останнього планового інспектування на відповідність ліцензійним умовам, з врахуванням протоколу аналізу ризиків відповідно до додатку 15 цього Порядку, Держлікслужбою приймається рішення щодо видачі Сертифіката, який оформлюється відповідно до пункту 12 цього розділу Порядку за формою згідно з додатком 3 (Форма 1) до цього Порядку із зазначенням у розділі Сертифіката « Будь-які обмеження або пояснення, що мають відношення до цього сертифіката» інформації щодо застосування процедури оцінки ризиків під час його видачі.
Строк дії виданого Сертифіката становить один або півтора роки враховуючи проведений аналізів ризиків відповідно до додатку 15 цього Порядку.
Рішення про відмову у видачі Сертифіката за процедурою оцінки ризиків приймається у разі відсутності в Держлікслужбі документальних підтверджень усунення суттєвих та несуттєвих порушень, встановлених Держлікслужбою під час останнього інспектування на відповідність виробництва вимогам GMP або останнього планового інспектування на відповідність ліцензійним умовам (для виробників-резидентів, якщо підтвердження відповідності умов виробництва лікарських засобів вимогам GMP здійснювалося Держлікслужбою за результатами планової перевірки додержання ліцензійних умов).
16. Строки підтвердження відповідності умов виробництва лікарських засобів, незареєстрованих в Україні, але зареєстрованих компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстрованих компетентним органом Європейського Союзу за централізованою процедурою, які закуповуються особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я чинним в Україні вимогам належної виробничої практики, включаючи строки проведення інспектування за місцем провадження діяльності (за потреби у передбачених законодавством випадках), становлять не більше 40 календарних днів. До зазначеного строку не включається час, необхідний заявнику для виправлення ним помилок у поданих документах, усунення виявлених порушень та/або для надання додаткових документів.
ІV. Порядок проведення інспектування на відповідність умов виробництва лікарських засобів вимогам GMP
1. Інспектування здійснюється з метою оцінки відповідності умов виробництва лікарських засобів чинним в Україні вимогам GMP.
2. За результатами проведеної спеціалізованої експертизи не пізніше ніж через 5 робочих днів після її проведення Заявнику (представнику Заявника) надсилається повідомлення щодо необхідності проведення інспектування та надання до Держлікслужби України інформації про пропоновані з боку Заявника (представника Заявника) строки проведення інспектування. Строки проведення інспектування не можуть перевищувати шести місяців з дати відправлення такого повідомлення Заявнику (представнику Заявника), якщо немає інших строків, запропонованих Заявником (представником Заявника) із зазначенням об’єктивних причин.
Для лікарських засобів, призначених для профілактики, діагностики та лікування туберкульозу, ВІЛ/СНІД, вірусних гепатитів, онкологічних та рідкісних (орфанних) захворювань, для лікарських засобів, що пройшли процедуру прекваліфікації ВООЗ та включені до переліку ВООЗ прекваліфікованих лікарських засобів, для лікарських засобів, які реєструються в Україні за спрощеною процедурою реєстрації згідно Закону України « Про лікарські засоби», для лікарських засобів, які включені до протоколів лікування України у випадку офіційного визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, для лікарських засобів, незареєстрованих в Україні, але зареєстрованих компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстрованих компетентним органом Європейського Союзу за централізованою процедурою, які закуповуються особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я, у разі зазначення цієї інформації у відповідній Заяві інспектування здійснюється позачергово.інспектування здійснюється позачергово.
У разі ненадання Заявником (представником Заявника) відповіді щодо пропозицій до проведення інспектування протягом трьох місяців з дати відправлення такого повідомлення Заявнику (представнику Заявника) Заява на видачу Сертифіката (Заява на видачу Висновку) за рішенням, яке оформлюється наказом Держлікслужби України, залишається без розгляду (із зазначенням причин), про що письмово повідомляється Заявник (представникЗаявника (представника Заявника).
У разі надання Заявником (представником Заявника) без зазначення об’єктивних причин пропозицій щодо проведення інспектування у строки, що перевищують шість місяців з дати відправлення повідомлення Заявнику (представнику Заявника), Заява на видачу Сертифіката (Заява на видачу Висновку) за рішенням, яке оформлюється наказом Держлікслужби, залишається без розгляду, про що письмово повідомляється Заявник (представник Заявника).
При врахуванні Держлікслужбою наданих Заявником (представником Заявника) об’єктивних причин інспектування може бути проведено у строк не більше одного календарного року від дати подання до Держлікслужби Заяви на видачу Сертифіката (Заяви на видачу Висновку). У разі не проведення такого інспектування Заява на видачу Сертифіката (Заява на видачу Висновку) за рішенням, яке оформлюється наказом Держлікслужби, залишається без розгляду, про що письмово повідомляється Заявник (представник Заявника).
3. За необхідності під час спеціалізованої експертизиперед проведенням інспектування інспектори мають право ознайомитися із реєстраційними матеріалами на зареєстровані лікарські засоби та/або на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію) або при внесенні відповідних змін до реєстраційних матеріалів на зареєстровані в Україні лікарські засоби., про що повідомляється Заявника (представника Заявника). Спеціалізована експертиза може бути подовжена на час, який необхідний Заявнику (представнику Заявника) з метою надання таких документів, якщо про це надано письмове звернення з боку Заявника (представника Заявника). Реєстраційні матеріали подаються до Держлікслужби з супровідним листом.
У разі ненадання Заявником (представником Заявника) зазначених реєстраційних матеріалів у строки, що перевищують шість місяців з дати відправлення повідомлення Заявнику (представнику Заявника) про необхідність їх подання з метою завершення спеціалізованої експертизи та подальшого інспектування, Заява на видачу Сертифіката (Заява на видачу Висновку) за рішенням, яке оформлюється наказом Держлікслужби, залишається без розгляду, про що письмово повідомляється Заявник (представник Заявника).
4. Інспектування здійснюється у таких випадках:
у разі звернення Заявника (представника Заявника);
для нерезидентів, які не мають офіційних документів щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданих уповноваженим органом країни-члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною;PIC/S;
у разі відсутності копій реєстраційних посвідчень (marketing authorization), виданих компетентним органом країни ЄС, уповноважений орган якої видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, або виданих компетентними органами інших країн — членів ЄС, Великої Британії або країн, які мають угоду про взаємне визнання з ЄС або з Україною (подається для лікарських засобів, виробництво хоча б однієї стадії яких здійснюється не в країні — члені ЄС, Великої Британії або в країні, яка не має угоди про взаємне визнання з ЄС або з Україною, включаючи контрактні виробничі дільниці) (окрім періоду визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, що унеможливлює проведення інспектування за місцем провадження діяльності, в тому числі враховуючи санітарно-епідеміологічну ситуацію);
у разі неможливості встановлення у звіті, складеного за результатами останньої перевірки, проведеної уповноваженим органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною, інформації щодо лікарських засобів, які були предметом інспектування, в тому числі інформації щодо виробничих потужностей, на яких здійснюється виробництво та яке було предметом інспектування, наявності розбіжностей у звіті та досьє виробничої дільниці (Site Master File) тощо;
у разі відмови у видачі Сертифікату або Висновку за результатами останнього інспектування, проведеного Держлікслужбою згідно цього Порядку, виробничої дільниці, що подається у Заяві на видачу Сертифікату (Заяві на видачу Висновку) з метою підтвердження відповідності умов вимогам GMP;
у разі прийняття рішень щодо вилучення з обігу в установленому порядку серій лікарського засобу, які вироблялись на даній дільниці, що пов’язані з якістю лікарського засобу;
у разі встановлення під час проведення експертизи поданих документів ознак критичних порушень вимог GMP (зокрема, можливість виробництва лікарських засобів критичного рівня ризику та/або лікарських засобів високого ступеня ризику на одних і тих самих виробничих лініях або їх виробництва в умовах, що можуть призвести до перехресної контамінації, або виробництво цих лікарських засобів не відповідає встановленим в Україні вимогам тощо), внаслідок чого виробництво може бути визнано таким, що не відповідає вимогам GMP, або ознак виробництва фальсифікованих лікарських засобів.
5. Для здійснення інспектування, експертиз, виконання окремих робіт у сфері підтвердження відповідності, вивчення окремих питань, які вимагають спеціальних знань, Держлікслужба України може залучати уповноважені організації, учених та фахівців (за їх згодою).
6. Інспектування здійснюється відповідно до затверджених плану та програми інспектування, де визначено мету, об’єкти, дати проведення інспектування, призначено інспектора або групу інспекторів. Копії плану та програми інспектування надаються Заявнику або представнику Заявника або надсилаються факсом, що зазначений в Заяві на видачу Сертифіката (Заяві на видачу Висновку), або в сканованому вигляді електронною поштою за місцезнаходженням Заявника (представника Заявника) у строки, визначені розділом ІІІ цього Порядку.
При складанні плану та програми інспектування враховуються інформація щодо результатів проведення інспектувань з боку Держлікслужби України, у тому числі при залученні уповноважених організацій, учених та фахівців, даної виробничої дільниці за попередні роки та наявність документальних підтверджень усунення критичних, суттєвих та несуттєвих порушень, встановлених Держлікслужбою України під час цих інспектувань. Перевірка усунення порушень повинна бути включена до плану та програми інспектування, крім випадків, якщо ця інформація вже була предметом перевірки з боку Держлікслужби України.
План та програма інспектування повинні охоплювати виробничі зони, зони контролю якості, у тому числі при здійсненні контролю якості за контрактом (договором), складські зони, у тому числі при контрактному зберіганні (за договором) активних фармацевтичних інгредієнтів, продукції « in-bulk» , стадії сертифікації серії лікарських засобів та готових лікарських засобів, сировини, пакувальних матеріалів, продукції «in-bulk» та готових лікарських засобів тощо.
7. Під час інспектування інспектор має фіксувати факти, що підтверджують відповідність умов виробництва лікарських засобів вимогам GMP, а також виявлені в ході інспектування порушення GMP. Під час присвоєння класифікації виявленому порушенню інспектор повинен користуватися алгоритмом, викладеним у додатку 10 до цього Порядку, де наведені, як приклади, найбільш типові порушення, які виявляються під час інспектування, та їх можлива класифікація, виходячи із оцінки ризиків для пацієнта. Даний перелік не є вичерпним та за необхідності можуть додаватися додаткові порушення.
7. Під час інспектування інспектор має фіксувати факти, що підтверджують відповідність умов виробництва лікарських засобів вимогам GMP, а також виявлені в ході інспектування порушення відповідно до класифікації, встановленої у Переліку типових порушень вимог GMP, які виявляються під час інспектування, та їх класифікації, виходячи із оцінки ризиків для пацієнта, наведених у додатку 10 до цього Порядку (далі — Перелік типових порушень), при цьому Перелік типових порушень не є вичерпним і за необхідності можуть додаватися додаткові порушення. При присвоюванні класифікації виявленому порушенню має враховуватися рівень ризику лікарського засобу, що виробляється на дільниці. У Переліку типових порушень, яким повинен користуватися інспектор, наведені, як приклади, найбільш типові порушення, які виявляються під час інспектування, та їх класифікація, виходячи із оцінки ризиків для пацієнта.
8. Якщо на виробництві, яке інспектується, випускаються лікарські засоби виключно низького рівня ризику, то виявленим порушенням, враховуючи алгоритм згідно додатку 10 до цього Порядкунаведеним в Переліку типових порушень чи схожим, зазвичай класифікація критичних порушень не присвоюється. Для таких виробництв до критичних порушень можуть бути віднесені тільки виняткові ситуації, такі як: навмисна підробка, викривлення даних,або фальсифікація продукції або даних; широко поширене перехресне забруднення; зараження/інвазія або антисанітарія.
В інших випадках, коли суттєві порушення, наведені в Переліку типових порушень, відмічені значком «*», їх класифікація може бути підвищена до критичної. Якщо таке відбувається, інспектором в звіті має бути представлене належне обґрунтування підвищення класифікації.
При підвищенні у звіті класифікації порушень, яка є відмінною від алгоритму згідно додатку 10 до цього Порядку, інспектором має бути представлене належне обґрунтування підвищення класифікації.
9. При виявленні в ході інспектування критичних порушень, в тому числі таких, що були зазначені в пункті 8 цього розділу, цей факт негайно доводиться інспектором до відома керівництва виробника, що інспектується. Керівництво Держлікслужби України також повинно бути проінформоване про це невідкладно.
У разі виявлення критичних порушень в процесі інспектування для обговорення таких порушень проводиться нарада з представниками виробника ув дні, коли такі порушення виявлені. На цій нараді виявлені порушення доводяться до відома уповноваженого представника виробництва та/або керівника виробника, що інспектується. Виробник має право надати, а інспектор зобов’язаний розглянути документи та матеріали, що підтверджують усунення порушень у ході перевірки або спростовують вищевказані порушення.
10. У разі обґрунтованого висновку інспектора та/або експерта та прийнятого відповідного рішення Держлікслужбою України щодо відмови у видачі Сертифіката або Висновку Держлікслужбою України можуть бути вжиті заходи відповідно до законодавства щодо зупинення обігу таких лікарських засобів до усунення порушень.
11. За результатами інспектування інспектор складає Ззвіт за результатами інспектування (далі — Звіт). Звіт складається українською мовою у двох примірниках за формою, наведеною в додатку 11 до цього Порядку. Додатково для нерезидентів Звіт та його переклад англійською мовою або російською мовами можуть бути оформлені у строк не пізніше ніж 15 робочих днів з дня складання Звіту українською мовою.
Звіт повинен містити висновок щодо відповідності або невідповідності виробництва (виробничої дільниці (виробничих дільниць), та/або виробничих ліній, та/або виробництва окремих лікарських засобів тощо) вимогам GMP, у тому числі усунення або неусунення порушень відповідності вимогам GMP тощо, та рекомендації інспектора/інспекторів щодо видачі Сертифіката або Висновку або відмови у видачі Сертифіката або Висновку, які розглядаються під час прийняття рішення Держлікслужбою України.
У разі ненадання Заявником та/або виробником інспектору/інспекторам всієї необхідної інформації з метою проведення інспектування, незабезпечення можливості проведення огляду виробничих, допоміжних, складських приміщень, обладнання, зон контролю якості тощо, незабезпечення можливості інтерв’ювання представників (персоналу) виробника, перешкоджання інспектору/інспекторам у проведенні інспектування, в разі присутності під час інспектування третіх осіб, що не є офіційними представниками Заявника та/або виробника, будь-яких інших дій, що вплинули на проведення інспектування в об’ємі згідно із затвердженими планом та програмою, інспектор/інспектори повинні про це зазначити у Звіті. Ця інформація повинна бути врахована під час формування у Звіті чіткого висновку щодо відповідності або невідповідності умов виробництва лікарських засобів (виробничої дільниці (виробничих дільниць), та/або виробничих ліній, та/або виробництва окремих лікарських засобів тощо) вимогам GMP.
У разі ненадання Заявником та/або виробником інспектору/інспекторам всієї необхідної інформації з метою проведення інспектування, незабезпечення можливості проведення огляду виробничих, допоміжних, складських приміщень, обладнання, зон контролю якості тощо, незабезпечення можливості інтерв’ювання представників (персоналу) виробника, перешкоджання інспектору/інспекторам у проведені інспектування, у разі присутності під час інспектування третіх осіб, що не є офіційними представниками Заявника та/або виробника, будь-яких інших дій, що вплинули на проведення інспектування в об’ємі згідно із затвердженими планом та програмою, інспектор/інспектори повинні про це зазначити в Звіті. Ця інформація повинна бути врахована під час формування в Звіті чіткого висновку щодо відповідності або невідповідності умов виробництва лікарських засобів (виробничої дільниці (виробничих дільниць), та/або виробничих ліній, та/або виробництва окремих лікарських засобів тощо) вимогам GMP.
12. Обговорення та узагальнення виявлених у процесі інспектування порушень та їх класифікація згідно з додатком 10 до цього Порядку здійснюються інспектором/інспекторами на заключній нараді під час інспектування з представниками виробника, а також оголошується загальний висновок інспектора/інспекторів щодо відповідності чи невідповідності виробництва вимогам GMP.
12. Обговорення та узагальнення виявлених в процесі інспектування порушень та їх класифікація згідно з Переліком типових порушень здійснюються інспектором/інспекторами на заключній нараді під час інспектування з представниками виробника, а також оголошується загальний висновок інспектора/інспекторів щодо відповідності чи невідповідності виробництва вимогам GMP.
У разі наявності зауважень щодо проведеного інспектування та/або класифікації порушень вони можуть бути викладені Заявником (представником Заявника) та/або виробником у протоколі наради українською, російською або англійською мовами. У цьому випадку протокол наради підлягає обов’язковому розгляду та врахуванню при розгляді Держлікслужбою України з метою прийняття рішення про видачу Сертифіката або Висновку або відмову в їх видачі.
13. При виявленні під час інспектування критичних порушень виробництва вимог GMP інспектору/інспекторам виробником негайно повинен бути наданийо план коригувальних та запобіжних дій щодо усунення виявлених критичних порушень, який надалі додається до першого примірника звіту за результатами інспектування.
14. У разі усунення виробником порушень під час інспектування інспектору повинні бути надані копії належним чином завірених виробником документальних підтверджень їх усунення, про що повинно бути зазначено в Звіті. При цьому в Звіті викладаються опис порушення, класифікація, опис дій виробника щодо усунення цього порушення, а також зазначається про факт його усунення під час інспектування. У висновках Звіту окремо зазначаються кількість та класифікація порушень, що усунуті під час інспектування.
Надання виробником копії документальних підтверджень усунення порушень повинно враховувати час, необхідний для їх оцінки з боку інспектора, та не перешкоджати проведенню інспекції згідно із затвердженими планами та програмами інспектування.
15. Один примірник Звіту надається Заявнику (представнику Заявника). Другий примірник Звіту та матеріали інспектування зберігаються в Держлікслужбі України протягом п’яти років після закінчення строку дії Сертифіката або Висновку., але не менше ніж три роки.
16. До другого примірника Звіту додаються:
план і програма інспектування;
протоколи наради за формою згідно з додатком 12 до цього Порядку;
аудіо- та відеоматеріали (за наявності);
протокол оцінки ризиків щодо розрахунку строку наступної інспекції виробництва лікарського засобу на відповідність вимогам GMP;
копії належним чином завірених виробником документальних підтверджень усунення під час інспектування порушень (якщо про це зазначено в Звіті) тощо.
17. Якщо в процесі інспектування було відібрано зразки для лабораторного аналізу їх якості, до Звіту додаються:
акт відбору зразків продукції;
направлення на випробування;
проєктпроект методів контролю якості лікарського засобу, що надається Заявником (представником Заявника);
письмовий висновок атестованої відповідно до Порядку проведення галузевої атестації лабораторій з контролю якості та безпеки лікарських засобів, затвердженого наказом Міністерства охорони здоров’я України від 14 січня 2004 року № 10, зареєстрованого у Міністерстві юстиції України 30 січня 2004 року за № 130/8729, лабораторії про якість серії лікарського засобу (після надання його зразків).
V. Порядок прийняття рішення про видачу або відмову у видачі Сертифіката або Висновку
1. У разі прийняття позитивного рішення за результатами проведеної спеціалізованої експертизи Держлікслужба України надає Заявнику Висновок у строки, зазначені у розділі ІІІ цього Порядку.
Висновок Держлікслужби України видається на строк дії офіційного документа щодо відповідності умов виробництва лікарських засобів вимогам GMP, виданого уповноваженим органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною., який є членом PIC/S.
Строк дії Висновку продовжується за рішенням Держлікслужби України до шести місяців у разі надання Заявником (представником Заявника) інформації щодо проведення інспектування на відповідність умов виробництва лікарських засобів вимогам GMP уповноваженим органом країни-члена PIC/S або ВООЗ, про що Держлікслужба України письмово повідомляє Заявнику (представнику Заявника) у строк не більше 20 робочих днів.
Строк дії Висновку продовжується Держлікслужбою до шести місяців у разі надання Заявником (представником Заявника) інформації від уповноваженого органу, який видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, про заплановане інспектування виробника на відповідність вимогам GMP або інформації щодо запланованого подовження уповноваженим органом офіційного документа щодо відповідності умов виробництва лікарських засобів вимогам GMP на основі процедури аналізу ризиків, про що Держлікслужба письмово повідомляє Заявнику (представнику Заявника) у строк не більше 20 робочих днів.
Дія Висновку продовжується Держлікслужбою:
- на строк до шести місяців у разі надання Заявником (представником Заявника) або виробником інформації від уповноваженого органу, який видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, стосовно проведення інспектування на відповідність умов виробництва лікарських засобів вимогам GMP уповноваженим органом, який видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, про що Держлікслужба повідомляє Заявника (представника Заявника) в паперовій або електронній формі у строк не більше 10 робочих днів;
- на строк подовження сертифіката GMP, виданого уповноваженим органом країни – члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною (за винятком випадків, коли в пояснювальних примітках сертифіката GMP зазначено інше), про що Держлікслужба повідомляє Заявника (представника Заявника) в паперовій або електронній формі у строк не більше 10 робочих днів. Звернення Заявника (представника Заявника) або виробника до Держлікслужби має містити належним чином засвідчену копію документа від уповноваженого органу, який видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, стосовно подовження відповідного сертифіката GMP та засвідчений Заявником (представником Заявника) переклад копії цього документа українською мовою або засвідчену Заявником (представником Заявника) роздруківку з бази даних EudraGMP або електронного реєстру FDA США із засвідченим перекладом на українську мову.
на строк подовження сертифіката GMP, виданого уповноваженим органом країни – члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною, у період визнання хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я (за винятком випадків, коли в пояснювальних примітках сертифіката GMP зазначено інше), про що Держлікслужба повідомляє Заявника (представника Заявника) в паперовій або електронній формі у строк не більше 10 робочих днів.
За необхідності Держлікслужбою може бути направлений відповідний запит до компетентного органу країни — члена ЄС або компетентного органу інших країн — членів ЄС, Великої Британії або країн, які мають угоду про взаємне визнання з ЄС або з Україною, та уповноважений орган якої видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP.
2. У разі наявності обґрунтованих зауважень з боку Заявника (представника Заявника) та/або виробника щодо проведеного інспектування та/або класифікації порушень Заявник (представник Заявника) та/або виробник може направити до Держлікслужби України відповідне письмове повідомлення не пізніше 5 робочих днів після проведення інспектування, яке для розгляду направляється інспекторам, які проводили інспектування, та розглядається в подальшому на засіданні робочої групи розглядається Держлікслужбою України з метою прийняття рішення щодо видачі або неможливості видачі Сертифіката або Висновку, яке приймається в строк до 15 робочих днів від дати надходження такого повідомлення до Держлікслужби України.
При розгляді Держлікслужбою України обґрунтованих зауважень у робочому засіданні може брати участь Заявник та/або виробник, та/або їх представник, якщо таке бажання зазначене в повідомленні. Дата та час проведення такого засідання повідомляються Держлікслужбою на офіційному вебсайті не пізніше, ніж за 3 робочі дні до проведення засідання.Дата та час проведення такого засідання повідомляються Держлікслужбою України на офіційному сайті не пізніше, ніж за 3 робочих дні до проведення засідання.
За результатами розгляду Звіту на робочих засіданнях Держлікслужбою України, враховуючи зауваження з боку Заявника, та/або виробника, та/або їх представника, розгляду додаткових, завірених Заявником, та/або виробником, та/або їх представником документальних підтверджень усунення порушень тощо Звіт може бути повернуто інспектору(ам) на доопрацювання строком не більше ніж 10 робочих днів. Час, потрібний для доопрацювання Звіту, не включається до строків оформлення та видачі Сертифіката або Висновку.
Результати розгляду зауважень повідомляються Заявнику, та/або виробнику, та/або їх представнику листом за зазначеним у Заяві на видачу Сертифіката (Заяві на видачу Висновку) місцезнаходженням не пізніше ніж через 5 робочих днів з дня прийняття рішення Держлікслужбою України щодо видачі або відмови у видачі Сертифіката або Висновку. У разі незгоди з результатами зауважень Заявник (представник Заявника) та/або виробник мають право оскаржити такі дії Держлікслужби України в порядку, встановленому законодавством України.
3. За результатами розгляду на робочому засіданні Держлікслужби України Звіту з врахуванням висновків за результатами інспектування та рекомендацій інспектора/інспекторів, наданих документальних підтверджень усунення порушень, результатів розгляду зауважень з боку Заявника/виробника (за наявності), результатів проведених експертиз тощо Держлікслужба України приймає рішення щодо видачі або відмови у видачі Сертифіката або Сертифікатів (у разі необхідності при інспектуванні різних лікарських форм тощо), або Висновку, про що письмово повідомляє Заявника або представника Заявника та видає Звіт.Висновку.
У разі прийняття рішення щодо видачі Сертифіката або Висновку Держлікслужба України видає заявнику Сертифікат або Висновок у строки, визначені розділом ІІІ цього Порядку. Строк дії Сертифіката становить три роки від дати проведення інспектування.
Видача Сертифікату/Сертифікатів або Висновку здійснюється після надання виробником/Заявником до Держлікслужби відповідно до пункту 11 цього розділу прийнятного плану коригувальних та запобіжних дій щодо усунення виявлених порушень за результатами інспектування виробничих дільниць або окремих лікарських засобів.
Строк наступної інспекції на відповідність виробництва вимогам GMP розраховується відповідно до методології проведення аналізу згідно додатку 15 цього Порядку та зазначається в окремому протоколі, який готується інспектором/інспекторами після проведення інспектування та подається до Держлікслужби разом зі Звітом. Остаточне рішення щодо наступного строку інспектування приймається Держлікслужбою. Строк наступної інспекції письмово повідомляться Заявнику (представнику Заявника) під час надання Звіту.
Строк дії Сертифіката становить три роки від дати проведення інспектування та може бути скороченим за рекомендацією інспекторів згідно протоколу оцінки ризиків щодо розрахунку строку наступної інспекції виробництва лікарського засобу на відповідність вимогам GMP.
У разі, якщо строк наступної інспекції визначено через рік та менше після проведення інспектування, Держлікслужбою повідомляється Заявника (представника Заявника) про необхідність його проведення. Заявник (представника Заявника) подає до Держлікслужби офіційний лист (разом із Заявою про видачу Сертифіката в додатку до листа) щодо згоди на проведення інспектування, в тому числі задіяних контрактних виробничих дільниць, лабораторій з контролю якості голових лікарських засобів, продукції in-bulk та активних фармацевтичних інгредієнтів та контрактних складів. Комплект документів до Заяви про видачу Сертифіката в цьому випадку не подається, водночас, Держлікслужбою можуть вимагатися реєстраційні матеріали на зареєстровані лікарські засоби в Україні, оновлений перелік лікарських засобів, у тому числі на електронному носії, Досьє виробничої дільниці для установ з отримання плазми та/або Досьє виробничої дільниці для місць зберігання плазми тощо.
4. Про видачу Сертифіката або Висновку приймається наказ Держлікслужби. До Сертифіката або Висновку додається перелік лікарських засобів, зареєстрованих або лікарських засобів, що знаходяться в процесі реєстрації/внесенні змін, згідно з додатком 13 до цього Порядку (далі — Перелік лікарських засобів), який є невід’ємною частиною Сертифіката або Висновку.
4. Про видачу Сертифіката або Висновку приймається наказ Держлікслужби України. До Сертифіката або Висновку додається перелік лікарських засобів, зареєстрованих або запланованих до реєстрації в Україні, згідно з додатком 13 до цього Порядку (далі — Перелік лікарських засобів), який є невід’ємною частиною Сертифіката або Висновку.
5. У разі якщо протягом строку дії Сертифіката або Висновку Заявник (представник Заявника) повідомляє Держлікслужбу України про зміну найменування виробника, сертифікованої виробничої дільниці або зміну ліцензії на виробництво лікарських засобів, у тому числі пов’язану зі зміною найменування Заявника, Держлікслужба України після проведення спеціалізованої експертизи переоформлює Сертифікат або Висновок у строки, зазначені у розділі ІІІ цього Порядку. Переоформлений Сертифікат або Висновок видається Заявнику (представнику Заявника), попередній Сертифікат або Висновок підлягає поверненню до Держлікслужби України.
5.6. Для резидентів у разі анулювання ліцензії на виробництво лікарських засобів також анулюється Сертифікат.
6.7. У разі негативного рішення Держлікслужба України інформує Заявника про вмотивовану відмову у видачі Сертифіката або Висновку у строки, зазначені у розділі ІІІ цього Порядку.
У разі незгоди з рішенням Держлікслужби щодо відмови у видачі Сертифіката або Висновку Заявник має право оскаржити таку відмову у судовому порядку.
7.8. Рішення про відмову у видачі Сертифіката або Висновку оформляється наказом Держлікслужби України та приймається у разі:
виявлення недостовірних відомостей у Заяві на видачу Сертифіката (Заяві на видачу Висновку) або документах, що додавалися до Заяви на видачу Сертифіката (Заяви на видачу Висновку) відповідно до цього Порядку;
виявлення в ході інспектування навмисної підробки, викривлення даних, фальсифікації продукції або даних;
виявлення в ході інспектування навмисної підробки або викривлення продукції або даних;
встановлення критичного/критичних порушення/порушень вимог GMP за результатами інспектування та їх неусунення в ході інспектування;
якщо в ході інспектування встановлені численні (не менше 6 у сукупності, по конкретних препаратах або процесах) суттєві порушення, які свідчать про те, що виробник не контролює належним чином процеси та виробничі операції;
якщо в ході інспектування встановлені численні (не менше 6 у сукупності, по конкретним препаратам або процесам) суттєві порушення, які свідчать про те, що виробник не контролює належним чином процеси та виробничі операції;
якщо в ході інспектування повторно встановлено, що більшість суттєвих та несуттєвих порушень, які були встановлені в ході попередніх інспектувань, не усунуті, що свідчить про те, що виробник не вживає належних запобіжних та коригувальних дій за результатами попередньої інспекції;
якщо в ході інспектування повторно встановлено, що критичні порушення, які були виявлені в ході попередніх інспектувань, не усунуті, що свідчить про те, що виробник не вживає належних запобіжних та коригувальних дій за результатами попередньої інспекції;
у випадку невиконання Заявником (представником Заявника) зобов’язань, викладених у пункті 3 розділу VIIІ цього Порядку, стосовно надання на запит інспектора всієї необхідної інформації, забезпечення можливості проведення огляду приміщень, обладнання, зон контролю якості, інтерв’ювання представників (персоналу) виробника, ознайомлення з необхідною документацією системи якості тощо, що унеможливлює надати оцінку виробництва лікарських засобів як такого, що відповідає вимогам GMP, про що зазначається у Звіті інспектора;
ненадання виробником/Заявником плану коригувальних та запобіжних дій щодо усунення виявлених порушень за результатами інспектування виробничих дільниць або окремих лікарських засобів та документальних підтверджень щодо усунення порушень у встановлені строки;
неусунення зауважень за результатами проведених експертиз у встановлені строки.
9. За наявності у Звіті критичних та/або численних (не менше 6 у сукупності, по конкретних лікарських засобахконкретним лікарським засобам або процесам) суттєвих порушень відповідності вимогам GMP виробничих дільниць або окремих лікарських засобів виробник вживає заходів щодо їх усунення, надає до Держлікслужби України план коригувальних та запобіжних дій щодо усунення виявлених порушень згідно з додатком 14 до цього Порядку у строк до 30 робочих днів від дати отримання Звіту. При цьому в плані коригувальних та запобіжних дій щодо усунення виявлених порушень повинні бути чітко зазначені заходи щодо поводження з лікарськими засобами, якщо такі вироблялись під час виявлення цих порушень.
Документальні підтвердження усунення порушень надаються до Держлікслужби України відповідно до строків усунення порушень, встановлених виробником згідно з планом коригувальних та запобіжних дій щодо усунення виявлених порушень.
10. Після усунення критичних та/або численних (не менше 6 у сукупності, по конкретних лікарських засобахконкретним лікарським засобам або процесам) суттєвих порушень відповідності вимогам GMP умов виробництва лікарських засобів або окремих лікарських засобів та надання до Держлікслужби України документальних підтверджень про усунення Заявник/представник Заявника/виробник може надати до Держлікслужби України письмове звернення щодо проведення інспектування з метою перевірки.
У разі підтвердження за результатами інспектування повного усунення цих порушень та у разі відсутності підстав щодо відмови у видачі Сертифіката або Висновку відповідно до пункту 78 розділу V цього Порядку Держлікслужба України приймає рішення про видачу Сертифіката згідно з додатком 3 до цього Порядку або Висновку згідно з додатком 4 до цього Порядку.
У разі підтвердження за результатами цього інспектування неусунення порушень та/або за наявності підстав щодо відмови у видачі Сертифіката або Висновку відповідно до пункту 78 розділу V цього Порядку Держлікслужба України приймає рішення про відмову у видачі Заявнику Сертифіката або Висновку.
Інспектування з метою перевірки усунення порушень може здійснюватися декілька разів, але у строк не більше одного календарного року від дати подання до Держлікслужби України Заяви на видачу Сертифіката (Заяви на видачу Висновку) та при своєчасному наданні до Держлікслужби України відповідних планів коригувальних та запобіжних дій щодо усунення виявлених порушень та документальних підтверджень про усунення порушень.
11. За наявності у Звіті суттєвих (менше 6 у сукупності, по конкретних лікарських засобах або процесам) та несуттєвих порушень вимог GMP виробник повинен вжити заходів щодо приведення виробництва у відповідність до вимог GMP, надати на експертизу до Держлікслужби України план коригувальних та запобіжних дій щодо усунення виявлених порушень згідно з додатком 14 до цього Порядку у строк до 9030 робочих днів від дати отримання Звіту. Експертиза наданих документів здійснюється протягом 15 робочих днів, результати якої повідомляються Заявнику/представнику Заявника/виробнику. Експертиза наданих документів для незареєстрованих в Україні, але зареєстрованих компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстрованих компетентним органом Європейського Союзу за централізованою процедурою, які закуповуються особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я, здійснюється протягом 5 робочих днів, результати якої повідомляються Заявнику / представнику Заявника / виробнику.
Строки усунення порушень встановлюються виробником, враховуючи рекомендації інспекторів згідно зі Звітом та результатами проведеної експертизи та планом коригувальних і запобіжних дій щодо усунення виявлених порушень, зазначаються в плані коригувальних і запобіжних дій та не можуть перевищувати один рік від дати проведення інспектування.
Документальні підтвердження усунення порушень надаються до Держлікслужби України відповідно до строків усунення порушень, встановлених в плані коригувальних та запобіжних дій щодо усунення виявлених порушень.
У разі ненадання виробником/Заявником плану коригувальних та запобіжних дій щодо усунення виявлених порушень у встановлені строки та/або відсутність його позитивної експертизи з боку Держлікслужби, Держлікслужба приймає рішення про зупинення дії Сертифікату/Сертифікатів або Висновку відповідно до пункту 7 розділу V цього Порядку. План коригувальних та запобіжних дій щодо усунення виявлених порушень може подаватися декілька разів, однак у строк, що не перевищує 90 робочих днів від дати отримання Звіту.
У разі ненадання виробником/Заявником документальних підтверджень щодо усунення порушень у встановлені строки Держлікслужба приймає рішення про зупинення дії Сертифіката або Висновку відповідно до пункту 4 розділу VІ цього Порядку.
У разі ненадання виробником/Заявником плану коригувальних та запобіжних дій щодо усунення виявлених порушень та документальних підтверджень щодо усунення порушень у встановлені строки Держлікслужба України приймає рішення про зупинення дії Сертифіката або Висновку відповідно до пункту 4 розділу VІ цього Порядку.
12. У разі виникнення необхідності у Заявника (представника Заявника) внесення змін та/або переоформлення Висновку чи Сертифіката та/або Переліку лікарських засобів, який додається до Висновку чи Сертифіката (з метою реєстрації лікарських засобів або внесення змін до реєстраційної документації, у тому числі зміни назви лікарського засобу, дозування, найменування виробника тощо, з метою виправлення технічних помилок), Заявник (представник Заявника) подає до Держлікслужби письмове звернення щодо необхідності внесення змін чи переоформлення Висновку чи Сертифіката.
12. У разі виникнення необхідності внесення змін до Висновку чи Сертифіката або до Переліку лікарських засобів, який додається до Висновку чи Сертифіката (з метою реєстрації, перереєстрації лікарських засобів або внесення змін до реєстраційної документації, у тому числі зміни назви лікарського засобу, дозування, найменування виробника тощо), Заявник (представник Заявника) подає до Держлікслужби України письмове звернення щодо необхідності внесення змін чи переоформлення Висновку чи Сертифіката.
З письмовим зверненням до Держлікслужби України надаються: загальний оновлений перелік номенклатури продукції у паперовому вигляді та на електронному носії інформації, засвідчений Заявником (представником Заявника), копія сертифіката лікарського засобу для міжнародної торгівлі (certificate of a pharmaceutical product) або копія реєстраційного посвідчення (marketing authorization), виданого компетентним органом країни виробника лікарського засобу або власника реєстраційного посвідчення (заявника) або іншим регуляторним органом країни із суворою регуляторною системою, на ринку якої розміщено лікарський засіб, із зазначенням назви документа та найменування компетентного органу, що його видав, дати видачі (для незареєстрованих лікарських засобів, які плануються до реєстрації або перереєстрації в Україні), копії інших документів, що підтверджують достовірність змін, які потребують внесення.
З письмовим зверненням до Держлікслужби надаються: загальний оновлений перелік номенклатури продукції у паперовому вигляді та на електронному носії інформації, засвідчений Заявником (представником Заявника), копія сертифіката лікарського засобу для міжнародної торгівлі (certificate of a pharmaceutical product), виданого компетентним органом країни виробника лікарського засобу або власника реєстраційного посвідчення (заявника), або іншим регуляторним органом країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною, на ринку якої розміщено лікарський засіб, із зазначенням назви документа та найменування компетентного органу, що його видав, дати видачі (для незареєстрованих лікарських засобів, які знаходяться в процесі реєстрації/внесенні змін в Україні), назви та адрес виробничих дільниць (для незареєстрованих лікарських засобів, які плануються до реєстрації в Україні); засвідчені Заявником (представником Заявника) копії реєстраційних посвідчень (marketing authorization), виданих компетентним органом країни ЄС, уповноважений орган якої видав офіційний документ щодо відповідності умов виробництва лікарських засобів вимогам GMP, або виданих компетентними органами інших країн — членів ЄС, Великої Британії або країн, які мають угоду про взаємне визнання з ЄС або з Україною (подається для лікарських засобів, виробництво хоча б однієї стадії яких здійснюється не в країні — члені ЄС, Великої Британії або в країні, яка не має угоди про взаємне визнання з ЄС або з Україною, включаючи контрактні виробничі дільниці); копії інших документів, що підтверджують достовірність змін, які потребують внесення.
У разі внесення додаткової виробничої дільниці, виробничої операції повинні бути надані відповідні документи згідно пункту 2 розділу ІІ цього Порядку.
При змінах, пов’язаних із зазначенням номерів реєстраційних посвідчень на лікарські засоби, на загальному оновленому переліку номенклатури продукції достатньо підпису та печатки (за наявності) Заявника (представника Заявника).
При проведенні експертизи у разі розширення Переліку лікарських засобів, який додається до Сертифіката або Висновку, беруться до уваги результати інспектування виробничої дільниці, на якій виробляються або плануються до виробництва лікарські засоби, що подаються на розширення, надання до Держлікслужби плану коригувальних та запобіжних дій щодо усунення виявлених порушень та його виконання з боку виробника, повідомлення Держлікслужбу про зміни у виробництві, контролі якості лікарських засобів, надання тощо.
Для лікарських засобів, що пройшли процедуру прекваліфікації ВООЗ, інспектування у разі розширення Переліку лікарських засобів не здійснюється, окрім підтвердження відповідності умов виробництва лікарських засобів вимогам GMP для резидентів та нерезидентів з метою отримання Сертифіката або Висновку для установ з отримання плазми та/або місць зберігання плазми, включно, якщо установи з отримання плазми та/або місця зберігання плазми є проміжними виробничими дільницями або контактними.
У разі відсутності підстав для відмови у переоформленні або внесенні змін до Сертифіката, Висновку або Переліку лікарських засобів, в тому числі враховуючи пункт 7 цього розділу та пункт 3 розділу VI цього Порядку, Держлікслужба протягом 15 робочих днів з дня отримання відповідних документів та їх спеціалізованої експертизи у разі позитивного висновку оформлює проєкт оновленого Переліку лікарських засобів, у разі переоформлення Сертифіката або Висновку — оформлює проєкт оновленого Сертифіката або Висновку з відповідним Переліком лікарських засобів. Проєкти надсилаються електронною поштою або факсом Заявнику (представнику Заявника) з метою їх погодження. Заявник (представник Заявника) засвідчує підписом проєкти документів та надає їх до Держлікслужби. Переоформлений Сертифікат або Висновок видається Заявнику (представнику Заявника).
Відповідні звернення, комплекти документів, листи Заявників та/або представників Заявників можуть подаватися в електронному вигляді за наявності запровадженого електронного порталу Держлікслужби для подання таких документів.
У разі подання відповідних документів через електронний портал Держлікслужби на електронні документи накладається електронний підпис Заявника (представника Заявника), що базується на кваліфікованому сертифікаті електронного підпису, відповідно до вимог Закону України «Про електронні довірчі послуги».
13. У разі оголошення Україною чи іншою країною — виробником надзвичайного стану, надзвичайної ситуації, воєнного стану, у разі стихійного лиха, у випадку офіційного визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, що унеможливлює проведення інспектування, в тому числі враховуючи санітарно-епідеміологічну ситуацію, у зв’язку із підвищеною фізичною небезпекою для інспектора (в тому числі загрози для життя та здоров’я інспектора чи з інших причин) Заява на видачу Сертифіката (для виробників резидентів або для виробників нерезидентів) може розглядатися Держлікслужбою за процедурою дистанційної оцінки.
Під час проведення спеціалізованої експертизи Заяви на видачу Сертифіката та комплекту документів Держлікслужбою надсилається лист Заявнику (представнику Заявника) щодо можливості здійснення дистанційної оцінки (дистанційної перевірки, інспектування) з метою подальшої видачі Сертифіката на основі документованого опитування виробника, яке має бути достатньо глибоким для оцінки відповідності вимогам GMP відповідної виробничої дільниці, та необхідності надання до Держлікслужби таких документів, як:
фотографічне представлення виробничої дільниці та засобів (ззовні/в приміщенні) (зовнішні загальні аерознімки, детальні знімки приміщень під час операцій, які в них проводяться (відбір проб, зважування, тощо));
мастер-план кваліфікації (приміщення та обладнання) (перелік приміщень, обладнання та середовищ, які використовуються у виробництві, із зазначенням їхнього статусу кваліфікації);
валідаційний мастер-план (технологічні процеси, процедури очищення, контроль якості) (перелік процесів, які проводяться для виробництва/ контролю продукту, із зазначенням їхнього валідаційного статусу);
звіт повного внутрішнього аудиту/зовнішнього аудиту стосовно певних лікарських засобів (звіт повинен містити блок-схему щодо продукту й повинен бути складений не більше одного року тому);
досьє серій відповідної продукції (останнє заповнене досьє серії разом із технологічним регламентом, у тому числі аналітична частина);
управління рекламаціями (актуалізований перелік рекламацій на всю продукцію, що виробляється на дільниці);
кількість відбракованих серій для всієї продукції;
кількість відбракованих серій певної продукції;
стосовно відповідного продукту та/або лікарської форми: процедура розслідувань результатів, які вийшли за межі специфікації, програма подальшого випробування стабільності, всі результати, які вийшли за межі специфікації та їх розслідування, усі звіти про відхилення від технологічного процесу, в тому числі документи на серії, які пройшли переробку та/або регенеровані, всі звіти про відхилення якості;
огляд якості певного продукту;
контракт між виробничою дільницею та заявником (за наявності).
Час, потрібний Заявнику (представнику Заявника) на надання документів до Держлікслужби, становить до тридцяти календарних днів від направлення повідомлення від Держлікслужби щодо проведення дистанційної оцінки, та не включається до строків проведення спеціалізованої експертизи, дистанційної оцінки, оформлення та видачі Сертифіката. Зі супровідним листом документи можуть бути направлені виробником/Заявником (представником Заявника) на адресу Держлікслужби поштовим відправленням або в сканованому вигляді на електронному носії інформації.
Після отримання Держлікслужбою документів дистанційна оцінка проводиться не більше, ніж 15 робочих днів з дати надходження документів до Держлікслужби. Для лікарських засобів, які:
включені до протоколів лікування України у випадку офіційного визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я;
зареєстровані за централізованою процедурою EMA;
пройшли процедуру прекваліфікації ВООЗ та включені до переліку ВООЗ прекваліфікованих лікарських засобів;
призначені для профілактики, діагностики та лікування туберкульозу, ВІЛ/СНІД, вірусних гепатитів, онкологічних та рідкісних (орфанних) захворювань;
реєструються в Україні за спрощеною процедурою реєстрації згідно із Законом України « Про лікарські засоби»
незареєстровані в Україні, але зареєстровані компетентним органом Сполучених Штатів Америки, Швейцарської Конфедерації, Японії, Австралії, Канади, держави — члена Європейського Союзу чи зареєстровані компетентним органом Європейського Союзу за централізованою процедурою, які закуповуються особою, уповноваженою на здійснення закупівель у сфері охорони здоров’я;
дистанційна оцінка проводиться не більше, ніж 10 робочих днів з дати надходження документів до Держлікслужби.
Під час проведення дистанційної оцінки можуть бути застосовані засоби відеозв’язку з виробником лікарських засобів із метою оцінки виробничої дільниці/лабораторії/складів (у тому числі за контрактом), виробничої документації та документації системи якості на відповідність вимогам GMP, про що повинно бути офіційно повідомлено (електронною поштою/телефонним зв’язком) Заявника (представника Заявника), який повинен сприяти його організації.
У разі позитивного висновку за результатами спеціалізованої експертизи та дистанційної оцінки Держлікслужбою приймається рішення щодо видачі Сертифіката, який оформлюється відповідно до пункту 12 цього розділу Порядку за формою згідно з додатком 3 (Форма 2) до цього Порядку.
Строк дії Сертифіката становить два роки від дати проведення дистанційної оцінки.
Дистанційна оцінка може замінити інспектування лише один раз.
Рішення про відмову у видачі Сертифіката за процедурою дистанційної оцінки може бути прийнято у разі ненадання протягом тридцяти календарних днів документів для оцінки відповідності вимогам GMP відповідної виробничої дільниці, встановлення фактів під час проведення дистанційної оцінки, які свідчать про невідповідність виробництва лікарських засобів вимогам GMР, подання недостовірних відомостей, відмови у організації відеозв’язку із боку виробника.
Після врегулювання питань надзвичайного стану, надзвичайної ситуації, воєнного стану, стихійного лиха, надзвичайної ситуації в галузі світової охорони здоров’я та пандемії, відсутності підвищеної фізичної небезпеки для інспектора (з причин загрози для життя та здоров’я чи з інших причин) Держлікслужбою може бути призначено позапланове інспектування за місцем провадження діяльності з метою підтвердження відповідності умов виробництва вимогам належної виробничої практики.
Дистанційна оцінка не може бути проведена:
у разі, якщо виробнича дільниця раніше не проходила інспектування з боку Держлікслужби, уповноваженого органу країни – члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною (окрім випадків надання до Держлікслужби від дипломатичних представництв України за кордоном інформації щодо неможливості проведення інспектування у зв’язку з оголошенням країною – виробником надзвичайного стану, надзвичайної ситуації, воєнного стану, у разі стихійного лиха, у випадку офіційного визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, що унеможливлює проведення інспектування);
у разі, якщо виробнича дільниця раніше не проходила інспектування з боку Держлікслужби, уповноваженого органу країни — члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною;
у разі наявності критичних порушень та/або численних (не менше 6 в сукупності, по конкретних лікарських засобах або процесах) суттєвих порушень відповідності вимогам GMP виробничих дільниць або окремих лікарських засобів, виявлених з боку Держлікслужби під час останнього інспектування цієї виробничої дільниці на відповідність виробництва вимогам GMP або ліцензійним умовам;
у разі відсутності документальних підтверджень усунення суттєвих та несуттєвих порушень, встановлених Держлікслужбою під час останнього інспектування на відповідність виробництва вимогам GMP або ліцензійним умовам;
у разі, якщо Держлікслужба має підстави вважати, що є факти, які можуть вплинути на якість лікарських засобів, які подаються на процедуру підтвердження відповідності умов виробництва вимогам належної виробничої практики (виробництво розташоване в країні, що офіційно визнана Україною як країна-агресор тощо).
При проведенні експертизи у разі розширення Переліку лікарських засобів, який додається до Сертифіката або Висновку, враховуються результати інспектування виробничої дільниці, на якій виробляються або плануються до виробництва лікарські засоби, що подаються на розширення, надання до Держлікслужби України плану коригувальних та запобіжних дій щодо усунення виявлених порушень та його виконання з боку виробника тощо.
Для лікарських засобів, що пройшли процедуру прекваліфікації ВООЗ, інспектування у разі розширення Переліку лікарських засобів не здійснюється.
Держлікслужба України протягом 15 робочих днів з дня отримання відповідних документів та їх спеціалізованої експертизи у разі позитивного висновку оформлює проект оновленого Переліку лікарських засобів, у разі переоформлення Сертифіката або Висновку — оформлює проект оновленого Сертифіката або Висновку з відповідним Переліком лікарських засобів. Проекти надсилаються електронною поштою або факсом Заявнику (представнику Заявника) з метою їх погодження. Заявник (представник Заявника) засвідчує підписом проекти документів та надає їх до Держлікслужби України.
При розширенні Переліку лікарських засобів один його примірник надається Заявнику (представнику Заявника), другий зберігається в Держлікслужбі України. Заявник (представник Заявника) повертає оригінал попереднього Переліку лікарських засобів не пізніше дати отримання оновленого Переліку лікарських засобів.
VI. Контроль за дотриманням вимог належної виробничої практики протягом строку дії Сертифіката або Висновку
1. Заявник є відповідальним за дотримання вимог GMP у виробництві лікарських засобів протягом строку дії Сертифіката або Висновку.
2. Виробництво лікарських засобів, яке згідно з цим Порядком отримало підтвердження відповідності вимогам GMP, підлягає позаплановому інспектуванню на дотримання вимог GMP протягом строку дії Сертифіката або Висновку за наявності відповідних підстав, зазначених у пункті 3 цього розділу.
3. Підставами для позапланового інспектування виробництва (або окремих виробничих дільниць, контрактних лабораторій та контактних складів) (спрямована інспекція) з метою перевірки дотримання виробником вимог GMP можуть бути:
звернення Заявника/представника Заявника/виробника;
наявність документально підтверджених фактів або ознак виробництва лікарських засобів, які можуть бути небезпечними для здоров’я і життя людей або можуть призвести до тяжких наслідків для здоров’я людей внаслідок можливих порушень технології виробництва та/або методів контролю якості;
розширення номенклатури лікарських засобів, що виробляються на сертифікованому виробництві (у тому числі якщо виробництво цих лікарських засобів створює ризик контамінації або перехресної контамінації);
у разі внесення змін до переліку лікарських засобів після реєстрації в Україні (внесення номерів реєстраційних посвідчень), за умови, що інспектування проводилося Держлікслужбою до реєстрації цих лікарських засобів в Україні та/або реєстраційні матеріали не були доступні інспекторам (окрім періоду визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, що унеможливлює проведення інспектування за місцем провадження діяльності, в тому числі враховуючи санітарно-епідеміологічну ситуацію);
ненадання до Держлікслужби документальних підтверджень усунення порушень відповідно до строків, встановлених виробником згідно з планом коригувальних та запобіжних дій щодо усунення виявлених порушень, та/або їх невиконання в встановлені строки;
наявність приписів про повну заборону обігу та/або рішень органів державного нагляду (контролю) щодо вилучення з обігу лікарських засобів трьох серій (для стерильних та асептично виготовлених лікарських засобів — однієї серії), які вироблялись на даній дільниці, якщо дефект якості лікарського засобу можливо пов’язаний із технологією виробництва та/або методами його контролю, та/або умовами зберігання та транспортування;
наявність приписів про повну заборону обігу та/або рішень органів державного нагляду (контролю) щодо вилучення з обігу лікарських засобів трьох серій (для інфузійних та ін’єкційних лікарських засобів — однієї серії), які вироблялись на даній дільниці, якщо дефект якості лікарського засобу можливо пов’язаний із технологією виробництва та/або методами його контролю;
наявність фактів виробництва неякісних або фальсифікованих лікарських засобів (у тому числі у разі підозри щодо можливого виробництва фальсифікованої продукції);
встановлення факту виробництва лікарських засобів, не внесених до загального переліку номенклатури продукції;
встановлення факту виробництва лікарських засобів, які можуть бути шкідливими для здоров’я та життя людини, при їх виробництві на одних і тих самих виробничих лініях (наприклад, лікарські засоби з використанням субстанції та/або продукції «іn-bulk», які вважаються високосенсибілізуючими, сильнодіючими або високотоксичними; лікарські засоби, які містять живі клітини, гормони, сульфаніламіди, бета-лактамні антибіотики, такі як пеніциліни, цефалоспорини, пенеми, карбацефеми, монобактами, інші високосенсибілізуючі матеріали, патогенні організми, цитотоксини) або які мають певну небезпеку (наприклад, радіофармацевтичні);
введення в технологічну схему виробництва нової технологічної стадії, технологічної операції або нової одиниці критичного технологічного обладнання;, змін методів контролю якості лікарських засобів;
змін контрактних лабораторій або контактних складів;
технічне переоснащення виробництва із заміною одиниць обладнання, суттєва модернізація або реконструкція виробничої дільниці, у тому числі систем забезпечення виробництва технологічними середовищами;
зміни технологічних параметрів критичних технологічних стадій, якщо заявником не надано матеріалів валідаційних досліджень;
перенесення виробничої дільниці на інші площі або в інші будівлі;
невиконання гарантійних зобов’язань щодо повідомлення стосовно змін щодо перенесення виробничої дільниці на інші площі або в інші будівлі, у тому числі для проміжних виробничих дільниць, включно із контрактними виробничими дільницями, лабораторіями та складами, що задіяні у виробництві лікарського засобу, контролі якості, зберіганні та транспортуванні тощо;.
скасування обмежень, що були підставою для видачі Сертифіката за процедурою оцінки ризиків або за процедурою дистанційної оцінки (у зв’язку з оголошенням країною – виробником надзвичайного стану, надзвичайної ситуації, воєнного стану, у разі стихійного лиха, у випадку офіційного визнання ВООЗ хвороби пандемією та надзвичайною ситуацією в галузі світової охорони здоров’я, що унеможливлює проведення інспектування);
встановлення дат наступних інспектувань відповідно до протоколу оцінки ризиків щодо розрахунку строку наступної інспекції виробництва лікарського засобу на відповідність вимогам GMP.
невиконання гарантійних зобов’язань щодо повідомлення стосовно змін щодо перенесення виробничої дільниці на інші площі або в інші будівлі, у тому числі для проміжних виробничих дільниць, включно із контрактними виробничими дільницями, що задіяні у виробництві лікарського засобу, тощо.
4. У разі виявлення невідповідності виробництва лікарських засобів вимогам GMP, ненадання Заявником/представником Заявника/виробником плану коригувальних та запобіжних дій щодо усунення виявлених порушень та документальних підтверджень щодо усунення порушень вимог GMP у строки, визначені у розділі V цього Порядку, невиконання гарантійних зобов’язань або встановлення факту виробництва лікарських засобів, не внесених до загального переліку номенклатури продукції, Держлікслужба України приймає рішення про зупинення дії або анулювання Сертифіката або Висновку та надає припис про усунення порушень вимог GMP із зазначенням строку його виконання, про що повідомляє Заявнику (представнику Заявника) протягом 10 робочих днів після прийняття відповідного рішення. Після усунення порушень вимог GMP у встановлені строки Держлікслужба України приймає рішення щодо поновлення дії Сертифіката або Висновку (у разі зупинення їх дії).
4. У разі виявлення невідповідності виробництва лікарських засобів вимогам GMP, наявність фактів виробництва неякісних або фальсифікованих лікарських засобів (у тому числі у разі підозри щодо можливого виробництва фальсифікованої продукції), наявність документально підтверджених фактів або ознак виробництва лікарських засобів, які можуть бути небезпечними для здоров’я і життя людей або можуть призвести до тяжких наслідків для здоров’я людей внаслідок можливих порушень технології виробництва та/або методів контролю якості, зберігання та транспортування, ненадання Заявником/представником Заявника/виробником плану коригувальних та запобіжних дій щодо усунення виявлених порушень та документальних підтверджень щодо усунення порушень вимог GMP у строки, визначені у розділі V цього Порядку, та/або його невиконання, невиконання гарантійних зобов’язань, встановлення факту виробництва лікарських засобів, які можуть бути шкідливими для здоров’я та життя людини, при виробництві на одних і тих самих виробничих лініях, та згідно інших підстав пункту 3 цього розділу Держлікслужба приймає рішення про зупинення дії або анулювання Сертифіката або Висновку, про що повідомляє Заявнику (представнику Заявника) протягом 10 робочих днів після прийняття відповідного рішення. Після усунення порушень вимог GMP у встановлені строки Держлікслужба приймає рішення щодо поновлення дії Сертифіката або Висновку (у разі зупинення їх дії).
5. При здійсненні позапланового інспектування з підстав, визначених розділом VI цього Порядку, з метою підтвердження відповідності умов виробництва лікарських засобів вимогам GMP для резидентів та нерезидентів, інспектуванню підлягають лише ті питання, необхідність перевірки яких стала підставою для проведення позапланового інспектування, з обов’язковим зазначенням цих питань у документах на проведення інспектування. Не підлягає перевірці період, який уже був предметом під час перевірки, крім випадків, встановлених за рішенням суду, яке набрало законної сили, або з метою перевірки усунення порушень, що були виявлені під час останнього інспектування. У разі відмови Заявника (представника Заявника) від проведення інспектування за рішенням Держлікслужби, що оформлюється наказом, зупиняється дія Сертифікату або Висновку.
6. При здійсненні позапланового інспектування з підстав, визначених розділом VI цього Порядку, з метою підтвердження відповідності умов виробництва лікарських засобів вимогам GMP для резидентів та нерезидентів установ з отримання плазми та/або місць зберігання плазми, інспекторам повинні бути доступні Досьє виробничої дільниці для установ з отримання плазми та/або Досьє виробничої дільниці для місць зберігання плазми.
5. При здійсненні позапланового інспектування з підстав, визначених розділом VI цього Порядку, інспектуванню підлягають лише ті питання, необхідність перевірки яких стала підставою для проведення позапланового інспектування, з обов’язковим зазначенням цих питань у документах на проведення інспектування. Не підлягає перевірці період, який уже був предметом під час перевірки, крім випадків, встановлених за рішенням суду, яке набрало законної сили, або з метою перевірки усунення порушень, що були виявлені під час останнього інспектування.
VII. Права та обов’язки інспектора при проведенні процедури підтвердження відповідності вимогам GMP
1. Інспектор при здійсненні інспектування виробництва має право:
ознайомлюватися з усіма необхідними для проведення інспектування документами, які стосуються вимог GMP і матеріалів реєстраційного досьє, та одержувати від Заявника, та/або виробника, та/або їх представника необхідні відомості з питань, що належать до його компетенції;
безперешкодно відповідно до Закону України «Про основні засади державного нагляду (контролю) у сфері господарської діяльності» проводити огляд виробничих, складських, допоміжних приміщень (зон), приміщень (зон) контролю якості та інших приміщень (зон) Заявника з метою їх інспектування для з’ясування питань, зазначених в плані та програмі інспектування;
відповідно до Закону України «Про основні засади державного нагляду (контролю) у сфері господарської діяльності» фіксувати процес здійснення інспектування чи кожну окрему дію засобами аудіо- та відеотехніки, не перешкоджаючи здійсненню такого заходу та не порушуючи комерційну таємницю Заявника, про що Заявник та/або виробник має бути попереджений під час вступної наради;
вимагати припинення дій, які перешкоджають здійсненню процедури підтвердження відповідності умов виробництва лікарських засобів вимогам GMP;
призначати експертизу, одержувати пояснення, довідки, документи, матеріали, відомості з питань, що виникають під час процедури підтвердження відповідності вимогам GMP;
відбирати зразки лікарських засобів для лабораторної перевірки їх якості згідно з чинним законодавством України в разі встановлення порушень технології виробництва, вимог щодо якості, умов та/або правил зберігання лікарських засобів, що можуть призвести до виробництва неякісних лікарських засобів та/або оптової, роздрібної торгівлі неякісними лікарськими засобами;
отримувати належним чином завірені копії необхідних документів (витягів з документів), пов’язаних з інспектуванням виробництва на відповідність вимогам GMP;
одержувати від Заявника письмові пояснення з питань, що виникають під час інспектування.
2. Інспектор повинен дотримуватись вимог щодо:
дотримання конфіденційності щодо інформації про Заявника, та/або виробника, та/або їх представника, у тому числі отриманої від нього під час інспектування;
принципів класифікації виявлених під час інспектування порушень;
забезпечення об’єктивності, повноти та достовірності інформації результатів інспектування, в тому числі інформації, що міститься у Звіті та є підставою для прийняття рішення про видачу Сертифіката або Висновку;
відсутності конфлікту інтересів при проведенні робіт із підтвердження відповідності умов виробництва лікарських засобів вимогам GMP, у тому числі під час інспектування;
нерозголошення конфіденційної інформації та інформації, що є комерційною таємницею Заявника та/або виробника, що стає доступною інспектору у процесі підтвердження відповідності умов виробництва лікарських засобів вимогам GMP;
виконання законодавства України, у тому числі положень цього Порядку, та рекомендацій PIC/S.
3. Інспектор зобов’язаний:
дотримуватися ділової етики у взаємовідносинах із Заявником, та/або виробником, та/або їх представником;
не втручатися і не перешкоджати здійсненню господарської діяльності під час здійснення процедури підтвердження відповідності умов виробництва лікарських засобів вимогам GMP, якщо це не вимагається обставинами, які безпосередньо свідчать про виробництво лікарських засобів з критичними порушеннями;
надати Звіт в Держлікслужбу України в строки, передбачені розділом IІІ цього Порядку.
VIIІ. Права та обов’язки Заявника та/або виробника при проведенні процедури підтвердження відповідності умов виробництва лікарських засобів вимогам GMP
1. Заявник та/або виробник є відповідальними за достовірність наданої інформації.
2. Заявник та/або виробник мають право:
вимагати від інспекторів додержання вимог чинного законодавства України;
не допустити інспектора/інспекторів до інспектування без пред’явлення ним/ними документа, що засвідчує особу;
перевіряти наявність в інспектора документа, що засвідчує особу, і одержувати копії документів на проведення інспектування;
бути присутніми під час здійснення інспектування;
вимагати нерозголошення конфіденційної інформації та інформації, що є комерційною таємницею Заявника та/або виробника;
фіксувати процес здійснення інспектування чи кожну окрему дію засобами аудіо- та відеотехніки, не перешкоджаючи здійсненню такого заходу, про що інспектор має бути попереджений під час вступної наради;
надавати обґрунтовані зауваження щодо проведеного інспектування та за бажанням бути присутнім при розгляді результатів інспектування;
одержувати Звіт, а також інші передбачені цим Порядком документи у строки, встановлені цим Порядком;
звернутися до Держлікслужби України з проханням залишити без розгляду Заяву про видачу Сертифіката (Заяву про видачу Висновку) або повідомлення щодо необхідності внесення змін чи переоформлення Переліку лікарських засобів;
у всіх випадках незгоди з результатами проведених експертиз, процесом інспектування та результатами інспектування, включаючи, але не обмежуючись, розгляд зауважень та заперечень Заявника та/або виробника, прийняті рішення щодо видачі Сертифіката або Висновку або відмови у їх видачі, зупинення або анулювання дії Сертифіката або Висновку тощо, оскаржувати їх в установленому законодавством порядку.
3. Заявник та/або виробник зобов’язаний:
повідомляти Держлікслужбу України про зміни, які стосуються виробничої дільниці (у тому числі про зміну ліцензії на виробництво лікарських засобів, зміну найменування Заявника, його місцезнаходження, перенесення виробничої дільниці на інші площі тощо);
надавати для ознайомлення на запит Держлікслужби та/або залучених уповноважених організацій, учених та фахівців перед проведення інспектування та під час інспектування реєстраційні матеріали на зареєстровані лікарські засоби та/або на лікарські засоби, що подаються на державну реєстрацію або при внесенні відповідних змін до реєстраційних матеріалів на зареєстровані в Україні лікарські засоби;
надавати на запит інспектора всю необхідну інформацію, забезпечувати можливість проведення огляду виробничих, допоміжних, складських приміщень, обладнання, зон контролю якості, інтерв’ювання представників (персоналу) виробника, ознайомлення з необхідною реєстраційної документацією та документацією системи якості тощо, ознайомлення та огляд яких необхідні для з’ясування викладених у плані та програмі інспектування питань;
виконувати вимоги Держлікслужби України щодо усунення виявлених порушень вимог GMP та чинного законодавства України;
виконувати передбачені цим Порядком вимоги Держлікслужби України щодо усунення виявлених під час первинної або спеціалізованої експертиз або під час інспектування порушень вимог чинного законодавства України;
надавати копії документів, зразки продукції, пояснення, довідки, відомості, матеріали з питань, що виникають під час процедури підтвердження відповідності вимогам GMP.
I. Загальні положення
1.1. Цей Порядок розроблено відповідно до Закону України «Про лікарські засоби», з урахуванням вимог директив 2001/83/ЄС, 2003/94/ЄС Європейського Парламенту та Ради Європейського Союзу (далі – ЄС), рекомендацій міжнародної Системи співробітництва фармацевтичних інспекцій (PIC/S) (документ РІ 002) та Всесвітньої організації охорони здоров’я (WHO TRS № 908, 2003).
1.2. Проведення підтвердження відповідності умов виробництва лікарських засобів чинним в Україні вимогам належної виробничої практики (далі – GMP) запроваджено з метою доведення, що лікарські засоби постійно виробляються і контролюються згідно із стандартами якості, які відповідають їх призначенню, а також відповідно до вимог реєстраційного досьє або специфікації на цю продукцію. Проведення підтвердження відповідності умов виробництва активних фармацевтичних інгредієнтів (субстанцій) вимогам GMP здійснюється за бажанням заявника.
1.3. Підтвердження відповідності умов виробництва вимогам GMP для резидентів та нерезидентів здійснюється Державною службою України з лікарських засобів (далі – Держлікслужба України) шляхом проведення експертизи документів, поданих відповідно до цього Порядку, та інспектування виробництва у випадках, передбачених цим Порядком.
1.4. Відповідно до цього Порядку проводиться підтвердження відповідності умов виробництва лікарських засобів вимогам GMP на виробничих дільницях, згідно із відповідною заявою:
на видачу сертифіката відповідності вимогам належної виробничої практики згідно здодатком 1 до цього Порядку (далі – Заява на видачу Сертифіката);на видачу висновку щодо підтвердження відповідності вимогам належної виробничої практики згідно з додатком 2 до цього Порядку (далі – Заява на видачу Висновку) (у разі наявності у виробника офіційного документа щодо відповідності виробництва лікарських засобів вимогам GMP, виданого уповноваженим органом країни – члена PIC/S).
1.5. Згідно з цим Порядком Держлікслужба України видає документи, що підтверджують відповідність виробництва лікарських засобів вимогам GMP:
сертифікат відповідності вимогам належної виробничої практики;висновок щодо підтвердження відповідності вимогам належної виробничої практики.
1.6. У цьому Порядку терміни вживаються у таких значеннях:
активний фармацевтичний інгредієнт (лікарська речовина, діюча речовина, субстанція) (далі – АФІ або діюча речовина) – будь-яка речовина чи суміш речовин, що призначена для використання у виробництві лікарського засобу і під час цього використання стає його активним інгредієнтом. Такі речовини мають фармакологічну чи іншу безпосередню дію на організм людини, у складі готових форм лікарських засобів їх застосовують для лікування, діагностики чи профілактики захворювання, для зміни стану, структур або фізіологічних функцій організму, для догляду, обробки та полегшення симптомів;
атестована лабораторія – лабораторія з контролю якості та безпеки лікарських засобів, яка пройшла галузеву атестацію Держлікслужбою України відповідно до Порядку проведення галузевої атестації лабораторій з контролю якості та безпеки лікарських засобів, затвердженого наказом Міністерства охорони здоров’я України від 14 січня 2004 року № 10, зареєстрованим у Міністерстві юстиції України 30 січня 2004 року за № 130/8729;
виробник лікарських засобів – суб’єкт господарювання (юридична особа), який здійснює хоча б один із етапів виробництва лікарських засобів та має ліцензію (дозвіл) на виробництво лікарських засобів (якщо останнє передбачено національним законодавством країни, на території якої знаходяться виробничі потужності виробника);
виробництво лікарських засобів – діяльність, пов’язана із серійним випуском лікарських засобів, яка включає всі або хоча б одну зі стадій технологічного процесу, у тому числі закупівлю матеріалів і продукції, фасування, пакування та/або маркування, зберігання, відповідний контроль, видачу дозволу на випуск, а також оптову торгівлю (дистрибуцію) продукцією власного виробництва;
висновок щодо підтвердження відповідності виробництва лікарського засобу вимогам належної виробничої практики (GMP) (далі – Висновок) – документ, виданий Держлікслужбою України, який засвідчує, що за результатами проведеної експертизи поданих документів офіційний документ щодо відповідності виробництва лікарських засобів вимогам GMP, виданий уповноваженим органом країни – члена PIC/S, вважається таким, що підтверджує відповідність виробництва лікарських засобів чинним в Україні вимогам GMP;
заявник – юридична або фізична особа (суб’єкт господарювання) – власник реєстраційного посвідчення (торгової ліцензії) та/або ліцензії на виробництво лікарських засобів, яка подає до Держлікслужби України, особисто або через уповноважену особу (представника), що знаходиться в Україні, заяву на видачу Сертифіката або Висновку, та яка відповідає за достовірність наданої інформації та документів;
зразок (проба) від серії – частина від серії, відібрана таким чином і в такій кількості, що є репрезентативною для всієї серії;
інспектор – посадова особа Держлікслужби України та/або фахівець, які мають вищу освіту за однією з таких спеціальностей: фармація, промислова фармація, технологія фармацевтичних препаратів, хімія, біологія, мікробіологія, біотехнологія, мають досвід роботи у виробництві лікарських засобів, контролі якості, управлінні (забезпеченні) якістю або створенні лікарських засобів та мають підтвердження компетентності з питань GMP або проходить навчання з цих питань;
інспектування (перевірка) – процедура оцінки відповідності системи забезпечення якості підприємства (виробничої дільниці) та фактичного стану наявного виробництва лікарських засобів чинним в Україні вимогам GMP за місцем провадження діяльності (адресою розташування виробничих потужностей);
країна – член PIC/S – країна, що має уповноважений орган у сфері контролю якості лікарських засобів, який є членом міжнародної Системи співробітництва фармацевтичних інспекцій (Pharmaceutical Inspection Cooperation Scheme, PIC/S);
критичне порушення вимог GMP – порушення (невідповідність) вимог GMP або вимог реєстраційного досьє на лікарський засіб, яке призвело або може призвести до виробництва неякісного лікарського засобу, оптової, роздрібної торгівлі неякісними лікарськими засобами, що можуть завдати шкоди здоров’ю або життю людини;
лабораторний аналіз якості зразків лікарських засобів – аналіз зразків лікарських засобів на відповідність вимогам специфікації якості за методами контролю якості лікарських засобів, які зазначені в матеріалах реєстраційного досьє або методами, встановленими Державною фармакопеєю України, шляхом
проведення відповідних випробувань в атестованій лабораторії, результатом якої є письмовий висновок про якість серії лікарського засобу;
належна виробнича практика (Good Manufacturing Practice, GMP) – частина системи забезпечення якості, яка гарантує, що лікарські засоби постійно виробляються і контролюються відповідно до стандартів якості, які відповідають їх призначенню, а також відповідно до вимог реєстраційного досьє та специфікації на цю продукцію;
несуттєве порушення вимог GMP – порушення (невідповідність) вимог GMP, яке не може призвести до виробництва неякісного лікарського засобу, оптової, роздрібної торгівлі неякісними лікарськими засобами та яке не належить до критичних або суттєвих порушень;
офіційний документ щодо відповідності виробництва вимогам GMP, виданий уповноваженим органом країни – члена PIC/S, – сертифікат відповідності виробництва вимогам GMP, або ліцензія на виробництво лікарських засобів, або інший документ щодо відповідності виробництва вимогам GMP, виданий уповноваженим органом країни – члена PIC/S;
первинна експертиза – перевірка комплектності поданих документів, визначення необхідності уточнення поданих чи надання додаткових відомостей, яка проводиться працівниками Держлікслужби України;
підтвердження відповідності вимогам GMP – процедура письмового підтвердження Держлікслужбою України відповідності виробництва лікарських засобів чинним в Україні вимогам GMP;
представник Заявника (уповноважена особа, що виступає від імені Заявника) – юридична або фізична особа, яка діє на підставі відповідного доручення (довіреності), в якому Заявником надано право представляти його інтереси при проведенні процедур підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (GMP), реєстрації, перереєстрації та/або внесення змін до реєстраційних матеріалів лікарських засобів на території України;
прекваліфікація лікарського засобу – стандартизована процедура оцінки якості лікарського засобу Всесвітньою організацією охорони здоров’я (далі – ВООЗ) з метою оцінки якості, безпечності та ефективності;
препарат обмеженого застосування (препарат-сирота) – лікарський засіб, що призначений для діагностики, профілактики чи лікування рідкісного захворювання, тобто захворювання, що загрожує життю чи призводить до втрати працездатності зазвичай не більше 5 осіб з кожних 10000 жителів на момент подання заяви про державну реєстрацію;
продукція «in bulk» – будь-який лікарський засіб, призначений для виробництва готового лікарського засобу, який пройшов усі стадії технологічного процесу, крім стадії фасування та/або кінцевого пакування і маркування;
сертифікат відповідності вимогам належної виробничої практики (далі – Сертифікат) – документ, виданий Держлікслужбою України за результатами інспектування, який засвідчує відповідність виробництва лікарських засобів чинним в Україні вимогам GMP;
спеціалізована експертиза – експертиза поданих документів на відповідність вимогам GMP, аналіз їх повноти і достовірності наданої інформації;
суттєве порушення вимог GMP – порушення (невідповідність) вимог GMP, яке призвело або може призвести до виробництва неякісного лікарського засобу, оптової, роздрібної торгівлі неякісними лікарськими засобами, але не може завдати шкоди здоров’ю або життю людини, або порушення (невідповідність) вимог реєстраційного досьє на лікарський засіб, або поєднання декількох несуттєвих порушень (невідповідностей), жодне з яких не може бути класифіковано як суттєве, але які у сукупності являють собою суттєве порушення (невідповідність) і повинні тлумачитися та зазначатися як таке.
ІІ. Етапи підтвердження відповідності вимогам GMP
2.1. Процедура підтвердження відповідності вимогам GMP включає такі етапи:
подання до Держлікслужби України Заяви на видачу Сертифіката або Заяви на видачу Висновку та комплекту документів, передбаченого цим Порядком;перевірку та опрацювання поданої Заяви на видачу Сертифіката або Заяви на видачу Висновку та комплекту документів (включаючи первинну експертизу та спеціалізовану експертизу, які здійснюються на безоплатній основі);інспектування (перевірку) виробництва лікарських засобів за місцем провадження діяльності у випадках, передбачених цим Порядком;прийняття рішення щодо видачі документа про відповідність виробництва лікарських засобів чинним в Україні вимогам GMP або вмотивованого висновку про відмову у його видачі;внесення змін до чинного документа про відповідність виробництва лікарських засобів чинним в Україні вимогам GMP у випадках, передбачених цим Порядком.
2.2. Для підтвердження відповідності виробництва лікарських засобів вимогам GMP Заявник (представник Заявника) подає до Держлікслужби Заяву на видачу Сертифіката за формою згідно з додатком 1 до цього Порядку або Заяву на видачу Висновку за формою згідно з додатком 2 до цього Порядку, до яких додаються такі документи:
1) копія заяви про державну реєстрацію (перереєстрацію) лікарського засобу, що була подана до МОЗ України, засвідчена підписом і печаткою Заявника або його представника (за наявності) – для лікарських засобів, що подаються на державну реєстрацію (перереєстрацію) або при внесенні відповідних змін, що стосуються зміни виробника або його виробничих потужностей або внесення додаткового виробника до реєстраційних матеріалів зареєстрованих в Україні лікарських засобів (за наявності);
2) засвідчена в установленому порядку копія офіційного документа, який дає право на здійснення господарської діяльності з виробництва лікарських засобів та виданий відповідним державним органом країни, де розташоване виробництво, на виробничу дільницю, що вказана в Заяві, та засвідчений в установленому порядку переклад українською та англійською мовами (для нерезидентів). Якщо згідно із законодавством країни-виробника ліцензія на виробництво існує лише в електронному вигляді, мають бути надані роздруківка із посиланням на відповідний офіційний сайт, засвідчена підписом/печаткою Заявника, та переклад українською мовою.
Якщо вищезазначений документ внесено до бази даних EudraGMP, Заявник надає посилання на цю базу даних. При цьому копію такого документа засвідчує Заявник;
3) засвідчена в установленому порядку копія офіційного документа, виданого державним органом країни, де розташовано виробництво, про відповідність вимогам GMP виробничої дільниці, що вказана в Заяві (за наявності); засвідчені в установленому порядку копії додатків до цього документа з переліком лікарських засобів (за наявності) та засвідчені в установленому порядку переклади українською та англійською мовами цих документів.
Якщо вищезазначені документи внесено до бази даних EudraGMP, Заявник надає посилання на цю базу даних. При цьому копію такого документа з додатками (за наявності) засвідчує Заявник;
4) засвідчена в установленому порядку копія офіційного документа щодо відповідності виробництва вимогам GMP, виданого уповноваженим органом країни – члена PIC/S (за наявності); засвідчені в установленому порядку копії додатків до такого документа з переліком лікарських засобів (за наявності) та засвідчені в установленому порядку переклади цих документів українською та англійською мовами.
Якщо вищезазначені документи внесено до бази даних EudraGMP, Заявник надає посилання на цю базу даних. При цьому копію документа з додатками (за наявності) засвідчує Заявник.
5) копія досьє виробничої дільниці (Site Master File) та його переклад на українську та/або англійську мову, засвідчені Заявником (для нерезидентів, за винятком виробників, виробничі потужності яких знаходяться на території країн- членів PIC/S). У разі повторної процедури підтвердження відповідності вимогам GMP копія досьє виробничої дільниці подається за наявності суттєвих змін;
6) засвідчена Заявником копія звіту, складеного за результатами останньої перевірки, проведеної уповноваженим органом країни – члена PIC/S (для нерезидентів, виробничі потужності яких розташовані за межами території країн – членів PIC/S). При цьому перевірка повинна бути проведена не пізніше ніж за 3 роки до подання Заяви. У разі відмови виробника у наданні копії звіту, Заявник може звернутися до Держлікслужби України із клопотанням про здійснення запиту щодо надання такого звіту уповноваженим органом країни – члена PIC/S, що здійснював зазначену перевірку (до листа-звернення додається копія листа відмови виробника);
7) інформація щодо останньої перевірки, проведеної за програмою прекваліфікації ВООЗ. При цьому перевірка повинна бути проведена не пізніше ніж за 3 роки до подання Заяви (для лікарських засобів, що постачаються в Україну Глобальним фондом і пройшли прекваліфікацію ВООЗ (за наявності);
8) довідка про якість продукції, що виробляється, згідно з додатком 3 до цього Порядку;
9) довідка про результати перевірок виробничої дільниці, проведених органами державного контролю, за формою згідно з додатком 4 до цього Порядку, що зазначена в Заяві;
10) перелік лікарських засобів, які зареєстровані в Україні та/або плануються до реєстрації і виробництво яких вже здійснюється (за наявності) або планується здійснювати на виробничій дільниці, що вказана в Заяві, за формою згідно з додатком 5 до цього Порядку. Такий перелік подається в письмовій формі та на електронному носії інформації (файл Excel);
11) копії сертифікатів лікарського засобу (СРР) для міжнародної торгівлі (для незареєстрованих лікарських засобів, які плануються до реєстрації або перереєстрації в Україні);
12) гарантійні листи згідно з додатком 6 (за Формою 1 – про суттєві зміни, які стосуються виробничої дільниці, що пройшла підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (GMP); за Формою 2 – про завершення процедури підтвердження або надання звіту останньої перевірки, проведеної уповноваженим органом країни – члена PIC/S).
У випадку, якщо будь-який документ(и) із зазначеного вище переліку, який подано до Держлікслужби з метою отримання Висновку, містить конфіденційну інформацію, яку виробник не може розкрити представнику Заявника в Україні, виробник може надіслати такий документ(и) безпосередньо до Держлікслужби України. Після отримання такого документа(ів), Держлікслужба своїм листом інформує представника Заявника про їх надходження на розгляд у строк до 10 робочих днів або розміщує цю інформацію на сайті Держлікслужби України.
2.3. Для виробників-резидентів підтвердження відповідності вимогам GMP здійснюється Держлікслужбою України за результатами планової перевірки додержання Ліцензійних умов провадження господарської діяльності з виробництва лікарських засобів, оптової, роздрібної торгівлі лікарськими засобами, затверджених наказом МОЗ України від 31 жовтня 2011 року № 723, зареєстрованих у Міністерстві юстиції України 7 грудня 2011 року за № 1420/20158 (далі – планова перевірка додержання Ліцензійних умов), проведеної відповідно до Порядку контролю за додержанням Ліцензійних умов провадження господарської діяльності з виробництва лікарських засобів, оптової, роздрібної торгівлі лікарськими засобами, затвердженого наказом МОЗ України від 31 жовтня 2011 року № 724, зареєстрованим у Міністерстві юстиції України 7 грудня 2011 року за № 1421/20159.
За відсутності критичних порушень в акті планової перевірки додержання Ліцензійних умов Держлікслужба України відповідно до розділу V цього Порядку протягом 30 робочих днів видає ліцензіату Сертифікат. Для цього ліцензіат протягом 10 робочих днів після проведення планової перевірки надає до Держлікслужби України перелік номенклатури продукції(зареєстрованих в Україні лікарських засобів) за формою згідно з додатком 5 до цього Порядку (в письмовому вигляді та на електронному носії інформації (файл Excel).
У разі наявності критичних порушень, виявлених у ході останньої планової перевірки додержання Ліцензійних умов, та у разі відсутності документальних підтверджень про їх усунення Держлікслужба України приймає рішення про відмову у видачі Сертифіката згідно зрозділом V цього Порядку. За наявності документальних підтверджень про усунення критичних порушень, виявлених під час останньої планової перевірки додержання Ліцензійних умов, проводиться інспектування за місцем провадження виробництва (виробничої дільниці) відповідно до поданої ліцензіатом заяви на видачу сертифіката.
2.4. Заява та документи, що додаються до неї, приймаються за описом документів, що додаються до Заяви на видачу Сертифіката або Заяви на видачу Висновку, згідно з додатком 7 до цього Порядку, копія якого видається Заявнику з відміткою про дату прийняття документів Держлікслужбою України та підписом відповідальної особи.
2.5. Держлікслужба України здійснює первинну експертизу поданих документів з метою перевірки їх комплектності, а також аналізу повноти наданої інформації.
2.6.Для проведення лабораторного аналізу якості зразків лікарських засобів та інспектування Держлікслужбою України можуть залучатися підприємства, установи, організації (за згодою).
2.7. Для нерезидентів, які не мають офіційних документів щодо відповідності виробництва вимогам GMP, виданих уповноваженим органом країни – члена PIC/S, або якщо виробництво лікарських засобів здійснюється у країні, з якою Україна не має міжнародного договору про взаємне визнання результатів інспектування на відповідність виробництва лікарських засобів вимогам GMP, додатково до проведення експертизи документів здійснюється інспектування виробництва (виробничої дільниці) відповідно до розділу ІV цього Порядку.
2.8. Для лікарських засобів, що пройшли прекваліфікацію ВООЗ, та які постачає або планує постачати Глобальний фонд, інспектування для нерезидентів не здійснюється.
2.9. При проведенні підтвердження виробництва вимогам GMP мають бути зазначені усі проміжні виробничі дільниці (включно з контрактними дільницями), що задіяні у процесі виробництва готового лікарського засобу. Для проведення підтвердження виробництва, яке здійснює випуск готових лікарських засобів із форми «in bulk», виробництво всієї продукції у формі «in bulk», яка використовується в процесі випуску цих лікарських засобів, повинно матиСертифікати або Висновки, видані згідно з цим Порядком, окрім випадків, зазначених упідпунктах 2.9.1 та 2.9.2 цього пункту.
2.9.1. У разі якщо сертифікація серій готового лікарського засобу та видача дозволу на їх випуск здійснюються виробником на території країни – члена ЄС або на території країни, із якою ЄС укладено договір про взаємне визнання результатів інспектування, і якщо уповноважений орган відповідної вказаної країни є членом PIC/S, Заявник разом із Заявою на видачу Висновку подає:
перелік документів відповідно до пункту 2.2 цього розділу – для виробника, що здійснює видачу дозволу на випуск серій;засвідчені підписом та печаткою (за наявності) Заявника або представника Заявника копії документів та їх переклади українською мовою, зазначені у підпунктах 2 та 4 пункту 2.2 цього розділу – для проміжних виробничих дільниць, у тому числі контрактних, що задіяні у виробництві лікарського засобу та розташовані на території країни – члена ЄС, або на території країни, із якою ЄС укладено договір про взаємне визнання результатів інспектування, а також мають офіційні документи щодо відповідності виробництва вимогам GMP, видані уповноваженим органом країни -ч лена PIC/S;засвідчені підписом та печаткою (за наявності) Заявника або представника Заявника копії документів та їх переклади українською мовою, зазначені у підпунктах 2, 4, 6 пункту 2.2 цього розділу – для проміжних виробничих дільниць, включно із контрактними виробничими дільницями, що задіяні у виробництві лікарського засобу та розташовані поза територією країни – члена ЄС і поза територією країни, із якою ЄС укладено договір про взаємне визнання результатів інспектування, які мають офіційні документи щодо відповідності виробництва вимогам GMP, видані уповноваженим органом країним – члена PIC/S. Копія документа, зазначеного у підпункті 6 пункту 2.2 цього розділу, для проміжної стадії виробництва (уключаючи контрактну виробничу ділянку), подається не пізніше шести місяців після отримання Висновку під гарантійні зобов’язання Заявника. У разі ненадання Заявником копії документа, зазначеного у підпункті 6 пункту 2.2 цього розділу, у шестимісячний строк Держлікслужба України приймає рішення про анулювання виданого Висновку або його переоформлення шляхом вилучення цього лікарського засобу із переліку лікарських засобів, який є невід’ємною частиною Висновку.
При цьому видача Держлікслужбою України окремих Висновків для проміжних виробничих дільниць (уключаючи контрактні виробничі дільниці) не здійснюється.
2.9.2. У разі якщо сертифікація серій готового лікарського засобу та видача дозволу на їх випуск здійснюються виробником, який має офіційний документ щодо відповідності виробництва вимогам GMP, виданий уповноваженим органом країни – члена PIC/S, Заявник разом із Заявою на видачу Висновку подає:
перелік документів, визначений пунктом 2.2 цього розділу, – для виробника, що здійснює видачу дозволу на випуск серій;
документи, зазначені в підпунктах 2, 4, 6 пункту 2.2 цього розділу, – для проміжних виробничих дільниць, уключаючи контрактні виробничі дільниці, що задіяні у виробництві лікарського засобу, які мають офіційні документи щодо відповідності виробництва вимогам GMP, видані уповноваженим органом країни – члена PIC/S.
При цьому видача Держлікслужбою України окремих Висновків для проміжних виробничих дільниць (уключаючи контрактні виробничі дільниці), що мають офіційні документи щодо відповідності виробництва вимогам GMP, видані уповноваженим органом країни – члена PIC/S, не здійснюється.
Для лікарського засобу, проміжні стадії виробництва (уключаючи контрактні виробничі дільниці) якого здійснюються на виробничих дільницях, що не мають офіційних документів щодо відповідності виробництва вимогам GMP, виданих уповноваженим органом країни – члена PIC/S, на підставі гарантійних зобов’язань Заявника щодо завершення в строк не більше шести місяців процедури підтвердження відповідності вимогам GMP Держлікслужбою України видається Висновок. У разі невиконання Заявником гарантійних зобов’язань або прийняття Держлікслужбою України негативного рішення щодо підтвердження відповідності вимогам GMP Держлікслужба України приймає рішення про анулювання виданого Висновку або його переоформлення шляхом вилучення такого лікарського засобу із переліку лікарських засобів, який є невід’ємною частиною Висновку.
2.10. Підтвердження відповідності вимогам GMP виробництва препаратів обмеженого застосування (препаратів-сиріт) здійснюється позачергово без проведення інспектування за зверненням Заявника або МОЗ України (у разі необхідності).
ІІІ. Строки підтвердження відповідності вимогам GMP
3.1. Строк проведення первинної експертизи поданих документів, що проводиться Держлікслужбою України з метою перевірки їх комплектності, відповідності форми таких документів законодавству, у тому числі вимогам цього Порядку, становить не більше 5 робочих днів після реєстрації Заяви.
3.2. Спеціалізована експертиза, що проводиться Держлікслужбою України з метою складання вмотивованого висновку щодо підтвердження відповідності виробництва лікарських засобів вимогам GMP, проводиться у такі строки:
за умови надання офіційного документа щодо відповідності виробництва вимогам GMP, виданого уповноваженим органом країни – члена PIC/S, – не більше ніж 10 робочих днів після проведення первинної експертизи;за умови надання інформації щодо останньої перевірки, проведеної за програмою прекваліфікації ВООЗ, – не більше ніж 10 робочих днів;за умови існування міжнародних договорів України щодо взаємного визнання результатів інспектування між Україною та країною, де розташовано виробництво Заявника, – не більше ніж 10 робочих днів після проведення первинної експертизи;в усіх інших випадках – не більше ніж 15 робочих днів після проведення первинної експертизи.
3.3. У разі некомплектності або невідповідності вимогам цього Порядку доданих до Заяви документів, виявлених під час проведення первинної або спеціалізованої експертизи, Заявнику надається письмове повідомлення. Час, необхідний для усунення Заявником виявлених порушень або для надання необхідних документів, не включається до строків проведення первинної або спеціалізованої експертизи.
3.4. Якщо Заявник протягом 30 робочих днів після отримання повідомлення не усуває виявлені порушення або не надає необхідного комплекту документів відповідно до вимог цього Порядку, Заява залишається без розгляду, про що Держлікслужба України в письмовій формі повідомляє Заявника. У разі необхідності продовжити строк надання необхідної інформації Заявник повинен надати відповідне обґрунтування причини і необхідного йому додаткового строку.
3.5. Копії плану та програми інспектування надсилаються за місцезнаходженням Заявника або представника Заявника у строк не пізніше ніж за 5 робочих днів до дати початку інспектування. Призначення дати інспектування здійснюється у строк, що не перевищує шести місяців з дати подання заяви Заявником, якщо немає інших строків, запропонованих Заявником.
3.6. Проведення інспектування за місцем провадження діяльності (виробничих дільниць) має становити не більше 15 робочих днів.
3.7. Складання звіту за результатами інспектування виробництва (виробничої дільниці) становить не більше 10 робочих днів з дати закінчення інспектування.
3.8. Лабораторний аналіз якості зразків лікарських засобів, що були відібрані при проведенні інспектування, становить не більше ніж 14 робочих днів з дня надходження відібраних зразків до лабораторії з контролю якості та безпеки лікарських засобів або в строк, передбачений відповідними методами контролю якості лікарських засобів виробника. При цьому наявність необхідних стандартних зразків забезпечує Заявник. Час, потрібний Заявнику для забезпечення стандартними зразками, не включається до строків виконання лабораторного аналізу.
3.9. Оформлення та видача Сертифіката або Висновку, або письмового повідомлення щодо неможливості видачі Сертифіката або Висновку становлять не більше 10 робочих днів після оформлення звіту про інспектування або отримання результатів спеціалізованої експертизи.
3.10. Проект Сертифіката або Висновку з відповідним переліком лікарських засобів надсилається електронною поштою або факсом Заявнику з метою погодження. Заявник у строк, що не перевищує 5 робочих днів, засвідчує підписом проект Сертифіката або Висновку з відповідним переліком лікарських засобів. Час, потрібний Заявнику для погодження проекту Сертифіката або Висновку з відповідним переліком лікарських засобів, не включається до строків оформлення та видачі Сертифіката або Висновку.
3.11. Оформлення внесення змін до Висновку, Сертифіката, або переліку лікарських засобів до Висновку чи Сертифіката здійснюється у порядку, визначеному пунктом 5.10 розділу V цього Порядку, у строк не більше ніж 10 робочих днів.
ІV. Порядок проведення інспектування на відповідність вимогам належної виробничої практики (GMP)
4.1. Інспектування виробництва (виробничої дільниці) здійснюється з метою підтвердження відповідності виробництва лікарського засобу вимогам до виробництва лікарських засобів в Україні.
4.2. За необхідності перед проведенням інспектування виробництва (виробничої дільниці) група інспекторів має право ознайомитися із реєстраційними матеріалами на зареєстровані лікарські засоби та/або на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію), або при внесенні відповідних змін до реєстраційних матеріалів зареєстрованих в Україні лікарських засобів.
4.3. Інспектування виробництва (виробничої дільниці) здійснюється:
у разі звернення Заявника;для нерезидентів, які не мають офіційних документів щодо відповідності виробництва вимогам GMP, виданих уповноваженим органом країни – члена PIC/S;для виробництв лікарських засобів, які розташовані у країнах, з якими Україна не має договору про взаємне визнання результатів інспектування;у разі прийняття рішень щодо вилучення з обігу в установленому порядку серій лікарського засобу, які вироблялись на даній дільниці, що пов’язані з якістю лікарського засобу;у разі встановлення під час проведення експертизи ймовірності виробництва лікарських засобів, які можуть бути небезпечними для здоров’я і життя людей або можуть призвести до тяжких наслідків для здоров’я людей, або фальсифікованих лікарських засобів.
4.4. Інспектування виробництва (виробничої дільниці) здійснюється відповідно до плану та програми інспектування, де визначено мету, об’єкти, дати проведення інспектування, призначено інспектора або групу інспекторів. Копії плану та програми інспектування надсилаються за місцезнаходженням Заявника у строки, визначені розділом ІІІ цього Порядку.
4.5. Для здійснення інспектування виробництва, виконання окремих робіт, участі у вивченні окремих питань Держлікслужба України може залучати учених і фахівців (за їх згодою).
4.6. За результатами інспектування виробництва інспектор складає звіт українською мовою у двох примірниках за формою, наведеною в додатку 8 до цього Порядку. Додатково для нерезидентів звіт може бути оформлений англійською або російською мовами у строк не пізніше ніж 15 робочих днів з дня складання звіту українською мовою.
4.7. Один примірник звіту надається Заявнику або представнику Заявника. Інший примірник звіту та матеріали інспектування зберігаються в Держлікслужбі України протягом строку дії Сертифіката або Висновку, але не менше ніж три роки.
4.8. Якщо в процесі інспектування було відібрано зразки для лабораторного аналізу їх якості, до звіту додаються:
акт відбору зразків продукції;направлення на випробування;проект методів контролю якості лікарського засобу, що надається Заявником;письмовий висновок атестованої лабораторії про якість серії лікарського засобу (після надання його зразків).
V. Порядок прийняття рішення про видачу або відмову у видачі Сертифіката або Висновку
5.1. У разі прийняття позитивного рішення за результатами проведеної спеціалізованої експертизи Держлікслужба України (на безоплатній основі) надає Заявнику Висновок за формою згідно з додатком 10 до цього Порядку у строки, зазначені у розділі ІІІ цього Порядку.
Висновок Держлікслужби України видається на строк дії офіційного документа щодо відповідності виробництва вимогам GMP, виданого уповноваженим органом, який є членом PIC/S.
Строк дії Висновку продовжується за рішенням Держлікслужби України до шести місяців у разі надання Заявником інформації щодо проведення інспектування на відповідність вимогам GMP уповноваженим органом країни – члена PIC/S, про що Держлікслужба України письмово повідомляє Заявнику у строк не більше 10 робочих днів.
5.2. Після проведення інспектування виробництва (виробничої дільниці) або експертизи поданих документів у разі позитивного висновку, що міститься у звіті, з урахуванням результатів експертизи документів Держлікслужба України у строки, визначені розділом ІІІцього Порядку, видає заявнику Сертифікат за формою згідно з додатком 9 до цього Порядку або Висновок за формою згідно з додатком 10 до цього Порядку. Строк дії Сертифіката становить три роки від дати проведення інспектування.
У разі якщо строк дії ліцензії закінчився (для нерезидентів) у період дії Сертифіката, Заявник надає засвідчену в установленому порядку копію ліцензії до Держлікслужби України у тримісячний строк з дня отримання нової ліцензії.
Уразі ненадання Заявником засвідченої в установленому порядку копії ліцензії Держлікслужба України приймає рішення щодо зупинення дії Сертифіката.
5.3. Про видачу Сертифіката або Висновку приймається наказ Держлікслужби України. До Сертифіката або Висновку додається перелік лікарських засобів, зареєстрованих або запланованих до реєстрації в Україні, згідно з додатком 11 до цього Порядку, який є невід’ємною частиною Сертифіката або Висновку.
5.4. За наявності у звіті порушень (невідповідностей) вимогам належної виробничої практики Заявник повинен вжити заходів щодо приведення виробництва у відповідність до правил GMP, надати до Держлікслужби України план коригувальних та запобіжних дій щодо усунення виявлених порушень (невідповідностей) за формою згідно з додатком 12 до цього Порядку та документальні підтвердження щодо усунення порушень (невідповідностей) у строк до 90 календарних днів. У разі ненадання Заявником плану коригувальних та запобіжних дій та документальних підтверджень щодо усунення порушень (невідповідностей) у встановлені строки Держлікслужба України може прийняти рішення про зупинення дії Сертифікатавідповідно до пункту 6.4 розділу VІ цього Порядку.
5.5. У разі якщо протягом строку дії Сертифіката або Висновку Заявник повідомляє Держлікслужбу України про зміну найменування сертифікованої виробничої дільниці або зміну ліцензії на виробництво лікарських засобів, у тому числі пов’язану зі зміною найменування Заявника, Держлікслужба України переоформлює Сертифікат або Висновок у строки, зазначені у розділі ІІІ цього Порядку. Переоформлений Сертифікат або Висновок видається Заявнику, попередній Сертифікат або Висновок підлягає поверненню до Держлікслужби України.
5.6. Для резидентів у разі анулювання ліцензії на виробництво лікарських засобівСертифікат анулюється наказом Держлікслужби України.
5.7. У разі негативного рішення Держлікслужба України інформує Заявника про вмотивовану відмову в наданні Сертифіката або Висновку у строки, зазначені у розділі ІІІцього Порядку.
5.8. Рішення про відмову у видачі Сертифіката або Висновку оформляється наказом Держлікслужби України та приймається у разі:
виявлення недостовірних відомостей у Заяві або документах, що додавалися до Заяви відповідно до цього Порядку;встановлення критичних порушень вимог GMP за результатами інспектування.
5.9. За наявності у звіті критичних порушень (невідповідностей) вимогам GMP Заявник вживає заходи щодо їх усунення, надає до Держлікслужби України план коригувальних та запобіжних дій щодо усунення виявлених порушень (невідповідностей) згідно з додатком 12 до цього Порядку та документальні підтвердження про усунення порушень (невідповідностей). Заявник може надати до Держлікслужби України письмове звернення щодо проведення інспектування з метою перевірки усунення порушень (невідповідностей). У разі підтвердження за результатами інспектування усунення порушень (невідповідностей) Держлікслужба України приймає рішення про видачу Заявнику Сертифіката згідно з додатком 9 до цього Порядку абоВисновку згідно з додатком 10 до цього Порядку.
5.10. У разі виникнення необхідності внесення змін до Висновку чи Сертифіката, або до переліку лікарських засобів, які додаються до Висновку чи Сертифіката (поновлення реєстрації в Україні; зміна назви лікарського засобу, найменування виробника чи його місцезнаходження), Заявник інформує Держлікслужбу України.
Заявник після реєстрації, або перереєстрації лікарських засобів, або внесення змін до реєстраційної документації (зокрема зміни місця виробництва) подає до Держлікслужби України відповідне повідомлення, перелік номенклатури продукції зі змінами згідно з додатком 5 до цього Порядку (у паперовому вигляді та на електронному носії інформації) та копії реєстраційних посвідчень на лікарські засоби. Держлікслужба України протягом 10 робочих днів з дня отримання відповідних документів складає і затверджує оновлений перелік лікарських засобів, виробництво яких здійснюється на сертифікованій дільниці. Один примірник такого переліку надається Заявнику, другий – зберігається в Держлікслужбі України.
Заявник зобов’язаний повернути оригінал попереднього переліку лікарських засобів не пізніше дати отримання оновленого переліку.
VI. Контроль за дотриманням правил належної виробничої практики протягом строку дії Сертифіката або Висновку
6.1. Заявник відповідає за дотримання вимог GMP протягом строку дії Сертифіката.
6.2. Виробництво, яке згідно з цим Порядком отримало підтвердження відповідності вимогам GMP, підлягає позаплановому інспектуванню на дотримання вимог GMP протягом строку дії Сертифіката за наявності відповідних підстав, зазначених у пункті 6.3 цього розділу.
6.3. Підставами для позапланового інспектування виробництва (або його частини) з метою перевірки дотримання Заявником вимог GMP є:
звернення Заявника;встановлення фактів виробництва лікарських засобів, які можуть бути небезпечними для здоров’я і життя людей або можуть призвести до тяжких наслідків для здоров’я людей;наявність фактів виробництва неякісних або фальсифікованих лікарських засобів (у тому числі у разі підозри щодо можливого виробництва фальсифікованої продукції);розширення номенклатури лікарських засобів, що виробляються на сертифікованому виробництві (за необхідності);наявність приписів або рішень органів державного контролю щодо вилучення з обігу лікарського засобу, виробництво якого здійснюється на виробничій дільниці (за необхідності).
6.4. У разі виявлення невідповідності виробництва лікарських засобів вимогам GMP, ненадання Заявником плану коригувальних та запобіжних дій та документальних підтверджень щодо усунення порушень (невідповідностей) вимогам належної виробничої практики у строки, визначені у пункті 5.4 розділу V цього Порядку, невиконання гарантійних зобов’язань або встановлення факту виробництва лікарських засобів, не внесених до переліку номенклатури продукції (додаток 5), Держлікслужба України може прийняти рішення про зупинення дії або анулювання Сертифіката або Висновку та надати припис про усунення порушень вимог GMP із зазначенням строку його виконання, про що повідомляє Заявнику протягом 10 робочих днів після прийняття відповідного рішення. Після усунення порушень вимог GMP у встановлені строки Держлікслужба України може прийняти рішення щодо відновлення дії Сертифіката або Висновку (у разі зупинення їх дії).
6.5. Підставами для позапланового інспектування у разі змін у виробництві лікарських засобів, які можуть вплинути на якість лікарських засобів, можуть бути:
розширення номенклатури лікарських засобів, що виробляються на дільниці;введення в технологічну схему виробництва нової технологічної стадії, технологічної операції або нової одиниці критичного технологічного обладнання;зміни технологічних параметрів критичних технологічних стадій;перенесення виробничої дільниці, технічне переоснащення виробництва, модернізація або реконструкція виробничої дільниці.
VII. Права та обов’язки інспектора при проведенні процедури підтвердження відповідності вимогам GMP
7.1. Інспектор при здійсненні інспектування виробництва має право:
ознайомлюватися з усіма необхідними для проведення інспектування документами, які стосуються вимог GMP і матеріалів реєстраційного досьє, та одержувати від Заявника та/або виробника необхідні відомості з питань, що належать до його компетенції;безперешкодно відповідно до Закону України «Про основні засади державного нагляду (контролю) у сфері господарської діяльності» проводити огляд виробничих, складських, допоміжних приміщень (зон), приміщень (зон) контролю якості та інших приміщень (зон) Заявника, їх інспектування для з’ясування питань, безпосередньо пов’язаних з додержанням Заявником правил GMP;відповідно до Закону України «Про основні засади державного нагляду (контролю) у сфері господарської діяльності» фіксувати процес здійснення інспектування чи кожну окрему дію засобами аудіо- та відеотехніки, не перешкоджаючи здійсненню такого заходу;вимагати припинення дій, які перешкоджають здійсненню процедури підтвердження відповідності вимогам GMP;призначати експертизу, одержувати пояснення, довідки, документи, матеріали, відомості з питань, що виникають під час процедури підтвердження відповідності вимогам GMP;відбирати зразки лікарських засобів для лабораторної перевірки їх якості згідно з чинним законодавством України в разі встановлення порушень технології виробництва, вимог щодо якості, умов та/або правил зберігання лікарських засобів, що можуть призвести до виробництва неякісних лікарських засобів та/або оптової, роздрібної торгівлі неякісними лікарськими засобами;отримувати належним чином завірені копії (ксерокопії) необхідних документів (витягів з документів), пов’язаних з інспектуванням виробництва на відповідність вимогам GMP;одержувати від Заявника письмові пояснення з питань, що виникають під час інспектування.
7.2. У випадку невиконання Заявником зобов’язань, викладених у пункті 8.3 розділу VIIІцього Порядку, стосовно надання на запит інспектора всієї необхідної інформації, забезпечення можливості проведення огляду приміщень, обладнання, зон контролю якості, інтерв’ювання представників (персоналу) виробника, ознайомлення з необхідною документацією системи якості тощо про це повідомляється керівництву Держлікслужби України та зазначається у звіті інспектора.
7.3. Інспектор повинен дотримуватись вимог щодо:
дотримання конфіденційності щодо інформації про Заявника та/або виробника, у тому числі отриманої від нього під час інспектування;об’єктивності, повноти і достовірності результатів інспектування;достовірності інформації, що міститься у звіті та є підставою для прийняття рішення про видачу Сертифіката;нерозголошення конфіденційної інформації та інформації, що є комерційною таємницею Заявника, що стає доступною інспектору у процесі підтвердження відповідності вимогам GMP.
7.4. Інспектор зобов’язаний:
дотримуватися ділової етики у взаємовідносинах із Заявником та/або виробником;не втручатися і не перешкоджати здійсненню господарської діяльності під час здійснення процедури підтвердження відповідності вимогам GMP виробництва лікарських засобів, якщо це не загрожує життю та здоров’ю людей;надати звіт за результатами інспектування в Держлікслужбу України в строки, передбаченірозділом IІІ цього Порядку.
VIIІ. Права та обов’язки Заявника та/або виробника при проведенні процедури підтвердження відповідності вимогам GMP
8.1. Заявник та/або виробник відповідають за достовірність наданої інформації.
8.2. Заявник та/або виробник мають право:
вимагати від інспекторів додержання вимог чинного законодавства України;перевіряти наявність в інспектора службового посвідчення або іншого документа, який засвідчує його особу, і одержувати копії документів на проведення інспектування;бути присутніми під час здійснення інспектування;вимагати нерозголошення конфіденційної інформації та інформації, що є комерційною таємницею Заявника та/або виробника;одержувати та ознайомлюватися зі звітом за результатами інспекції у строки, встановлені цим Порядком;оскаржувати в установленому законодавством порядку рішення або неправомірні дії Держлікслужби України та її посадових осіб.
8.3. Заявник та/або виробник зобов’язаний:
- повідомляти Держлікслужбу України про зміни, які стосуються виробничої дільниці (у тому числі про зміну ліцензії на виробництво лікарських засобів, зміну найменування Заявника, його місцезнаходження);
- надавати на запит інспектора всю необхідну інформацію, забезпечувати можливість проведення огляду виробничих, допоміжних, складських приміщень, обладнання, зон контролю якості, інтерв’ювання представників (персоналу) виробника, ознайомлення з необхідною документацією системи якості тощо;
- виконувати вимоги Держлікслужби України щодо усунення виявлених порушень вимог чинного законодавства України;
- надавати документи, зразки продукції, пояснення, довідки, відомості, матеріали з питань, що виникають під час процедури підтвердження відповідності вимогам GMP, відповідно до вимог чинного законодавства України;
- одержувати примірник звіту за результатами інспекції у строки, встановлені цим Порядком.
| Начальник Управління лікарських засобівта медичної продукціїЗаступник начальникаУправління фармацевтичної діяльностіта якості фармацевтичної продукції |
Ю.М. КедаЛ.В. Коношевич |
Додаток 1
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 5 розділу І)
ДержлікслужбаДержавна служба України з лікарських засобів
Державна служба України
з лікарських засобів
та контролю за наркотиками
ЗАЯВА
на видачу сертифіката відповідності умов виробництва лікарських засобів вимогам належної виробничої практики
Дата надходження: «____»_______ 20____ року Зареєстровано за № _______
|
ЗАЯВНИК (найменування ліцензіата або власника реєстраційного посвідчення (торговельної ліцензії) на лікарський засіб або найменування/прізвище, ім’я, по батькові представника заявника) ______________________________________________________________________________ Місцезнаходження (місце проживання) ______________________________________________________________________________ П. І. Б., посада керівника заявника __________________________________________________________________________________ Контактні телефони, факс____________________________________________________________________ ВИРОБНИК (найменування суб’єкта господарювання та найменування виробничої(их) дільниці(ць), заявленої(их) для процедури підтвердження відповідності вимогам GMP (за наявності))_________________________________________________ Місце провадження діяльності виробника ____________________________________________________________________ DUNS номер адреси виробника та GPS координати _________________________________________________________ П. І. Б., посада керівника підприємства, тел./факс____________________________________________________________________ П. І. Б., посада керівника підрозділу з виробництва, тел./факс____________________________________________________________________ П. І. Б., посада керівника служби якості (Уповноваженої особи), тел./факс____________________________________________________________________ П. І. Б., посада керівника відділу контролю якості, тел./факс____________________________________________________________________ Інші контактні адреси (у тому числі e-mail) ____________________________________________________________________ Місце провадження діяльності, DUNS номери та GPS координати лабораторій, що здійснюють контроль якості за контрактом (договором), складських зон за контрактом (договором) _______________________________ Згода на проведення інспектування керівника суб’єкта господарювання, де здійснюється контроль якості за контрактом, зберігання лікарських засобів тощо:П. І. Б., посада керівника, підпис ______________________________________ |
Згідно з пунктом 2 розділу ІІ цього Порядку додаються такі документи:
Примітки (в тому числі зазначаються підстави для позачергової експертизи та/або інспектування):
___________________________________________________________________
Достовірність наданої інформації гарантую:
__________________________________________________________________
(П. І. Б., посада і підпис керівника (представника) заявника)
Дата складання «___»_________ 20__ року М. П. (за наявності)
Додаток 2
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 5 розділу І)
ДержлікслужбаДержавна служба України з лікарських засобів
Державна служба України
з лікарських засобів
та контролю за наркотиками
ЗАЯВА
на видачу висновку щодо підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики
Дата надходження: «___»_______ 20____ року Зареєстровано за № ______
|
ЗАЯВНИК (найменування ліцензіата або власника реєстраційного посвідчення (торговельної ліцензії) на лікарський засіб або найменування/прізвище, ім’я, по батькові представника заявника)_________________________________________ Місцезнаходження (місце проживання) ___________________________________________________________________ П.І.Б., посада керівника заявника ________________________________________________________________________ Контактні телефони, факс___________________________________________________________________ ВИРОБНИК (найменування суб’єкта господарювання та найменування виробничої(их) дільниці(ць), заявленої(их) для процедури підтвердження відповідності вимогам GMP (за наявності))________________________________________ Місце провадження діяльності виробника_________________________________________________ П.І.Б., посада керівника підприємства, тел./факс____________________________________________________________________ П.І.Б., посада керівника підрозділу з виробництва, тел./факс____________________________________________________________________ П.І.Б., посада керівника служби якості (уповноваженої особи), тел./факс____________________________________________________________________ П. І. Б., посада керівника відділу контролю якості, тел./факс____________________________________________________________________ Інші контактні адреси (у тому числі e-mail) ____________________________________________________________________ |
Згідно з пунктом 2 розділу ІІ цього Порядку додаються такі документи:
Примітки (в тому числі зазначаються підстави для позачергової експертизи та/або інспектування):
___________________________________________________________________
Достовірність наданої інформації гарантую:
_____________________________________________________________
(П. І. Б., посада і підпис керівника (представника) заявника)
Дата складання «___»_________ 20__ року М. П. (за наявності)
Додаток 3
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 6 розділу І)
(Форма 1)
Державний Герб України
УКРАЇНА
Ukraine
сертифікат відповідності умов виробництва лікарських засобів вимогам належної виробничої практики
CERTIFICATE OF GMP COMPLIANCE
Сертифікат №: // Certificate No: Строк дії до: // Valid till: дд мм рррр
| Частина 1 | Part 1 |
| Державна служба України з лікарських засобів та контролю за наркотиками (Держлікслужба)Державна служба України з лікарських засобів (Держлікслужба України) засвідчує: | State Service of Ukraine on Medicines and Drugs Control (SMDC) State Serviсе of Ukraine on Medicinal Products and Drugs ControlState Administration of Ukraine on Medicinal Products (SAUMP) confirms the following: |
| Найменування виробника, місцезнаходження | Manufacturer’s name, registered place of business: |
| Найменування виробничої(их) дільниці(ць): | Name(s) of manufacturing site(s): |
| Місце провадження діяльності: | Manufacturing site address: |
| Ліцензія на виробництво лікарських засобів | Manufacturing authorization for medicinal products |
| від «___»____________ _____ № __________ | ______ ______________ No. __________ |
| Місце виробництва систематично проходить інспектування зі встановленою періодичністю на відповідність вимогам GMP згідно зі встановленим порядком. | Facilities of above mentioned manufacturer are subject to GMP inspections at suitable intervals in accordance with the National certification procedure. |
|
За результатами інспектування цього виробника, останнє з яких було проведене… … / … … / … … (дата),встановлено, що він відповідає вимогам належної виробничої практики, зазначеним в______________________________________________,(нормативний акт)що відповідають вимогам належної практики при виробництві і контролі якості Системи співробітництва фармацевтичних інспекцій (PIC/S), директивам ЄC та рекомендаціям Всесвітньої організації охорони здоров’я відносно продукції, що призначена для торгівлі та дистрибуції в країні походження або для експорту. Цей сертифікат відображає стан виробничої дільниці на момент інспектування, зазначеного вище, і не може використовуватися для підтвердження відповідності, якщо з моменту проведення цього інспектування пройшло більше ніж ….3 роки.Цей сертифікат включає частини 1, 2 та додаток.Чинність цього сертифіката може бути підтверджена органом, що його видав. |
From the knowledge gained during inspection of this manufacturer, the latest of which was conducted on… … / … … / … … (date),it is considered that it complies with the Good Manufacturing Practice requirements1 referred to in the_______________________________________________(name of regulation document) which is harmonized with the requirements of Good practices in the manufacture and quality control of the Pharmaceutical Inspection Convention/Co-operation Scheme (PIC/S), EU Directives, and World Health Organization recommendations in respect of products to be sold or distributed within the county of origin or to be exported. This certificate reflects the status of the manufacturing site at the time of the inspection noted above and should not be relied upon to reflect the compliance status if more than ….three years have elapsed since the date of that inspection.This certificate includes the Parts 1, 2 and Annex.The authenticity of this certificate may be verified with the issuing authority. |
| Частина 2 | Part 2 |
| Лікарські засоби для людини | Human Medicinal Products |
| 1. ВИРОБНИЧІ ОПЕРАЦІЇ — ЛІКАРСЬКІ ЗАСОБИ* | 1. MANUFACTURING OPERATIONS — MEDICINAL PRODUCTS* |
| 1.1. Стерильні лікарські засобипродукти
1.1.1. Асептично виготовлені (виробничі операції для наступних лікарських форм) 1.1.1.1. Рідини в упаковках великого об’єму 1.1.1.2. Ліофілізати 1.1.1.3. М’які 1.1.1.4. Рідини в упаковках малого об’єму 1.1.1.5. Тверді та імплантанти 1.1.1.6. Інші асептично виготовлені лікарські засобипродукти (зазначити) 1.1.2. Що піддаються кінцевій стерилізації (виробничі операції для наступних лікарських форм) 1.1.2.1. Рідини в упаковках великого об’єму 1.1.2.2. М’які 1.1.2.3. Рідини в упаковках малого об’єму 1.1.2.4. Тверді та імплантанти 1.1.2.5. Інші лікарські засобипродукти, що піддаються кінцевій стерилізації (зазначити) 1.1.3. Сертифікація серій |
1.1. Sterile products
1.1.1. Aseptically prepared (processing operations for the following dosage forms) 1.1.1.1. Large volume liquids 1.1.1.2. Lyophilisates 1.1.1.3. Semi-solids 1.1.1.4. Small volume liquids 1.1.1.5. Solids and implants 1.1.1.6. Other aseptically prepared products <free text> 1.1.2. Terminally sterilised (processing operations for the following dosage forms) 1.1.2.1. Large volume liquids 1.1.2.2. Semi-solids 1.1.2.3. Small volume liquids 1.1.2.4. Solids and implants 1.1.2.5. Other terminally sterilised prepared products <free text> 1.1.3. Batch certification |
| 1.2. Нестерильні лікарські засобипродукти
1.2.1. Нестерильні лікарські засобипродукти (виробничі операції для наступних лікарських форм) 1.2.1.1. Капсули, тверді 1.2.1.2. Капсули, м’які 1.2.1.3. Жувальні гуми 1.2.1.4. Імпрегновані матриці 1.2.1.5. Рідини для зовнішнього застосування 1.2.1.6. Рідини для внутрішнього застосування 1.2.1.7. Медичні гази 1.2.1.8. Інші тверді лікарські форми 1.2.1.9. Препарати під тиском 1.2.1.10. Генератори радіонуклідів 1.2.1.11. М’які 1.2.1.12. Супозиторії 1.2.1.13. Таблетки 1.2.1.14. Трансдермальні пластирі 1.2.1.15. Стоматологічні матеріали 1.2.1.16. Інші нестерильні лікарські засоби (зазначити) 1.2.2. Сертифікація серій |
1.2. Non-sterile products 1.2.1. Non-sterile products (processing operations for the following dosage forms) 1.2.1.1. Capsules, hard shell 1.2.1.2. Capsules, soft shell 1.2.1.3. Chewing gums 1.2.1.4. Impregnated matrices 1.2.1.5. Liquids for external use 1.2.1.6. Liquids for internal use 1.2.1.7. Medicinal gases 1.2.1.8. Other solid dosage forms 1.2.1.9. Pressurised preparations 1.2.1.10. Radionuclide generators 1.2.1.11. Semi-solids 1.2.1.12. Suppositories 1.2.1.13. Tablets 1.2.1.14. Transdermal patches 1.2.1.15. Intraruminal devices 1.2.1.16. Other non-sterile medicinal product <free text > 1.2.2 Batch certification |
|
1.3. Біологічні лікарські засоби 1.3.1. Біологічні лікарські засоби 1.3.1.1. Препарати крові 1.3.1.2. Імунобіологічні лікарські засоби 1.3.1.3. Лікарські засоби клітинної терапії 1.3.1.4. Лікарські засоби генної терапії 1.3.1.5. Біотехнологічні лікарські засоби 1.3.1.6. Препарати, екстраговані з тканин людини або тварин 1.3.1.7. Лікарські засоби тканинної інженерії 1.3.1.8. Інші біологічні лікарські засоби (зазначити) 1.3.2. Сертифікація серій (перелік) 1.3.2.1. Препарати крові 1.3.2.2. Імунобіологічні лікарські засоби 1.3.2.3. Лікарські засоби клітинної терапії 1.3.2.4. Лікарські засоби генної терапії 1.3.2.5. Біотехнологічні лікарські засоби 1.3.2.6. Препарати, екстраговані з тканин людини або тварин 1.3.2.7. Лікарські засоби тканинної інженерії 1.3.2.8. Інші біологічні лікарські засоби (зазначити) |
1.3. Biological medicinal products
1.3.1. Biological medicinal products 1.3.1.1. Blood products 1.3.1.2. Immunological products 1.3.1.3. Cell therapy products 1.3.1.4. Gene therapy products 1.3.1.5. Biotechnology products 1.3.1.6. Human or animal extracted products 1.3.1.7. Tissue engineered products 1.3.1.8. Other biological medicinal products <free text > 1.3.2. Batch certification (list of product types) 1.3.2.1. Blood products 1.3.2.2. Immunological products 1.3.2.3. Cell therapy products 1.3.2.4. Gene therapy products 1.3.2.5. Biotechnology products 1.3.2.6. Human or animal extracted products 1.3.2.7. Tissue engineered products 1.3.2.8. Other biological medicinal products <free text > |
| 1.4. Інші лікарські засобипродукти або виробнича діяльність
1.4.1. Виробництво: 1.4.1.1. Лікарські засобиПродукти з рослинної сировини 1.4.1.2. Гомеопатичні лікарські засобипрепарати 1.4.1.3. Інші (зазначити) 1.4.2 Стерилізація активних речовин/допоміжних речовин/готової продукції 1.4.2.1. Фільтрація 1.4.2.2. Сухожарова стерилізація 1.4.2.3. Стерилізація паром 1.4.2.4. Хімічна 1.4.2.5. Гамма-випромінювання 1.4.2.6. Електронно-променева 1.4.3. Інші (зазначити) |
1.4. Other products or processing activity
1.4.1. Manufacture of: 1.4.1.1. Herbal products 1.4.1.2. Homoeopathic products 1.4.1.3. Other <free text > 1.4.2. Sterilisation of active substances/excipients/finished product: 1.4.2.1.Filtration 1.4.2.2. Dry heat 1.4.2.3. Moist heat 1.4.2.4. Chemical 1.4.2.5. Gamma irradiation 1.4.2.6. Electron beam 1.4.3. Others <free text> |
| 1.5. Пакування
1.5.1. Первинне пакування 1.5.1.1. Капсули, тверді 1.5.1.2. Капсули, м’які 1.5.1.3. Жувальні гуми 1.5.1.4. Імпрегновані матриці 1.5.1.5. Рідини для зовнішнього застосування 1.5.1.6. Рідини для внутрішнього застосування 1.5.1.7. Медичні гази 1.5.1.8. Інші тверді лікарські форми 1.5.1.9. Препарати під тиском 1.5.1.10. Генератори радіонуклідів 1.5.1.11. М’які 1.5.1.12. Супозиторії 1.5.1.13. Tаблетки 1.5.1.14. Трансдермальні пластирі 1.5.1.15. Стоматологічні матеріали 1.5.1.16. Інші нестерильні лікарські засоби (зазначити) 1.5.2. Вторинне пакування |
1.5.Packaging
1.5.1. Primary packing 1.5.1.1. Capsules, hard shell 1.5.1.2. Capsules, soft shell 1.5.1.3. Chewing gums 1.5.1.4. Impregnated matrices 1.5.1.5. Liquids for external use 1.5.1.6. Liquids for internal use 1.5.1.7. Medicinal gases 1.5.1.8. Other solid dosage forms 1.5.1.9. Pressurised preparations 1.5.1.10. Radionuclide generators 1.5.1.11. Semi-solids 1.5.1.12. Suppositories 1.5.1.13. Tablets 1.5.1.14. Transdermal patches 1.5.1.15. Intraruminal devices 1.5.1.16. Other non-sterile medicinal products <free text> 1.5.2. Secondary packing |
| 1.6. Проведення випробувань в рамках контролю якості
1.6.1. Мікробіологічні: стерильність 1.6.2. Мікробіологічні: мікробіологічна чистота 1.6.3. Фізичні/хімічні 1.6.4. Біологічні |
1.6. Quality control testing
1.6.1. Microbiological: sterility 1.6.2. Microbiological: non-sterility 1.6.3. Chemical/Physical 1.6.4. Biological |
| 2. ВИРОБНИЧІ ОПЕРАЦІЇ — АКТИВНІ ФАРМАЦЕВТИЧНІ ІНГРЕДІЄНТИ* | 2. MANUFACTURING OPERATIONS — ACTIVE SUBSTANCES |
| Активний(і) фармацевтичний(і) інгредієнт(и): | Active Substance(s): |
| 2.1. Виробництво активної речовини шляхом хімічного синтезу
2.1.1. Виробництво активних проміжних речовин 2.1.2. Виробництво неочищеного активного фармацевтичного інгредієнта 2.1.3. Солеутворення / очищення: (зазначити) (наприклад, кристалізація) 2.1.4. Інші (зазначити) |
2.1. Manufacture of Active Substance by Chemical Synthesis
2.1.1. Manufacture of active substance intermediates 2.1.2. Manufacture of crude active substance 2.1.3. Salt formation / Purification steps : <free text> (e.g. crystallisation) 2.1.4. Other <free text> |
| 2.2. Отримання активного фармацевтичного інгредієнта з природних джерел
2.2.1. Отримання речовини з рослин 2.2.2. Отримання речовини з тварин 2.2.3. Отримання речовини з людського джерела 2.2.4. Отримання речовини з мінерального джерела 2.2.5. Модифікація отриманої речовини (зазначити джерело) 2.2.6. Очищення отриманої речовини (зазначити джерело) 2.2.7. Інше (зазначити) |
2.2. Extraction of Active Substance from Natural Sources
2.2.1. Extraction of substance from plant source 2.2.2. Extraction of substance from animal source 2.2.3. Extraction of substance from human source 2.2.4. Extraction of substance from mineral source 2.2.5. Modification of extracted substance <specify source > 2.2.6. Purification of extracted substance <specify source > 2.2.7. Other <free text> |
| 2.3. Виробництво активного фармацевтичного інгредієнта з використанням біологічних процесів | 2.3. Manufacture of Active Substance using Biological Processes |
|
2.3.1. Ферментація 2.3.2. Культура клітин (зазначити тип клітин) (наприклад, ссавців / бактеріальні) 2.3.3. Виділення / Очищення 2.3.4. Модифікація 2.3.5. Інше (зазначити) |
2.3.1. Fermentation 2.3.2. Cell Culture <specify cell type> (e.g. mammalian / bacterial) 2.3.3. Isolation / Purification 2.3.4. Modification 2.3.5. Other <free text> |
| 2.4. Виробництво стерильного активного фармацевтичного інгредієнта (розділи 3.1, 3.2, 3.3, заповнюються за необхідності) | 2.4. Manufacture of sterile active substance (sections 3.1, 3.2, 3.3. to be completed as applicable) |
|
2.4.1. Асептично виготовлені 2.4.2. Препарати, що піддаються кінцевій стерилізації |
2.4.1. Aseptically prepared 2.4.2. Terminally sterilized |
| 2.5. Ступені загальної обробки | 2.5. General Finishing Steps |
|
2.5.1 Ступені фізичної обробки (зазначити) (наприклад, сушіння, подрібнення / мікронізація, просіювання) 2.5.2. Первинне пакування (закупорювання / герметизація активного фармацевтичного інгредієнта пакувальним матеріалом, який знаходиться в прямому контакті з речовиною) 2.5.3. Вторинне пакування (розміщення герметичної первинної упаковки всередині зовнішнього пакувального матеріалу або контейнера. Це також включає в себе будь-яке маркування матеріалу для ідентифікації або простежуваності (нумерація серії) активного фармацевтичного інгредієнта) 2.5.4. Інше (зазначити) (для операцій, не описаних вище) |
2.5.1. Physical processing steps < specify > (e.g. drying, milling / micronisation, sieving) 2.5.2. Primary Packaging (enclosing / sealing the active substance within a packaging material which is in direct contact with the substance) 2.5.3. Secondary Packaging (placing the sealed primary package within an outer packaging material or container. This also includes any labelling of the material which could be used for identification or traceability (lot numbering) of the active substance) 2.5.4. Other <free text> (for operations not described above) |
| 2.6. Проведення випробувань в рамках контролю якості | 2.6. Quality Control Testing |
|
2.6.1. Фізичні/хімічні випробування 2.6.2. Мікробіологічні випробування (виключаючи випробування стерильності) 2.6.3. Мікробіологічні випробування (включаючи випробування стерильності) 2.6.4. Біологічні випробування |
2.6.1. Physical / Chemical testing 2.6.2. Microbiological testing (excluding sterility testing) 2.6.3. Microbiological testing (including sterility testing) 2.6.4. Biological Testing |
| 3. ІНША ДІЯЛЬНІСТЬ — АКТИВНІ ФАРМАЦЕВТИЧНІ ІНГРЕДІЄНТИ (зазначити)* | 3. OTHER ACTIVITIES — ACTIVE SUBSTANCES <free text> |
| Будь-які обмеження або пояснення, що мають відношення до цього сертифіката:……………………………………….. | Any restrictions or clarifying remarks related to the scope of this certificate:………………………………… |
| підпис відповідальної особи, М.П.……./……./……. [дата] | signature of the Executive officer (see left)……./……./……. [date] |
| Державна служба України з лікарських засобів та контролю за наркотиками
Місцезнаходження: Тел.: Факс: www.dls.gov.uaЕлектронна адреса:http://www.diklz.gov.ua ___________________ * Залишити потрібне. |
State Service of Ukraine on Medicines and Drugs ControlState Administration of Ukraine on Medicinal Products
Address: Phone: Fax: www.dls.gov.uae-mail: http://www.diklz.gov.ua This English translation is for reference only and is not part of the official certificateНомер сторінки / Загальна кількість сторінок |
Додаток 4
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 6 розділу І)
Бланк Державної служби України з лікарських засобів та контролю за наркотиками
Бланк Держлікслужби України
ВИСНОВОК
щодо підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики
На підставі розгляду заяви від «__» ___ 20__ року № _____________________
____________________________________________________________________________________________,
(найменування заявника та/або виробника)
документів, що додаються до неї, та, враховуючи позитивні результати проведеної спеціалізованої експертизи (експертний висновок від «__» ___ 20__ року № ___________), сертифікат відповідності виробництва лікарських засобів вимогам GMP № ______________ від «__» ___ 20__ року, виданий
____________________________________________________________________________________________,
(найменування уповноваженого органу країни-члена ЄС, Великої Британії або країни, яка має угоду про взаємне визнання з ЄС або з Україною)PIC/S)
виробничій дільниці ________________________________________________________________________,
(найменування виробника/виробничої дільниці)
адреса місця провадження діяльності: ______________________________________________________,
строком дії до «__» ___ 20__ року, вважається таким, що підтверджує відповідність виробництва лікарських засобів чинним в Україні вимогам GMP.
Дія цього висновку розповсюджується на такі форми лікарських засобів, як:
____________________________________________________________________________________________.
Перелік лікарських засобів, що виробляються на дільниці
______________________________________________________________________,
(найменування, місце провадження (адреса) виробника (виробничої дільниці))
наведено в додатку до цього висновку і є його невід’ємною частиною.
_____________ ____________ __________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
«____»_________ 20___ року М. П. (за наявності)
Додаток 5
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(підпункт 8 пункту 2 розділу IІ)
ДОВІДКА
про якість продукції, що виробляється
на_________________________________________________________________________________________
(найменування виробничої дільниці, що вказана в заяві)
______________________________________________________________________________________________
(найменування заявника)
з 20___ по 20___ р.
(навести дані за останні три роки, рахуючи від дати подання заяви)
|
№ з/п |
Відомості про претензії і відкликання продукції | Усього | Перелік найменувань і номерів серій лікарських засобів |
|---|---|---|---|
| 1 | Кількість обґрунтованих претензій до якості продукції: | ||
| 1.1 | за результатами державного контролю | ||
| 1.2 | за зверненнями споживачів | ||
| 2 | Кількість відкликань продукції з мережі реалізації в Україні: | ||
| 2.1 | за приписами державних органів контролю | ||
| 2.2 | за рішенням виробника | ||
| 3 | Кількість відкликаної продукції з мережі реалізації країни, де розташоване виробництво (для нерезидентів): | ||
| 3.1 | за приписами державних органів країни, де розташоване виробництво | ||
| 3.2 | за рішенням виробника | ||
| 4 | Кількість відкликаної продукції з мережі реалізації в інших країнах: | ||
| 4.1 | за приписами відповідних державних органів країн, де здійснювалася реалізація продукції | ||
| 4.2 | за рішенням виробника |
Дата складання «____» ____________ 20___ року
Керівник
підприємства
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
М. П. (за наявності)
Керівник служби якості (уповноважена особа)
________________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
Додаток 6
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(підпункт 9 пункту 2 розділу IІ)
ДОВІДКА
про результати перевірок виробничої дільниці, проведених органами державного контролю
на _________________________________________________________________________________________
(найменування виробничої дільниці та найменування заявника)
з 20___ по 20___ р.
(указати за останні три роки до дати подання заяви)
|
№ з/п |
Найменування уповноваженого органу | Вид перевірки (інспектування)(планова, позапланова) | Період, дата(и) перевірки | Звіт/акт від ____
(дата) №__ |
Результат перевірки (навести посилання на документ та надати короткі висновки, наведені у звіті/акті) |
|---|---|---|---|---|---|
| 1 | Орган державного контролю лікарських засобів в Україні | ||||
| 2 | Державний або уповноважений орган у сфері контролю лікарських засобів країни, де розташоване виробництво (для нерезидентів) | ||||
| 3 | Уповноважені органи у сфері контролю лікарських засобів, країни яких є членами ЄС, Великої Британії або мають угоди про взаємне визнання з ЄС або з Україноюякі є членами PIC/S | ||||
| 4 | Уповноважені органи у сфері контролю лікарських засобів інших країн |
Дата складання «____» ____________ 20___ року
Керівник виробника
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
М. П. (за наявності)
Керівник служби якості (уповноважена особа)
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
Додаток 7
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(підпункт 10 пункту 2 розділу IІ)
(Форма 1)
ЗАГАЛЬНИЙ
ПЕРЕЛІК НОМЕНКЛАТУРИ ПРОДУКЦІЇ1
_________________________________________________________________________
(найменування виробничої дільниці)
_________________________________________________________________________
(місце провадження діяльності)
_________________________________________________________________________
(країна виробника)
| № з/п | Торговельна назва2 | Міжнародна непатентована назва (МНН)3 | Реєстраційне посвідчення в Україні | Реєстраційне посвідчення (торгова ліцензія) в країні, де здійснюється виробництвовід «__»___ № ___ | Інформація про виробників4 | |||||||||
| торговельна назва (укр.) | торговельна назва (англ.) | лікарська форма (укр.) | лікарська форма (англ.) | номер | рік видачі | місяць видачі | день видачі | виробник нерозфасованого продукту | первинна упаковка | вторинна упаковка | дозвіл на випусксерій5 | |||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
Дата складання «______» _______________ 20____ року
Керівник виробника
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
М. П. (за наявності)
Керівник служби якості/Уповноважена особа
________________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
Керівник виробництва
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
________________
1 Для нерезидентів цей документ має бути складено англійською мовою, його переклад українською мовою має бути засвідчений підписом Заявника або представником Заявника.
2 Зазначити повну назву лікарського засобу, зазначену в реєстраційному досьє, поданому до уповноваженого органу України або країни, де розташоване виробництво (українською мовою — у разі реєстрації лікарського засобу в Україні, англійською мовою — у разі якщо лікарський засіб не зареєстрований в Україні).
3 Зазначити (виключно англійською мовою) міжнародну непатентовану назву діючої речовини лікарського засобу; для багатокомпонентних (комбінованих) лікарських засобів навести перелік всіх діючих речовин.
4 Ці колонки мають бути заповнені для всіх назв лікарських засобів.
5 Найменування виробника, Уповноважена особа якого надає дозвіл на випуск серій продукції.
(Форма 2)
ЗАГАЛЬНИЙ ПЕРЕЛІК НОМЕНКЛАТУРИ ПРОДУКЦІЇ1
________________________________________________________________________________
(найменування виробничої дільниці)
________________________________________________________________________________
(місце провадження діяльності)
________________________________________________________________________________
(країна виробника)
| № з/п | Торговельна назва2 | Міжнародна непатентована назва (МНН)3 | КодАТС | Реєстраційне посвідчення в Україні | Реєстраційне посвідчення(торгова ліцензія) в країні, де здійснюється виробництвовід «__»___ № _ | Інформація про виробників4 | Інформація про контрактні лабораторії, складські зони6 | |||||||||
| торговельна назва (укр.) | торговельна назва (англ.) | лікарська форма (укр.) | лікарська форма (англ.) | номер | рік видачі | місяць видачі | день видачі | виробник нерозфасованого продукту | первинна упаковка | вторинна упаковка | дозвіл на випусксерій5 | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 |
Дата складання «______» _______________ 20____ року
Керівник виробника
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
М. П. (за наявності)
Керівник служби якості/ Уповноважена особа
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
Керівник виробництва
_______________ ____________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
________________
1 Для нерезидентів цей документ має бути складено англійською мовою, його переклад українською мовою має бути засвідчений підписом Заявника або представником Заявника.
2 Зазначити повну назву лікарського засобу, зазначену в реєстраційному досьє, поданому до уповноваженого органу України або країни, де розташоване виробництво (українською мовою — у разі реєстрації лікарського засобу в Україні, англійською мовою — у разі якщо лікарський засіб не зареєстрований в Україні).
3 Зазначити (виключно англійською мовою) міжнародну непатентовану назву діючої речовини лікарського засобу; для багатокомпонентних (комбінованих) лікарських засобів навести перелік всіх діючих речовин.
4 Ці колонки мають бути заповнені для всіх назв лікарських засобів.
5 Найменування виробника, Уповноважена особа якого надає дозвіл на випуск серій продукції.
6 Ці колонки мають бути заповнені у разі здійснення за контрактом (договором) контролю якості лікарських засобів, їх зберігання.
Додаток 8
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(підпункт 12 пункту 2 розділу IІ)
(Бланк заявника)
(Форма 1)
_____________ № _________
(дата)
Державна служба України з лікарських засобів та контролю за наркотиками
ГАРАНТІЙНИЙ ЛИСТ
про суттєві зміни, які стосуються виробничої дільниці, що пройшла підтвердження відповідності умов виробництва лікарських засобів вимогам GMP
Від
_______________________________________________________________________________,
(заявник)
в особі ________________________________________________________________________,
що діє на підставі _____________________________________________________________,
гарантує, що Держлікслужбу України буде повідомлено про зміни щодо виробничої дільниці, що пройшла підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (GMP), включаючи зміни у проміжних (контрактних) виробничих дільницях, які задіяні у виробництві лікарського засобу (у тому числі про зміну ліцензії на виробництво лікарських засобів, зміну найменування виробника, його місцезнаходження (юридичної адреси) та/або адреси виробничих потужностей тощо)
_________________________________________________________________________
ВИРОБНИК
(найменування суб’єкта господарювання, місце провадження діяльності):
____________________________________________
Контактні дані керівника Заявника / керівника
представника Заявника: ____________________________________________________________________
(телефон, факс, електронна адреса)
До гарантійного листа додається:
копія документа, що підтверджує повноваження особи, яка підписала гарантійний лист.
Керівник Заявника /представника Заявника
________________ ________________________
(підпис) (ініціали та прізвище)
М. П. (за наявності)
(Бланк заявника)
(Форма 2)
_____________ № _________
(дата)
Державна служба України з лікарських засобів та контролю за наркотиками
ГАРАНТІЙНИЙ ЛИСТ
про завершення процедури підтвердження або надання звіту останньої перевірки, проведеної уповноваженим органом країни-члена PIC/S
________________________________________________________________________,
(заявник)
в особі ______________________________________________________________________,
що діє на підставі ___________________________________________________________,
гарантує завершення процедури підтвердження протягом шестимісячного строку з дня отримання Висновку на готовий лікарський засіб або надання до Держлікслужби України копії звіту останньої перевірки проміжної виробничої ділянки (уключаючи контрактні дільниці), проведеної уповноваженим органом країни-члена РІС/S (для нерезидентів, виробництво лікарських засобів яких розташоване за межами території країни-члена ЄС і за межами території країни, із якою ЄС укладено договір про взаємне визнання результатів інспектування)
_________________________________________________________________________
ВИРОБНИК
(найменування суб’єкта господарювання, місце провадження діяльності): _______________________________________________
Контактні дані керівника Заявника / керівника
представника Заявника: _____________________________________________________________________
(телефон, факс, електронна адреса)
До гарантійного листа додається:
копія документа, що підтверджує повноваження особи, яка підписала гарантійний лист.
Керівник Заявника / представника Заявника
________________ ________________________
(підпис) (ініціали та прізвище)
М. П. (за наявності)
Додаток 9
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 4 розділу IІ)
Державна служба України
з лікарських засобів та контролю за наркотиками
ОПИС № ________
документів, що додаються до заяви на видачу сертифіката відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (до заяви на видачу висновку щодо підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики)
від _________________________________________________________________
(найменування заявника)
Дата і номер реєстрації заяви «_____» __________ 20____ року № __________
|
№ з/п |
Найменування документа | Кількість аркушів у документі | Відмітка про наявність документів (наявні, відсутні) | Примітки |
| 1 | 2 | 3 | 4 | 5 |
Прийняв ____________________ документів __________________________ ____________
(цифрами і словами) (підпис відповідальної особи) (П.І.Б.)
«_____»______________ 20____ року
Копію опису отримав
_______________________________ ________________
(підпис представника заявника) (П.І.Б.)
«_____»______________ 20____ року
Додаток 10
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 8 розділу ІV)
(пункт 7 розділу IV)
ПЕРЕЛІК
типових порушень вимог GMP, які виявляються під час інспектування, та їх класифікація, виходячи із оцінки ризиків для пацієнта
Цей Перелік не охоплює всі можливі порушення, які виявляються під час інспектування, але може бути основою для присвоєння класифікації порушень, виходячи із оцінки ризиків для пацієнтів. Класифікація деяких порушень, які в цьому Переліку зазначені як суттєві, може бути підвищена до критичних при виробництві лікарських засобів критичного або високого рівня ризику. Такі порушення позначені в цьому Переліку знаком (*). Підвищення інспектором класифікації виявленого порушення до критичного має бути обґрунтованим.
Персонал
Порушення, які відносяться до критичних
Уповноважена особа на підприємстві з виробництва лікарських засобів з критичним або високим рівнем ризику не відповідає встановленим законодавством вимогам до відповідної освіти і досвіду роботи.
Порушення, які відносяться до суттєвих
Уповноважена особа на підприємстві з виробництва лікарських засобів з низьким рівнем ризику або на підприємстві, яке здійснює виключно пакування/маркування лікарських засобів або виключно контроль якості лікарських засобів, не відповідає встановленим законодавством вимогам до відповідної освіти і досвіду роботи.
Передача обов’язків Уповноваженої особи особі, яка не відповідає встановленим законодавством вимогам до відповідної освіти і досвіду роботи.
Недостатньо кваліфікований персонал контролю якості та виробництва, що призводить до високої вірогідності помилки.
Недостатнє навчання персоналу, залученого до виробництва та контролю якості, що призводить до порушень вимог GMP.
Порушення, які відносяться до несуттєвих
Неналежні протоколи про проведення навчання.
Неповна програма навчання в письмовому вигляді.
Приміщення
Порушення, які відносяться до критичних
Відсутня система фільтрації повітря для його очистки від аерозольних часток, які можуть утворитися під час виробництва або пакування.
Загальна несправність вентиляційної системи з доведеною широко поширеною перехресною контамінацією.
Неналежне відокремлення виробничих зон або зон для контролю якості від інших виробничих зон, де виготовляється продукція з високим рівнем ризику.
Порушення, які відносяться до суттєвих
Несправність вентиляційної системи, що може стати причиною можливої обмеженої або поодинокої перехресної контамінації.
Не проводиться технічне обслуговування/періодична перевірка системи нагрівання, вентиляції та кондиціонування повітря (HVAC), така як заміна повітряного фільтра, моніторинг перепадів тиску. (*)
Допоміжні системи забезпечення (пара, стиснене повітря, азот, збір пилу тощо) не кваліфіковані.
Система нагрівання, вентиляції та кондиціонування повітря (HVAC) та система підготовки та розподілу води очищеної не кваліфіковані. (*)
Не контролюються та не перевіряються температура і вологість у приміщеннях, де це необхідно (наприклад, умови зберігання не відповідають вимогам, зазначеним на маркуванні).
Пошкодження (отвори, тріщини або фарба, що лущиться) стін/стель безпосередньо поруч або над виробничими зонами або обладнанням, де знаходиться відкритий продукт.
Важкодоступні для чищення поверхні внаслідок розташування трубопроводів, затискачів, отворів, які знаходяться безпосередньо над продукцією або виробничим обладнанням.
Покриття поверхонь (підлоги, стін та стелі), яке унеможливлює проведення ефективної очистки.
Негерметична пориста поверхня у виробничих зонах з наявними фактами контамінації (пліснява, цвіль, порошкоподібні залишки від попереднього виробництва тощо). (*)
Обмежений виробничий простір, що може призвести до переплутування. (*)
Неуповноважений персонал має доступ до зони фізичного та електронного карантину / зона фізичного карантину погано позначена та/або позначень не дотримуються. (*)
Відсутня відокремлена зона / недостатні засоби для попередження контамінації або перехресної контамінації під час відбору проб сировини.
Порушення, які відносяться до несуттєвих
Персонал користується дверима, які ведуть безпосередньо назовні з виробничих приміщень чи приміщень для пакування.
Незахищені / не обладнані вловлювачами трапи в підлозі.
Неідентифіковані матеріальні лінії для рідин та газів.
Пошкоджені поверхні, які безпосередньо не контактують чи не знаходяться над відкритим продуктом.
У виробничих зонах здійснюється невиробнича діяльність.
Приміщення для відпочинку, гардеробні, санвузли та засоби для миття в неналежному стані.
Обладнання
Порушення, які відносяться до критичних
Обладнання, яке використовується для складних виробничих операцій при виробництві лікарських засобів критичного рівня ризику, не кваліфіковано; наявна несправність або відсутність належного контролю.
Порушення, які відносяться до суттєвих
Обладнання експлуатується не в межах своїх специфікацій. (*)
Обладнання, яке використовується під час критичних етапів виробництва, пакування/маркування і випробування, в тому числі й комп’ютеризовані системи, не кваліфіковане. (*)
Ємності для виробництва рідких засобів та мазей не обладнані затискачами у санітарному виконанні.
Обладнання під час зберігання не захищене від контамінації. (*)
Неналежне виробниче обладнання: поверхні пористі та не піддаються очищенню / матеріал поверхонь обладнання виділяє частинки речовин. (*)
Встановлення контамінації продукції сторонніми матеріалами, наприклад, мастилом, іржею та частинками від обладнання. (*)
Ємності, лотки і подібне виробниче обладнання не має кришок.
Не вживається достатньо запобіжних заходів, коли в обладнанні, такому як сушарка або автоклав, знаходиться більше ніж один продукт (існує можливість перехресної контамінації або переплутування). (*)
Місце розташування обладнання не запобігає перехресній контамінації або можливому переплутуванню внаслідок робіт, що виконуються в спільній зоні. (*)
Не проводиться технічне обслуговування системи води очищеної, система не експлуатується так, щоб забезпечувати виробництво водою відповідної якості. (*)
Протікання ущільнень з потенційним впливом на якість продукту. (*)
Відсутні програми калібрування для автоматичного, механічного, електронного або вимірювального обладнання / не ведуться відповідні записи.
Відсутні програми профілактичного обслуговування основного обладнання/ не ведуться відповідні записи.
Відсутні журнали використання обладнання.
Порушення, які відносяться до несуттєвих
Недостатня відстань між обладнанням та стінами, що заважає проводити належне очищення.
Основа нерухомого обладнання недостатньо ущільнена в місцях контакту.
Використання тимчасових засобів чи пристроїв для ремонту.
Несправне обладнання або таке, яким не користуються, не переміщено з виробничих зон або неналежним чином марковане.
Допоміжне обладнання, що використовується для виготовлення некритичної продукції, не кваліфіковане.
Документація
Порушення, які відносяться до критичних
Факт фальсифікації або викривлення даних в протоколі.
Порушення, які відносяться до суттєвих
Відсутня або неповна основна виробнича документація.
Документація від постачальників не отримується вчасно.
Відсутні або неповні звіти з дистрибуції.
Відсутнє або недостатнє протоколювання скарг щодо якості лікарських засобів.
Порушення, які відносяться до несуттєвих
Неповні плани та специфікації для виробничих споруд.
Невідповідний строк зберігання документальних матеріалів та протоколів.
Відсутні організаційні діаграми.
Неповні протоколи стосовно програм санітизації.
Виробництво
Порушення, які відносяться до критичних
Відсутня основна виробнича рецептура в письмовому вигляді.
Основна рецептура або документація на виробництво серії показує серйозні відхилення чи суттєві похибки в розрахунках.
Встановлення фальсифікації або викривлення послідовності стадій виробництва та пакування у порівнянні із затвердженими.
Порушення, які відносяться до суттєвих
Основна рецептура підготовлена/перевірена некваліфікованими працівниками.
Відсутність або незавершеність валідаційних випробувань/звітів для критичних виробничих процесів (немає оцінювання/затвердження). (*)
Неналежна валідація процедур переналаштування. (*)
Не затверджені/не задокументовані основні зміни у порівнянні з основною виробничою документацією. (*)
Відхилення від інструкцій під час виробництва не задокументоване та не схвалене службою якості.
Не досліджена розбіжність у виході продукції та не здійснено співставлення кількості продукції після виробництва.
Очищення виробничої лінії між виробництвом різних лікарських засобів не описується в СОП та не задокументоване.
Відсутні регулярні перевірки вимірювальних пристроїв, відсутні відповідні записи.
Відсутня належна ідентифікація виробничих приміщень та продукції у виробничому процесі, що призводить до високої вірогідності переплутування.
Неналежне маркування/зберігання відбракованих матеріалів та продуктів, що може призвести до переплутування.
Після отримання нерозфасовані лікарські засоби та лікарські засоби в процесі виробництва, сировина і пакувальні матеріали не зберігаються в карантині до отримання дозволу підрозділу з контролю якості до їх використання.
Неналежним чином контролюється маркування. (*)
Виробничий персонал працює з нерозфасованими лікарськими засобами та лікарськими засобами в процесі виробництва, сировиною та упаковкою, попередньо не схваленими службою контролю якості. (*)
Неналежне/неточне маркування нерозфасованих лікарських засобів / лікарських засобів в процесі виробництва, сировини та пакувальних матеріалів.
Розподіл вихідної сировини не проводиться відповідними особами згідно із СОП.
Основна рецептура помилкова або призводить до похибок в процесі виробництва
Зміни об’єму серії не складені/не дозволені кваліфікованим персоналом.
Неточна/неповна інформація у документах виробництва/пакування серії.
Об’єднання серій хоч і документується, але здійснено без схвалення служби контролю якості/не описано в СОП.
Відсутні письмові інструкції з пакування.
Відхилення під час процесу пакування не досліджуються кваліфікованим персоналом.
Недостатній контроль кодованого та некодованого пакувального матеріалу (включаючи зберігання, розподіл, друк, утилізацію).
Неправильне поводження із застарілим/зайвим пакувальним матеріалом.
Відсутня або неналежна програма самоінспекцій / програма не охоплює усі застосовні розділи Належної виробничої практики / протоколи самоінспекцій неповні або не ведуться.
Відсутня процедура відкликання продукції пов’язана з практикою дистрибуції, що унеможливлює проведення належного відкликання (відсутні або не ведуться протоколи дистрибуції продукції).
Неправильні процедури карантину та утилізації, що дозволяють повернення відкликаної/відбракованої продукції в продаж.
Порушення, які відносяться до несуттєвих
Неповні стандартні операційні процедури щодо поводження з матеріалами та продукцією.
Доступ до виробничих зон дозволений не тільки для персоналу, який має на це відповідні повноваження.
Недостатній контроль вихідних матеріалів.
Неповні письмові інструкції з пакування.
Неналежна процедура відкликання.
Неповний/неточний щорічний огляд якості продукції.
Санітарна підготовка приміщень та обладнання
Порушення, які відносяться до критичних
Встановлення наявності поширеного накопичення залишків / сторонніх речовин, що свідчить про неналежне очищення.
Встановлення явної інвазії.
Порушення, які відносяться до суттєвих
Відсутня письмова програма санітизації, але приміщення знаходяться в прийнятному стані чистоти.
Відсутні СОП для мікробіологічного контролю/контролю навколишнього середовища; немає встановлених меж, що вимагають вживання заходів для виробничих зон, в яких виготовляють вразливі нестерильні лікарські засоби.
Процедури очищення виробничого обладнання не валідовані (включаючи супутні аналітичні методи). (*)
Неналежні письмові вимоги щодо стану здоров’я та/або програми забезпечення гігієни.
Не дотримуються взагалі або не в повній мірі дотримуються вимоги щодо стану здоров’я та/або програми забезпечення гігієни.
Порушення, які відносяться до несуттєвих
Неповна письмова процедура санітизації.
Неповне впровадження письмової процедури санітизації.
Контроль якості
Порушення, які відносяться до критичних
На виробничій дільниці відсутня Уповноважена особа.
Підрозділ з контролю якості не є відокремленим та незалежним підрозділом, який наділений правом приймати рішення, з фактами того, що рішення служби контролю якості часто ігноруються виробничим відділом або адміністрацією.
Порушення, які відносяться до суттєвих
Неналежні виробничі приміщення, невідповідні персонал та випробувальне обладнання.
Відсутність права доступу до виробничих зон. (*)
Відсутні затверджені та доступні стандартні операційні процедури щодо відбору проб, контролю та випробування матеріалів.
Продукція відпускається для продажу без схвалення службою контролю якості. (*)
Служба контролю якості допускає до продажу продукцію без належної перевірки виробничої документації та документації з пакування.
Основна виробнича документація не відповідає матеріалам реєстраційного досьє. (*)
Результати випробувань поза межами специфікацій; відхилення та гранична відповідність належним чином не досліджені та не задокументовані відповідно до СОП. (*)
Сировина/пакувальний матеріал використовується у виробництві без попереднього дозволу підрозділу з контролю якості.
Повторна обробка або переробка продукції проводилась без попереднього дозволу служби контролю якості. (*)
Відсутня або неналежна система роботи зі скаргами та рекламаціями.
Повернені лікарські засоби знову надходять у продаж без оцінювання та/або дозволу служби контролю якості.
СОП для операцій, які можуть вплинути на якість продукції, наприклад, транспортування, зберігання тощо, не погоджені підрозділом з контролю якості / не запроваджені.
Неналежні докази того, що умови зберігання та транспортування є відповідними.
Відсутня або незадовільна система контролю управління змінами.
У випробувальних лабораторіях (власні лабораторії чи лабораторії за контрактом) наявні системи та засоби контролю для відповідної кваліфікації, експлуатації, калібрування та технічного обслуговування обладнання, а також стандартні зразки, розчини та протоколи випробувань, що зберігаються, не гарантують, що отримані результати й висновки є точними, правильними і надійними. (*)
Продукція випробовується на закордонній дільниці або дільниці за контрактом, яка не має ліцензії на відповідну діяльність. (*)
Випробування на стерильність не проводяться в умовах класу А в оточенні класу В чи в ізоляторі класу А в приміщенні з обмеженим доступом для не залученого персоналу.
Порушення, які відносяться до несуттєвих
Між контрактною лабораторією та підприємством, що виробляє лікарські засоби, відсутня угода про проведення випробовувань.
У встановлені строки не проводяться розслідування випадків невідповідності.
Випробування вихідної сировини
Порушення, які відносяться до критичних
Факт фальсифікації або викривлення результатів аналітичних випробувань.
Відсутній сертифікат аналізу постачальника/виробника активних фармацевтичних інгредієнтів (далі — АФІ) та не проведений контроль цієї вихідної АФІ виробником готового лікарського засобу.
Порушення, які відносяться до суттєвих
В наявності скорочений обсяг контролю вихідної сировини без належної перевірки постачальників.
Вода, яка застосовується в рецептурі, неналежної якості.
Недостатнє випробування вихідної сировини.
Неповні специфікації.
Специфікації не затверджені службою контролю якості.
Методи аналізу не валідовані.
Використання сировини після спливу терміну повторного тестування без проведеного належного повторного тестування.
Використання сировини після закінчення терміну придатності.
Декілька серій тієї самої сировини в складі одного постачання не вважаються такими, що підлягають окремому відбору проб, випробуванню та дозволу на використання.
Відсутня СОП для умов транспортування та зберігання.
Затвердження брокерів та оптових продавців без належної документації.
Порушення, які відносяться до несуттєвих
Серії сировини, що знаходяться в процесі підтверджуючих випробувань, використовуються у виробництві без схвалення їх службою контролю якості.
Неповна валідація методів аналізу.
Випробування пакувального матеріалу
Порушення, які відносяться до суттєвих
В наявності скорочений план випробувань без належної перевірки постачальників.
Випробування пакувального матеріалу не проводились взагалі або проводились неналежним чином. (*)
Неналежні специфікації.
Специфікації не затверджені службою контролю якості.
Виробник, що здійснює пакування/маркування, не проводить тест на ідентичність після отримання матеріалів на підприємство.
Затвердження постачальників проводиться без належного документування.
Порушення, які відносяться до несуттєвих
Неналежні процедури транспортування та зберігання.
Неналежні умови та/або запобіжні заходи для того, щоб запобігти контамінації пакувального матеріалу під час відбору проб.
Випробування готової продукції
Порушення, які відносяться до критичних
Відсутні докази того, що продукція випробовувалась виробником.
Факт фальсифікації або викривлення результатів випробувань / підробки сертифіката аналізу.
<spanПорушення, які відносяться до суттєвих</span
У продаж надійшла продукція, яка не відповідає вимогам. (*)
Неповна/неналежна специфікація.
Специфікації на готову продукцію не затверджені службою контролю якості.
Неповне випробування. (*)
Валідація методів аналізу не проводилася взагалі або проводилася неналежним чином. (*)
Відсутня СОП для умов транспортування та зберігання.
Використання принципів унікальної ідентифікації не відповідає прийнятній практиці.
Порушення, які відносяться до несуттєвих
Неналежний перенос до лабораторії валідованого аналітичного методу.
Звіт про валідацію методів не конкретизує версію аналітичного методу, що використовується під час валідації.
Відбір зразків
Порушення, які відносяться до суттєвих
Не зберігаються архівні зразки готових лікарських засобів.
Ненадання архівних зразків за умови забезпечення альтернативними зразками.
Порушення, які відносяться до несуттєвих
Відсутні зразки вихідних матеріалів.
Недостатня кількість зразків готових лікарських засобів або АФІ.
Незадовільні умови зберігання.
Стабільність
Порушення, які відносяться до критичних
Відсутні дані для визначення терміну придатності продукції.
Факт фальсифікації або викривлення даних про стабільність / підробки сертифіката аналізу.
Порушення, які відносяться до суттєвих
Неналежна кількість серій для визначення терміну придатності.
Неналежні дані для визначення терміну придатності.
Не вживаються заходи, коли дані свідчать про те, що продукція не відповідає своїй специфікації до закінчення терміну придатності. (*)
Відсутня або незадовільна програма подальшого вивчення стабільності.
Не проводяться дослідження стабільності, пов’язані зі змінами на виробництві (в рецептурі) або змінами пакувального матеріалу.
Методи аналізу не валідовані.
Не беруться до уваги «найгірші випадки» (наприклад, повторно оброблені/перероблені серії).
Незадовільні умови зберігання зразків для вивчення стабільності.
Порушення, які відносяться до несуттєвих
Перевірка стабільності не проводиться в строки, вказані в письмовій програмі.
Перевірка даних про стабільність не проводиться вчасно.
Стерильна продукція
Порушення, які відносяться до критичних
Відсутня або неналежна валідація критичних циклів стерилізації.
Система отримання, зберігання та розподілу води для ін’єкцій не валідована зі встановленням наявності проблем, таких як мікробне число / число ендотоксинів, що не відповідає специфікаціям.
Не проводиться тест наповнення поживними середовищами, щоб довести валідацію процесів асептичного наповнення.
Відсутній контроль умов навколишнього середовища / не проводиться мікробіологічний контроль чистих зон під час наповнення для продукції з асептичним наповненням.
Продовжується асептичне наповнення навіть після отримання незадовільних результатів випробувань, що моделюють процес наповнення поживними середовищами.
Серії, результати первинного тестування стерильності яких були незадовільні, допущені до реалізації на основі другого тестування без належного розслідування.
Незадовільні умови навколишнього середовища для проведення асептичних операцій.
Не проводиться перевірка герметичності ампул.
Порушення, які відносяться до суттєвих
Засоби на водній основі не підлягають кінцевій стерилізації парою без належних обґрунтувань чи без затвердження такої стерилізації в реєстраційному досьє.
Неналежна класифікація приміщень для операцій обробки/наповнення. (*)
Асептичні виробничі блоки приміщень з від’ємним тиском у порівнянні з чистими зонами C-D класів. Чисті зони C-D класів під від’ємним тиском у порівнянні з некласифікованими зонами. (*)
Відібрано недостатню кількість зразків для моніторингу умов навколишнього середовища / неналежні методи відбору проб. (*)
Неналежний контроль навколишнього середовища / неналежний моніторинг життєздатних мікроорганізмів під час операції наповнення продукції в асептичних умовах. (*)
Приміщення та обладнання не спроектовані або не обслуговуються так, щоб звести контамінацію / виділення часток до мінімуму. (*)
Неналежне технічне обслуговування систем води очищеної та води для ін’єкцій.
Незадовільна повторна валідація систем води очищеної та води для ін’єкцій після ремонту, модернізації, трендів до виходу за межі специфікацій.
Незадовільне навчання персоналу.
Персонал залучається до асептичного наповнення до того, як він успішно провів тест наповнення поживними середовищами.
Неналежні процедури доступу у чисті та асептичні зони.
Неналежна програма санітизації / дезінфекції.
Неналежні процедури / незадовільні заходи з мінімізації контамінації або попередження переплутування.
Не валідовані проміжки часу між очисткою, стерилізацією та використанням компонентів, ємностей та обладнання.
Перед стерилізацією не враховується біологічне навантаження.
Не валідовані проміжки часу між початком виробництва та стерилізацією або фільтрацією.
Неналежна програма виконання тесту наповнення поживними середовищами.
Не демонструється здатність поживних середовищ забезпечувати ріст широкого спектру мікроорганізмів.
Неправильне тлумачення результатів тесту наповнення поживними середовищами.
Недостатня кількість зразків для перевірки на стерильність, або вони не є репрезентативними відносно усієї серії продукції.
Кожне завантаження стерилізатора не вважається окремою серією для перевірки на стерильність.
Вода очищена не використовується як живильна основа для системи води для ін’єкцій та генератора чистої пари.
Неналежний план випробування води для ін’єкцій. (*)
Вода для ін’єкцій, що використовується для фінального промивання ємностей та компонентів, які використовуються для парентеральних лікарських засобів, не перевіряється на ендотоксини, коли ці ємності та компоненти не проходять процес депірогенізації в подальшому.
Невідповідне навколишнє середовище / неналежні контролі обтиснення ковпачків після асептичного наповнення.
Неналежний контроль часток та дефектів. (*)
Гази, які використовуються для продувки розчинів чи захисного шару, не проходять через стерилізуючий фільтр. (*)
Неналежна перевірка цілісності стерилізаційних та дихальних фільтрів. (*)
Порушення, які відносяться до несуттєвих
Пара для стерилізації не перевіряється для забезпечення прийнятної якості.
Недостатній контроль максимальної кількості персоналу, який присутній в чистих та асептичних зонах.
Алгоритм з класифікації порушень
При класифікації порушення як «Критичне» інспектори повинні визначити чи існують чіткі докази, враховуючи ризик шкоди, як зазначено у визначенні (приклад наведений у блок-схемі, рисунок 1).
Коли «Критичне» порушення не є чітко очевидним, порушення може бути оцінене як «Критичне», «Суттєве» або «Несуттєве». Необхідно визначити класифікацію, за якою можна дотримуватися зазначених нижче вказівок.
Провести детальну оцінку порушення для визначення початкової класифікації згідно з блок-схемою, рисунки 2–5.
Провести оцінку факторів, які або збільшують, або зменшують ризик, незалежно від початкової класифікації, як описано в поясненнях щодо факторів, що можуть вплинути на підвищення або зменшення ризику.
Прийняти рішення щодо того, чи може початкова класифікація ризику бути такою, як описано в блок-схемі, рисунок 1:
підвищити за рахунок ефектів, які збільшують ризик, тобто впливу, що збільшує ризик;
залишити без змін, або знизити внаслідок ефектів, які зменшують ризик, тобто впливають на зниження ризику.
Формат написання та групування порушень також може бути чинником, що впливає на класифікацію порушення.
Блок-схема, рисунок 1 — Процес класифікації — Огляд
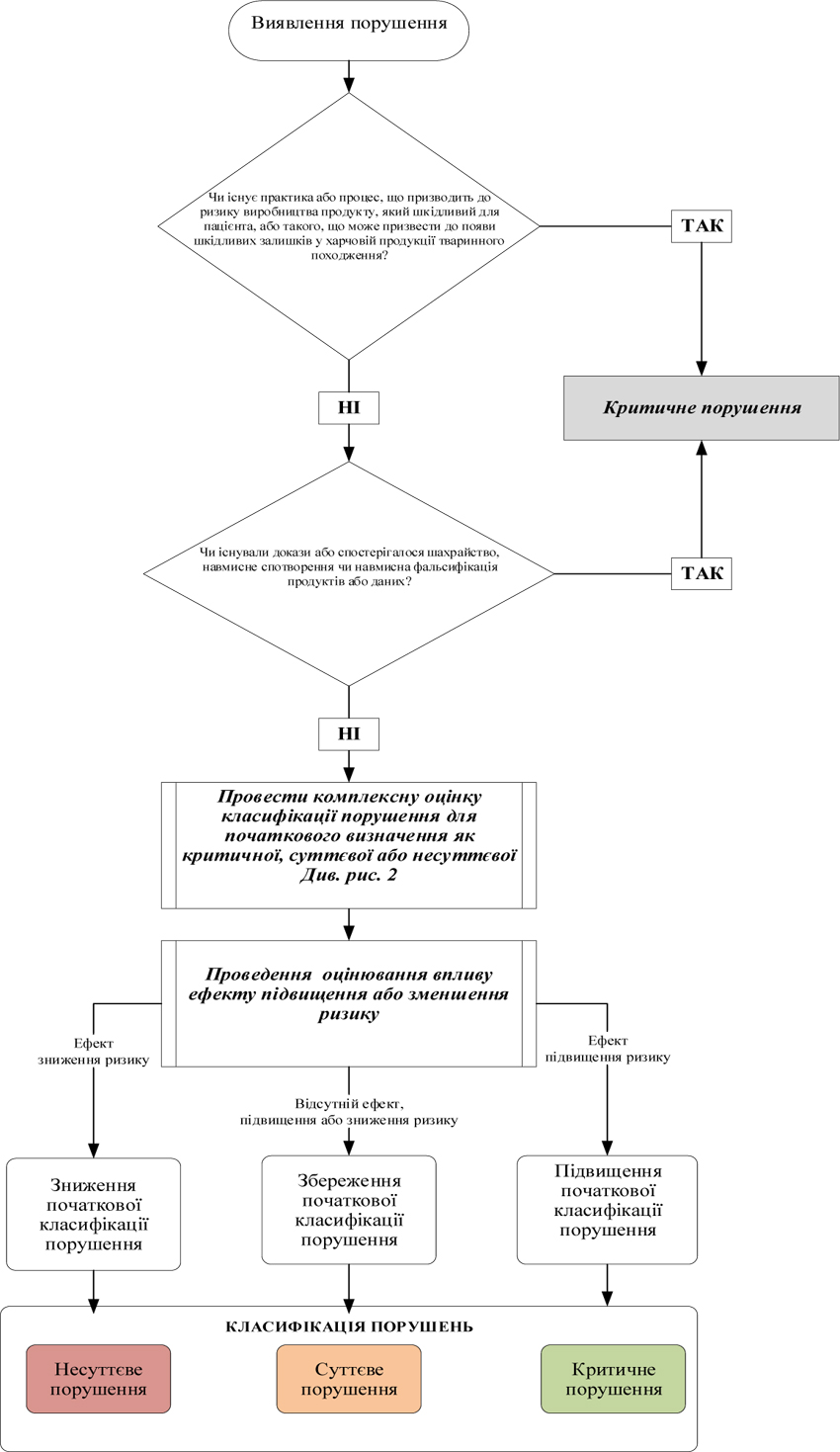
Блок-схема, рисунок 2 — Процес класифікації — Огляд (продовження)
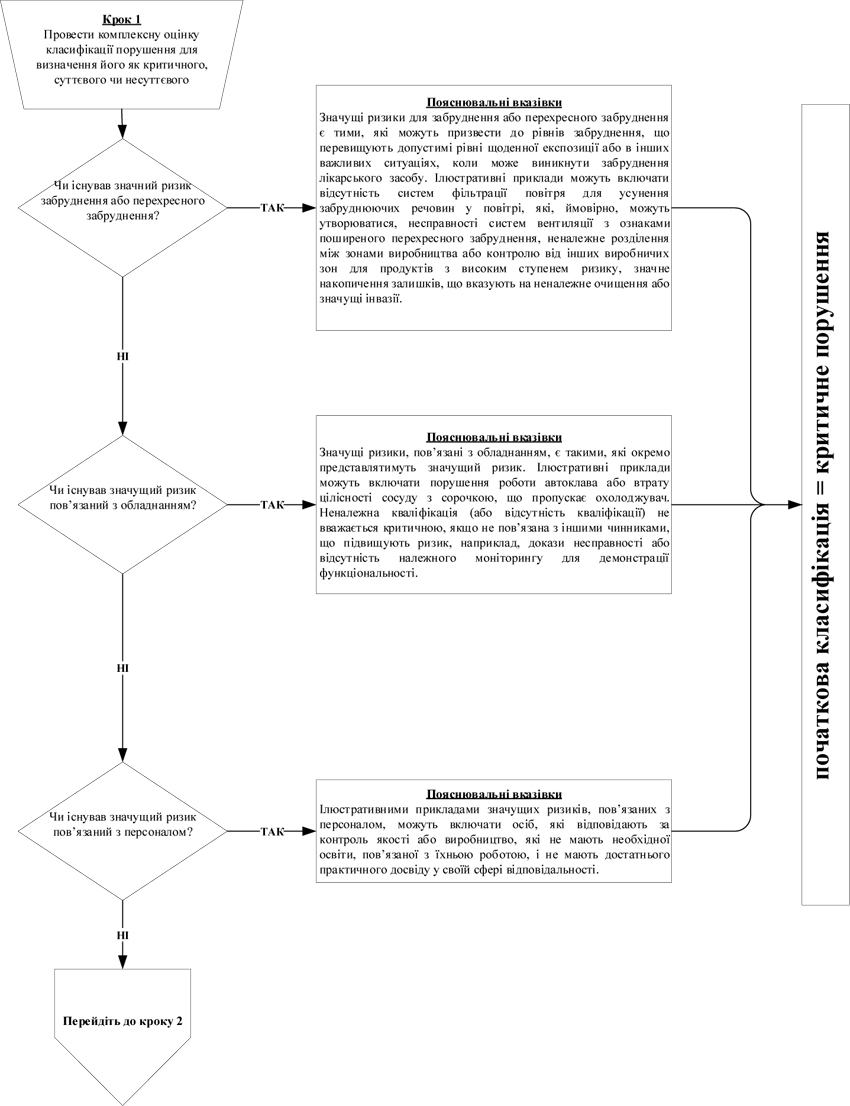
Блок-схема, рисунок 3 — Процес класифікації — Огляд (продовження)

Блок-схема, рисунок 4 — Процес класифікації — Огляд (продовження)
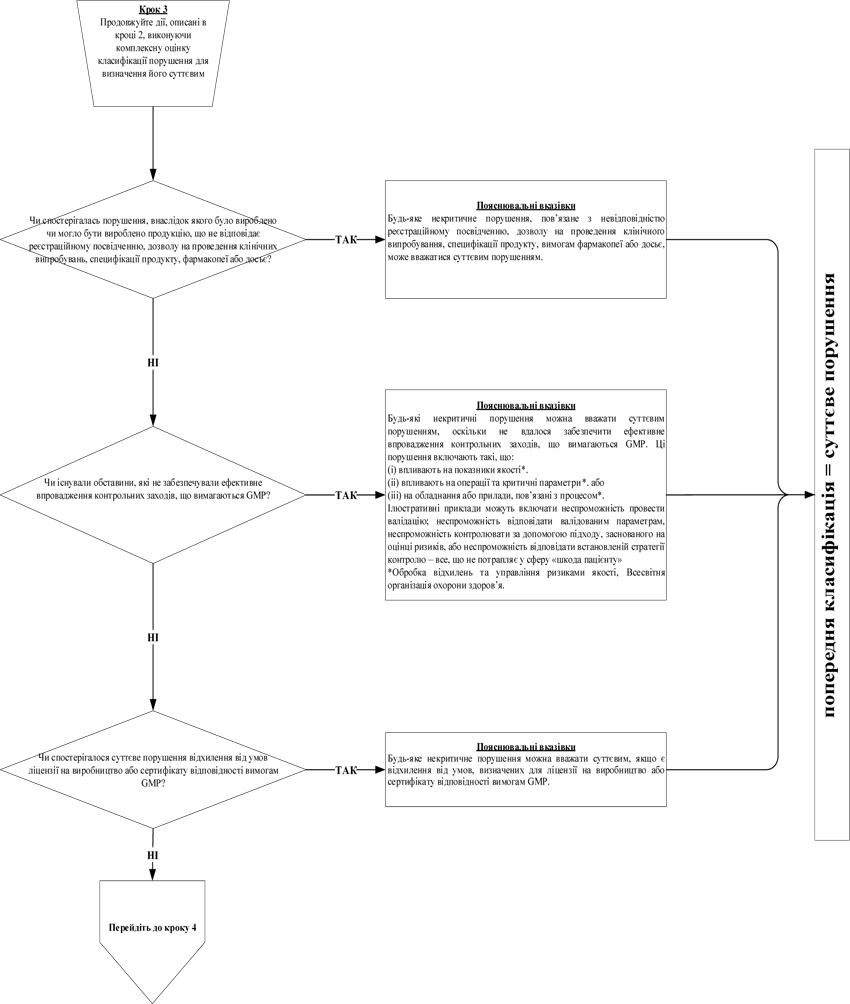
Блок-схема, рисунок 5 — Процес класифікації — Огляд (продовження)
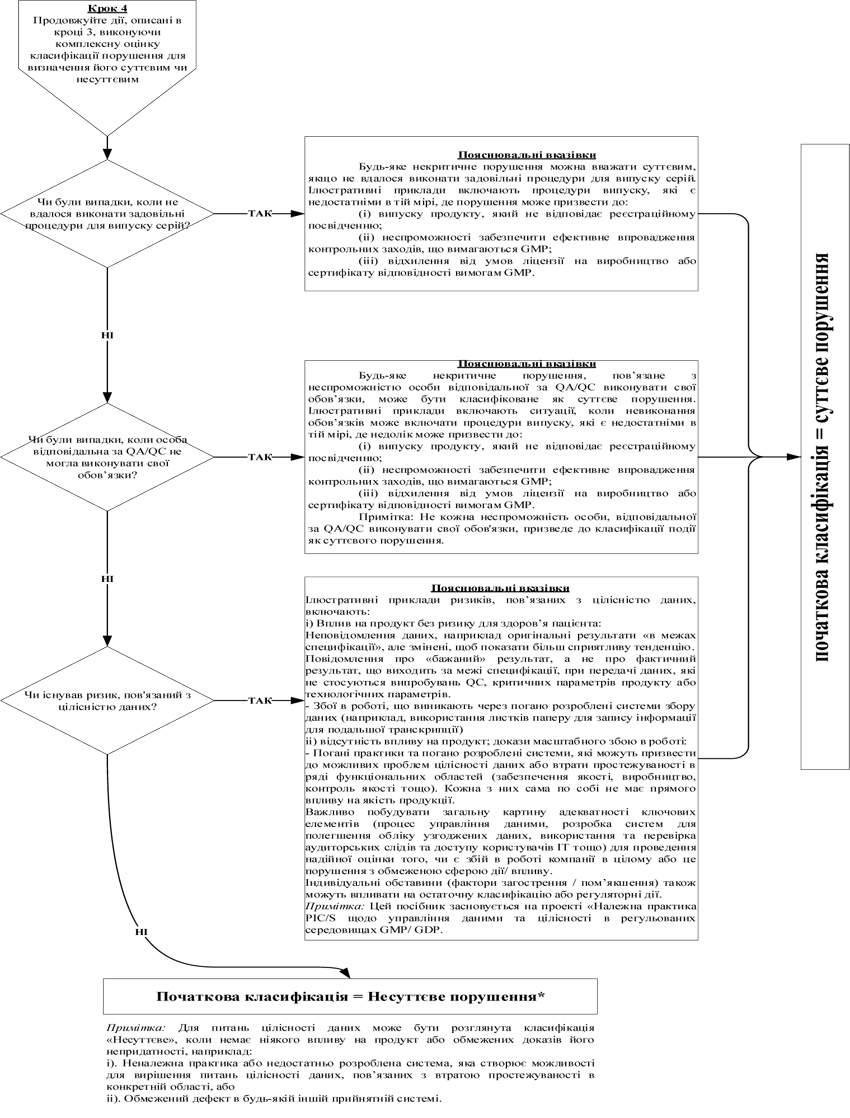
ПОЯСНЕННЯ ЩОДО ФАКТОРІВ, ЩО МОЖУТЬ ВПЛИНУТИ НА ПІДВИЩЕННЯ АБО ЗМЕНШЕННЯ РИЗИКУ
1. Фактори, що збільшують ризик — підвищення початкової класифікації
«Суттєві» та «Несуттєві» порушення можуть бути підвищені на один рівень до «Критичного» або «Суттєвого» порушення, відповідно, коли можуть існувати умови, що відповідають сутності визначення підвищеної класифікації ризиків. Вважається, що це досягається, коли існують певні фактори, що підвищують ризик.
Фактори збільшення ризику включають:
повторне або постійне порушення (пункт 3 пояснень);
групу або комбінацію порушень (пункт 4 пояснень);
ризик, пов’язаний з продуктом (пункт 5 пояснень);
нездатність керівництва виробника визначити та вжити обґрунтованих заходів для зменшення ризику для пацієнта до прийнятного рівня для продукції, що перебуває в дистрибуції, і для майбутнього виробництва внаслідок невідповідної практики або процесу.
2. Фактори, що зменшують ризик — зниження початкової класифікації
«Критичне» та «Суттєве» порушення можуть бути знижені на один рівень до «Суттєвого» або «Несуттєвого» порушення, відповідно, коли можуть існувати умови для зниження класифікації ризиків. Вважається, що це досягається, коли існують певні фактори, що знижують ризик.
При розгляді факторів, що знижують ризик, важливо забезпечити, щоб ці фактори були послідовними та ефективними.
Фактори, що знижують ризик, включають:
мінімізацію ризику, пов’язаного з продуктом (пункт 5 пояснень);
мінімізацію ризику шкоди для пацієнта;
інші фактори зниження ризику (пункт 6 пояснень);
дії, вжиті виробником, наприклад, план попереджувальних і коригувальних дій для зниження ризику дефіциту.
Вплив продукту, який вже постачається на ринок, слід враховувати при зниженні категорії критичного порушення.
3. Повторні або повторювані порушення — підвищення початкової класифікації
Повторні або часто повторювані порушення — це порушення, які також були виявлені при попередній перевірці, коли відповідні попереджувальні або коригувальні дії не були вжиті.
У певних випадках повторювані порушення можуть розглядатися як такі, що підвищують ризик, що дозволяє підвищити початкову класифікацію ризику, зокрема, якщо очевидно, що існують навмисні або незадовільні зусилля для усунення порушення. Ефект, що підвищує ризик, слід враховувати, коли:
існує серйозний недолік в системі якості, за допомогою якої не можна задовільно визначити потенційні першопричини невідповідності або не можна адекватно розглянути ці причини без наявності інших факторів, що зменшують ризик, або
існують й інші фактори для розгляду, які підпадають під визначення підвищеної класифікації ризиків, наприклад, необґрунтовано тривале впровадження коригувальних дій.
Примітка: Очікується, що підвищення ризику повторюваної невідповідності потребуватиме розуміння потенційних факторів, які, можливо, призвели до повторення.
4. Група або комбінація порушень — оновлення початкової класифікації
Різні питання/проблеми, виявлені під час перевірки, можуть бути згруповані або об’єднані в одне порушення, якщо кожне питання/проблема супроводжує або стосується зазначеного основного порушення.
Ефект підвищення ризику, може бути застосований для підвищення початкової класифікації ризику на один рівень, коли визначення підвищеної класифікації ризику було застосоване.
Приклади декількох «Несуттєвих» порушень, жодне з яких саме по собі не може бути «Суттєвим», але які разом можуть представляти «Суттєве» порушення, слід пояснити і повідомити про це.
5. Ризик, пов’язаний з продуктом — підвищення або зниження початкової класифікації
На деяких виробничих дільницях є продукти та процеси, які пов’язані зі значно більшими ризиками, ніж інші.
Визначення класифікації ризиків, пов’язаних з продуктом:
продукти з високим ступенем ризику, які мають високу чутливість до забруднення в процесі виробництва, включаючи термін придатності, наприклад мікробного або хімічного;
продукти з низьким ступенем ризику, які мають меншу ймовірність забруднення в процесі виробництва, включаючи термін зберігання.
Фактор, що збільшує ризик, і той що знижує ризик, можуть застосовуватися після розгляду ризиків, пов’язаних з продуктом, таким чином:
для деяких продуктів з високим ступенем ризику певні порушення, що класифікуються як «Суттєве» або «Несуттєве», можуть бути відповідно підвищені до «Критичного» або «Суттєвого» порушення. Це може бути застосовано, коли обставини порушення, що розглядаються, відповідають інтерпретації визначення «Критичного» порушення;
для деяких продуктів з низьким ступенем ризику певні порушення, що класифікуються як «Критичні» або «Суттєві», можуть бути відповідно знижені до «Суттєвого» порушення або «Несуттєвого» порушення. Для продуктів з низьким ступенем ризику «Критичне» порушення може бути знижено до «Суттєвого», якщо воно не буде підпадати під визначення «Критичного» порушення.
6. Інші фактори, що зменшують ризик
Коли інші фактори, що зменшують ризик, очевидні для мінімізації ризику, пов’язаного з порушенням, то оцінка ризику може бути знижена.
Інші фактори, що знижують ризик, зазвичай можна розглядати лише тоді, коли існує вторинна система, яка може мінімізувати ризики, пов’язані з порушеннями. Наприклад, кваліфікована система пакування з системою візуальної інспекції упаковки, яка забезпечує 100% контроль кожного упакованого продукту, може розглядатися як фактор, що знижує ризик для порушення, пов’язаного головним чином з друкованими матеріалами, що зберігаються невпорядковано, що може призвести до переплутування.
Якщо існує ряд факторів, що збільшують ризик і зменшують ризик, слід розглянути одночасно всі фактори ризику, а потім визначити загальну оцінку ризику для підвищення або зниження початкового ризику.
ПРИКЛАДИ КЛАСИФІКАЦІЇ ПОРУШЕНЬ
Наданий список є допоміжним інструментом і не є вичерпним, або обов’язковим.
1. Приклади критичних порушень:
відсутність валідації стерилізації (стосується всіх стерильних продуктів);
відсутність належних заходів контролю, що призводять до фактичного або значного ризику перехресної контамінації, що перевищує максимально допустимий рівень впливу у наступних продуктах;
докази зараження паразитами/шкідниками (стосується всіх виробників);
фальсифікація або хибне подання результатів аналізів чи записів (стосується всіх виробників);
неможливість забезпечити якість та/або ідентичність вихідної сировини (стосується всіх виробників);
відсутність основних документів щодо виготовлення серії (стосується всіх виробників);
відсутність, фальсифікація або хибне подання записів щодо виробництва та пакування (стосується всіх виробників);
не проведена валідація системи водопостачання для стерильних продуктів (стосується виробників стерильних продуктів);
не проведена валідація системи вентиляції та кондиціювання повітря для стерильних продуктів (стосується виробників стерильних продуктів);
непридатні приміщення з високим або ймовірним ризиком контамінації (стосується всіх виробників);
відсутні підтвердження, що процедури санкціонованого відкликання були дотримані (стосується всіх виробників).
2. Приклади суттєвих невідповідностей:
не проведена валідація для критичних процесів (застосовується до всіх лікарських засобів, але може бути перекваліфіковане в «критичне» для продуктів з низькою дозою/сильнодіючих; зокрема для процесів стерилізації для стерильних продуктів);
відсутність або явно неналежна фільтрація повітря (застосовується до всіх виробників лікарських засобів ‒ може бути перекваліфіковане в «критичне», коли забруднюючі речовини можуть становити проблему безпеки та є «критичними» для стерильних лікарських засобів);
відсутні або неефективні заходи контролю, що забезпечують належну впевненість у тому, що перехресна контамінація буде контролюватися у відповідних межах допустимого впливу на здоров’я для наступних продуктів
(буде «критичним», якщо перехресна контамінація перевищує чи може перевищити допустимий рівень впливу);
пошкодження (отвори, тріщини, відшаровування фарби) на стінах/ стелі у виробничих приміщеннях, де продукт знаходиться в нестерильних зонах;
конструкція виробничих зон, що не дозволяє ефективно проводити очищення;
невідповідне виробниче приміщення, що може призвести до переплутування;
відсутні місця відбору проб вихідної сировини для виробників лікарських засобів (якщо вжито належних запобіжних заходів, можна класифікувати як «Несуттєве») ;
для виробництва рідини/крему не використовується технічна арматура у санітарному виконанні;
обладнання, що зберігається, не захищено від забруднення;
особи, відповідальні за контроль якості/виробництво, не відповідають кваліфікації за освітою, компетентністю та досвідом;
неналежна початкова та поточна підготовка персоналу та/або відсутність записів з навчання;
процедури очищення не документовані та/або відсутні записи про очищення;
не проведена валідація процедури очищення виробничого обладнання;
скорочено контроль якості вхідної сировини без відповідних підтверджуючих даних від постачальників;
неповне випробування/тестування сировини;
не проведена валідація методів випробування;
не проведена валідація складних виробничих процесів для некритичних продуктів;
незатверджені/ незареєстровані зміни до технологічного регламенту або еквівалентних документів;
відхилення від інструкцій не схвалені;
відсутня або неналежна програма самоінспекцій;
відсутність належного випуску для процедури постачання;
продукт перероблений без належного схвалення;
немає системи/ процедури розгляду скарг або повернення продуктів;
неналежне випробування/тестування пакувальних матеріалів;
немає поточної програми випробування стабільності та/або недоступні дані про стабільність для всіх продуктів;
недостатнє освітлення у виробничих зонах або зонах контролю;
не ідентифіковані контейнери, з яких були відібрані проби;
не здійснюється моніторинг і відсутня аварійна/сигнальна система сигналізації щодо значень температур для критичних зон зберігання з контролем температур;
неналежна система управління змінами;
неналежна система управління відхиленнями;
не виконуються розслідування стосовно аварійних сигналів та виходів температури за межі відхилень від вимог щодо зберігання та транспортування.
Додаток 11
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 11 розділу ІV)
ЗВІТ ЗА РЕЗУЛЬТАТАМИ Інспектування
І. Загальні положення
| Виробник: |
найменування виробника, місцезнаходження (юридична адреса); _________________________________________ найменування виробничої(их) дільниці(ць), місце провадження діяльності, DUNS номер та GPSкоординати ____________________________________________________ |
| Лабораторії, що здійснюють контроль якості за контрактом (договором), складські зони за контрактом (договором) | найменування, місце провадження діяльності, DUNS номери та GPS координати________________________________________ |
| Види діяльності, які інспектувались: | |
(зазначити потрібне знаком «Х»)
| Виробництво активних фармацевтичних інгредієнтів (субстанцій) | |
| Виробництво готових лікарських засобів (ГЛЗ) | |
| Виробництво досліджуваних лікарських засобів | |
| Виробництво проміжних продуктів, нерозфасованих продуктів (продукції «in bulk») | |
| Упаковка (тільки) | |
| Лабораторний контроль якості лікарських засобів | |
| Контроль кожної серії та дозвіл на реалізацію серій лікарських засобів | |
| Виробництво та аналіз за контрактом (зовнішня (аутсорсингова) діяльність) | |
| Зберігання, реалізація та транспортування (дистрибуція) | |
| Інше __________________________________________________________ |
Дати проведення інспектування:
_____________________________________________________________________
(за місцями розташування виробничих дільниць, контрактних лабораторій та складських зон)
Інспектори:
___________________________
(П.І.Б., посади інспекторів)
На виконання наказу від _____________________________ № ________________________________________
(інформація щодо конфіденційності)
Нормативна база:
Чинна версія GMP ЄС.
Настанова «Лікарські засоби. Належна виробнича практика», затверджена МОЗ України, яка гармонізована з чинною версією GMP ЄС.
Вступ
(навести коротку інформацію про підприємство, яке було проінспектовано, включаючи стислі відомості щодо найменування і адреси виробництва (виробничих дільниць), лабораторії, у тому числі що здійснюють контроль якості за контрактом (договором), складські зони, наявність системи забезпечення якості відповідно до чинників GMP (за розділами досьє виробничої дільниці), у тому числі щодо дозвільних документів, змін, що відбулися, тощо)
_________________________________________________________________________
Відомості про ліцензовану діяльність, сертифікати GMP
_________________________________________________________________________
Зміни, що відбулися на виробництві з моменту попереднього інспектування (за наявності)
_________________________________________________________________________
Інформація про хід інспектування
Мета інспектування
(номер, дата і короткий зміст наказу про інспектування)
_________________________________________________________________________
Масштаб і об’єкти
(навести перелік об’єктів (процеси, служби та системи), які були проінспектовані згідно із програмою та планом інспектування, а також тих, що не були предметом інспекції;
навести назви лікарських форм, виробництво яких було проінспектовано (наприклад: стерильні лікарські засоби (перелік форм), нестерильні лікарські засоби (перелік форм);
навести інформацію щодо відхилень від програми (перестановки пунктів програми між днями та/або інтервалами часу тощо), якщо такі мали місце під час інспекції, та про причини, що їх зумовили)
_________________________________________________________________________
Працівники підприємства, які брали участь в інспектуванні
(навести перелік із зазначенням посад)
_________________________________________________________________________
II. Результати інспектування
Загальний опис виробництва та спостереження під час інспектування
| Фармацевтична система якості | |
| Персонал | |
| Приміщення та обладнання | |
| Документація | |
| Технологічний процес | |
| Контроль якості | |
| Зовнішня (аутсорсингова) діяльність | |
| Рекламації та відкликання продукції | |
| Самоінспекції | |
| Зберігання, реалізація та транспортування продукції (дистрибуція) | |
| Досьє виробничої дільниці (Site Master File, SMF) | Відповідність SMF вимогам, встановленим до його змісту та оформлення, загальна оцінка відповідності фактичного стану виробничих дільниць інформації, наведеній у відповідних частинах SMF, та вимогам GMP |
| Інші специфічні питання (за наявності) | |
| Відбір зразків під час інспекції (якщо такий проводився) | Інформація про відбір зразків, виконаний під час інспекції |
| Результати виконання заходів щодо усунення порушень, виявлених під час попередньої інспекції (за наявності) |
Детальний перелік установлених фактів невідповідності вимогам GMP та їх класифікація*:
|
№ з/п |
Пункт настанови | Детальний опис виявленого порушення | Класифікація порушення (критичне, суттєве, несуттєве) |
__________
* Усі встановлені порушення мають бути оцінені відповідно до вимог GMP з посиланнями на пункти нормативних документів та, якщо необхідно, документів, рекомендованих PIC/S. Встановлені невідповідності мають бути відображені у звіті, навіть якщо під час інспекції було вжито відповідних коригувальних заходів для їх усунення. У разі якщо невідповідності стосуються реєстраційних матеріалів, це має бути чітко констатовано.
| Кількість копій звіту та їх розповсюдження | |
| Додатки до звіту | План і програма інспекції тощо |
| Висновки | За результатами інспекції можна констатувати наявність невідповідностей вимогам GMP, які викладені і класифіковані в цьому звіті, всього: ______, з них:критичних — ______суттєвих — ________несуттєвих — _______Якщо в процесі інспектування порушення усунуті, про це повинно бути зазначено.Наявний стан виробництва та наявність виявлених під час інспектування невідповідностей дають/не дають можливість надати оцінку підприємству як такому, що відповідає/не відповідає вимогам GMPПри повторному інспектуванні зазначаються класифікація та кількість неусунутих порушень. |
| Рекомендаціїінспекторів** |
Інспектори:
__________________________ ________________ _________________
(посада) (підпис, дата) (П.І.Б.)
__________________________ ________________ _________________
(посада) (підпис, дата) (П.І.Б.)
__________
** Група інспекторів у строки, зазначені в цьому Порядку, інформує Держлікслужбу України щодо встановлених порушень вимог належної виробничої практики, висновків за результатами інспекції та надає до Держлікслужби України цей звіт. Виробнику має бути вказано на необхідність інформування Держлікслужби України щодо запланованих коригувальних заходів, строків та результатів їх виконання.
Додаток 12
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 17 розділу ІV)
ПРОТОКОЛ
наради / Meeting minutes
вступна нарада / opening meeting Дата/ Date ______________
заключна нарада / final meeting
| Загальна інформація щодо даного інспектування/ General information on given inspection | |
| Найменування суб’єкта господарської діяльності/ Name of the business entity | |
| Місце провадження діяльності/ Address of the business activity | |
| Мета перевірки/ Object of the inspection | |
| Інспектори / Inspectors | |
| Ця частина протоколу зустрічі заповнюється на заключній зустрічі виключно посадовими особами, що здійснюють перевірку суб’єкта господарювання/Only public servants conducting the inspection of business entity fill this part of the meeting minutes during the final meeting | Так/Yes | Ні/No |
| Класифікацію порушень (невідповідностей), виявлених під час інспектування, оголошено/Is the classification of deficiencies (nonconformities) identified during the inspection announced? | | |
| Надано відповідні документальні підтвердження усунення порушень (невідповідностей) протягом проведення інспектування /Is the relevant documentary evidence for deficiencies (nonconformities) correction during the inspection provided?(надаються у разі усунення порушень (невідповідностей) протягом проведення інспектування)/(provided in the case of deficiencies (nonconformities) correction during the inspection) | | |
| Надано план коригувальних та запобіжних дій щодо усунення виявлених під час інспектування критичних порушень (невідповідностей) / Is the corrective and preventive action plan (САРА) on correction of critical deficiencies (nonconformities) revealed during the inspection provided?(вимагається за наявності критичних порушень (невідповідностей))/(required in the case of critical deficiencies (nonconformities)) | | |
| Наявні зауваження щодо проведеного інспектування та/або класифікації порушень (невідповідностей) з боку Заявника та/або виробника /Are there comments on conducted inspection and/or classification of deficiencies (nonconformities) by the Applicant and/or manufacturer? | | |
Стор. з
| Перелік значущих спостережень, які були оцінені в порядку значимості /List of significant observations ranked in order of significance. | |
| П.І.Б. інспекторів / Inspectors Full Name | Підпис / Signature |
| Опис зауважень щодо проведеного інспектування та/або класифікації порушень (невідповідностей) з боку Заявника та/або виробника /Comments on conducted inspection and/or classification of deficiencies (nonconformities) by the Applicant and/or manufacturer | ||
| Посада представника Заявника та/або виробника/Position of the Applicant’s and/or manufacturer’s representative | П.І.Б. / Full Name | Підпис/ Signature |
| Особи, що беруть участь у заході / Participants of the event: | ||
| П.І.Б. учасника зустрічіFull name of the meeting participant | Посада / Position | Підпис/Signature |
| Примітки/ Notes |
Стор. з
Додаток 13
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 4 розділу V)
ПЕРЕЛІК ЛІКАРСЬКИХ ЗАСОБІВ, ЗАРЕЄСТРОВАНИХ АБО ЗАПЛАНОВАНИХ ДО РЕЄСТРАЦІЇ В УКРАЇНІ–1
LIST OF PRODUCTS, AUTHORISED OR PLANNED TO BE AUTHORISED IN UKRAINE
| Додаток до Висновку / до Сертифіката | від |
| Annex to Conclusion / to Certificate | from |
| виробник | |
| manufacturer |
до Висновку / до Сертифіката _____________ строком дії до
to Conclusion / to Certificate _____________ valid till
| №з/п | Назва лікарського засобу | Реєстраційне посвідчення (торгова ліцензія) № ___
(в Україні) |
||
| назва та лікарська форма лікарського засобу (українською мовою) | назва та лікарська форма лікарського засобу (англійською мовою) | міжнародна непатентована назва діючої(их) речовини(ин), у тому числі їх перелік — для багатокомпонентних (комбінованих) (англійською мовою) | ||
__________________________ ________________ ___________________________
(посада) (підпис, дата) (прізвище, ім’я, по батькові)(П.І.Б.)
«___»___________ 20___ року М. П.
__________
1 Інформація в цьому додатку має бути викладена українською та англійською мовами із зазначенням відповідних стадій виробництва (нерозфасована продукція, первинне пакування, вторинне пакування, сертифікація серії або за повним циклом виробництва).
Додаток 14
до Порядку проведення
підтвердження відповідності умов виробництва
лікарських засобів вимогам належної
виробничої практики
(пункт 13 розділу ІV)
ПЛАН
коригувальних та запобіжних дій щодо усуненнявиявлених порушень
| №з/п | Порушення | Класифікація порушення (критичне, суттєве, несуттєве) | Коригувальні/запобіжні дії | Строк виконання | Відмітка про виконання | Примітки |
Дата складання «____» __________ 20___ року
Керівник виробника
__________________________ ________________ ____________________
(посада) (підпис, дата) (прізвище, ім’я, по батькові)(П.І.Б.)
М. П. (за наявності)
Керівник служби якості (уповноважена особа)
__________________________ ________________ ____________________
(посада) (підпис, дата) (прізвище, ім’я, по батькові)(П.І.Б.)
Додаток 15
до Порядку проведення
підтвердження відповідності
умов виробництва лікарських
засобів вимогам належної
виробничої практики
(пункт 3 розділу V)
Методологія проведення оцінки ризиків щодо розрахунку строку наступної інспекції виробництва лікарського засобу на відповідність вимогам GMP
Розрахунок строку проведення наступної інспекції є наслідком дати проведення останньої інспекції та процесу оцінювання інспекторами та Держлікслужбою ризику, згідно з цією процедурою, яка використовує інструмент управління ризиком для якості, для чого необхідно заповнити таблиці для кожної виробничої дільниці, що оцінюється, наведеної у таблиці 1. Ця таблиця складається з семи частин, від А до G.
У частині А — документується попередня інформація про виробничу дільницю, зокрема наводяться назва та адреса виробничої дільниці, дозволи, що надані виробничій дільниці, тощо.
У частині В — наводиться внутрішній ризик, пов’язаний з виробничою дільницею, який початково властивий для цієї виробничої дільниці. Існують два фактори, які потрібно враховувати під час оцінювання внутрішнього ризику: складність виробничої дільниці, технологічні процеси та лікарські засоби, що виробляються на виробничій дільниці, а також їх критичність та/або критичність послуг, що надаються виробничою дільницею, наприклад, послуги лабораторії за контрактом.
Таблиця 2 містить рекомендації щодо оцінки складності та критичності виробничої дільниці, наведених у частині В таблиці 1.
Оцінка 1, 2 чи 3 присвоюється показнику складності, й це документується в частині В таблиці 1 (складність 3 рівня становить найвищу складність; складність 1 рівня становить найнижчу складність).
Оцінка 1, 2 чи 3 присвоюється показнику критичності, й це документується в таблиці 1 у частині В (складність 3 рівня становить найвищу критичність; складність 1 рівня становить найнижчу критичність).
Таблиця у вигляді матриці, наведена в таблиці 1, надається для поєднання цих двох оцінок для отримання розрахункового значення внутрішнього ризику виробничої дільниці шляхом множення цифр на перетинанні відповідних стовпчиків і строк, пов’язаного з виробничою дільницею, й це також документується в частині В (складність та критичність), та як здійснювати оцінювання кожного.
Таблиця 1.1 розрахунок внутрішнього ризику виробничої дільниці
| Критичність | |||
| Складність | 1 | 2 | 3 |
| 1 | 1 (Низька) | 2 (Низька) | 3 (Середня) |
| 2 | 2 (Низька) | 4 (Середня) | 6 (Висока) |
| 3 | 3 (Середня) | 6 (Висока) | 9 (Висока) |
Кількість присвоєних балів дає остаточний результат для внутрішнього ризику.
Матриця внутрішніх ризиків:
Загальне значення 1 чи 2 становить низький внутрішній ризик;
загальна значення 3 чи 4 становить середній внутрішній ризик;
загальна значення 6 чи 9 становить високий внутрішній ризик.
У частині С — оцінюється ризик, пов’язаний із порушення вимог належної виробничої практики. Оцінювання базується виключно на невідповідностях (порушеннях), які виявлені протягом останньої інспекції виробничої дільниці. Якщо остання інспекція не була плановою (регулярною) або повною, враховуються порушення, які виявлені протягом останньої планової (регулярної) або повної інспекції, а у разі відсутності таких перевірок враховуються порушення, які виявлені під час останньої нерегулярної інспекції.
Пов’язаний з невиконанням вимог ризик оцінюється як високий, середній та низький, у залежності від кількості й типу невідповідностей (порушень), та документується в таблиці 1 у частині С. Наступна таблиця наводиться в якості керівництва при оцінюванні ризику, пов’язаного виявленими порушеннями протягом інспектування.
Таблиця 1.2 Таблиця ризиків порушення вимог
| Виявлені порушення протягом інспектування |
Оцінка ризику, пов’язаного з відповідністю вимогам
|
| 1 чи більше критичних порушень чи більше 5 суттєвих порушень | Високий |
| Від 1 до 5 суттєвих порушень | Середній |
| Відсутні суттєві чи критичні порушень | Низький |
Виробничі дільниці з високим ризиком можуть потребувати повторного інспектування дуже скоро після проведення інспекції, якщо виявлено низький рівень відповідності вимогам. Таким виробничим дільницям також може бути надане розпорядження про зупинення обігу лікарських засобів, зупинена дія ліцензії з виробництва лікарських засобів до тих пір, поки не буде підтверджено відповідний рівень вимогам протягом наступної інспекції.
У зв’язку з цим необхідно зазначити наступне: такі подальші інспекції за визначенням є нерегулярними й відносяться до інспекцій «за наявності обґрунтованих підстав» чи «екстреними» (позаплановими) інспекціями, й вони можуть відбуватись у випадку виявлення критичного чи багатьох суттєвих порушень, наприклад, 6 чи більше суттєвих порушень.
Цей інструмент оцінки ризиків не застосовується до планування наступної інспекції як інспекції «за наявності обґрунтованих підстав» чи «екстреної», тобто до планування інспекцій по усуненню порушень (або позапланової перевірки по усуненню порушень).
Використання цього інструменту поновлюється після завершення інспекції по усуненню порушень (або позапланової перевірки по усуненню порушень) для розрахунку чергової планової (регулярної) або повної інспекції, при цьому оцінка ризику, пов’язаного з відповідністю вимогам, повинна враховувати невідповідності (порушення), які виявлені протягом первинної інспекції, так і під час наступної інспекції (інспекція по усуненню порушень або позапланова перевірка по усуненню порушень).
Частина D — «Рейтинг ризику, який присвоєно виробничій дільниці»
Матриця, яку зображено в таблиці 1.3, відображає розрахунок рейтингу ризику — це комбінація внутрішнього ризику та ризику, пов’язаного з відповідністю вимогам.
Таблиця 1.3 Матриця рейтингу ризику
| Внутрішній ризик | |||
|
Ризик, пов’язаний з відповідністю вимогам
|
Низький | Середній | Високий |
| Низький | Рейтинг ризику = А | Рейтинг ризику = А | Рейтинг ризику = В |
| Середній | Рейтинг ризику = А | Рейтинг ризику = В | Рейтинг ризику = С |
| Високий | Рейтинг ризику = В | Рейтинг ризику = С | Рейтинг ризику = С |
Існують три можливі рейтинги ризику: A, B та C («А» представляє виробничу дільницю з відносно низьким ризиком і «С» представляє виробничу дільницю з відносно високим ризиком).
Частина E — це періодичність інспектування, при цьому використовується рейтинг ризику з частини D для документування рекомендованої періодичності регулярних інспекцій на виробничій дільниці:
виробничі дільниці з рейтингом ризику «А» мають як мінімум одну оцінку низького ризику стосовно внутрішнього ризику чи ризику, пов’язаного з відповідністю вимог. Під час планування програм регулярних (повних) інспекцій такі виробничі дільниці можуть інспектуватися зі зниженою періодичністю, наприклад, не менше, ніж раз на два роки (наприклад, одна інспекція кожні 2- 3 роки);
виробничі дільниці з рейтингом ризику «В» під час планування програм регулярних (повних) інспекцій можуть інспектуватись із середньою періодичністю, наприклад, у проміжок між 12 та 24 місяцями;
виробничі дільниці з рейтингом ризику «С» мають як мінімум одну оцінку високого ризику стосовно внутрішнього ризику чи ризику, пов’язаного з відповідністю вимог. Під час планування програм регулярних (повних) інспекцій такі виробничі дільниці можуть інспектуватись із підвищеною періодичністю, наприклад, як мінімум щорічно чи навіть частіше.
У нижченаведеній таблиці 1.4 зображений спосіб призначення періодичності інспектування на основі рейтингу ризику.
Таблиця 1.4 Рекомендована періодичність інспекцій для кожного рейтингу ризику
| Рейтинг ризику | Рекомендована періодичність інспектування |
| А | Знижена періодичність, від 2 до 3 років |
| В | Середня періодичність, від 1 до 2 років |
| С | Підвищена періодичність, < 1 року |
Примітка 1: Вищенаведена матриця рейтингу ризику призначена для того, щоб жодній виробничій дільниці зі ступенем високого внутрішнього ризику чи високого ризику, пов’язаного з відповідністю вимог не було призначено знижену періодичність інспектування. Це пов’язано з тим, що вважається доцільним проводити політику інспектування всіх виробничих дільниць зі ступенем високого внутрішнього ризику чи високого ризику, пов’язаного з відповідністю вимог як мінімум кожні два роки під час здійснення програм регулярного (повного) інспектування. Однак, коли виробничій дільниці присвоєно ступінь високого ризику порушення вимог, на виробничій дільниці може вимагатись проведення нерегулярної інспекції (позапланової, екстреної) за наявності обґрунтованих підстав, і це може мати можливий вплив на застосування цього інструмента.
Примітка 2: Необхідно зазначити, що періодичність інспектування, зображена у вищенаведеній таблиці 1.4, представлена у вираженні інтервалів часового діапазону, а не абсолютних часових інтервалів. Наприклад:
для виробничих дільниць із присвоєним рейтингом ризику «В» часовий діапазон періодичності інспектування встановлюється на 1-2 роки; це не абсолютні 2 роки;
фактична періодичність інспектування, що призначена виробничій дільниці в межах будь-якого рейтингу ризику (A, B чи C), повинна відображати кількість та тип порушень, що були виявлені протягом останньої інспекції, зокрема, якщо двом виробничим дільницям присвоєно категорію ризику B, однак, якщо на одній виробничій дільниці результат останньої інспекції гірший за іншу виробничу дільницю (наприклад, п’ять суттєвих порушень у порівнянні з одним суттєвим порушенням) точна періодичність інспектування, призначена першій виробничій дільниці, повинна бути у більш обмежувальному кінці часового діапазону (тобто періодичність інспекції ближче до одного року ніж до двох років);
періодичність інспектування, призначена виробничим дільницям з однаковими рейтингами ризику може враховувати окремі оцінки внутрішнього ризику та ризику порушення вимог. Зокрема, коли виробнича дільниця має високий внутрішній ризик і високий ризик, пов’язаний з відповідністю вимог, що призведе до отримання рейтингу ризику «С», призначена періодичність інспектування (наприклад, 9 місяців) може бути вищою за періодичність виробничої дільниці з високим внутрішнім ризиком, але середнім ризиком, пов’язаним з відповідністю вимог, що також призводить до отримання рейтингу ризику «С».
Примітка 3: У разі, коли інспектор(и), який(і) востаннє інспектував(ли) виробничу дільницю, може(уть) не погодитись із періодичністю інспектування, що призначається виробничій дільниці із застосуванням цієї методології.
Якщо таке трапляється, і інспектор(и) вважають, що виробничій дільниці слід призначити іншу періодичність інспектування, причини цього повинні бути офіційно задокументовані. Фактори, що можуть тут бути корисними для розгляду:
надійність системи управління якістю, в тому числі її підхід до управління ризиком для якості;
загальна історія відповідності виробничої дільниці вимогам GMP з урахуванням повторюваних випадків невідповідності (порушень) вимогам і неповне усунення невідповідностей (порушень), які виявляються під час інспектування;
недостатність та неефективність вжитих заходів для усунення невідповідностей (порушень) GMP тощо.
Водночас, оскільки оцінка ризику з використанням цього інструменту може бути суб’єктивною та невизначеною, інспектор або Держлікслужба може запропонувати свій власний підхід при виникненні подібних ситуацій, методології і такі підходи можуть відрізнятись від представлених вище, та має право змінювати рекомендовану періодичність перевірки.
Частина F — зазначається рекомендований обсяг наступної інспекції
Ця частина повинна бути заповнена негайно після проведення інспекції і одночасно з попередніми частинами таблиці. В частині F необхідно заповнити чотири наступні розділи:
рекомендований фокус та глибина наступної регулярної або повної інспекції;
необхідна тривалість наступної регулярної або повної інспекції виробничої дільниці;
необхідна кількість інспекторів, що мають бути призначені на наступну регулярну або повну інспекцію виробничої дільниці;
чи вимагатиметься будь-яка спеціальна компетенція чи знання в інспекційний групі при проведенні наступної регулярної інспекції виробничої дільниці.
Після заповнення частин E та F у таблиці 1 будуть задокументовані рекомендована періодичність та обсяг наступної регулярної або повної інспекції. Персонал, який займається плануванням інспекції, може в подальшому використовувати цю інформацію при плануванні програми регулярних або повних інспекцій для виробничих дільниць.
В частині G — зазначається хто і коли провів оцінку ризику (документуються імена осіб, які його здійснили, фіксується підпис та дата).
Результати оцінки з управління ризиком та рейтинг ризиків можуть бути змінені Держлікслужбою при отриманні нової інформації, яка може змінити рейтинг ризику та призвести до зміни об’єму та періодичності наступної інспекції. Такою новою інформацією може бути інформація про дефекти якості, інформація про відклики лікарських засобів з обігу, результати досліджень при відкликах, інформація розслідувань, змін виробничої дільниці, тощо;
зміни до реєстраційного посвідчення чи ліцензії на виробництво можуть означати, що діяльність виробничої дільниці підлягає розширенню або суттєво змінена, що може значно вплинути на складність або критичність, які пов’язані з дільницею, і такі зміни розглядаються як нова інформація . Наприклад, зміна до реєстраційного посвідчення/ліцензії на виробництво для переходу зі скляних до пластикових ампул як первинного пакувального компоненту для продукту може вимагати впровадження технології продувки/наповнення/запаювання на виробничій дільниці;
суттєві зміни в кількості персоналу можуть вказувати на зміни складності виробничої дільниці, що може вплинути на внутрішній ризик або, можливо, вказувати на скрочення доступності ресурсів для забезпечення якості, що може у подальшому призвести до проблем з відповідністю вимогам;
звіт фармацевтичного підприємства по результатам після останнього інспектування також може розглядатися як нова інформація. Інспектор, який його розглядає, може вирішити, що деякі аспекти повинні бути ретельно перевірені під час наступного інспектування, що може вплинути на об’єм наступного регулярного або повного інспектування.
Вищевказані типи нової інформації можуть вплинути не тільки на зміну рекомендованого об’єму наступної регулярної або повної інспекції, а також вимагати зміни рекомендованої періодичності наступної регулярної або повної інспекції.
Рекомендується проводити офіційний періодичний перегляд таких оцінювань ризику:
Лист контролю редакцій
| Дата | № версії | Причини редакції |
Таблиця 1: Відомість, що застосовується з інструментом управління ризиком для якості та при розрахунку періодичності підтвердження терміну дії сертифікату належної виробничої практики
| ЧАСТИНА A — Інформація про виробничу дільницю | |||||||||||||
| Назва виробничої дільниці | |||||||||||||
| Адреса виробничої дільниці | |||||||||||||
| Номер ліцензії | |||||||||||||
| Виробник готового лікарського засобу, продукції in-bulk, АФІ | |||||||||||||
| Дата останньої інспектування | |||||||||||||
| ПІБ головного інспектора групи, який проводив інспектування | |||||||||||||
| ЧАСТИНА B — Внутрішній ризик, пов’язаний з відповідністю вимог | |||||||||||||
| Фактор ризику | Оцінка ризику | Матриця для розрахунку внутрішнього ризику | |||||||||||
| Критичність | |||||||||||||
| Складність виробничої дільниці, виробничих процесів та продукції розглядається як: |
1 2 3 Потрібне обвести |
Складність | 1 | 2 | 3 | ||||||||
| Критичність продукції, що виробляється виробничою дільницею, або критичність методів досліджень, або послуг, що надаються, розглядаються як: |
1 2 3 Потрібне обвести |
||||||||||||
| 1 |
1 (Низька) |
2 (Низька) |
3 (Середня.) | ||||||||||
| 2 |
2 (Низька) |
4 (Середня) |
6 (Висока) |
||||||||||
| 3 |
3 (Середня) |
6 (Висока) |
9 (Висока) |
||||||||||
|
Використовуйте вищенаведену матрицю та вкажіть внутрішній ризик, пов’язаний з виробничою дільницею, нижче: Низький □ Середній □ Високий □ |
|||||||||||||
| ЧАСТИНА C — Ризик, пов’язаний з відповідністю вимогам, на підставі останньої регулярної або повної інспекції | |||||||||||||
| Ризик визначається по профілю невідповідностей (порушень), які виявлені під час останнього інспектування: |
Низький □ Середній □ Високий □
|
– Відсутні суттєві чи критичні порушення – Від 1 до 5 суттєвих порушень – 1 чи більше критичних порушень чи більше 5 суттєвих порушень (Примітка. Застосовується за необхідності) |
|||||||||||
| ЧАСТИНА D — Рейтинг ризику виробничій дільниці | |||||||||||||
| Заповніть матрицю нижче шляхом поєднання оцінки внутрішнього ризику та ризику, пов’язаного з відповідністю вимогам, для визначення рейтингу ризику виробничої дільниці. | |||||||||||||
| Внутрішній ризик | |||||||||||||
| Ризик, пов’язаний з відповідністю вимог | Низький | Середній | Високий | ||||||||||
| Низький | Рейтинг ризику = A | Рейтинг ризику = A | Рейтинг ризику = B | ||||||||||
| Середній | Рейтинг ризику = A | Рейтинг ризику = B | Рейтинг ризику = C | ||||||||||
| Високий | Рейтинг ризику = B | Рейтинг ризику = C | Рейтинг ризику = C | ||||||||||
| Рейтинг ризику виробничої дільниці: A □ B □ C □ | |||||||||||||
| ЧАСТИНА E — Рекомендована періодичність регулярної або повної інспекції виробничої дільниці | |||||||||||||
| A | Знижена періодичність, від 2 до 3 років |
Із використанням рейтингу ризику 1) розрахункова дата наступного інспектування: ………………………… 2) відкладення повторного інспектування на: макс.………………………………..…….(місяці/роки) 3) дата наступного інспектування з боку Держлікслужби …………………………………… |
|||||||||||
| B | Середня періодичність, від 1 до 2 років | ||||||||||||
| C |
Підвищена періодичність, < 1 року |
||||||||||||
| ЧАСТИНА F — Рекомендований обсяг наступної регулярної інспекції | |||||||||||||
| Примітка: у випадку, коли до початку чергового інспектування отримана нова інформація про виробничу дільницю, яка вимагає зміни рейтингу ризику та обсягу такої інспекції, слід оновити частину F. Зокрема, інформація може бути про дефекти якості, відкликання, результати досліджень, розслідувань, що пов’язані з якістю, а також інші зміни такі як: внесення змін до реєстраційного посвідчення, інформація про суттєві зміни на виробничій дільниці (на що можливо вказує заява на внесення зміни до реєстраційного посвідчення чи ліцензії на виробництво) тощо. | |||||||||||||
| Справа задокументується рекомендовану область та глибину наступної регулярної або повної інспекції.
Примітка: Слід взяти до уваги наступне: сфери, в яких були виявлені порушення протягом останньої інспекції на виробничій дільниці, зокрема суттєві та критичні порушення; сфери, що не проходили інспектування (або не проходили детального інспектування) протягом останньої інспекції на виробничій дільниці; сфери, для інспектування яких не вистачило достатньо ресурсів; заплановані зміни на виробничій дільниці, що можуть вплинути на складність або критичність, та вплинути на рейтинг ризику виробничої дільниці; будь-яка інша сфера, яку вважає за потрібним перевірити інспектор протягом наступної інспекції. |
|||||||||||||
| Справа задокументується необхідна тривалість наступної регулярної або повної інспекції (кількість днів): | |||||||||||||
| Справа задокументується необхідна кількість інспекторів, що повинні бути призначені на наступну регулярну або повну інспекцію: | |||||||||||||
| Справа задокументується необхідність в конкретній компетенції чи експертних знань, які знадобляться інспекційній групі під час наступної регулярної або повної інспекції | |||||||||||||
| ЧАСТИНА G — Підписи та дати | |||||||||||||
|
Особи, які здійснили оцінку ризику: ПІБ, підпис, дата: ________________________ ПІБ, підпис, дата: ________________________ ПІБ, підпис, дата: ________________________ ПІБ, підпис, дата: ________________________ |
|||||||||||||
Керівництво методів оцінювання факторів внутрішнього ризику
| № | Фактор внутрішнього ризику і механізм його оцінювання | |
| 1 |
Складність. Це стосується складності виробничої дільниці, її процесів та продукції Примітка: досьє виробничої дільниці (за наявності) і звіт з останньої інспекції GMP можуть бути корисними джерелами інформації, на підставі якої присвоюється оцінка складності. Існують три можливі оцінки: 1, 2 і 3. Відомо, що виробничі дільниці з оцінкою фактора низького ризику в цій сфері мають низький рівень складності планування виробничої дільниці, її продукції та процесів. При оцінюванні фактору ризику необхідно врахувати наступне: Загальними, але вживаними показниками складності виробничої дільниці є: розмір виробничої дільниці — великі виробничі дільниці оцінюються як більш складні ніж менші за розмірами дільниці; кількість різних виробничих чи дистрибуційних процесів, що застосовуються на виробничій дільниці — більші кількості, як правило, обумовлюють більшу складність; рівень спеціалізації обладнання та приміщень (наприклад, установки з підготовки повітря), наявний на виробничій дільниці — виробничі дільниці з низьким рівнем спеціалізації вважаються складнішими за інші дільниці; кількість персоналу на виробничій дільниці — більші кількості, як правило, обумовлюють більшу складність; кількість комерційних ринків/країн, до яких виробнича дільниця здійснює постачання — більші кількості, як правило, обумовлюють більшу складність; кількість клієнтів, яких обслуговує виробнича дільниця — більші кількості, як правило, обумовлюють більшу складність; якщо виробнича дільниця є контрактним виробником чи контрактною лабораторією, вона вважається відносно складною. Загальними, але вживаними показниками складності процесів є: стерильні та асептичні виробничі процеси завжди вважаються процесами високої складності; операції з випуску за параметрами — як правило, вважаються процесами високої складності; кількість критичних етапів, що повинні бути під контролем в межах процесу — як правило, процеси з великою кількістю критичних етапів можуть вважатись складнішими процесами; тип продукції, що виробляється — деякі типи продукції, наприклад, лікарські форми низької концентрації/сильнодіючі лікарські форми й лікарські форми з уповільненим вивільненням можуть бути складнішими з огляду виробництва, ніж інші типи продукції (як, наприклад, таблетки зі швидким вивільненням), і складність їх виробничого процесу повинна оцінюватись вище в такому випадку; кількість типових операцій у нестерильному виробничому процесі — більші кількості, як правило, обумовлюють більшу складність. операції з перепакування — перепакування вже запакованої серії може вважатись процесом від середньої до високої складності; ступінь обробки чи переробки, що відбувається на виробничій дільниці: такі операції можуть додати складності процесу; біологічні процеси; застосування договорів з субпідрядниками, використання контрактних виробників, виробничі дільниці, склади або лабораторії, що розташовані за межами основної виробничої дільниці, в тому числі контактні, як правило, обумовлюють складність; у випадку імпорту — складність процесу імпорту, випуску серій продукції і процесів дистрибуції продукції, інколи існуючі домовленості з імпорту можуть бути доволі складними. Загальними, але вживаними показниками складності продукції є: кількість компонентів, що складають будь-яку одну пачку продукту — більші кількості одиниць в пачці, як правило, обумовлюють більшу складність продукту. Наприклад, пачка ін’єкційного продукту може мати 4 одиниці в своєму складі (флакон з ліофілізатом, флакон з розчинником, голка-перехідник і технічний листок-вкладиш, в той час, як пачка таблетованого продукту може містити блістер і листок-вкладиш з інформацією для пацієнтів всередині); продукти, що вимагають спеціальних умов зберігання та дистрибуції (наприклад, управління продуктами холодового ланцюга і швидкопсувними продуктами, як радіофармацевтичні препарати, може бути складним). У випадках, коли немає достатньо інформації чи знань про складність, що пов’язана з виробничою дільницею, її процесами та продукцією, слід присвоїти середню оцінку 2.
|
|
| 2 |
Критичність: Це стосується того, наскільки критичною є продукція, що виробляється виробничою дільницею, з точки зору організації постачань чи наскільки критичними є послуги, що надаються дільницею. Прикладом критичної послуги, що надається дільницею, може бути послуга контрактної лабораторії. Примітка: досьє виробничої дільниці (за наявності) і звіт з останньої інспекції можуть бути корисними джерелами інформації, на підставі якої присвоюється оцінка складності. Існують три можливі оцінки: 1, 2 і 3. Керівництво з оцінювання: Високу оцінку (3) присвоюють виробничим дільницям, що виробляють основні продукти чи надають основну послугу, що не є загальнодоступною в будь-яких інших місцях: це можуть бути виробничі дільниці, що є основним чи єдиним постачальником основного продукту (наприклад, важлива вакцина, критичний препарат крові, тощо). Примітка: вважається, що виконання ролі основного чи єдиного постачальника основного продукту не представляє будь-якого ризику для якості продукту, скоріше це представляє ризик для доступності продукту; методи досліджень (і пов’язане обладнання), що використовуються цими виробничими дільницями, не можуть бути з легкістю чи швидко виконані чи використані іншими лабораторіями; це можуть бути виробничі дільниці, що надають послуги контрактного виробництва чи дослідження ряду інших виробників, і збій у наданні таких послуг мав би значний вплив на доступність продукту. Низьку оцінку (1) присвоюють виробничим дільницям, що, як відомо, виробляють лише неосновні продукти чи відомі як дільниці, що не надають основних послуг: це можуть бути виробничі дільниці, що не є єдиним постачальником будь-яких важливих продуктів (наприклад, важлива вакцина, критичний препарат крові, тощо); методи досліджень (і пов’язане обладнання), що використовуються цими виробничими дільницями, не належать до таких, що не можуть з легкістю виконуватись чи використовуватись іншими лабораторіями; це не виробничі дільниці, що надають послуги контрактного виробництва чи досліджень ряду інших виробників, де збій у наданні таких послуг мав би значний вплив на доступність продукту. Середню оцінку (2) присвоюють виробничим дільницям, що знаходяться між цими вищенаведеними типами виробничих дільниць. У випадках, коли немає достатньо інформації чи знань про критичність, що пов’язана з виробничою дільницею, її процесами та продукцією, слід присвоїти середню оцінку 2. |
|
Керівництво про відкладення наступного інспектування
Кроки процедури:
1. Зазначте ризик порушення вимог, отриманого внаслідок останньої інспекції Держлікслужби (згідно з частиною C таблиці 1);
2. Зазначте внутрішній ризик виробничої дільниці (згідно з частиною B таблиці 1) та рейтинг ризику;
3. Зазначте рейтинг ризику виробничої дільниці (згідно з частиною D таблиці 1);
4. Відкладіть інспектування з боку Держлікслужби відповідно до таблиці нижче і задокументуйте це в частині E протоколу таблиці 1.
| Об’єкт оцінки | Крок 1 | Крок 2 | Крок 3 | Крок 4 |
| Ризик порушення вимог після останньої інспекції | Внутрішній ризик | Рейтинг ризику |
Відкладення інспектування (+ макс. років)
|
|
|
Виробнича дільниця (зазначити) |
Низький | Високий | В |
+1
|
| Низький /середній | Середній | А/В |
+1,5/+1+1,5
|
|
| Низький/середній | Низький | А |
+2/+1,5
|
Додаток 1до Порядку проведення сертифікаціївиробництва лікарських засобів27.12.2012 р. № 1130
Державна служба України з лікарських засобів
ЗАЯВАна видачу сертифіката відповідності вимогам належної виробничої практики
Дата надходження:
«_______» ______________ 20______ року Зареєстровано за № ___________
ЗАЯВНИК (найменування ліцензіата або власника реєстраційного посвідчення (торговельної ліцензії) на лікарський засіб)
Місцезнаходження
П. І. Б., посада керівника заявника
Контактні телефони, факс
ВИРОБНИК (найменування підприємства, найменування виробничої/их/дільниці/ь/), заявленої/их/ для сертифікації
Адреса місця провадження діяльності
П. І. Б., посада керівника підприємства, тел./факс
П. І. Б., посада керівника підрозділу з виробництва, тел./факс
П. І. Б., посада керівника служби якості (уповноваженої особи), тел./факс
П. І. Б., посада керівника відділу контролю якості, тел./факс
Інші контактні адреси (у тому числі e-mail)
Згідно з пунктом 3.2 розділу ІІІ цього Порядку додаються такі документи:
Достовірність наданої інформації гарантую: (П. І. Б., посада і підпис керівника (представника) заявника)
Дата складання «_____»___________ 20____ року М.П.
Додаток 2до Порядку проведення сертифікаціївиробництва лікарських засобів
Державна служба України з лікарських засобів
ЗАЯВАна видачу висновку щодо підтвердження відповідності вимогам належної виробничої практики
Дата надходження:
«_______» ______________ 20______ року Зареєстровано за № ___________ЗАЯВНИК (найменування ліцензіата або власника реєстраційного посвідчення (торговельної ліцензії) на лікарський засіб)
Місцезнаходження
П. І. Б., посада керівника заявника
Контактні телефони, факс
ВИРОБНИК (найменування підприємства, найменування виробничої/их/дільниці/ь/), заявленої/их/ для сертифікації
Адреса місця провадження діяльності
П. І. Б., посада керівника підприємства, тел./факс
П. І. Б., посада керівника підрозділу з виробництва, тел./факс
П. І. Б., посада керівника служби якості (уповноваженої особи), тел./факс
П. І. Б., посада керівника відділу контролю якості, тел./факс
Інші контактні адреси (у тому числі e-mail)
Згідно з пунктом 3.2 розділу ІІІ цього Порядку додаються такі документи:
Достовірність наданої інформації гарантую: (П. І. Б., посада і підпис керівника (представника) заявника)
Дата складання «_____»___________ 20____ року М.П.
Додаток 3до Порядку проведення сертифікації
виробництва лікарських засобів
ДОВІДКАпро якість продукції, що виробляється
на ____________________________________________________________
(найменування виробничої дільниці, що вказана в заяві)
______________________________________________________________
(найменування заявника)
за 20___ і 20___ роки
(навести дані за останні три роки, рахуючи від дати подання заяви)
| № з/п | Відомості про претензії і відкликання продукції | Усього | Перелік найменувань і номерів серій лікарських засобів |
|---|---|---|---|
| 1 | Кількість обґрунтованих претензій до якості продукції: | ||
| 1.1 | за результатами державного контролю | ||
| 1.2 | за зверненнями споживачів | ||
| 2 | Кількість відкликань продукції з мережі реалізації в Україні: | ||
| 2.1 | за приписами державних органів контролю | ||
| 2.2 | за рішенням підприємства заявника | ||
| 3 | Кількість відкликаної продукції з мережі реалізації країни, де розташоване виробництво (для нерезидентів): | ||
| 3.1 | за приписами державних органів країни, де розташоване виробництво | ||
| 3.2 | за рішенням підприємства заявника | ||
| 4 | Кількість відкликаної продукції з мережі реалізації в інших країнах: | ||
| 4.1 | за приписами відповідних державних органів країн, де здійснювалася реалізація продукції | ||
| 4.2 | за рішенням підприємства заявника |
Дата складання «______» _______________ 20____ року
Керівник підприємства _________________ (посада) (підпис) (прізвище, ім’я, по батькові)
М.П.
Керівник служби якості _________________ ____________ (уповноважена особа) (посада) (підпис) (прізвище, ім’я, по батькові)
Додаток 4до Порядку проведення сертифікаціївиробництва лікарських засобів
ДОВІДКАпро результати перевірок, проведених органами державного контролю
на____________________________________________
(найменування виробничої дільниці та найменування заявника)
за 20___ і 20___ роки
(указати за останні три роки до дати подання заяви)
| № з/п | Найменування уповноваженого органу | Вид перевірки (інспектування) (планова, позапланова) | Період, дата(и) перевірки | Звіт/акт від _____(дата)№ ___ | Результат перевірки (навести посилання на документ та надати короткі висновки, наведені у звіті/акті) |
|---|---|---|---|---|---|
| 1 | Орган державного контролю лікарських засобів в Україні | ||||
| 2 | Державний або уповноважений орган у сфері контролю лікарських засобів країни, де розташоване виробництво (для нерезидентів) | ||||
| 3 | Уповноважені органи у сфері контролю лікарських засобів, які є членами PIC/S | ||||
| 4 | Уповноважені органи у сфері контролю лікарських засобів інших країн |
Дата складання «______» _______________ 20____ року
Керівник підприємства _________________ (посада) (підпис) (прізвище, ім’я, по батькові)
М.П.
Керівник служби якості _________________ ____________ (уповноважена особа) (посада) (підпис) (прізвище, ім’я, по батькові)
Додаток 5до Порядку проведення сертифікаціївиробництва лікарських засобів
ЗАГАЛЬНИЙ ПЕРЕЛІК НОМЕНКЛАТУРИ ПРОДУКЦІЇ1
_____________________________________
(найменування виробничої дільниці)
_____________________________________
(адреса виробничих потужностей (місця провадження діяльності))
_____________________________________
(країна виробника)
| Частина (А/В)1 | № з/п | Торговельна назва2 | Міжнародна непатентована назва (МНН)3 | Реєстраційне посвідчення в Україні | Реєстраційне посвідчення (торгова ліцензія) в країні, де здійснюється виробництво від «__»____ ____ № ___ | Інформація про виробників4 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Торговельна назва (укр.) | Торговельна назва (англ.) | Лікарська форма (укр.) | Лікарська форма (англ.) | номер | рік видачі | місяць видачі | день видачі | виробник нерозфасованого продукту | первинна упаковка | вторинна упаковка | дозвіл на випуск серій5 | ||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
Дата складання «______» _______________ 20____ року
Керівник підприємства _________________ ____________ (посада) (підпис) (прізвище, ім’я, по батькові)
М.П.
Керівник служби якості _________________ ____________ (уповноважена особа) (посада) (підпис) (прізвище, ім’я, по батькові)Керівник виробництва _________________ ____________ (посада) (підпис) (прізвище, ім’я, по батькові)
Додаток 6 (Форма 1)до Порядку проведення сертифікаціївиробництва лікарських засобів(Бланк заявника)
_____________ № _________(дата)
Державна служба України з лікарських засобів
ГАРАНТІЙНИЙ ЛИСТ
________________________
(заявник)
в особі___________________________
що діє на підставі________________________
зобов’язується повідомляти Держлікслужбу України про зміни, які стосуються виробничої дільниці, що пройшла підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (GMP) (у тому числі зміну ліцензії на виробництво лікарських засобів, зміну найменування виробника, його місцезнаходження (юридичної адреси) та/або адреси виробничих потужностей тощо), та відповідати на всі письмові запити Держлікслужби України.
Згоден з тим, що у разі ненадання повідомлення, дія документа, що підтверджує відповідність виробництва лікарських засобів вимогам GMP, буде припинена.
Місцезнаходження підприємства, установи, організації або місце проживання фізичної особи — підприємця:
Контактні дані керівника підприємства, установи, організації або фізичної особи — підприємця, або уповноваженої ними особи: (телефон, факс, електронна адреса)
До гарантійного листа додається:
копія документа, що підтверджує повноваження особи, яка підписала гарантійний лист.
Керівник /уповноважена особа: (підпис) (ініціали та прізвище)М.П.*
Додаток 6 (Форма 2)до Порядку проведення сертифікаціївиробництва лікарських засобів(Бланк заявника)_____________ № _________(дата)
Державна служба України з лікарських засобів
ГАРАНТІЙНИЙ ЛИСТпро завершення процедури підтвердженняабо надання звіту останньої перевірки,проведеної уповноваженим органом країни-члена PIC/S
в особі_________________
що діє на підставі________________
зобов’язується у шестимісячний строк після отримання Висновку на готовий лікарський засіб завершити процедуру підтвердження або надати до Держлікслужби України копію звіту останньої перевірки проміжної виробничої ділянки (включно з контрактними ділянками), проведеної уповноваженим органом країни-члена PIC/S (для нерезидентів, виробництво лікарських засобів яких розташоване поза межами території країни — члена ЄС і поза межами території країни, із якою ЄС укладено угоду про взаємне визнання результатів інспектування). Заявник погоджується, що у разі ненадання копії вказаного документу Держлікслужба України приймає рішення про анулювання виданого Висновку відповідно до пункту 7.4 Порядку.
Згоден з тим, що у разі ненадання повідомлення, дія документа, що підтверджує відповідність виробництва лікарських засобів вимогам GMP, буде припинена.
Місцезнаходження підприємства, установи, організації або місце проживання фізичної особи — підприємця:
Контактні дані керівника підприємства, установи, організації або фізичної особи — підприємця, або уповноваженої ними особи: (телефон, факс, електронна адреса)
До гарантійного листа додається:
копія документа, що підтверджує повноваження особи, яка підписала гарантійний лист.
Керівник/уповноважена особа: (підпис) (ініціали та прізвище)
М.П.*
*Для фізичних осіб — підприємців — за наявності.
Додаток 7до Порядку проведення сертифікаціївиробництва лікарських засобів
Державна служба України з лікарських засобів
ОПИС № ________документів, що додаються до заяви на видачу сертифіката відповідності вимогам належної виробничої практики(до заяви на видачу висновку щодо підтвердження відповідності вимогам належної виробничої практики)
від________________________
(найменування заявника)
Дата і номер реєстрації заяви «_____» __________ 20____ року № __________
| № з/п | Найменування документа | Кількість аркушів у документі | Відмітка про наявність документів (наявні, відсутні) | Примітки |
|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 |
Прийняв ______________________ документів _____________________ (цифрами і словами) (підпис відповідальної особи) (П.І.Б.)
«_______»__________________ 20____ року
Копію опису отримав ______________________________ (підпис представника заявника) (П.І.Б.)
«_______»__________________ 20____ року
Додаток 8до Порядку проведення сертифікаціївиробництва лікарських засобів
ЗВІТ ЗА РЕЗУЛЬТАТАМИ ІНСПЕКТУВАННЯ
І. ЗАГАЛЬНІ ПОЛОЖЕННЯ
Підприємство:_________________________________________________________________________________________________
найменування, місцезнаходження суб’єкта господарювання;
______________________________адреса(и) місця провадження діяльності;
______________________________найменування виробничої(их) дільниці(ць)
Види діяльності, які інспектувались: (зазначити потрібне знаком «Х»)
| Виробництво активних фармацевтичних інгредієнтів (субстанцій) | |
| Виробництво готових лікарських засобів (ГЛЗ): | |
| Виробництво проміжних продуктів, нерозфасованих продуктів (продукції in bulk) | |
| Упаковка (тільки) | |
| Лабораторний контроль якості лікарських засобів | |
| Посерійний контроль та дозвіл на реалізацію серій лікарських засобів | |
| Виробництво та аналіз за контрактом | |
| Зберігання та дистрибуція | |
| Виробництво досліджуваних лікарських засобів | |
| Інше _____________________________________________________________________ |
Дати проведення: (за місцями розташування виробничих дільниць)
Інспектори: (П.І.Б., посади, обов’язки інспекторів)
На виконання наказу від _____________ № ____________ (відповідальність щодо конфіденційності інформації)
Нормативна база:
Чинна версія GMP ЄС.
Настанова «Лікарські засоби. Належна виробнича практика», затверджена МОЗ України, яка гармонізована з чинною версією GMP ЄС.
Вступ
(навести коротку інформацію про підприємство, яке було проінспектовано, включаючи стислі відомості щодо найменування і адреси виробництва (виробничих дільниць), наявності системи забезпечення якості відповідно до чинників GMP (за розділами досьє виробничої дільниці), у тому числі щодо дозвільних документів, змін, що відбулися тощо)
Відомості про ліцензовану діяльність, сертифікати GMP
Зміни, що відбулися на виробництві з моменту попереднього інспектування (за наявності)
Інформація про хід інспектування
Мета інспектування (номер, дата і короткий зміст наказу Держлікслужби України)
Масштаб і об’єкти(Навести перелік об’єктів (процеси, служби та системи), які були проінспектовані згідно із затвердженою та узгодженою програмою, а також тих, що не були предметом інспекції.Навести назви лікарських форм, виробництво яких було проінспектовано (наприклад: стерильні лікарські засоби: (перелік форм), нестерильні лікарські засоби: (перелік форм).Навести інформацію щодо відхилень від програми (перестановки пунктів програми між днями та/або інтервалами часу тощо), якщо такі мали місце під час інспекції, та причини, що їх зумовили.)
Працівники підприємства, які брали участь в інспектуванні (навести перелік із зазначенням посад)
II. РЕЗУЛЬТАТИ ІНСПЕКТУВАННЯ
Загальний опис виробництва та спостереження під час інспектування
| Забезпечення якості/управління якістю | |
| Персонал | |
| Приміщення та обладнання | |
| Документація | |
| Технологічний процес | |
| Контроль якості | |
| Виробництво та аналіз за контрактом | |
| Рекламації та відкликання продукції | |
| Самоінспекції | |
| Реалізація та транспортування продукції | |
| Досьє виробничої дільниці (Site Master File, SMF) | Відповідність SMF вимогам, встановленим до його змісту та оформлення, загальна оцінка відповідності фактичного стану виробничих дільниць інформації, наведеній у відповідних частинах SMF та вимогам GMP. |
| Інші специфічні питання (за наявності) | |
| Відбір зразків під час інспекції (якщо такий проводився) | Інформація про відбір зразків, виконаний під час інспекції. |
| Результати виконання заходів щодо усунення порушень, виявлених під час попередньої інспекції (за наявності) |
Детальний перелік установлених фактів невідповідності вимогам GMP та їх класифікація*:
| Пункт настанови | Детальний опис виявленого порушення | Класифікація порушення (критичне, суттєве, несуттєве) |
|---|---|---|
| Кількість копій звіту та їх розповсюдження | |
|---|---|
| Додатки до звіту | План і програма інспекції тощо |
| Висновки | За результатами інспекції можна констатувати наявність невідповідностей вимогам GMP, які викладені і класифіковані в цьому звіті, всього: ______, з них:Критичних — ______Суттєвих — ________Несуттєвих — _______Наявний стан виробництва та наявність виявлених під час інспектування невідповідностей дають/не дають можливість надати оцінку підприємству як такому, що відповідає/не відповідає вимогам GMP. |
| Рекомендації інспекторів | Група інспекторів в строки, зазначені в цьому Порядку, має поінформувати Держлікслужбу України щодо встановлених невідповідностей, висновків за результатами інспекції та надати до Держлікслужби України цей звіт.Підприємству має бути вказано про необхідність інформування Держлікслужби України щодо запланованих коригувальних заходів, строків та результатів їх виконання. |
Інспектори:______________ _______________ ___________________
(посада) (підпис, дата) (П.І.Б.)
______________ _______________ ___________________
(посада) (підпис, дата) (П.І.Б.)
Додаток 9до Порядку проведення сертифікаціївиробництва лікарських засобів
Державний Герб України
УКРАЇНАUKRAINEСЕРТИФІКАТ ВІДПОВІДНОСТІ ВИМОГАМ НАЛЕЖНОЇ ВИРОБНИЧОЇ ПРАКТИКИ1 CERTIFICATE OF GMP COMPLIANCE1
Сертифікат №: // Certificate No: Строк дії до: // Valid till: дд мм рррр
| Частина 1 | Part 1 |
| Державна служба України з лікарських засобів(Держлікслужба України) засвідчує наступне: | State Administration of Ukraine on Medicinal Products(SAUMP) confirms the following: |
| Найменування виробника, місцезнаходження: | Manufacturer’s name, registered place of business: |
| Найменування виробничої(их) дільниці(ць): | Name(s) of manufacturing site(s): |
| Адреса місця провадження діяльності: | Manufacturing site address: |
| Ліцензія на виробництво лікарських засобів в Україні | Manufacturing authorization for medicinal products in Ukraine2 |
| від “___”____________ _____ № __________ | ___________ ______________ No. __________ |
| Місце виробництва систематично проходить інспектування зі встановленою періодичністю на відповідність вимогам GMP згідно зі встановленим порядком.3 | Facilities of above mentioned manufacturer are subject to GMP inspections at suitable intervals in accordance with the National certification procedure.3 |
| За результатами інспектування цього виробника, останнє з яких було проведене4… … / … … / … … [дата],встановлено, що система забезпечення якості, приміщення та обладнання з виробництва лікарських засобів, перелік яких наведено у частині 2 цього сертифіката та додатку до нього, відповідають вимогамНАЛЕЖНОЇ ВИРОБНИЧОЇ ПРАКТИКИ,прийнятим в Україні:_________________________________________________,(державний керівний документ)що відповідають вимогам належної практики при виробництві і контролі якості Системи співробітництва фармацевтичних інспекцій (PIC/S), директивам ЄC та рекомендаціям Всесвітньої організації охорони здоров’я у відношенні продукції, що призначена для торгівлі та дистрибуції в країні походження, або для експорту.Цей сертифікат відображає статус виробництва на момент проведеного інспектування, зазначеного вище, і є чинним до вказаної вище дати.Чинність цього сертифіката може бути підтверджена органом, що його видав. | From the knowledge gained during inspection of this manufacturer, the latest of which was conducted on… … / … … / … … [date],it is considered that quality assurance system, premises and equipment for medicinal products, listed in part 2 of this certificate and addition to it, complies with the requirements ofGOOD MANUFACTURING PRACTICElaid down in Ukrainian Guideline:_______________________________________________(name of regulation document)which is harmonized with the requirements of Good practices in the manufacture and quality control of the Pharmaceutical Inspection Convention/Co-operation Scheme (PIC/S), EU Directives , and World Health Organization recommendations in respect of products to be sold or distributed within the county of origin or to be exported.This certificate reflects the status of the manufacturing site at the time of the inspection noted above and valid till the date referred above.The authenticity of this certificate may be verified with the issuing authority. |
П.І.Б., підпис посадової особи Держлікслужби України** М.П.
Name and signature of the Executive officer of the SAUMP**…../……/…..…
Дата/date
| Державна служба України з лікарських засобівпідпис відповідальної особи, печаткаАдреса:Тел.:Факс:mailto:www.diklz.gov.ua | State Administration of Ukraine on Medicinal Products
signature of the Executive officer (see left)Address:Phone:Fax:This English translation is for reference only and is not part of the official certificate Номер сторінки / Загальна кількість сторінок |
1 COMMUNITY FORMAT FOR A GMP CERTIFICATE (EMEA/INS/GMP/313556/2006).
2 У сертифікатах для закордонних виробників навести найменування відповідної країни.
3 Цей пункт навести тільки в сертифікатах, що видаються резидентам.
4 У разі сертифікації закордонного виробництва вказати найменування державного органу відповідної країни.
| Частина 2 | Part 2 |
| Лікарські засоби для людини*Досліджувані лікарські засоби для людини*І, ІІ, ІІІ фази клінічних досліджень* | Human Medicinal Products*Human Investigational Medicinal Products*for phase I, II, III clinical trials* |
| 1.ВИРОБНИЧІ ОПЕРАЦІЇ* | 1. MANUFACTURING OPERATIONS* |
| ліцензовані виробничі операції включають повне та часткове виробництво (включаючи різні процеси розділення, пакування або маркування), випуск і сертифікацію серій, зберігання і дистрибуцію визначених лікарських форм, якщо не поінформовані про інше; | authorized manufacturing operations include total and partial manufacturing (including various processes of dividing up,packaging or presentation), batch release and certification, storage and distribution of specified dosage forms unless informed to the contrary; |
| проведення контролю якості та/або випуску і сертифікації серій без виробничих операцій слід вказати для відповідних пунктів; | quality control testing and/or release and batch certification activities without manufacturing operations should be specified under the relevant items; |
| якщо підприємство, задіяне у виробництві продукції з особливими властивостями, такої як радіофармацевтична або продукти, що містять пеніцилін, сульфаніламіди, цитотоксини, цефалоспорини, активні гормони або інші потенційно небезпечні активні інгредієнти, це має бути вказано для відповідного типу продукції та лікарської форми | if the company is engaged in manufacture of products with special requirements e.g. radiopharmaceuticals or products containing penicillin, sulphonamides, cytotoxics, cephalosporins, substances with hormonal activity or other or potentially hazardous active ingredients this should be stated under the relevant product type and dosage form. |
| 1.1 Стерильні продукти | 1.1 Sterile Products |
| 1.1.1 Асептично виготовлені (перелік лікарських форм) | 1.1.1 Aseptically prepared (list of dosage forms) |
| 1.1.1.1 Рідини в упаковках великого об’єму | 1.1.1.1 Large volume liquids |
| 1.1.1.2 Ліофілізати | 1.1.1.2 Lyophilisates |
| 1.1.1.3 М’які | 1.1.1.3 Semi-solids |
| 1.1.1.4 Рідини в упаковках малого об’єму | 1.1.1.4 Small volume liquids |
| 1.1.1.5 Тверді та імплантанти | 1.1.1.5 Solids and implants |
| 1.1.1.6 Інші (зазначити) | 1.1.1.6 Other aseptically prepared products |
| 1.1.2. Термічно стерилізовані (перелік лікарських форм) | 1.1.2. Terminally sterilised (list of dosage forms) |
| 1.1.2.1 Рідини в упаковках великого об’єму | 1.1.2.1 Large volume liquids |
| 1.1.2.2 М’які | 1.1.2.2 Semi-solids |
| 1.1.2.3 Рідини в упаковках малого об’єму | 1.1.2.3 Small volume liquids |
| 1.1.2.4 Тверді та імплантанти | 1.1.2.4 Solids and implants |
| 1.1.2.5 Інші (зазначити) | 1.1.2.5 Other terminally sterilised prepared products |
| 1.1.3 Тільки сертифікація серій | 1.1.3 Batch certification only |
| Державна служба України з лікарських засобів
підпис відповідальної особи, печатка Адреса: Тел.: Факс: mailto: www.diklz.gov.ua |
State Administration of Ukraine on Medicinal Products
signature of the Executive officer (see left)Address:Phone:Fax:This English translation is for reference only and is not part of the official certificate Номер сторінки / Загальна кількість сторінок |
| 1.2 Нестерильні продукти | 1.2 Non-sterile products |
| 1.2.1 Нестерильні продукти (перелік лікарських форм) | 1.2.1 Non-sterile products (list of dosage forms) |
| 1.2.1.1 Капсули, тверді желатинові | 1.2.1.1 Capsules, hard shell |
| 1.2.1.2 Капсули, м’які желатинові | 1.2.1.2 Capsules, soft shell |
| 1.2.1.3 Жувальна гума | 1.2.1.3 Chewing gums |
| 1.2.1.4 Імпрегновані матриці | 1.2.1.4 Impregnated matrices |
| 1.2.1.5 Рідини для зовнішнього застосування | 1.2.1.5 Liquids for external use |
| 1.2.1.6 Рідини для внутрішнього застосування | 1.2.1.6 Liquids for internal use |
| 1.2.1.7 Медичні гази | 1.2.1.7 Medicinal gases |
| 1.2.1.8 Інші тверді лікарські форми | 1.2.1.8 Other solid dosage forms |
| 1.2.1.9 Препарати під тиском | 1.2.1.9 Pressurised preparations |
| 1.2.1.10 Джерела радіонуклідів | 1.2.1.10 Radionuclide generators |
| 1.2.1.11 М’які | 1.2.1.11 Semi-solids |
| 1.2.1.12 Супозиторії | 1.2.1.12 Suppositories |
| 1.2.1.13 Таблетки | 1.2.1.13 Tablets |
| 1.2.1.14 Трансдермальні пластирі | 1.2.1.14 Transdermal patches |
| 1.2.1.15 Стоматологічні матеріали | 1.2.1.15 Intraruminal devices |
| 1.2.1.16 Ветеринарні премікси | 1.2.1.16 Veterinary premixes |
| 1.2.1.17 Інші нестерильні лікарські засоби (зазначити) | 1.2.1.17 Other non-sterile medicinal product |
| 1.2.2 Тільки сертифікація серій | 1.2.2 Batch certification only |
| 1.3 Біологічні лікарські засоби | 1.3 Biological medicinal products |
| 1.3.1 Біологічні лікарські засоби | 1.3.1 Biological medicinal products |
| 1.3.1.1 Препарати крові | 1.3.1.1 Blood products |
| 1.3.1.2 Імунобіологічні лікарські засоби | 1.3.1.2 Immunobiological products |
| 1.3.1.3 Клітиннотерапевтичні лікарські засоби | 1.3.1.3 Cell therapy products |
| 1.3.1.4 Геннотерапевтичні лікарські засоби | 1.3.1.4 Gene therapy products |
| 1.3.1.5 Біотехнологічні лікарські засоби | 1.3.1.5 Biotechnology products |
| 1.3.1.6 Екстраговані препарати з тканин людини або тварин | 1.3.1.6 Human or animal extracted products |
| 1.3.1.7 Інші біологічні медичні продукти | 1.3.1.7 Other biological medicinal products |
| 1.3.2 Тільки сертифікація серій (перелік) | 1.3.2 Batch certification only (list of product types) |
| 1.3.2.1 Препарати крові | 1.3.2.1 Blood products |
| 1.3.2.2 Імунобіологічні лікарські засоби | 1.3.2.2 Immunological products |
| 1.3.2.3 Клітиннотерапевтичні лікарські засоби | 1.3.2.3 Cell therapy products |
| 1.3.2.4 Геннотерапевтичні лікарські засоби | 1.3.2.4 Gene therapy products |
| 1.3.2.5 Біотехнологічні лікарські засоби | 1.3.2.5 Biotechnology products |
| 1.3.2.6 Екстраговані препарати з тканин людини або тварин | 1.3.2.6 Human or animal extracted products |
| 1.3.2.7 Інші біологічні лікарські засоби | 1.3.2.7 Other biological medicinal products |
|
Державна служба України з лікарських засобів підпис відповідальної особи, печатка Адреса: Тел.: Факс: mailto: www.diklz.gov.ua |
State Administration of Ukraine on Medicinal Products signature of the Executive officer (see left)Address:Phone:Fax:This English translation is for reference only and is not part of the official certificate Номер сторінки / Загальна кількість сторінок |
| 1.4 Інші продукти або виробнича діяльність(будь-які інші види виробничої діяльності/типи продуктів, що не вказані вище, наприклад, стерилізація активних субстанцій, виробництво біологічних активних вихідних речовин (якщо це вимагається національним законодавством), продукти з рослинної сировини або гомеопатичні препарати, виробництво нерозфасованих продуктів або виробництво за повним циклом тощо) |
1.4 Other products or manufacturing activity (any other relevant manufacturing activity/product type that is not covered above e.g. sterilisation of active substances, manufacture of biological active starting materials (when required by national legislation), herbal or homeopathic products, bulk or total manufacturing, etc). |
| 1.4.1 Виробництво: | 1.4.1 Manufacture of: |
| 1.4.1.1 Продукти з рослинної сировини | 1.4.1.1 Herbal products |
| 1.4.1.2 Гомеопатичні препарати | 1.4.1.2 Homoeopathic products |
| 1.4.1.3 Біологічні активні вихідні речовини | 1.4.1.3 Biological active starting materials |
| 1.4.1.4 Інші (зазначити) | 1.4.1.4 Other |
| 1.4.2 Стерилізація активних речовин/допоміжних речовин/готової продукції | 1.4.2 Sterilisation of active substances/excipients/ finished product: |
| 1.4.2.1 Фільтрація | 1.4.2.1 Filtration |
| 1.4.2.2 Сухожарова стерилізація | 1.4.2.2 Dry heat |
| 1.4.2.3 Стерилізація паром | 1.4.2.3 Moist heat |
| 1.4.2.4 Хімічна | 1.4.2.4 Chemical |
| 1.4.2.5 Гамма-випромінювання | 1.4.2.5 Gamma irradiation |
| 1.4.2.6 Електронне проміння | 1.4.2.6 Electron beam |
| 1.4.3 Інші (зазначити) | 1.4.3 Others |
| 1.5 Тільки пакування | 1.5 Packaging only |
| 1.5.1 Первинне пакування | 1.5.1 Primary packing |
| 1.5.1.1 Капсули, тверді желатинові | 1.5.1.1 Capsules, hard shell |
| 1.5.1.2 Капсули, м’які желатинові | 1.5.1.2 Capsules, soft shell |
| 1.5.1.3 Жувальна гума | 1.5.1.3 Chewing gums |
| 1.5.1.4 Імпрегновані матриці | 1.5.1.4 Impregnated matrices |
| 1.5.1.5 Рідини для зовнішнього застосування | 1.5.1.5 Liquids for external use |
| 1.5.1.6 Рідини для внутрішнього застосування | 1.5.1.6 Liquids for internal use |
| 1.5.1.7 Медичні гази | 1.5.1.7 Medicinal gases |
| 1.5.1.8 Інші тверді лікарські форми | 1.5.1.8 Other solid dosage forms |
| 1.5.1.9 Препарати під тиском | 1.5.1.9 Pressurised preparations |
| 1.5.1.10 Джерела радіонуклідів | 1.5.1.10 Radionuclide generators |
| 1.5.1.11 М’які | 1.5.1.11 Semi-solids |
| 1.5.1.12 Супозиторії | 1.5.1.12 Suppositories |
| 1.5.1.13 Tаблетки | 1.5.1.13 Tablets |
| 1.5.1.14 Трансдермальні пластирі | 1.5.1.14 Transdermal patches |
| 1.5.1.15 Стоматологічні матеріали | 1.5.1.15 Intraruminal devices |
| 1.5.1.16 Ветеринарні премікси | 1.5.1.16 Veterinary premixes |
| 1.5.1.17 Інші нестерильні лікарські засоби | 1.5.1.17 Other non-sterile medicinal products |
| 1.5.2 Вторинне пакування | 1.5.2 Secondary packing |
| 1.6 Випробування контролю якості | 1.6 Quality control testing |
| 1.6.1 Мікробіологічні: стерильність | 1.6.1 Microbiological: sterility |
| 1.6.2 Мікробіологічні: мікробіологічна чистота | 1.6.2 Microbiological: non-sterility |
| 1.6.3 Фізичні/хімічні | 1.6.3 Chemical/Physical |
| 1.6.4 Біологічні | 1.6.4 Biological |
| Державна служба України з лікарських засобів
підпис відповідальної особи, печатка Адреса: Тел.: Факс: mailto:www.diklz.gov.ua |
State Administration of Ukraine on Medicinal Products
signature of the Executive officer (see left)Address:Phone:Fax:This English translation is for reference only and is not part of the official certificateНомер сторінки / Загальна кількість сторінок |
| 2. ІМПОРТ ЛІКАРСЬКИХ ЗАСОБІВ* | 2. IMPORTATION OF MEDICINAL PRODUCTS* |
| Діяльність з імпорту без виробничих операцій | importation activities without manufacturing activity |
| Діяльність з імпорту включає зберігання і дистрибуцію, якщо не поінформовано про повернення інше | importation activities include storage and distribution unless informed to the contrary |
| 2.1 Випробування контролю якості імпортованих лікарських засобів | 2.1 Quality control testing of imported medicinal products |
| 2.1.1 Мікробіологічні: стерильність | 2.1.1 Microbiological: sterility |
| 2.1.2 Мікробіологічні: мікробіологічна чистота | 2.1.2 Microbiological: non-sterility |
| 2.1.3 Хімічні/фізичні | 2.1.3 Chemical/Physical |
| 2.1.4 Біологічні | 2.1.4 Biological |
| 2.2 Сертифікація серії імпортованих лікарських засобів | 2.2 Batch certification of imported medicinal products |
| 2.2.1 Стерильні продукти | 2.2.1 Sterile Products |
| 2.2.1.1 Асептично виготовлені | 2.2.1.1 Aseptically prepared |
| 2.2.1.2 Фінішна стерилізація | 2.2.1.2 Terminally sterilised |
| 2.2.2 Нестерильні продукти | 2.2.2 Non-sterile products |
| 2.2.3 Біологічні лікарські засоби | 2.2.3 Biological medicinal products |
| 2.2.3.1 Продукти крові | 2.2.3.1 Blood products |
| 2.2.3.2 Імунобіологічні препарати | 2.2.3.2 Immunological products |
| 2.2.3.3 Клітиннотерапевтичні препарати | 2.2.3.3 Cell therapy products |
| 2.2.3.4 Геннотерапевтичні продукти | 2.2.3.4 Gene therapy products |
| 2.2.3.5 Біотехнологічні продукти | 2.2.3.5 Biotechnology products |
| 2.2.3.6 Екстраговані з тканин людини чи тварин | 2.2.3.6 Human or animal extracted products |
| 2.2.3.7 Інші біологічні лікарські засоби | 2.2.3.7 Other biological medicinal products |
| 2.2.4 Інша діяльність з імпорту (інша важлива діяльність з імпорту, не приведена вище, наприклад, імпорт радіофармацевтичних, медичних газів, рослинних або гомеопатичних препаратів тощо) | 2.2.4 Other importation activities (any other relevant importation activity that is not covered above e.g. importation of radiopharmaceuticals, medicinal gases, herbal or homeopathic products, etc.) |
| 2.2.4.1 Радіофармацевтичні/джерела радіонуклідів | 2.2.4.1 Radiopharmaceuticals/Radionuclide generators |
| 2.2.4.2 Медичні гази | 2.2.4.2 Medicinal gases |
| 2.2.4.3 Продукти з рослинної сировини | 2.2.4.3 Herbal products |
| 2.2.4.4 Гомеопатичні | 2.2.4.4 Homoeopathic products |
| 2.2.4.5 Біологічні активні вихідні речовини | 2.2.4.5 Biological active starting materials |
| 2.2.4.6 Інші | 2.2.4.6 Other |
| ВИРОБНИЦТВО АКТИВНИХ РЕЧОВИН (за наявності)
Назви речовин, які були об’єктом інспекції: |
MANUFACTURE OF ACTIVE SUBSTANCES (if present)
Names of substances subject to inspection: |
| Будь-які обмеження або пояснення, що мають відношення до цього сертифіката* | Any restrictions or clarifying remarks related to the scope of this certificate*: |
П.І.Б., підпис посадової особи Держлікслужби України**
М.П.
Name and signature of the Executive officer of the State Administration of Ukraine on Medicinal Products **…../……/…..…
Дата/date
|
Державна служба України з лікарських засобів підпис відповідальної особи, печатка Адреса: Тел.: Факс: mailto:www.diklz.gov.ua |
State Administration of Ukraine on Medicinal Products
signature of the Executive officer (see left)Address:Phone:Fax:This English translation is for reference only and is not part of the official certificateНомер сторінки / Загальна кількість сторінок |
Додаток 10до Порядку проведення сертифікаціївиробництва лікарських засобів
Бланк Держлікслужби України
ВИСНОВОКЩОДО ПІДТВЕРДЖЕННЯ ВІДПОВІДНОСТІ ВИРОБНИЦТВА ЛІКАРСЬКИХ ЗАСОБІВ ВИМОГАМ НАЛЕЖНОЇ ВИРОБНИЧОЇ ПРАКТИКИ (GMP)
На підставі розгляду заяви від «__» ___ 20__ року № ___________ (назва заявника та/або виробника)документів, що додаються до неї та, враховуючи позитивні результати проведеної спеціалізованої експертизи (експертний висновок від «__» ___ 20__ року № ___________), сертифікат відповідності виробництва лікарських засобів вимогам GMP № ______________ від «__» ___ 20__ року, виданий,(назва уповноваженого органу країни-члена PIC/S) виробничій дільниці,(назва виробника/виробничої дільниці)адреса місця провадження діяльності: ____________________________________,
терміном дії — до «__» ___ 20__ року, вважається таким, що підтверджує відповідність виробництва лікарських засобів чинним в Україні вимогам GMP.Дія цього висновку розповсюджується на такі форми лікарських засобів, як:
Перелік лікарських засобів, що виробляються на дільниці, (назва та адреса виробника/виробничої дільниці) наведений в додатку до цього висновку і є його невід’ємною частиною.
_________________________________ ____________________________ (посада) (підпис) (прізвище, ім’я, по батькові)
«______» _______________ 20___ року М.П.
Додаток 11до Порядку проведення сертифікаціївиробництва лікарських засобів
ПЕРЕЛІК ЛІКАРСЬКИХ ЗАСОБІВ, ЗАРЕЄСТРОВАНИХАБО ЗАПЛАНОВАНИХ ДО РЕЄСТРАЦІЇ В УКРАЇНІ1
виробництва ________________________________________________________________________2 до сертифіката № ________________ строком дії до «_______» ____________ 20____ року
| № з/п | Найменування лікарського засобу | Реєстраційне посвідчення (торгова ліцензія) № ___ (в Україні) | ||
|---|---|---|---|---|
| торговельна назва (українською мовою) | торговельна назва (англійською мовою) | міжнародна непатентована назва діючої(их) речовини(ин), у тому числі їх перелік — для багатокомпонентних (комбінованих) — англійською мовою | ||
____________________________________ ___________________________
(посада) (підпис) (прізвище, ім’я, по батькові)
«______» _______________ 20___ року М.П.
Додаток 12до Порядку проведення сертифікаціївиробництва лікарських засобів
ПЛАН КОРИГУВАЛЬНИХ/ЗАПОБІЖНИХ ДІЙ
| № з/п | Суть невідповідності (порушення) | Класифікація порушення (критичне, суттєве, несуттєве) | Коригувальні/запобіжні дії | Термін виконання | Відмітка про виконання | Примітки |
|---|---|---|---|---|---|---|

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим