|
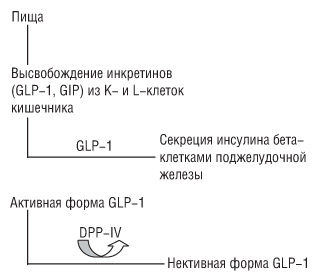
Открытию ингибиторов DPP-IV предшествовало наблюдение, что у пациентов с СД II-го типа снижен уровень эндогенного GLP-1, функция которого состоит в том, что, связываясь со своими рецепторами на бета-клетках поджелудочной железы, он стимулирует высвобождение инсулина. Период жизни активной формы GLP-1 короткий — 1–2 мин, после чего DPP-IV инактивирует его (рисунок). У больных СД II-го типа количество инкретинов (в том числе и GLP-1) — недостаточное для выполнения физиологической функции. Поэтому вводя в организм устойчивые к действию DPP-IV агонисты рецепторов GLP-1 или продлевая период жизни эндогенного GLP-1 (например ингибируя DPP-IV), можно добиться лечебного эффекта, то есть нормализовать секрецию инсулина.
|
Действие препаратов производных мочевины также основано на усилении секреции инсулина, но, в отличие от препаратов двух вышеуказанных групп, не зависит от концентрации глюкозы в крови. Именно поэтому их применение сопряжено с риском развития гипогликемии и увеличения массы тела. Напротив, применение ингибиторов DPP-IV (разработаны формы для перорального приема) не приводит к увеличению массы тела, а инъекционные аналоги GLP-1 могут способствовать даже небольшому уменьшению ее.
Есть мнения, что ингибиторы DPP- IV могут привести к частичному или полному вытеснению с рынка препаратов производных мочевины. Поскольку действие ингибиторов DPP- IV и агонистов GLP-1 — взаимодополняющее, в перспективе возможно применение этих препаратов в комбинации, для усиления терапевтического эффекта. Потенциальный риск применения ингибиторов DPP-IV может быть связан с ингибицией ими действия некоторых гормонов, нейропептидов, хемокинов. Ну а пока высказывается мнение (Mest H.J., Mentlein R., 2005), что применение ингибиторов DPP-IV рационально на ранних стадиях заболевания в качестве монотерапии или в комбинации с другими препаратами.
Ингибиторы DPP-IV
Привлекает внимание коммерческий успех первого и все еще единственного представителя этого класса — Januvia™ (ситаглиптин, «Merck&Co.»), объем продаж которого с момента появления на мировом рынке составил: 42 млн дол. в IV квартале 2006 г., 87 млн дол. в I квартале 2007 г., 144 млн дол. во II квартале. Ожидается, что вскоре на рынке появится еще один представитель этого класса — Galvus® (вилдаглиптин, «Novartis»). Выдача разрешения на маркетинг в ЕС Galvus® ожидается в конце октября этого года, а Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) в феврале 2007 г. направило компании одобрительное письмо (approvable letter) и сейчас продолжается рассмотрение материалов, касающихся безопасности препарата.
КИ III фазы проходит BMS-477118 (саксаглиптин, «Bristol-Myers Squibb»/«AstraZeneca plc.»), предназначенный для перорального применения 1 раз в сутки у больных СД II-го типа. Согласно результатам КИ, применение саксаглиптина в течение 24 нед в комбинации с метформином позволяет достичь статистически значимого улучшения контроля гликемии по сравнению с монотерапией метформином (то есть уровня гликозилированного гемоглобина (HbA1c) ниже 7,0%, при котором минимизируется риск возникновения осложнений). В дополнительном исследовании была продемонстрирована хорошая переносимость ситаглиптина, без токсических эффектов и изменений желудочковой проводимости, в дозе от 2,5 до 400 мг.
На поздней стадии разработки находится SYR- 322 (алоглиптин бензоат, «Takeda Pharmaceutical Co. Ltd.») — будущий конкурент вышеназванных препаратов, разработанный компанией «Syrrx Inc.» и перешедший к «Takeda» в следствие поглощения. На конференции также были представлены результаты КИ ранних фаз, в ходе которых алоглиптин в дозе 25–400 мг 1 раз в сутки значительно снижал (по сравнению с плацебо) содержание глюкозы в крови в течение 4 ч после приема пищи и при этом хорошо переносился во всех дозах.
Среди других компаний, имеющих разработкиингибиторов DPP-IV — японская компания «Sanwa Kagaku Kenkyusho Co. Ltd.» с SK-0403, который хорошо переносится в дозе до 400 мг и обладает четким дозозависимым эффектом в повышении уровня глюкагоноподобного пептида 1 (GLP-1); и «Abbott Laboratories» с ABT-279 для перорального применения, который также обладает четким дозозависимым эффектом и хорошо переносится в дозе до 1000 мг. «Boehringer Ingelheim Pharmaceuticals» представила результаты КИ I/II-й фаз для BI 1356. Этот аналог ксантина, похоже, тоже имеет большие шансы стать одним из лучших представителей класса. При его применении 1 раз в сутки развития гипогликемии (и серьезных побочных эффектов) не наблюдалось. Частота возникновения побочных эффектов при применении BI 1356 в ходе 12- и 28-дневных курсов лечения в КИ II-й фазы, не превышала таковую в группе плацебо.
Агонисты GLP-1
Кроме нормализации секреции инсулина (см. выше), GLP-1 ингибирует высвобождение глюкагона в организме, тормозя глюконеогенез в печени. Также GLP-1 замедляет опорожнение желудка, благодаря чему появляется чувство его заполненности и снижается вероятность переедания. Однако применение GLP-1 в высоких нефизиологических концентрациях может вызывать тошноту и рвоту, длительную задержку опорожнения желудка, поэтому разработчики фокусируют внимание на создании лекарственных форм с замедленным высвобождением GLP-1 или на агонистах рецепторов GLP-1 с приемлемыми фармакокинетическими показателями.
Канадская компания «ConjuChem Biotechnologies» представила исследования инсулинотропного агента PC-DAC™: Exendin-4 (эксендин-4, конъюгат с альбумином), являющегося агонистом GLP-1 длительного действия. В ходе КИ I/II-й фаз для препарата в форме подкожных инъекций была продемонстрирована хорошая переносимость в дозе до 3 мг, а серьезные побочные эффекты, связанные с применением препарата, не наблюдались. В виде монотерапии или в комбинации с метформином инъекция PC-DAC™: Exendin-4 позволяла достичь удовлетворительного контроля гликемии как минимум в течение 1 нед после однократной инъекции.
Повышенный интерес присутствующих вызвали доклады компании «Novo Nordisk» о результатах КИ II-й фазы агониста GLP-1 лираглутида, для которого в феврале 2006 г. были начаты КИ III-й фазы. Прием лираглутида 1 раз в сутки перорально значительно улучшал контроль гликемии у участников КИ, снижая уровень глюкозы в крови как натощак, так и после еды. Лираглутид хорошо переносится, и что касается эффективности, то у 75% пациентов, принимавших 0,9 мг ежедневно, удалось добиться контроля гликемии без случаев гипогликемии.
Ингибиторы SGLT2
Сразу несколько компаний представило результаты испытаний лекарственных средств, принадлежащих к новому классу — ингибиторов SGLT2. SGLT2 находятся на клетках почечного канальца и отвечают за обратный захват глюкозы из мочи и поступление ее в кровь. Соответственно, ингибирование SGLT2 предотвращает реабсорбцию глюкозы в проксимальном отделе почечных канальцев, в результате чего глюкоза интенсивнее выводится с мочой. В результате снижение уровня глюкозы в крови достигается независимо от действия инсулина. Ингибиторы SGLT2, похоже, не оказывают никакого влияния при нормогликемии и не нарушают баланс электролитов. Считается, что ингибиторы SGLT2 смогут послужить для дополнения комбинированной терапии при СД II-го типа. И BMS-512148 (дапаглифлозин, «Bristol-Myers Squibb»/«AstraZeneca»), и серглифлозин («Kissei Pharmaceutical»/«GlaxoSmithKline») представили результаты КИ II-й фазы. В обоих случаях сообщается о благоприятном профиле безопасности и способности к контролю гликемии. Кроме того, известно, что разработку лекарственного средства, принадлежащего к классу ингибиторов SGLT2, проводит и «sanofi-aventis», которая в ежегодном отчете за 2006 г. пообещала представить в IV кв. 2007 г. данные КИ IIb фазы препарата AVE2268.
Другие мишени для терапии СД и его осложнений
Можно предотвратить избыточную продукцию глюкозы у пациентов с СД II-го типа, ингибируя глюконеогенез в печени — эту идею взялись воплотить в жизнь «Metabasis Therapeutics» и «Sankyo», приступившие к разработке препарата под названием CS-917. Результаты КИ I/IIa фаз доказали, что после применения CS- 917 у пациентов с СД II-го типа значительно снижается уровень глюкозы в крови, без случаев гипогликемии и лактоацидоза. Сейчас для CS-917 проводятся КИ IIb фазы с целью установить наиболее эффективную дозу. Разработчики полны оптимизма и считают, что CS- 917 имеет потенциал стать препаратом первой линии для монотерапии или в комбинации с сульфонилмочевиной и сенситизаторами инсулина. Поживем — увидим.
Американская компания «DiObex Inc.» представила результаты КИ фазы IIa препарата DIO-902 (2S4R-энантиомер кетоконазола). DIO-902 является ингибитором 11-бета-гидроксилазы, поэтому при его применении у больных СД II-го типа происходит торможение синтеза кортизола. Применение DIO- 902 в дозах 200, 400 и 600 мг на протяжении 14 дней на фоне коррекции образа жизни и применения метформина позволяло улучшить контроль гликемии (нормализация показателей HbA1c, фруктозамина и глюкозы). Кроме того, у пациентов значительно снижался уровень С-реактивного белка, а также наблюдалось дозозависимое снижение уровней общего холестерина и холестерина липопротеидов низкой плотности. Переносимость энантиомера кетоконазола была хорошей, исключение — высокая частота слабых побочных эффектов со стороны пищеварительного тракта. Исследователи считают, что DIO-902 является многообещающей разработкой и сможет стать новым препаратом для терапии СД II-го типа и метаболического синдрома.
Что касается новых разработок в области терапии осложнений СД II-го типа, то новаторским можно назвать исследование агониста грелина TZP-101, разработанного канадской биотехнологической компанией «Tranzyme Pharma». На конференции она представила позитивные результаты применения TZP-101 в форме инъекций для ускорения опорожнения желудка при тяжелых формах гастропареза или постоперационной кишечной непроходимости. Начало полномасштабных КИ II-й фазы запланировано на III кв. 2007 г., а в 2008 г. компания планирует начать КИ препарата для перорального применения.
Для лечения нейропатической боли у больных с СД II-го типа «Chwarz Pharma» предлагает применять лакозамид, и представила данные одного из 3 КИ III-й фазы. Обладая преимуществом перед плацебо по уменьшению выраженности болевого синдрома, лакозамид в дозе 200 и 400 мг продемонстрировал благоприятный профиль безопасности (частота возникновения побочных эффектов была сравнимой с таковой в группе плацебо).
Интересным был доклад о свойствах уже зарегистрированного препарата для снижения уровня холестерола в крови у пациентов с первичной гиперхолестеролемией WelChol® (колесевелам гидрохлорид, «Daiichi Sankyo»). Согласно результатам КИ III-й фазы, у пациентов с СД II-го типа добавление колесевелама в схему противодиабетческой терапии улучшало и липидный профиль, и контроль гликемии.
Несмотря на высокую активность разработки, существует неудовлетворенная потребность в лекарственных средствах, которые были бы одновременно и безопасными, и эффективными, и обеспечивали высокую приверженность пациентов к лечению. Противодиабетические средства, выведенные на рынок в течение последних 20 лет — ингибиторы альфа-гликозидазы, тиазолидиндионы, аналоги GLP и амилина, ингибиторы DPP-IV — по некоторым данным, менее эффективны, чем по-явившиеся в 20–50-х годах XX ст. (инсулин, производные мочевины, бигуаниды) (таблица).
Таблица
Эффективность основных классов противодиабетических средств (Nathan D., 2007)
|
Лекарственное средство |
Путь введения |
Появление первого представителя класса на рынке США, год |
Эффективность в качестве монотерапии для снижении концентрации HbA1c, % |
| Инсулин | парентерально | 1921 | ≥2,5 |
| Препараты сульфонилмочевины | перорально | 1946 | 1,5 |
| Бигуаниды (метформин) | перорально | 1957 (в мире; с 1995 — в США) | 1,5 |
| Ингибиторы альфа-гликозидазы | перорально | 1995 | 0,5—0,8 |
| Тиазолидиндионы | перорально | 1997 | 0,8—1,0 |
| Аналоги GLP | парентерально | 2005 | 0,6 |
| Аналоги амилина | парентерально | 2005 | 0,6 |
| Ингибиторы DPP-IV | перорально | 2006 | 0,5—0,9 |
Несмотря на интенсивные разработки в этой области, в ближайшие несколько лет не стоит ожидать появления на полках аптек противодиабетических суперлекарств.
Пресс-служба «Еженедельника АПТЕКА»

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим