НОРМАТИВНА БАЗА
Як відомо, 12 лютого Президент України Указом № 82/2025 увів у дію рішення Ради національної безпеки і оборони (РНБО) України від 12.02.2025 р. «Про додаткові заходи щодо забезпечення доступності лікарських засобів для українців».
На виконання рішення РНБО 12 лютого Верховною Радою України ухвалено Закон України № 4239-IX (далі — Закон), яким, серед іншого, передбачено створення Національного каталогу цін. При цьому реалізація лікарських засобів за цінами, що перевищують ціни в Національному каталозі цін, з урахуванням граничних постачальницько-збутових та граничних торговельних (роздрібних) надбавок та податку на додану вартість (ПДВ), забороняється, крім випадків, передбачених законодавством. А у разі відсутності задекларованої ціни на лікарський засіб у Національному каталозі цін забороняється випуск такого лікарського засобу в обіг, крім випадків, передбачених законодавством.
Згідно із Законом до Національного каталогу цін вноситься задекларована ціна виробника або імпортера лікарського засобу, яка не може перевищувати ціну, розраховану як середній показник 3 найнижчих цін відповідного препарату (за міжнародним непатентованим найменуванням) у референтних країнах.
Тобто Законом передбачено референтне ціноутворення на всі лікарські засоби, що реалізуються на роздрібному ринку України.
4 квітня 2025 р. Уряд ухвалив постанову № 439, якою затверджено:
- Порядок реферування цін на лікарські засоби;
- Порядок декларування цін на лікарські засоби в Національному каталозі цін;
- Порядок створення та управління Національним каталогом цін.
ПРИНЦИПИ ЦІНОУТВОРЕННЯ
Граничні референтні ціни визначаються з урахуванням таких ідентичних характеристик, як торговельна назва, міжнародне непатентоване найменування, форма випуску, дозування, кількість одиниць лікарського засобу в упаковці, за наявності — інформація про виробника препарату та/або власника реєстраційного посвідчення на лікарський засіб (далі — ідентичні характеристики) у не менш як 4 референтних країнах. Допускається відмінність торговельної назви в референтній країні та Україні за умови збігу всіх ідентичних характеристик.
Порядком реферування передбачено, що розрахунок граничних референтних цін не здійснюється на:
1) лікарські засоби, що закуповуються відповідно до договорів керованого доступу;
2) оригінальні (інноваційні) препарати, дозволені для медичного застосування в Україні;
3) лікарські засоби, інформація про ціни на які наявна менш ніж у 4 референтних країнах;
4) радіофармацевтичні, наркотичні, психотропні препарати (крім лікарських засобів, які містять малу кількість наркотичного засобу та/або психотропної речовини, що не перевищує встановлену законодавством гранично допустиму норму), медичні гази, а також лікарські засоби (крім комбінованих), які містять прекурсори;
5) ліки, які на період проведення розрахунку граничних референтних цін не мають зареєстрованих в Україні аналогів (за міжнародним непатентованим найменуванням або складом діючих речовин, формою випуску);
6) генеричні або подібні біологічні лікарські засоби, які мають аналогічні до оригінального (інноваційного) препарату, дозволеного до застосування в Україні (на який задекларована оптово-відпускна ціна в Національному каталозі цін), міжнародне непатентоване найменування (склад діючих речовин), дозування та схожу форму випуску;
7) ліки, торговельні назви яких зазначені в переліку лікарських засобів, які підлягають реімбурсації за програмою державних гарантій медичного обслуговування населення, затвердженого МОЗ.
Для лікарських засобів, які виключені з-під реферування, застосовуватиметься принцип декларування цін у Національному каталозі цін.
До сегмента «Менше 4 референтних країн» ми віднесли лікарські засоби вітчизняного виробництва, адже малоймовірно, що для них знайдуться ціни в ≥4 референтних країнах і для них також буде застосовуватися принцип декларування цін.
Враховуючи ці критерії, ми розподілили увесь роздрібний ринок на сегменти відповідно до принципів їх ціноутворення та оцінили їх частку в загальному обсязі роздрібної реалізації ліків (табл. 1).
| Сегмент препаратів | Частка в упак., %, 2024 р. | Частка в грн, %, 2024 р. | Ціноутворення |
| Оригінальні / інноваційні (перелік ДЕЦ станом на 2.05.2024 р.) | 12 | 24 | Декларування |
| Генерики до оригінальних препаратів (декларування не вище 75% від ціни оригінатора) | 17 | 19 | Декларування |
| Програма «Доступні ліки» | 8 | 6 | Окреме ціноутворення* |
| Наркотичні, психотропні, радіофармацевтичні ліки | 2 | 1 | Декларування** |
| Менше 4 референтних країн (ліки вітчизняного виробництва) | 44 | 24 | Декларування |
| Включені до Нацпереліку | 3 | 4 | Реферування |
| Rx, не включені до Нацпереліку | 5 | 11 | Реферування |
| ОТС, не включені до Нацпереліку | 9 | 12 | Реферування |
Отже, загалом під реферування може підпасти близько 17% від загальних обсягів продажу препаратів в упаковках та 27% у гривневому вираженні.
Однак, враховуючи, що на більшість препаратів ОТС-сегмента не знайдеться референтних цін, то фактично під реферування може підпасти близько 8% ринку в упаковках та 15% у гривневому вираженні, але й не на всі ці препарати можуть бути наявні ціни хоча б у 4 референтних країнах.
Так, левова частка ринку підпаде під процедуру вільного декларування цін.
РЕФЕРУВАННЯ
Слід зазначити, що Законом установлено, що перше декларування цін на лікарські засоби, зареєстровані в Україні, здійснюється не пізніше 120 днів з дня набрання чинності цим законом, крім:
- першого декларування цін на всі препарати, включені до Національного переліку основних лікарських засобів (далі — Нацперелік), що здійснюється не пізніше 60 днів з дня набрання чинності Законом;
- першого декларування цін на всю групу рецептурних препаратів, зареєстрованих в Україні (крім лікарських засобів, включених до Нацпереліку), що здійснюється не пізніше 90 днів з дня набрання чинності цим законом.
Закон набрав чинності 1 березня 2025 р. Згідно із його положеннями, перше декларування цін на препарати з Нацпереліку мало завершитися 29 квітня 2025 р., а для рецептурних препаратів, що не входять до Нацпереліку, має завершитися 29 травня. Загалом же декларування цін має завершитися до 28 червня 2025 р.
Водночас станом на 14.05.2025 р. граничні оптово-відпускні ціни розраховані лише на препарати з Нацпереліку. Тобто наразі МОЗ реалізує ще перший етап реферування / декларування, визначений Законом.
Згідно з наказом МОЗ від 10.05.2025 р. № 795 граничні референтні ціни розраховані для 198 позицій лікарських засобів, включених до Нацпереліку, з яких лише 70 реалізовувалося на роздрібному ринку у 2024 р. Їх частка в загальному обсязі ринку становить 0,4% в упаковках і 0,5% у грошовому вираженні від загальних обсягів продажу ліків у 2024 р.
У квітні 2025 р. на роздрібному ринку реалізовувалася 61 торговельна назва лікарських засобів із 198, на які визначено референтні ціни. Для 42 препаратів визначено граничну роздрібну ціну, розраховану на підставі референтних цін з урахуванням граничних націнок та ПДВ (гранична роздрібна ціна), яка є нижчою за поточну середньозважену роздрібну вартість у квітні 2025 р. Для 24 препаратів референтна ціна є вищою.
При цьому для 24 препаратів розрахована гранична роздрібна ціна є нижчою за поточну ринкову на >50%, що може призвести до виведення цих препаратів з ринку.
Якщо припустити, що всі ліки реалізовуватимуться за граничними роздрібними цінами, то загалом реферування сприятиме зниженню середньозваженої роздрібної вартості на ці препарати на 12% порівняно із такою у квітні 2025 р. Однак, враховуючи незначну кількість та невеликі обсяги продажу препаратів, для яких визначено референтні ціни, то загалом це не матиме суттєвого впливу на ринок. Вплив оцінюється на рівні <0,1%.
Варто відзначити, що референтна ціна розраховувалася і на деякі оригінальні лікарські засоби з переліку, опублікованого ДП «Державний експертний центр МОЗ України» (далі — ДЕЦ), та генерики до них, а також на препарати, вартість яких відшкодовується державою. Якщо відкинути ці позиції, то загалом за підсумками 2024 р. на ринку реалізовувалося лише 48 позицій лікарських засобів, для яких розраховано граничну оптово-відпускну ціну. Тобто реальний вплив буде ще меншим.
У квітні 2025 р. на роздрібному ринку реалізовувалося 39 торговельних назв препаратів, для яких розраховано граничну оптово-відпускну ціну на підставі референтних цін.
Порівняння поточної середньозваженої роздрібної вартості 1 упаковки та граничної роздрібної ціни наведено в табл. 2.
| Повна назва лікарського засобу | Гранична оптово-відпускна ціна в перерахунку на одиницю лікарської форми***, грн | Гранична роздрібна ціна за упаковку, грн**** | Середньозважена роздрібна вартість за упаковку у квітні 2025 р., грн |
| АСЕНТРА®, КРКА (Словенія), табл., в/плівк. обол., 100 мг, № 28 | 14,08 | 546,55 | 577,96 |
| БІСЕПТОЛ®, Адамед Фарма (Польща), табл. 100 мг + 20 мг, блістер, № 20 | 1,99 | 57,53 | 80,34 |
| БІСЕПТОЛ®, Адамед Фарма (Польща), табл. 400 мг + 80 мг, блістер, № 20 | 4,42 | 127,57 | 166,16 |
| БОНАБЛАСТ, Містрал Кепітал Менеджмент (Великобританія), табл., в/плівк. обол., 50 мг, блістер, № 28 | 115,59 | 4114,24 | 4802,45 |
| ВЕРОШПІРОН, Гедеон Ріхтер (Угорщина), капс. 50 мг, № 30 | 3,68 | 153,14 | 227,32 |
| ГАЛОПЕРИДОЛ-РІХТЕР, Гедеон Ріхтер (Угорщина), р-н д/ін. 5 мг, амп. 1 мл, № 5 | 17,49 | 126,32 | 159,39 |
| ДЕКСАМЕТАЗОН КРКА, КРКА (Словенія), табл. 20 мг, блістер, № 10 | 90,20 | 2293,09 | 711,68 |
| ДЕКСАМЕТАЗОН КРКА, КРКА (Словенія), табл. 4 мг, блістер, № 30 | 17,69 | 490,52 | 600,65 |
| ДОПЕГІТ®, Егіс (Угорщина), табл. 250 мг, фл., № 50 | 5,32 | 368,55 | 262,71 |
| ЕНАП®, КРКА (Словенія), табл. 10 мг, блістер, № 20 | 3,48 | 100,50 | 73,43 |
| ЕНАП®, КРКА (Словенія), табл. 20 мг, блістер, № 20 | 5,04 | 139,81 | 111,72 |
| ЗАРСІО®, Сандоз (Швейцарія), р-н д/ін. та інф. 30 млн МО, шприц 0,5 мл, № 5 | 370,25 | 2353,25 | 5540,63 |
| ЗАРСІО®, Сандоз (Швейцарія), р-н д/ін. та інф. 48 млн МО, шприц 0,5 мл, № 5 | 727,65 | 4624,83 | 7147,64 |
| КАРБОПА, Аккорд Хелскер (Великобританія), конц. д/р-ну д/інф. 10 мг/мл, фл. 15 мл, № 1 | 447,10 | 620,01 | 1164,26 |
| КАРБОПА, Аккорд Хелскер (Великобританія), конц. д/р-ну д/інф. 10 мг/мл, фл. 45 мл, № 1 | 1301,06 | 1653,85 | 2661,84 |
| КАРБОПА, Аккорд Хелскер (Великобританія), конц. д/р-ну д/інф. 10 мг/мл, фл. 60 мл, № 1 | 2244,66 | 2853,32 | 3166,26 |
| КВЕНТІАКС®, КРКА (Словенія), табл., в/плівк. обол., 100 мг, блістер, № 30 | 5,29 | 220,12 | 283,41 |
| КВЕНТІАКС®, КРКА (Словенія), табл., в/плівк. обол., 25 мг, блістер, № 30 | 2,20 | 95,17 | 232,12 |
| КВЕНТІАКС®, КРКА (Словенія), табл., в/плівк. обол., 300 мг, блістер, № 30 | 12,54 | 521,52 | 257,12 |
| КОРІОЛ®, КРКА (Словенія), табл. 12,5 мг, № 28 | 2,57 | 103,88 | 234,60 |
| КОРІОЛ®, КРКА (Словенія), табл. 25 мг, № 28 | 3,29 | 132,93 | 266,78 |
| КОРІОЛ®, КРКА (Словенія), табл. 6,25 мг, № 28 | 1,77 | 71,43 | 209,65 |
| ЛОРІСТА®, КРКА (Словенія), табл., в/плівк. обол., 100 мг, блістер, № 30 | 3,57 | 148,65 | 293,54 |
| ЛОРІСТА®, КРКА (Словенія), табл., в/плівк. обол., 50 мг, блістер, № 30 | 2,44 | 105,55 | 283,61 |
| НІТРОМІНТ®, Егіс (Угорщина), спрей сублінгвальний 0,4 мг/1 доза, балон 180 доз, № 1 | 103,62 | 143,69 | 235,83 |
| ОКСАЛАК, Аккорд Хелскеа Польска (Польща), конц.д/п р-ну д/інф. 5 мг/мл, фл. 20 мл, № 1 | 656,18 | 872,03 | 2317,32 |
| ОМЕПРАЗОЛ-ТЕВА, Тева (Ізраїль), капс. гастрорезист. 20 мг, блістер, № 30 | 3,82 | 158,91 | 163,09 |
| ОСПАМОКС®, Сандоз (Швейцарія), пор. д/орал. сусп. 250 мг/5 мл фл., 6,6 г, д/п 60 мл сусп., № 1 | 48,60 | 70,20 | 293,52 |
| ОСПАМОКС®, Сандоз (Швейцарія), табл., в/плівк. обол., 1000 мг, № 12 | 7,47 | 129,41 | 221,68 |
| ОСПАМОКС®, Сандоз (Швейцарія), табл., в/плівк. обол., 500 мг, № 12 | 3,35 | 58,00 | 199,43 |
| ПАКЛІТАКСЕЛ АККОРД, Аккорд Хелскер (Великобританія), конц. д/р-ну д/інф. 6 мг/мл, фл. 50 мл, № 1 | 1701,31 | 2162,64 | 4535,92 |
| РИСПОЛЕПТ®, Янссен-Сілаг (Бельгія — Швейцарія), р-н орал. 1 мг/мл, фл. 30 мл | 716,87 | 952,68 | 830,94 |
| ТАЛЛІТОН®, Егіс (Угорщина), табл. 6,25 мг, блістер, № 28 | 1,59 | 64,18 | 51,00 |
| УНІФЛОКС, Унімед Фарма (Словацька Республіка), крап. оч./вуш. 0,3%, контейнер-крапельн. 10 мл, № 1 | 158,12 | 219,27 | 146,54 |
| ЦИПРИНОЛ®, КРКА (Словенія), конц. д/р-ну д/інф. 100 мг, амп. 10 мл, № 5 | 31,96 | 221,61 | 246,62 |
| ЦИПРИНОЛ®, КРКА (Словенія), р-н д/інф. 200 мг, фл. 100 мл, № 1 | 266,38 | 369,40 | 261,92 |
| ЦИПРИНОЛ®, КРКА (Словенія), табл., в/плівк. обол., 250 мг, № 10 | 4,77 | 68,83 | 210,05 |
| ЦИПРИНОЛ®, КРКА (Словенія), табл., в/плівк. обол., 500 мг, № 10 | 7,77 | 112,17 | 255,83 |
| ЦИСПЛАТИНА АККОРД, Аккорд Хелскер (Великобританія), конц. д/р-ну д/інф. 1 мг/мл фл., 50 мл, № 1 | 475,52 | 659,41 | 666,92 |
Також це може призвести до непорозуміння з боку виробників, адже вони не зможуть визначити, яку процедуру ціноутворення їм застосовувати. З одного боку, вони мають декларувати ціну, адже для них не здійснюється розрахунок референтних цін відповідно до порядку реферування, а з іншого боку — наказом МОЗ № 795 затверджено граничну оптово-відпускну ціну.
Наступним етапом має стати реферування цін на рецептурні препарати, що не включені до Нацпереліку. За підсумками 2024 р. їх частка у структурі роздрібної реалізації ліків у грошовому вираженні становить 11%. Враховуючи, що частка лікарських засобів з Нацпереліку, які підпадають під реферування, становить 4% у грошовому вираженні, а їх вплив на ринок — <0,1%, то можна пропорційно оцінити вплив на ринок від реферування рецептурних препаратів, що не включені до Нацпереліку, у близько 0,3%.
Фінальний етап реферування має відбуватися на ОТС-ліки, які не включені до Нацпереліку, але цін на ОТС-препарати принаймні в 4 референтних країнах буде знайдено ще менше, тож реферування цього сегмента майже не вплине на ринок.
Тобто загалом вплив на ринок від реферування цін становитиме <0,5%.
ДЕКЛАРУВАННЯ
МОЗ розпочало процедуру декларування цін на оригінальні / інноваційні лікарські засоби, станом на 2.05.2025 р. в проєкті Національного каталогу задекларовано ціни на 380 торговельних назв препаратів.
Аналіз свідчить, що різниця між середньозваженою роздрібною вартістю, розрахованою на підставі задекларованих цін, та ринковою в березні становить близько 15% (рисунок).
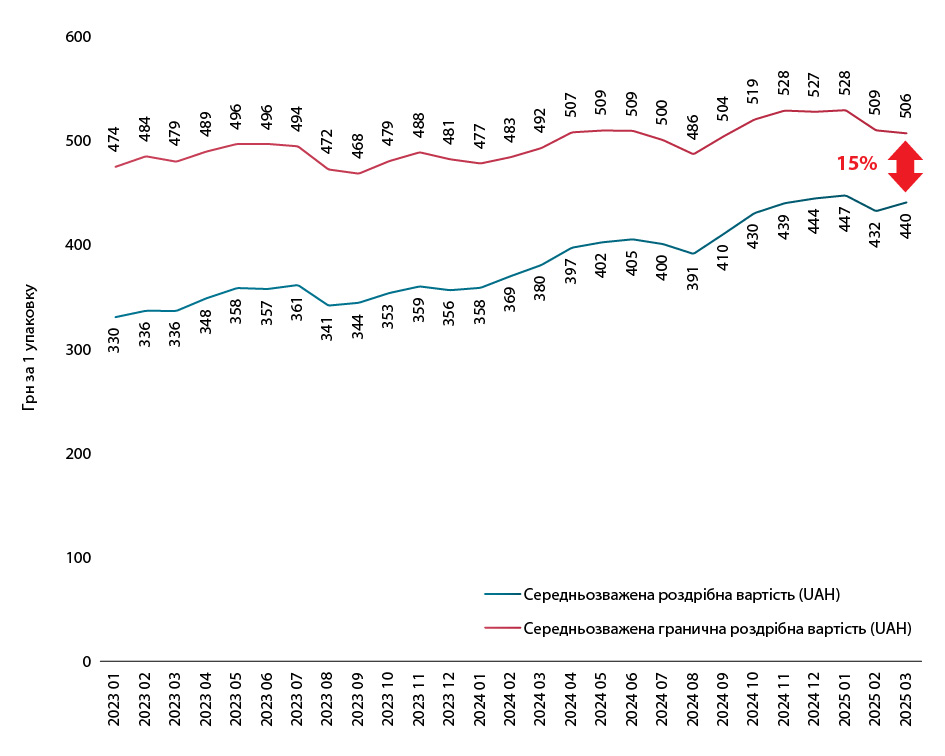
Тобто держава стимулює можливість підвищення цін на оригінальні лікарські засоби на 15%?
Також триває прийом заяв на декларування цін генериків до оригінальних ліків, яка не має перевищувати 75% від задекларованої ціни на оригінальний препарат, та на лікарські засоби з Нацпереліку, для яких визначено граничну оптово-відпускну ціну на підставі цін у референтних країнах.
Документи на декларування граничних оптово-відпускних цін на ліки, що включені до Переліку граничних референтних цін на лікарські засоби, які включені до Нацпереліку, подаються з 12 травня до 21 травня 2025 р. (включно).
Окрім того, до 21 травня 2025 р. (включно) подовжено термін прийому документів на декларування граничних оптово-відпускних цін на генеричні або подібні біологічні лікарські засоби, що включені до Нацпереліку.
ВПЛИВ НА РИНОК
На підставі наявних даних ми спробували оцінити загальний вплив на ринок нових правил ціноутворення.
Для оцінки цього впливу ми використовували наступний сценарій:
- ціна на оригінальні / інноваційні препарати може зрости в середньому на 15%;
- ціна на генерики до оригінальних також може підвищитися на 15%;
- вартість препаратів, що реімбурсуються, не зміниться;
- вартість наркотичних, психотропних, радіофармацевтичних ліків не змінюватиметься;
- ціна на вітчизняні препарати також може зрости на 15%;
- препарати з Нацпереліку, для яких розрахована референтна ціна, реалізовуватимуться за нею;
- ціна на ліки з Нацпереліку, для яких не розрахована референтна ціна, також може зрости на 15%;
- ціна на Rx-препарати, які не включені до Нацпереліку та підлягають реферуванню, може знизитися на 12% (на підставі даних щодо референтних цін за Нацпереліком);
- ціна на ОТС-препарати, які не включені до Нацпереліку, може підвищитися на 15%.
При такому сценарії середньозважена роздрібна вартість може зрости на 10% порівняно із такою у квітні 2025 р.
Цей сценарій містить багато припущень, тож фактична зміна роздрібної вартості може бути іншою.
Якщо оперувати наявними даними щодо задекларованих та розрахованих референтних цін, то зростання середньозваженої роздрібної вартості може становити 13% порівняно із такою у квітні 2025 р.
ВИСНОВКИ
За допомогою аналізу виявлено, що запроваджені ініціативи з цінового регулювання, які спрямовані на зниження цін, можуть мати зворотний ефект та спричинити їхнє зростання. За наявними даними, середнє підвищення цін може сягнути 13%.
Втім ефект від цінової регуляції можна буде оцінити після того, як задекларують ціни на всі оригінальні / інноваційні препарати та генерики до них, а також на вітчизняні лікарські засоби.
Крім того, ця ініціатива може призвести до закриття аптек з невеликим оборотом, зокрема в сільській місцевості. Адже неможливість гнучкого управління ціною на тлі заборони маркетингу від виробників може поставити такі невеликі аптеки у скрутне становище або довести до збитковості.
До того ж запроваджена регуляція створює нерівні умови для учасників ринку. На одні лікарські засоби держава дозволяє підвищувати ціну, а на інші — примушує знижувати.
Існують приклади референтних цін, коли на один і той самий бренд на 1 дозування компанія має знизити ціну, а на інше навпаки — підвищити в рази.
Нагадаємо, що при розгляді та ухваленні Закону не було надано економічного обґрунтування впливу його положень на ринок, хоча зафіксовано запити щодо цього від учасників робочої групи. Тож, на нашу думку, необхідно скасувати цей закон, адже його положення можуть мати негативні наслідки як для учасників ринку, так і пацієнтів. Спочатку необхідно розрахувати очікуваний вплив з урахуванням всіх аспектів, а потім впроваджувати регулювання. Адже, як свідчить постаналіз, очікуваний вплив може мати зворотний ефект.
Взагалі регулювання цін на вільному ринку не відповідає європейським практикам. У більшості країн ЄС ціни на вільному ринку не регулюються. Держава регулює ціни лише в тих сегментах, де вона є платником, таких як реімбурсація та закупівлі ліків.

Коментарі