FDA дало разрешение на продажу теста для диагностики определенных форм лейкоза и лимфомы
Управление по контролю за пищевыми продуктами и лекарственными средствами США (U.S. Food and Drug Administration — FDA) разрешило продажу реагентов теста ClearLLab (T1, T2, B1, B2, M). Этот продукт является первым утвержденным FDA тестом, который основан на методе проточной цитометрии и может помочь в выявлении определенных форм лейкоза и лимфомы, в частности хронического лейкоза, острого лейкоза, неходжкинской лимфомы, миеломы, миелодиспластического синдрома и миелопролиферативных новообразований. «Это […]
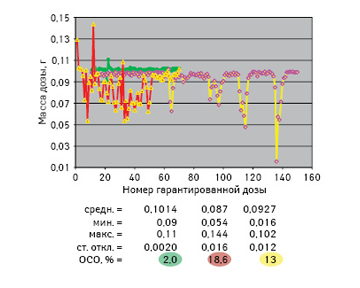
Проведение исследования по сравнению однородности массы доз и однородности дозирования в препаратах дозированных назальных спреев мометазона фуроата
Глюкокортикостероидные препараты широко используются в клинической практике для лечения целого ряда заболеваний, относящихся к различным направлениям медицины. Эти препараты оказывают выраженное и быстро проявляющееся противовоспалительное и иммуносупрессивное действие.
FDA стремится улучшить доступ к лекарствам за счет ускоренного выведения на рынок генериков
Управление по контролю за пищевыми продуктами и лекарственными средствами США (U.S. Food and Drug Administration — FDA) предпринимает 2 важных шага, направленных на повышение конкуренции на рынке рецептурных лекарственных средств и упрощение выведения на рынок генериков. Агентство опубликовало список непатентованных, брэндированных лекарств, не имеющих одобренных генериков, а также впервые внедрило новую политику, направленную на ускорение рассмотрения заявок на одобрение непатентованных лекарств в условиях ограниченной конкуренции. Это […]
ЕМА одобрило 2 новых препарата для лечения хронического вирусного гепатита С
Вирусный гепатит С (ВГС) является одной из основных проблем общественного здравоохранения и затрагивает около 0,4–3,5% населения в разных государствах — членах ЕС. Хроническая ВГС-инфекция также является наиболее распространенной причиной трансплантации печени в ЕС. У около 15 млн человек в странах ЕС отмечают хроническую ВГС-инфекцию. Несмотря на быстрое развитие медицины в направлении лечения данной патологии, по-прежнему существует потребность в ряде альтернативных вариантов терапии для […]
В США одобрен препарат для контроля редкого наследственного заболевания
Управление по контролю за пищевыми продуктами и лекарственными средствами США (U.S. Food and Drug Administration — FDA) одобрило первый препарат, относящийся к классу ингибиторов С1-эстеразы — Haegarda, предназначенный для предупреждения обострений редкого генетического заболевания — наследственного ангионевротического отека — у подростков и взрослых пациентов. Подкожный способ введения лекарственного средства позволяет облегчить проведение инъекции в домашних условиях. Наследственный ангионевротический отек — редкое заболевание, связанное с количественной […]
Регуляторы ЕС, Японии и США объединяют усилия для содействия разработке новых антибиотиков
Представители 3 регулирующих органов определили ряд направлений, где требования к данным могут быть модернизированы.
FDA отзывает опиодный анальгетик с рынка
Это первый случай, когда FDA предприняло шаги по удалению лицензированного продукта с рынка из-за рисков, связанных со злоупотреблением этим препаратом.
ВОЗ обновила перечень основных лекарственных средств
Обновленный Перечень включает 433 препарата
EMA опубликовало новый план поддержки предприятий малого и среднего бизнеса
Всего план содержит описание 16 мероприятий, намеченных для реализации в 2017–2020 гг.
FDA одобрило первый препарат для лечения опухолей любой локализации с определенной генетической характеристикой
Это первый случай, когда FDA одобрило лекарственное средство для лечения рака, основанное на общем биомаркере, а не на локализации опухоли.
Виробництво ліків
Про те, що дозволяє фармацевтичним компаніям йти в ногу з часом і
випереджати конкурентів: інновації, дослідження, технології або просто ― Research&Development.
У найближчі 5 років великі виробники оригінальних препаратів зіткнуться з проблемою закінчення термінів ринкової ексклюзивності для багатьох продуктів, що суттєво змінить ситуацію у сфері виробництва ліків. Аналітики вже
охрестили період 2010–2011 років. патентною чорною діркою, оскільки обсяг продажу
гігантів, які випускають брендовану продукцію, зменшиться на 28%. Проблема
Фарми не так у закінченні дії патентів, як у тому, що продажі нових
препаратів із чинним патентним захистом не зможуть заповнити втрати.
Фармацевтичне виробництво стоїть перед нелегким вибором нових рішень.
Якими будуть ці рішення, ви зможете дізнатися з публікацій у розділі R&D, де
висвітлено найактуальніші питання створення та виробництва лікарських засобів. Найсвіжіші новини про створення лікарських препаратів, їх лончі на ринку, про
схвалення або відкликання препаратів на світових ринках та в Україні ви зможете дізнатися
на сайті www.apteka.ua