|
|
Перспективы развития фармацевтической промышленности в XXI веке прежде всего связывают с достижениями в области биотехнологий. Особую роль в этом призван сыграть Проект человеческого генома (HGP — Human Genome Project). В 1990 г. Министерство энергетики США и Национальные институты здоровья приступили к реализации HGP, рассчитанного на 15 лет. Вскоре проект стал частью международного сотрудничества 18 государств — США, некоторых стран Европы, Японии и Китая. Основная задача HGP — идентифицировать и локализовать все гены в молекулах ДНК человека, определить последовательность расположения 3 млрд химических оснований, из которых состоит ДНК, создать базу данных генома человека и некоторых микроорганизмов и разработать средства для эффективного анализа генетических данных. Другой важной целью HGP является определение механизмов действия и взаимодействия генов в процессе развития человеческого организма и в патогенезе заболеваний.
Ожидают, что в результате реализации этого грандиозного проекта ученые получат доступ к «книге жизни» — к точному биохимическому коду каждого из 80–100 тыс. генов, составляющих геном человека. 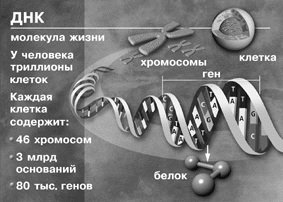
Всего несколько лет назад появилась наука геномика, которая изучает весь генетический материал человека. Сегодня на базе геномики уже заложены основы новых дисциплин: геномной медицины, фармакогеномики, протеомики, микробной геномики и др. Применение новых знаний в области генетики может кардинально изменить подходы к диагностике, лечению и профилактике сотен и даже тысяч не только наследственных генетических заболеваний (например, фенилкетонурии, муковисцидоза, талассемий), но и множества других широко распространенных болезней, в развитии которых участвуют как генетические факторы, так и факторы окружающей среды (например, болезни сердечно-сосудистой системы, сахарный диабет, некоторые формы злокачественных новообразований, психические и неврологические расстройства, инфекционные болезни, в том числе туберкулез и СПИД).
Кроме того, эти знания могут быть использованы для разработки новых источников энергии (биологического топлива), методов контроля за состоянием окружающей среды, современных способов безопасного и эффективного уничтожения токсических отходов. Потенциальные возможности в этой сфере очень велики, поскольку в настоящее время только 0,01% всех микроорганизмов культивированы и изучены. Поэтому с 1994 г. одновременно с программой изучения генома человека Министерство энергетики США осуществляет Программу изучения генома микроорганизмов (Microbal Genome Program).
Несмотря на огромную стоимость HGP — 3 млрд долларов США (в среднем около 200 млн в год), проект позволит сэкономить значительные средства за счет эффекта масштаба. Так, затраты на поиск одного гена, который обусловливает развитие наследственного заболевания (например, муковисцидоза), составляют около 100 млн долларов США. Поэтому расшифровка каждого гена в отдельности составила бы астрономическую сумму. Подсчитано, что системный подход к изучению всего генома обойдется намного дешевле и средняя стоимость обнаружения одного гена составит не более 30 тыс. долларов США. Гены занимают только 3% генома и могут иметь от одной тысячи до нескольких миллионов оснований. Весь геном человека состоит из 3 млрд пар оснований. В 1996 г. была достигнута одна из целей HGP — добиться определения последовательности оснований со скоростью 90 Mb в год (Megabase — 1х106 пар оснований) при стоимости определения последовательности 1 пары — 0,5 доллара США, а в соответствии с планами проекта до 2003 г. скорость определения последовательностей должна составить 500 Mb/год при стоимости 1 пары оснований 0,25 доллара. Учитывая общее количество оснований в геноме человека (3 Gb), снижение затрат на определение 1 пары оснований даже на 1 цент может принести экономию в 30 млн долларов. Снижению стоимости HGP и его более быстрой реализации способствовало совершенствование методов картирования ДНК и определения генетических последовательностей, а также применение активно развивающихся компьютерных технологий.
В 1995 г. впервые были полностью определены последовательности генома первого микроорганизма (Haemophilus influenzae), а в 1998 г. — первого животного организма (круглого червя Caenorhabditis elegans). Если геном H. influenzae насчитывает 1,9 Mb, то геном C. elegans — 97 Mb. К 1998 г. ученым удалось установить последовательности 7% человеческого генома. В настоящее время полностью расшифрованы геномы 20 микроорганизмов (111 Mb), в том числе M. tuberculosis, E. coli, H. pylori. 1 декабря 1999 г. было сообщено о завершении «первой главы книги жизни» — полном определении последовательностей одной из хромосом человека (XXII). Впервые ученые получили возможность взглянуть на организацию всей хромосомы на уровне химических оснований. Несмотря на то что полученная информация должна быть тщательно проанализирована, уже известно, что XXII хромосома может иметь отношение к функционированию иммунной системы, развитию врожденных заболеваний сердца, шизофрении, отставанию в умственном развитии, порокам физического развития, а также к некоторым злокачественным новообразованиям и лейкозам.
С учетом этих достижений в 1998 г. участники программы провели корректировку планов осуществления HGP. Решено, что проект будет завершен на 2 года раньше срока. Таким образом, полностью геном человека будет расшифрован не позже 2003 г., а предварительный проект генома будет представлен уже весной этого года. Под полной расшифровкой генома понимают точное определение расположения всех последовательностей ДНК, даже тех больших участков, которые не содержат генов (они составляют около 97% генома).
Однако над полной расшифровкой кода работают в основном государственные институты, а не частные компании. Например, специалисты компании «Genset» (Франция) в начале 2000 г. должны завершить составление карты только 60 тыс. наиболее важных участков и, сравнивая эти участки ДНК различных людей, выявить конкретные гены, которые действительно вызывают развитие определенного заболевания. Руководитель исследований по геномике компании «Genset» Д. Коуэн считает, что, например, из 100 тыс. генов только 200 могут иметь отношение к развитию 20 наиболее распространенных заболеваний, в 80% случаев являющихся причиной смерти людей, поэтому именно таким генам следует уделить особое внимание. Картирование генов частными компаниями, безусловно, способствует выполнению проекта, однако часто компании пытаются запатентовать отдельные участки ДНК или генов. В настоящее время вопросы патентования генетического материала недостаточно разработаны и заинтересованные стороны интенсивно работают над совершенствованием законодательства.
Данные о геноме человека и других организмов уже используют в таких областях медицины и фармации, как генная инженерия, генная терапия, фармакогенетика, протеомика, а также в создании генных вакцин.
Генное тестирование
В геноме человека около 2–5 тыс. генов могут вызывать или обусловливать предрасположенность к развитию заболеваний. В результате выполнения проекта появится реальная возможность диагностировать индивидуальную предрасположенность к заболеваниям и заблаговременно принимать соответствующие меры профилактики (например, путем изменения образа жизни, проведения целенаправленных профилактических осмотров или применения генной терапии).
В конечном счете целью проекта является разработка новых методов лечения (и излечения) и предупреждения множества заболеваний. Однако путь от выявления гена, ответственного за развитие определенного патологического состояния, до создания эффективного метода лечения достаточно долог и изобилует многочисленными препятствиями.
При генном тестировании с помощью новейших методик определяют наличие генетических заболеваний путем исследования самой молекулы ДНК.
Пока многие биотехнологические компании заняты разработкой коммерческих диагностических тестов, предназначенных для выявления измененных генов у лиц с подозрением на наличие определенного заболевания или с высоким риском его развития. Количество таких тестов на рынке постоянно увеличивается, хотя многие вопросы их практического применения пока еще недостаточно разработаны. В настоящее время большое количество диагностических лабораторий в США и странах Западной Европы проводят генетическое тестирование. Перечни лабораторий и информация о используемых ими методах генетических или генных (так называемое ДНК-тестирование) исследований можно найти в сети Интернет. Например, в г. Ловерваль (Бельгия) создан Европейский указатель ДНК-лабораторий, насчитывающий 314 учреждений, которые проводят ДНК-тестирование в отношении 507 генетических болезней (например, для выявления болезни Альцгеймера, атаксии-телеангиэктазии, бокового амиотрофического склероза, муковисцидоза, анемии Фанкони, ломкой Х-хромосомы, гемофилии А и B, дистрофической миотонии, серповидно-клеточной анемии, наследственной спиноцеребральной атаксии и др.).
Несмотря на то что некоторые из этих методов достаточно совершенны и играют важную роль в спасении человеческих жизней, среди врачей и ученых существуют разногласия о целесообразности проведения тестов и интерпретации результатов тестирования для выявления заболеваний, методы лечения которых отсутствуют. Кроме того, в США известны случаи, когда результаты генетического тестирования страховые компании или работодатели использовали во вред пациентам.
Генная терапия
Большинство методик генной терапии основано на введении с помощью различных методов генетического материала в клетки больного для замены, коррекции или блокирования дефектного гена. Генную терапию пытаются использовать для лечения пациентов с наследственными заболеваниями, злокачественными образованиями и СПИДом. Генная терапия является относительно новым методом лечения. В 1990 г. американский генетик У.Ф. Андерсон впервые применил генную терапию для лечения 4-летней девочки с тяжелым иммунодефицитом (дефицит фермента аденозиндезаминазы — АДА), при котором летальный исход наступает в первые месяцы или первые годы жизни. В качестве носителя (вектора) для переноса гена АДА в лимфоциты ex vivo был использован ретровирус. Эксперимент оказался успешным и пациентка до сир пор жива. Однако в этой области еще не решены многие фундаментальные проблемы и практические результаты достаточно скромны, хотя клинические исследования продолжаются. С 1990 г. и до настоящего времени (сентябрь 1999 г.) в мире было проведено или находилось в стадии проведения 396 клинических исследований, в которых приняли участие 3278 человек. Из них 310 исследований проведено в США, 68 — в странах Европы. Целью значительной части исследований (252) является лечение больных со злокачественными новообразованиями.
Фармакогеномика
«Фармакогеномика» — новый термин, под которым подразумевают использование данных геномики о вариабельности генов для оптимизации поиска и разработки лекарственных веществ и для более индивидуализированного подхода к лечению больных. 
Фармакогенетическими исследованиями подтверждено, что и на этническом, и на индивидуальном уровне имеются различия в механизмах обмена веществ в организме человека, которые могут значительно влиять на метаболизм лекарственных средств. Несмотря на то что имеется множество лекарственных средств, которые специфически действуют на определенные органы или ткани организма, они не всегда являются максимально эффективными из-за индивидуальных генетических различий или генетического полиморфизма (наличие нескольких аллелей одного гена, причем носители редкого аллеля данного гена составляют 2% популяции и более). В последние годы стало ясно, что вариабельность генов — более распространенное явление, чем считали ранее, и этим обусловлены многие случаи неэффективного лечения или развития побочных реакций. Ранее фармакогенетика развивалась главным образом на основе информации о генетических маркерах для генов, кодирующих определенные признаки, данных семейного анамнеза, сведений о расовых или этнических особенностях. Применение новых методов физического картирования генов или маркеров и «функционального клонирования» генов позволяет выяснить особенности генетических механизмов нарушения обмена веществ, то есть определить гены, кодирующие соответствующие измененные белковые продукты.
В клинической практике наибольшее значение имеет полиморфизм генов, ответственных за синтез ферментов, катализирующих метаболические процессы, например процессы окисления с участием системы цитохрома Р450 (фермент CYP2D6), ацетилирования с участием N-ацетилтрансферазы, S-метилирования (тиопуринметилтрансфераза), а также гидролиза эфиров (псевдохолинэстераза). Полиморфизм генов или кодируемых ими энзимов существенно влияет на метаболизм и соответственно на фармакокинетику и фармакодинамику большого количества лекарственных средств. Генетические исследования позволят с помощью аллельспецифической амплификации ДНК и генотипирования определять эффективную дозу лекарственного препарата и предупреждать случаи лекарственной токсичности, особенно для препаратов с ограниченной широтой терапевтического действия.
Генетические вакцины
Вакцины являются одним из важнейших достижений современной медицины. Благодаря их применению удалось ликвидировать многие смертельно опасные заболевания, воспрепятствовать распространению тяжелых болезней. Однако в отношении некоторых заболеваний обычные методы вакцинации являются неэффективными. Поэтому необходимы принципиально новые вакцины.
Перспективными считаются вакцины, созданные на основе генетического материала, участков молекул ДНК или РНК. Генетические вакцины могут обладать высокой иммуногенностью живых аттенуированных вакцин (поскольку они способны стимулировать как гуморальный, так и клеточный иммунный ответ) и безопасностью сплит- или субъединичных вакцин. Принцип действия генетических вакцин основан на введении в клетки человека только тех участков цепочки ДНК (плазмид) возбудителя, которые при поступлении в ядро клетки индуцируют синтез антигенных белковых молекул. В настоящее время несколько генетических вакцин находятся на различных стадиях разработки и даже проводится I фаза их клинических исследований.
Результаты, полученные при изучении генома человека, используют в фармацевтической промышленности. В патогенезе любого заболевания можно выделить генетический компонент, касается ли это наследственной патологии или реакции организма на воздействие различных вредных факторов окружающей среды, таких, как вирусы, токсины, канцерогены и др. По некоторым оценкам более 50 тыс. генов могут служить потенциальными «мишенями» (объектами) для фармакологического воздействия. Для сравнения: за последние 50 лет объектом изучения стали 500 биологических «мишеней». Все больше компаний занимаются исследованиями в области биотехнологий. По данным Consulting Resources Corporation Newsletter (1999), объем продаж такими компаниями технологий и продукции, полученной на основе использования ДНК, в 2009 г. превысит 45 млрд долларов.
В результате выполнения HGP ученые получат возможность исправлять нарушения в функционировании определенных генов. Разработка принципиально новых лекарственных средств ускорится благодаря более глубоким знаниям об этиологии полигенетических заболеваний, таких, как сахарный диабет, артериальная гипертензия, болезни сердца и новообразования. Использование баз данных HGP, доступных для общего пользования (например, генетическая база данных «GenBank» Национальных институтов здоровья США), ускорит создание олигонуклеотидных лекарственных средств, которые способны изменять транскрипцию ДНК. При разработке медикаментов, основу которых будут составлять белковые молекулы, особо полезной станет возможность пользоваться базами данных о последовательностях ДНК. Это облегчит прогнозирование трехмерной структуры белков и их функции. Кроме того, базы данных HGP облегчат поиск неорганических действующих веществ для лечения людей, относящихся к группам риска развития наследственных заболеваний, а также разработку стратегии исследования специфических лекарственных средств. Поэтому многие специалисты считают, что XXI век будет столетием компьютерных и биотехнологий.
Андрей Спасокукоцкий


Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим