FDA одобрило новый препарат для профилактического лечения мигрени
Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) одобрило Aimovig (эренумаб) для профилактики мигрени у взрослых. Лечение проводится ежемесячными единоразовыми самоинъекциями. Aimovig — первый препарат для профилактики мигрени нового класса, механизм действия которого заключается в блокировке активности пептида, связанного с геном кальцитонина, — одной из основных молекул, которые провоцируют приступ мигрени. «Aimovig предоставляет […]
FDA одобрило препарат для лечения рассеянного склероза у детей
Управление по контролю за пищевыми продуктами и лекарственными средствами США (U.S. Food and Drug Administration — FDA) одобрило Gilenya (финголимод) для лечения рецидивирующего рассеянного склероза у детей и подростков в возрасте от 10 лет и старше. Это первое одобрение FDA препарата для лечения рассеянного склероза у пациентов педиатрического профиля. Gilenya был впервые одобрен FDA в 2010 г. для лечения взрослых с рецидивирующим рассеянным […]
Через 2 года после запуска инициативы PRIME получены первые заявки на одобрение ЕМА
Цель данной инициативы — поддержка разработки новых препаратов, которые могут иметь терапевтическое преимущество по сравнению с существующими методами лечения или выгоду для здоровья пациентов с заболеваниями, не поддающимися терапии
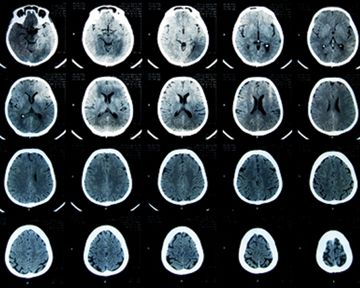
Нові дані щодо впливу променевої терапії на кількість гадолінію, що осаджується в мозку дітей
У травневому номері «Radiology» опубліковано попередні результати дослідження застосування контрастних засобів у педіатричній практиці, отримані науковцями Дитячої лікарні Лос-Анджелеса (Children’s Hospital Los Angeles), США. Чи впливає променева терапія при лікуванні пухлин головного мозку на кількість гадолінію, що осаджується в мозку дітей, які отримували контрастні засоби на основі гадолінію (Gadolinium-Based Contrast Agents — GBCA) під час МРТ-сканування? На це питання шукали відповідь дослідники. «Результати дослідження […]
В Европе обновили рекомендации относительно состава сезонной вакцинации от гриппа 2018/2019
Европейское агентство по лекарственным средствам (European Medicines Agency — EMA) выпустило обновленные рекомендации Европейского Союза (ЕС) о штаммах вируса гриппа, которые производители должны включить в состав вакцины для предотвращения сезонного гриппа с осени 2018 г. В настоящее время рекомендации также содержат решение о подходящих штаммах для живых, ослабленных (аттенуированных) вакцин. Был также обновлен список реагентов для стандартизации вакцин. Подробная информация, такая […]
В США одобрен первый препарат для терапии редкой унаследованной формы рахита
Управлением по контролю за пищевыми продуктами и лекарственными средствами США (U.S. Food and Drug Administration — FDA) одобрило Crysvita (буросумаб), первый препарат, предназначенный для лечения взрослых и детей в возрасте с 1 года с Х-сцепленной гипофосфатемией — редкой, унаследованной формой рахита. Это заболевание вызвано низким уровнем фосфора в крови, что приводит к нарушению роста и развития костей у детей и подростков и проблемам с минерализацией костей на протяжении всей жизни пациента. […]
Препарат Keytruda может помочь предотвратить рецедив меланомы
В новом исследовании утверждается, что вследствие приема препарата Keytruda после операции по прогрессирующей меланоме значительно снизился риск возвращения (рецидива) заболевания. В мае прошлого года Keytruda (pembrolizumab) стала первым лекарственным средством, одобренным Управлением по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) для борьбы с раковыми заболеваниями, основанным на специфическом генотипе опухолей, а не на их локализации. Доктор Дорис […]
Повышение надзора за производством АФИ за счет международного сотрудничества
Европейское агентство по лекарственным средствам (European Medicines Agency — EMA) и его европейские и международные партнеры успешно укрепили свои взаимоотношения для улучшения надзора за производителями активных фармацевтических ингредиентов (АФИ) во всем мире. Об этом утверждается в докладе Международной программы инспекции АФИ на 2011–2016 гг. (International API inspection programme report for 2011–2016), опубликованном 12 апреля. Это международное сотрудничество позволяет обмениваться информацией о результатах инспекций […]
Клинические исследования и клиническая практика. Европейский подход к преодолению разрыва эффективность-результативность
В «Еженедельнике АПТЕКА» № 11 (1132) от 19 марта 2018 г. мы рассказали читателям о новых подходах к определению эффективности и безопасности лекарственных средств и таком явлении, как разрыв эффективность-результативность (efficacy-effectiveness gap). В продолжение темы рассмотрим, насколько результаты клинических исследований соответствуют реальной клинической практике и какие подходы к преодолению разрыва эффективность-результативность применяются в странах ЕС. КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ В последнее время регуляторные органы, агентства по оценке технологий здравоохранения, операторы здравоохранения и фармацевтического […]
Аптечне виготовлення ліків: система якості та оцінка ризиків — світовий догмат
Екстемпорал вбачається найгуманнішим і «найчистішим» сегментом фармації, оскільки не містить елементу комерційної конкуренції — завжди двигуна для торгівлі, однак часто-густо гальма для лікування. Тішить він серце лікаря...
Виробництво ліків
Про те, що дозволяє фармацевтичним компаніям йти в ногу з часом і
випереджати конкурентів: інновації, дослідження, технології або просто ― Research&Development.
У найближчі 5 років великі виробники оригінальних препаратів зіткнуться з проблемою закінчення термінів ринкової ексклюзивності для багатьох продуктів, що суттєво змінить ситуацію у сфері виробництва ліків. Аналітики вже
охрестили період 2010–2011 років. патентною чорною діркою, оскільки обсяг продажу
гігантів, які випускають брендовану продукцію, зменшиться на 28%. Проблема
Фарми не так у закінченні дії патентів, як у тому, що продажі нових
препаратів із чинним патентним захистом не зможуть заповнити втрати.
Фармацевтичне виробництво стоїть перед нелегким вибором нових рішень.
Якими будуть ці рішення, ви зможете дізнатися з публікацій у розділі R&D, де
висвітлено найактуальніші питання створення та виробництва лікарських засобів. Найсвіжіші новини про створення лікарських препаратів, їх лончі на ринку, про
схвалення або відкликання препаратів на світових ринках та в Україні ви зможете дізнатися
на сайті www.apteka.ua