Згідно з повідомленням МОЗ України новий Національний перелік базується на 19-му виданні Базового переліку основних лікарських засобів, рекомендованих ВООЗ. Він складається з основного переліку, до якого включені лікарські засоби для лікування пріоритетних патологічних станів; додаткового переліку, до якого включені лікарські засоби для пріоритетних патологічних станів, що потребують спеціалізованого діагностичного або моніторингового обладнання та/або спеціалізованої медичної допомоги, та/або підготовки фахівців. Національний перелік містить зареєстровані та незареєстровані в Україні лікарські засоби за міжнародними непатентованими назвами. Препарати поділені за групами захворювань.
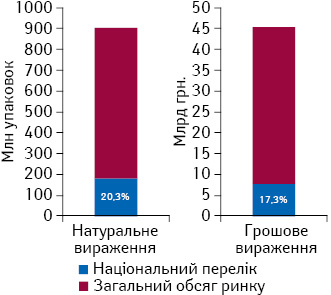
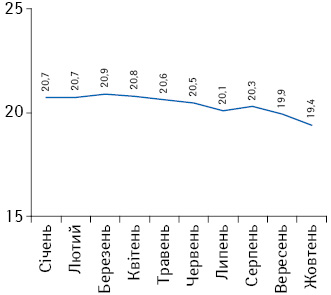
За підсумками 10 міс 2016 р. загальні обсяги аптечного продажу та госпітальних закупівель лікарських засобів становлять 45,3 млрд грн. за 903 млн упаковок. У досліджуваний період сумарна частка лікарських засобів, включених до нового Національного переліку, охоплює близько 17% ринку в грошовому і 20% в натуральному вираженні (рис. 1). Середня роздрібна націнка на лікарські засоби, включені до Національного переліку, за підсумками 10 міс поточного року становить у жовтні 19,4% (рис. 2).
В новий Національний перелік не включено близько 90 міжнародних непатентованих назв лікарських засобів у порівнянні із 19-м виданням Базового переліку основних лікарських засобів, рекомендованих ВООЗ (таблиця). У повідомленні не визначено, яким саме нормативно-правовим актом затверджений новий Національний перелік. На сьогодні залишається чинним Національний перелік основних лікарських засобів, затверджений постановою КМУ від 25.03.2009 р. № 333. Відповідно, незрозуміло, який статус має новий Національний перелік.
| Таблиця | Перелік МНН, які включені в 19-те видання примірного переліку ВООЗ, але не включені в Національний перелік основних лікарських засобів в Україні |
| № п/п | МНН |
|---|---|
| 1 | hyoscine hydrobromide |
| 2 | albendazole |
| 3 | levamisole |
| 4 | mebendazole |
| 5 | niclosamide |
| 6 | praziquantel |
| 7 | pyrantel |
| 8 | diethylcarbamazine |
| 9 | ivermectin |
| 10 | triclabendazole |
| 11 | oxamniquine |
| 12 | trimethoprim |
| 13 | clofazimine |
| 14 | saquinavir |
| 15 | lamivudine + nevirapine + stavudine |
| 16 | lamivudine + nevirapine + zidovudine |
| 17 | ombitasvir + paritaprevir + ritonavir |
| 18 | diloxanide |
| 19 | metronidazole |
| 20 | miltefosine |
| 21 | paromomycin |
| 22 | sodium stibogluconate or meglumine antimoniate |
| 23 | amodiaquine |
| 24 | artemether |
| 25 | artemether + lumefantrine |
| 26 | artesunate |
| 27 | artesunate + amodiaquine |
| 28 | artesunate + mefloquine |
| 29 | mefloquine |
| 30 | primaquine |
| 31 | quinine |
| 32 | sulfadoxine + pyrimethamine |
| 33 | proguanil |
| 34 | pyrimethamine |
| 35 | pentamidine |
| 36 | suramin sodium |
| 37 | eflornithine |
| 38 | melarsoprol |
| 39 | nifurtimox |
| 40 | benznidazole |
| 41 | whole blood |
| 42 | miconazole |
| 43 | selenium sulfide |
| 44 | terbinafine |
| 45 | mupirocin |
| 46 | potassium permanganate |
| 47 | silver sulfadiazine |
| 48 | betamethasone |
| 49 | calamine |
| 50 | benzoyl peroxide |
| 51 | coal tar |
| 52 | podophyllum resin |
| 53 | salicylic acid |
| 54 | urea |
| 55 | benzyl benzoate |
| 56 | permethrin |
| 57 | ethinylestradiol + levonorgestrel |
| 58 | ethinylestradiol + norethisterone |
| 59 | levonorgestrel |
| 60 | estradiol cypionate + medroxyprogesterone acetate |
| 61 | medroxyprogesterone acetate |
| 62 | norethisterone enantate |
| 63 | clomifene |
| 64 | HPV vaccine |
| 65 | pneumococcal vaccine |
| 66 | rotavirus vaccine |
| 67 | Japanese encephalitis vaccine |
| 68 | yellow fever vaccine |
| 69 | tick-borne encephalitis vaccine |
| 70 | cholera vaccine |
| 71 | hepatitis A vaccine |
| 72 | meningococcal meningitis vaccine |
| 73 | typhoid vaccine |
| 74 | influenza vaccine (seasonal) |
| 75 | varicella vaccine |
| 76 | bevacizumab |
| 77 | ascorbic acid |
| 78 | calcium |
| 79 | nicotinamide |
| 80 | pyridoxine |
| 81 | retinol |
| 82 | riboflavin |
| 83 | sodium fluoride |
| 84 | thiamine |
| 85 | acetic acid |
| 86 | xylometazoline |
У проекті постанови КМУ «Про референтне ціноутворення», яка оприлюднена на офіційному сайті МОЗ 17 листопада 2017 р., зазначено, що референтне ціноутворення поширюватиметься на препарати, включені до Національного переліку та списку лікарських засобів, що підлягають відшкодуванню. Нагадаємо, що до проекту переліку ліків, що підлягають реімбурсації, включено 21 молекулу. На сьогодні достеменно невідомо, на які переліки розповсюджуватимуться референтне ціноутворення та обмеження оптових та роздрібних надбавок. Незрозумілою також виглядає ситуація з препаратами інсуліну, які входять до нового Національного переліку. На них має поширюватися референтне ціноутворення відповідно до Порядку, який МОЗ України має розробити. Проте наказом МОЗ України від 21 листопада 2016 р. № 1264 затверджений реєстр референтних цін на препарати інсуліну. Порядок розрахунку референтних цін на них базується на цінах в 7 референтних країнах. А відповідно до проекту постанови КМУ «Про референтне ціноутворення» референтна ціна препаратів, включених до Національного переліку, визначатиметься серед 5 референтних країн.
Слід нагадати, що 9 листопада Уряд ухвалив постанови щодо референтного ціноутворення та реімбурсації. Але станом на 25.11.2016 р. вони не опубліковані.
Під час зустрічі Прем’єр-міністра України Володимира Гройсмана з представниками фармгалузі оператори ринку висловлювали занепокоєння з приводу того, що заявники можуть не встигнути вчасно зареєструвати оптово-відпускні ціни на лікарські засоби. А від оптово-відпускної ціни мають розраховуватися оптові та роздрібні націнки. Крім того, якщо обмежити для лікувально-профілактичних закладів закупівлі виключно ліками, які входять до Національного переліку, й не надати їм можливості придбавати за бюджетні кошти препарати, що входять до протоколів лікування, але не включені до цього переліку, то у закладів охорони здоров’я, особливо вузькопрофільних, не буде змоги забезпечити пацієнтів необхідними препаратами. Національний перелік включає лікарські засоби для задоволення базових потреб системи охорони здоров’я, але цього недостатньо для надання медичної допомоги.
Протягом майже 10 останніх років кожен новий Уряд вимагає від фармацевтичного бізнесу зниження цін на лікарські засоби. Нагадаємо, що у 2008 р. фармринок пережив аналогічну ситуацію, коли через непродумані дії Уряду реалізація лікарських засобів в аптечних закладах зупинилася. Тоді було ухвалено постанову КМУ від 17.10.2008 р. № 955, яка у першій редакції передбачала встановлення 10% оптової та 15% роздрібної націнки. Ця Урядова ініціатива призвела до страйку фармацевтичних працівників, і Віктор Ющенко, на той час Президент України, своїм Указом був вимушений зупинити дію низки постанов КМУ, у тому числі й № 955.
Пізніше наступні Уряди також робили спроби регулювати роздрібні націнки. Навіть запроваджувалися регресивні, які нещодавно були скасовані у рамках дерегуляції, й ринок повернувся до 25% граничної роздрібної надбавки на регульовані ліки.
Сьогодні Уряд знову взявся за регуляцію націнок, при цьому лунають пропозиції встановити роздрібну — на рівні 15% оптово-відпускної ціни. Це означає, що фактична роздрібна націнка становитиме 5–7%. Таке обмеження призведе до закриття невеликих аптек та консолідації ритейлу.
Якщо нова регуляція набуде чинності з 1 січня 2017 р. і розповсюджуватиметься на Національний перелік, то роздрібна реалізація та госпітальні закупівлі регульованих лікарських засобів зупиняться з об’єктивних причин. Справа у тому, що нараховувати націнки аптечні підприємства та дистриб’ютори мають на оптово-відпускну ціну, яка має розраховуватися з використанням механізму референтного ціноутворення. Це також ми вже проходили у 2011 р., коли замість декларування оптово-відпускних цін була запроваджена їх реєстрація. Ця ініціатива проіснувала недовго та була скасована, оскільки процедура реєстрації оптово-відпускних цін тривала дуже повільно та містила значну корупційну складову, що майже зупинило державні закупівлі.
Аптеки як заклади охорони здоров’я мають попередити пацієнтів про можливі перебої та забезпечити пацієнтів необхідним запасом лікарських засобів.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим