?
ЦЕФАРАНСИН
НАДЕЖНОЕ СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЛЕЙКОПЕНИИ У БОЛЬНЫХ, ПОДВЕРГШИХСЯ ХИМИО- И РАДИОТЕРАПИИ
«Томен Корпорейшн» — крупная торговая компания, которая, согласно данным журнала «Форчун», занимает 7-е место по объему продаж в Японии и 145-е — в мире. Штаб-квартира корпорации находится в Токио и Осаке. В настоящее время в корпорации, которая была основана в 1920 г., работают более чем 2600 человек, капитал составляет 32,2 трлн иен. Общий объем продаж продукции «Томен Корпорейшн» в 2000 г. составлял 1,225 трлн иен, общая операционная прибыль — 55,258 млрд иен, а чистый доход — 16,786 млрд иен. «Томен Корпорейшн» осуществляет коммерческую деятельность в области агрохимии, фармации, ветеринарии, легкой и тяжелой промышленности, средств коммуникации и альтернативной энергетики. В январе текущего года «Томен Корпорейшн» и компания «Ничимен» объявили о слиянии, целью которого является осуществление совместной деятельности в области агрохимии, фармации и ветеринарии. Вновь созданная компания, получившая название «Ариста Лайф Сайенс Корпорейшн», является одним из мировых лидеров в сфере агрохимии.
В 1996 г. открылось представительство «Томен Корпорейшн» в Украине, перед сотрудниками которого была поставлена задача — продвигать на украинский рынок агрохимическую, а с 2000 г. — фармацевтическую продукцию компании.
«Томен Корпорейшн» представляет препараты ведущих японских поизводителей — компаний «Ниппон Каяку», «Киова Хакко», «Санкио», «Такеда», «Мейджи Сейка», «Какен Шояку». В планах представительства продвижение на украинский фармацевтический рынок препаратов компании, предназначенных для лечения онкологических заболеваний.
24 мая в конференц-зале Института онкологии АМН Украины состоялся научно-практический симпозиум на тему «Презентация нового японского препарата ЦЕФАРАНСИН в Украине». Д-р Минору Оно, директор отдела исследований и развития компании «Какен Шояку» (Токио) и д-р Нобуо Такейчи, директор Медицинской клиники заболеваний щитовидной железы (Хиросима), в своих выступлениях привели доказательства, подтверждающие высокую эффективность ЦЕФАРАНСИНА в лечении лейкопении у больных онкологического и гематологического профиля. Кроме того, были представлены результаты экспериментальных исследований, касающиеся тонких молекулярных механизмов действия препарата.
ЦЕФАРАНСИН является фармакологически активным экстрактом из растения Stephania cepharantha. Фирма «Какен Шояку» производит ЦЕФАРАНСИН в форме таблеток, растворов для инъекций, порошка в различных дозах. В настоящее время в Украине препарат зарегистрирован в форме таблеток по 1 мг № 100.
Одна таблетка данного лекарственного средства содержит 1 мг сухого экстракта бис-бензилизохинолиновых алкалоидов, таких, как цефарансин, бербамин и изотетрандрин, выделенных их клубней Stephania cepharantha Hayata [1]. Указанные алкалоиды обладают мощными иммуномодулирующими свойствами, а также способствуют увеличению количества лейкоцитов в крови, что позволяет использовать ЦЕФАРАНСИН для лечения лейкопении, вызванной применением цитостатиков и воздействием ионизирующего излучения. К преимуществам препарата относятся отсутствие токсического воздействия даже при применении в высоких дозах [2], а также способность угнетать проявления интоксикации [3].
ПРОБЛЕМЫ СОВРЕМЕННОЙ ХИМИО- И РАДИОТЕРАПИИ
Химиотерапия и радиотерапия являются современными и эффективными методами лечения ряда онкологических заболеваний. Однако применение интенсивных программ химио- и радиотерапии может привести к развитию побочных эффектов, в частности лейкопении, вследствие токсического воздействия цитостатиков и радиоактивного излучения как на стволовые мультипотентные клетки костного мозга, так и непосредственно на лейкоциты. Возникающее при этом состояние вторичного иммунодефицита является благоприятным фоном для манифестации оппортунистической инфекции, что чревато септическими осложнениями и летальным исходом. Кроме того, может развиться одно из тяжелых осложнений цитостатической и радиотерапии — алопеция (облысение).
|
По этой причине использование химиопрепаратов и радиоактивного облучения в онкологической практике существенно ограничено. Фактически лейкопения вынуждает врача прекратить дальнейшее проведение химио- и радиотерапии. К сожалению, у некоторых больных лейкопения развивается раньше, чем наступает ремиссия. Вследствие этого существенно ухудшается прогноз и сокращается продолжительность жизни пациентов.
Существует острая потребность в лекарственных средствах, которые могли бы уменьшить токсическое воздействие цитостатиков и радиоактивного облучения на белые кровяные тельца и стволовые мультипотентные клетки костного мозга и замедлить развитие лейкопении. Это существенным образом расширило бы возможности химио- и радиотерапии и в ряде случаев позволило бы достичь полной ремиссии, а следовательно, увеличить продолжительность жизни пациентов.
МЕХАНИЗМ ДЕЙСТВИЯ ЦЕФАРАНСИНА
Цефарансин, основной компонент препарата ЦЕФАРАНСИН, является мембранотропным соединением, которое эффективно встраивается в фосфолипидный бислой клеточных мембран, стабилизируя их [4]. Известно, что при интоксикациях различного происхождения активируются процессы свободнорадикального окисления. При этом образуются активные формы кислорода, которые, вступая во взаимодействие с молекулами воды, образуют высокоактивные перекисные соединения, способные повреждать фосфолипиды мембран, белки и ДНК. Активация процессов свободнорадикального окисления в стволовых клетках костного мозга приводит к нарушению гемопоэза с последующим развитием лейкопении и вторичного иммунодефицита. Цефарансин эффективно подавляет процессы свободнорадикального окисления в клетках различных тканей, защищает липидный бислой от деструкции [5] и стабилизирует клеточную мембрану лейкоцитов, предохраняя эти клетки от деструкции. При этом цефарансин не угнетает их фагоцитарную функцию. Необходимо обратить внимание на тот факт, что цефарансин оказывает антилейкопеническое действие за счет стимулирующего влияния как на выход лейкоцитов [6], главным образом нейтрофильных гранулоцитов и лимфоцитов, из периферических депо, так и на стволовые гемопоэтические мультипотентные клетки костного мозга [7]. Учитывая перечисленные выше свойства цефарансина, обоснованным является применение препарата ЦЕФАРАНСИН в онкологической практике для профилактики и лечения лейкопении.

В работе симпозиума приняли участие директор Института онкологии АМН Украины, доктор медицинских наук, профессор С.А. Шалимов и заместитель директора по клинической работе, доктор медицинских наук А.А. Литвиненко
На сегодняшний день известны и другие важные аспекты фармакологического действия цефарансина. Результатами многочисленных исследований подтверждена важная роль фосфолипазы А2 (отщепляет главным образом арахидоновую кислоту от фосфатидилинозитола и фосфатидилхолина) и С (расщепляет фосфатидилинозитол и фосфатидилхолин на диацилглицерол и фосфорилированное основание) в процессах сигнальной трансдукции в клетке. При злокачественной трансформации и пролиферации клеток нарушаются процессы сигнальной трансдукции с участием этих фосфолипаз. В частности, такие известные стимуляторы злокачественной трансформации, как форболовые эфиры, способствуют накоплению диацилглицеролов, которые, активируя протеинкиназу С, вызывают неконтролируемый рост клеток [8].
Цефарансин эффективно подавляет активность указанных ферментов. Возможно, этим обусловлен и прямой противоопухолевый эффект [9, 10].
Кроме того, цефарансин оказывает выраженное иммуномодулирующее действие. Он эффективно подавляет репликацию некоторых ретровирусов, в том числе ВИЧ-1, активированную фактором некроза опухолей-альфа и форболовыми эфирами вследствие ингибирования экспрессии гена, отвечающего за воспроизводство данного вируса в моноцитах [11].
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА ЦЕФАРАНСИНА
ЦЕФАРАНСИН обладает широким спектром действия. Доказано, что в случае угнетения гемопоэза, вызванного влиянием радиоактивного облучения или применением цитостатических противоопухолевых средств, препарат восстанавливает кроветворение за счет активации клеток-предшественников и выхода белых кровяных телец из периферических депо. Препарат устраняет дисфункцию иммунокомпетентных клеток, уменьшает цитотоксическое воздействие химиопрепаратов и радиоактивного излучения на стволовые клетки костного мозга, нормализует продукцию антител и процессы активации макрофагов. ЦЕФАРАНСИН эффективно предотвращает развитие лейкопении, не влияя на содержание тромбоцитов в крови [12]. Имеются данные о благоприятном влиянии данного лекарственного средства на клиническую картину тромбоцитопенической пурпуры [13].
|
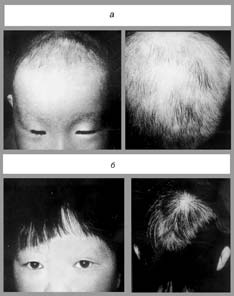
Волосяной покров пациентки, которой проводили химиотерапию: а – до назначения ЦЕФАРАНСИНА; б – после назначения ЦЕФАРАНСИНА |
ЦЕФАРАНСИН эффективно устраняет алопецию, вызванную приемом в высоких дозах цитостатиков и радиоактивным облучением. На фото можно видеть состояние волосяного покрова до и после лечения ЦЕФАРАНСИНОМ у девочки в возрасте 6 лет, которой была проведена химиотерапия. Назначение маленькой пациентке данного препарата привело к полному восстановлению волосяного покрова головы. Результаты биохимических исследований свидетельствует также о способности данного препарата эффективно восстанавливать структуру и функцию волосяного аппарата [14].
Цефарансин тормозит вызванную комплексом антиген—антитело реакцию выделения гистамина тучными клетками, обладает способностью повышать уровень адренокортикотропного гормона в крови вследствие стимулирующего влияния на гипофиз, что позволяет увеличить резервы адаптации у больного, которому проводится химио- и радиотерапия [15].
Ценным свойством цефарансина является его способность стимулировать избирательную аккумуляцию некоторых химиопрепаратов в раковых клетках [16]. Более того, данный алкалоид обладает способностью противодействовать развитию резистентности опухолевых клеток к цитостатикам [17].
ФАРМАКОКИНЕТИКА ЦЕФАРАНСИНА
При пероральном приеме в пищеварительном тракте всасывается более 70% препарата. После перорального приема однократной дозы препарата (10–60 мг) его концентрация в плазме крови у взрослых быстро повышается, достигая максимума в течение 1,1–2,5 ч, и снижается однофазно, при однократном приеме в дозе 120 мг — достигает максимальных значений в течение 1,2±0,3 ч и снижается двухфазно.
Действующие компоненты ЦЕФАРАНСИНА связываются с белками сыворотки крови. Уровень связывания после перорального приема составляет 73,9; 93 и 97,5% через 2, 10 и 24 ч соответственно. Высокое содержание ЦЕФАРАНСИНА отмечено в печени, легких, селезенке, почках, надпочечниках, щитовидной железе и гипофизе, низкое — в центральной нервной системе.
Метаболизм ЦЕФАРАНСИНА происходит в печени. Препарат выводится в основном с калом в виде полярных соединений. Более 70% препарата выводится с калом в течение 48 ч, с мочой — 5–6%. Период полувыведения составляет 4–9 ч при приеме в дозе 10–60 мг, при приеме в дозе 120 мг распад препарата происходит двухфазно — 1-я фаза составляет 3 ч, 2-я — 17 ч.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ, РЕЖИМ ДОЗИРОВАНИЯ, ВЗАИМОДЕЙСТВИЕ
Показанием к применению ЦЕФАРАНСИНА является лейкопения, обусловленная радиоактивным облучением и/или применением цитостатических препаратов.
ЦЕФАРАНСИН назначают перорально после еды в суточной дозе 3–6 мг, разделенной на 2–3 приема. Дозу препарата устанавливают индивидуально в зависимости от возраста пациента и тяжести заболевания.
Побочные эффекты незначительны и проявляются редко. В единичных случаях регистрировали головную боль и тошноту, иногда — нарушения со стороны пищеварительной системы (потеря аппетита, дискомфорт в эпигастральной области, диарея). Единственным противопоказанием к применению ЦЕФАРАНСИНА является повышенная чувствительность к его компонентам.
ЦЕФАРАНСИН потенцирует действие противомалярийного препарата хлорохина и противоопухолевых цитостатиков — алкалоидов барвинка (винкристин, винбластин и виндезин), доксорубицина, этопозида, флуороурацила, а также повышает избирательность их действия и позволяет избежать развития резистентности раковых клеток к химиопрепаратам.
|
Препарат нетоксичен. При исследовании влияния данного лекарственного средства, применяемого в дозах, которые значительно превышали рекомендованные, признаков острого и хронического отравления препаратом не наблюдалось.
ЗАКЛЮЧЕНИЕ
ЦЕФАРАНСИН является современным лекарственным препаратом, который эффективно устраняет лейкопению и ее клинические проявления, развивающиеся на фоне лечения цитостатическими препаратами и радиотерапии. За счет влияния на тонкие механизмы клеточной регуляции, этот препарат оказывает прямое противоопухолевое и противовирусное воздействие. Низкая токсичность ЦЕФАРАНСИНА позволяет существенно изменять режим дозирования в зависимости от клинических потребностей.
Несомненно, ЦЕФАРАНСИН, зарегистрированный в Украине в апреле текущего года, займет достойное место среди средств для адъювантной терапии при проведении курсов интенсивной лучевой и химиотерапии у больных онкологического и гематологического профиля.
Дистрибьюцией препарата в Украине будут заниматься фирмы «Анна» и «Людмила-Фарм» (г. Киев), которые специализируются на поставках препаратов, предназначенных для лечения онкологических заболеваний.
Дополнительную информацию о препарате ЦЕФАРАНСИН можно получить в представительстве «Томен Корпорейшн», тел./факс: (044) 490-26-93, 461-94-62.
Виктор Маргитич
Фото Евгения Кривши
|
СПИСОК ЛИТЕРАТУРЫ |
|
|



Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим