Перший Національний конгрес з біоетики, що відбувся у вересні (див. «Щотижневик АПТЕКА», № 37(308) від 24 вересня 2001 р.) викликав неабиякий резонанс в українському суспільстві, особливо серед науковців, лікарів, фармакологів та фармацевтів. Виробництво, клінічні випробування, маркетинг та масове застосування лікарських препаратів пов’язані з низкою етичних проблем, яким ще донедавна не приділялося належної уваги. Серед них важлива роль належить питанню побічної дії лікарських засобів.
16 липня 2001 р. МОЗ України видало наказ № 292 «Про удосконалення організації подання інформації про побічну реакцію лікарських засобів» (опублікований у «Щотижневику АПТЕКА», № 30 (301) від 6 серпня 2001 р.), яким започатковано моніторинг побічних реакцій лікарських препаратів в Україні (див. інтерв’ю з керівником відділу фармакологічного нагляду ДП «Державний фармакологічний центр» О.П. Вікторовим у «Щотижневику АПТЕКА», № 31(302) від 13 серпня 2001 р.). Продовжуючи цю тему, пропонуємо вашій увазі матеріали доповідей Володимира Коваленка, директора Інституту кардіології ім. М.Д. Стражеска АМН України, доктора медичних наук, професора, та Олексія Вікторова, керівника відділу фармаконагляду ДП «Державний фармакологічний центр», заввідділом клінічної фармакології Інституту кардіології ім. М.Д. Стражеска, доктора медичних наук, професора, на Першому Національному конгресі з біоетики.
Нині в Україні проводиться активна робота щодо створення та розбудови системи фармакологічного нагляду в структурі ДП «Державний фармакологічний центр». Працівники відділу фармаконагляду займаються питаннями збору інформації про побічні реакції лікарських засобів, що є на фармацевтичному ринку України, з метою здійснення контролю за безпекою застосування лікарських препаратів, а також наукового аналізу отриманих даних. Згідно з наказом № 347 МОЗ України від 19 грудня 2000 р. затверджено Інструкцію про здійснення нагляду за побічними реакціями лікарських засобів (див. «Щотижневик АПТЕКА», № 3 (274) від 22 січня 2001 р.), у якій викладено вимоги до порядку надання інформації про побічні реакції, зафіксовані під час проведення клінічних досліджень або терапії з використанням лікарських препаратів.
Необхідність впровадження системи фармакологічного нагляду за лікарськими засобами пов’язана з етичними проблемами, оскільки спрямована на виконання основного завдання — захист здоров’я і прав людини. Тому ще на етапі клінічного дослідження лікарських засобів інформація про будь-які негативні властивості досліджуваного препарату повинна реєструватися дослідником, замовником (виробником), повідомлятися в етичні комітети та регуляторні органи. Виявлені побічні реакції мають належним чином систематизуватися та аналізуватися. Однак остаточне уявлення про толерантність до лікарського засобу можна отримати тільки в ході його широкого застосування у клінічній практиці. У разі накопичення повідомлень про побічні реакції лікарського засобу може виникнути необхідність вжиття певних адміністративних заходів або прийняття відповідних рішень регуляторного характеру, а саме включити в Інструкцію нові дані про побічні реакції лікарського засобу, виправлену інформацію відносно показань та протипоказань до його застосування, обмеження використання і навіть заборону маркетингу лікарського засобу.
Лікарські препарати розглядають як засоби, що їх використовують з лікувальною метою. Втім таке уявлення є надзвичайно спрощеним. Насправді застосування лікарських засобів тісно пов’язане з низкою медико-біологічних, суспільних, економічних, геоекологічних та інших факторів. Найважливішою вимогою, що її ставлять до лікарських засобів, є забезпечення якомога високої якості життя людини. Тому головними критеріями оцінки якості лікарських засобів, згідно з рекомендаціями ВООЗ, є ефективність, безпека, доступність та прийнятність їх для пацієнта. Не випадково ключовим завданням фармакотерапії є попередження смертності або зниження її показників, а також поліпшення якості життя пацієнта.
Відсутність очікуваної клінічної ефективності фармакотерапевтичних заходів може негативно позначитися на життєдіяльності організму та погіршити результати лікування. Це в свою чергу здатне спричинити погіршення якості життя індивіда та економічні збитки для суспільства в цілому. Крім того, призначення пацієнтові неефективного лікарського засобу може призвести до зниження ефективності фармакотерапії (до рівня плацебо-ефекту), погіршення перебігу захворювання, збільшення частоти госпіталізації, витрат на лікування, показників смертності тощо. Тому, вирішуючи питання про призначення того чи іншого препарату, необхідно враховувати співвідношення користь/ризик. Наприклад, застосування лікарських засобів, що впливають на серцево-судинну систему, може спричинити ризик виникнення як некардіальних побічних ефектів (органна токсичність), так і кардіальних (аритмогенез та негативний інотропний ефект), що пов’язано зі збігом певних об’єктивних та суб’єктивних факторів.
Протягом другої половини XX ст. міжнародна спільнота активно працювала над розробленням правових механізмів інтеграції суспільства, які б гарантували дотримання прав людини у сфері охорони її здоров’я, зокрема, у разі застосування лікарських засобів. У різні роки з’явилися відповідні регулювальні документи ООН, ВООЗ, ЄС, Міжнародної медичної асоціації тощо. Україна у стислі терміни розробила відповідні власні нормативні акти та створила законодавчу базу щодо захисту прав людини у сфері охорони здоров’я, гармонізувавши їх з міжнародними рекомендаціями.
У повсякденну практику вітчизняної медицини впроваджуються критерії, які дають змогу належним чином оцінювати клінічні випробування лікарських засобів та їх практичне застосування з дотриманням етичних норм. Серед них важливими є критерії, що характеризують безпеку лікарського засобу. Здійснювати контроль за безпекою застосування препаратів покликана система фармакологічного нагляду, основним завданням якої є виявлення, вивчення, оцінка та профілактика негативних побічних реакцій. Система фармакологічного нагляду уможливлює гнучку регуляцію взаємин між виробником препарату, лікарем, державною системою охорони здоров’я та пацієнтом.
Згідно з даними ВООЗ, частота побічних реакцій у світовому масштабі досягає 10–20% усіх випадків застосування препаратів. Побічні реакції лікарських засобів є єдиною або основною причиною госпіталізації 3–5% пацієнтів. Летальність, пов’язана із застосуванням лікарських засобів, займає 5-те місце у світі в структурі загальної смертності, поступаючись тільки летальності від захворювань серцево-судинної системи, легень, онкологічної патології і травм, за винятком помилки лікарів та зловживання препаратами, летальність від яких складає 0,1%. Для порівняння: летальність унаслідок хірургічного втручання становить 0,01%.
Побічні реакції лікарських засобів негативно впливають на стан здоров’я населення та на суспільно-економічні показники його життя. За даними фармакоепідеміологічних досліджень, проведених у 1980–1995 pp. у Німеччині, середня тривалість перебування в стаціонарі із цієї причини складає 8,7 доби; середня величина фінансових витрат на госпіталізацію одного хворого — 261 дол. США; загальні витрати — 588 млн дол. США. Фахівці вважають, що в 30,7% випадків госпіталізації можна було б запобігти.
Працівники системи фармакологічного нагляду нашої країни вже отримали деякі попередні дані, що характеризують ситуацію стосовно побічних реакцій лікарських засобів в Україні (рис.1, 2). У 2000 р. в Україні зареєстровано 307 таких випадків. У 29,32% випадків стан хворих унаслідок розвитку побічної реакції лікарського засобу потребував проведення додаткової фармакотерапії. Основними причинами, що сприяють виникненню побічної дії, експерти ВООЗ вважають:
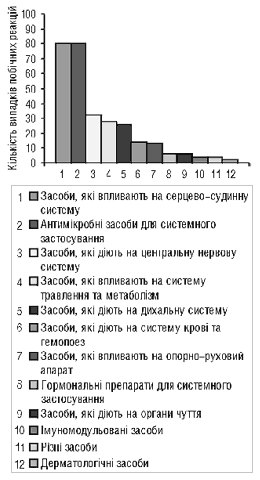
Рис. 1. Групи лікарських засобів (залежно від їх дії на орган або систему, а також від їх хімічних, фармакологічних і терапевтичних властивостей), на які реєструвалися побічні реакції у 2000 p.
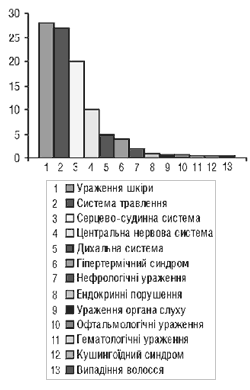
Рис. 2. Структура основних системних уражень при побічних реакціях лікарських засобів (інформація надійшла до Відділу фармаконагляду ДФЦ МОЗ України у 2000 p.)
1. Фактори, не пов’язані з дією лікарських засобів, а саме особливості організму хворого (вік, стать, генетичні особливості, схильність до алергічних реакцій, специфіка перебігу захворювання, шкідливі звички), зовнішні фактори (лікар, який проводить фармакотерапію, навколишнє середовище, умови праці тощо).
2. Фактори, пов’язані з побічною дією лікарського засобу: клініко-фармакологічна характеристика препарату; адекватність вибору препарату; метод застосування препарату; взаємодія лікарських засобів при поліпрагмазії.
Слід окремо наголосити на ймовірності допущення помилок з боку лікарів, медичних сестер та хворих.
Зазначене свідчить про необхідність підвищення пильності усіх, хто бере участь у фармакотерапевтичному процесі. Крім того, існує потреба підвищити пильність щодо виявлення побічної дії лікарських засобів і вжити таких заходів:
-
ретельний аналіз причин, які змусили припинити випробування, та причин смерті;
-
облік індивідуальних реакцій пацієнтів, порівняння небажаних ефектів з даними, що їх отримано в експериментах на тваринах;
-
наявність доказів того, що препарат, який випробовується, є ідентичним тому, що надійшов у роздрібний продаж;
-
всебічна характеристика даних фармакологічних досліджень (фармакодинаміка, фармакокінетика лікарського засобу) ще до початку клінічних досліджень.
Такі заходи дають змогу прогнозувати найповніший перелік як позитивних ефектів, так і побічних реакцій, що виникають унаслідок застосування лікарських засобів.
Організацію та контроль за виконанням етичних норм у разі застосування лікарських засобів згідно із законом України «Про лікарські засоби» покладено на МОЗ України. Інформація про побічні реакції лікарських препаратів може надходити з різних джерел на дореєстраційному (доклінічні та клінічні випробування) та постреєстраційному (спеціальні дослідження та спонтанні повідомлення) етапах. На сьогодні у світі склалася система інтеграційної співпраці та обміну інформацією про побічні реакції лікарських засобів на рівні міжнародних та національних органів охорони здоров’я, фармацевтичних компаній та лікувально-профілактичних установ. Банк даних Центру ВООЗ містить 1,9 млн повідомлень про небажані побічні реакції лікарських засобів. При цьому щороку до Центру надходить близько 200 тис. подібних повідомлень.
Вивчення побічних реакцій лікарських засобів під час клінічних досліджень має деякі суттєві недоліки, зокрема:
-
обмежена кількість хворих і тривалість дослідження порівняно з масштабами застосування препарату після надходження його у продаж;
-
збільшення кількості хворих, які приймають лікарський засіб (після надходження у продаж), без урахування груп ризику в ході клінічних випробувань;
-
неможливість урахування всього спектра взаємодії препарату, який випробовується, з іншими лікарськими засобами.
Лише 15-річний термін перебування лікарського засобу на фармацевтичному ринку за умови широкого його застосування у клінічній практиці може дати більш-менш об’єктивну картину щодо передбачуваних побічних реакцій. Це стосується як оригінальних брендів, так і препаратів-генериків. Стосовно більшості препаратів-генериків, що є на фармацевтичному ринку України, дані про їх хімічну, біологічну і терапевтичну еквівалентність оригінальному препарату відсутні.
Перед призначенням препарату лікар має відповісти на низку запитань:
-
Чи дійсно перебіг захворювання потребує призначення лікарського засобу? Яка мета фармакотерапії?
-
Чи можна досягти належного клінічного ефекту за допомогою певного лікарського засобу?
-
Чи є дані щодо ефективності лікарського засобу?
-
Чи доведено безпеку лікарського засобу?
-
Наскільки вірогідне зменшення тяжкості перебігу захворювання, а також його вплив на якість життя хворого? Яка вірогідність можливої шкоди побічної дії лікарського засобу (співвідношення користь/ризик)?
Окреслено лише деякі принципові питання, пов’язані з етичними проблемами, які виникають під час проведення фармакотерапії, але втілення їх у медичну практику завжди сприятиме здійсненню одного з головних гуманістичних принципів медицини — «не нашкодь». Постійний контроль з боку виробників, лікарів, дослідників та організаторів охорони здоров’я за побічними реакціями лікарських засобів дасть змогу вирішувати етичні проблеми, пов’язані із захистом здоров’я людей та якістю їхнього життя.

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим