Наверное, все помнят иллюстрации, составленные по сценариям, подобным описанному Реза Самени (Sameni R., 2020) (рис. 1). Суть их заключается в том, что, если не введены меры изоляции, социального дистанцирования и т.д., инфекция распространяется в равной степени каждым из зараженных. Учитывая то, что с 22 ноября (первый случай) до 23 января, когда на выезд из Ухани были введены ограничительные меры, столицу Хубэя ежедневно (!) покидали 3300 человек, можно было бы ожидать гораздо более равномерного распределения вспышек, чем оказалось впоследствии (Kucharski A.J. et al., 2020). Особенно принимая во внимание, что Европа начала закрываться почти 2 мес спустя.
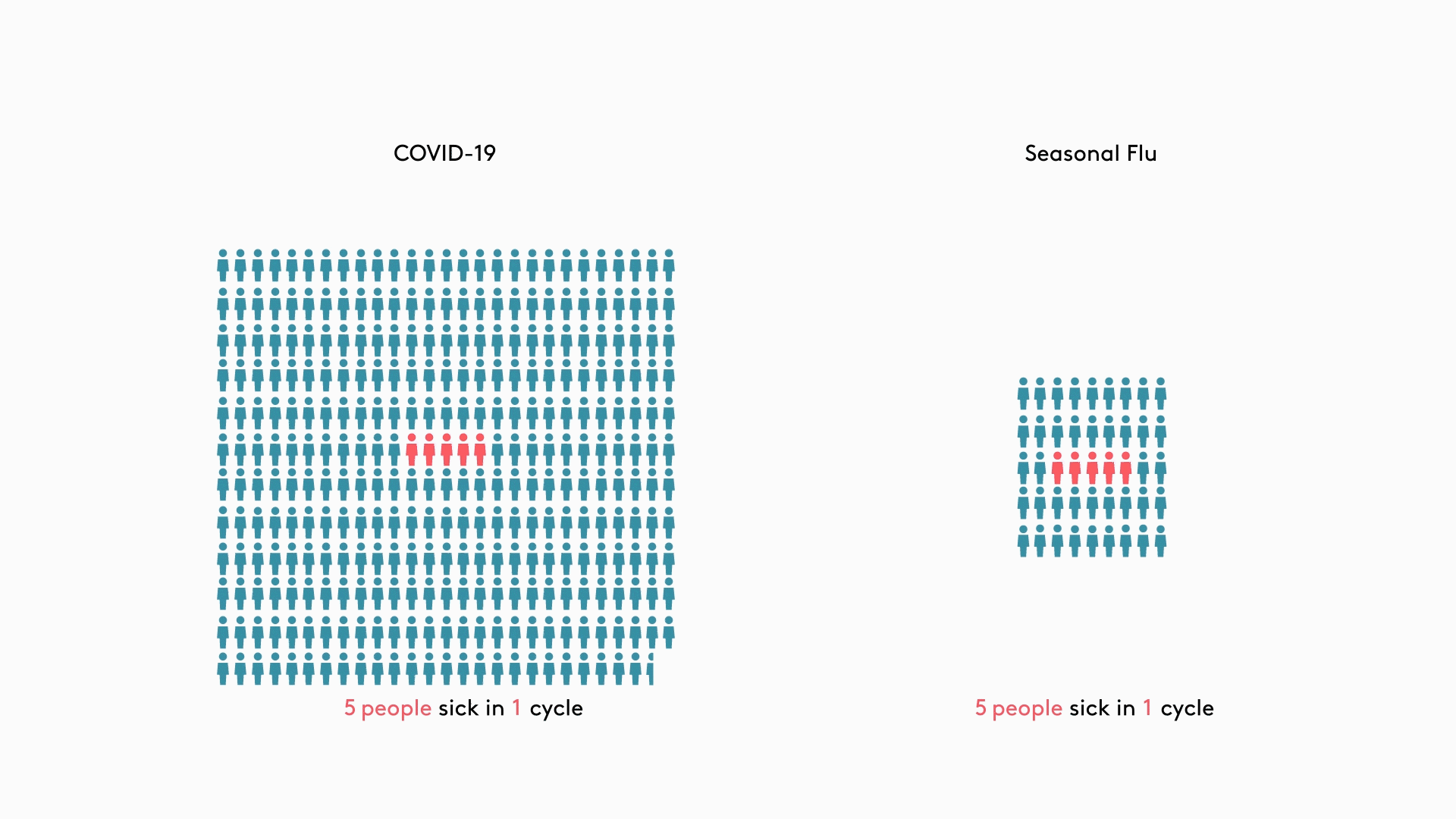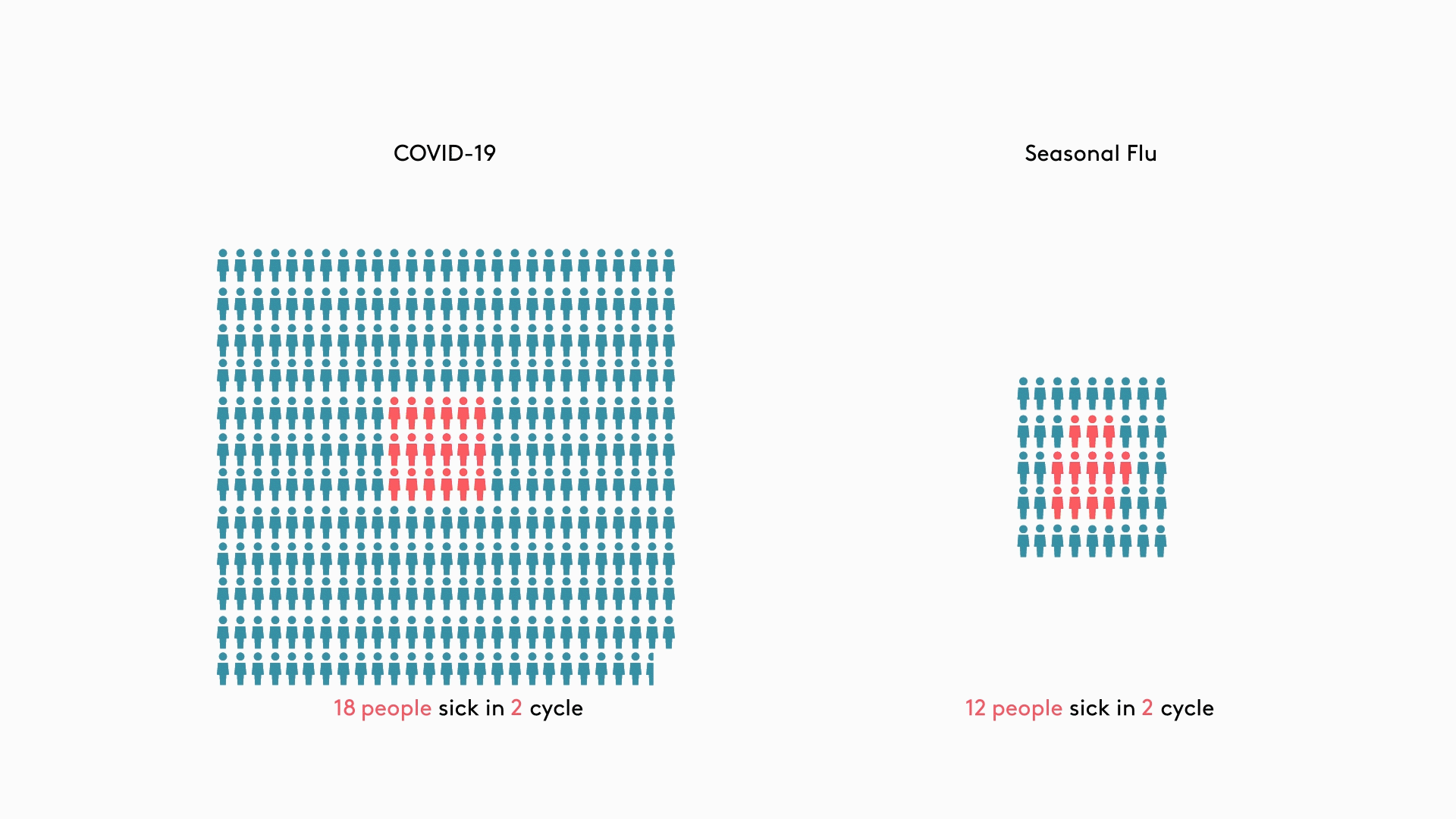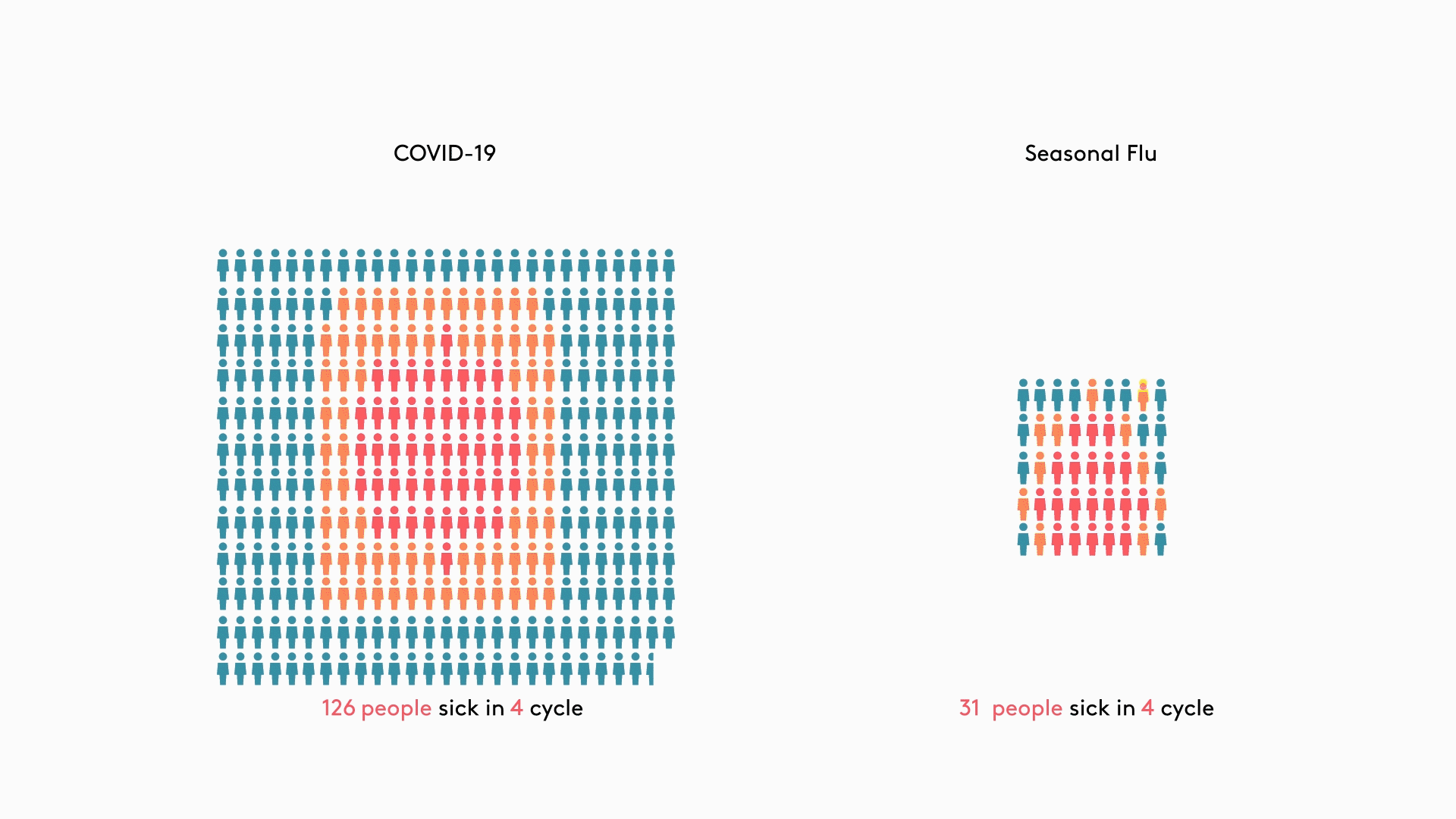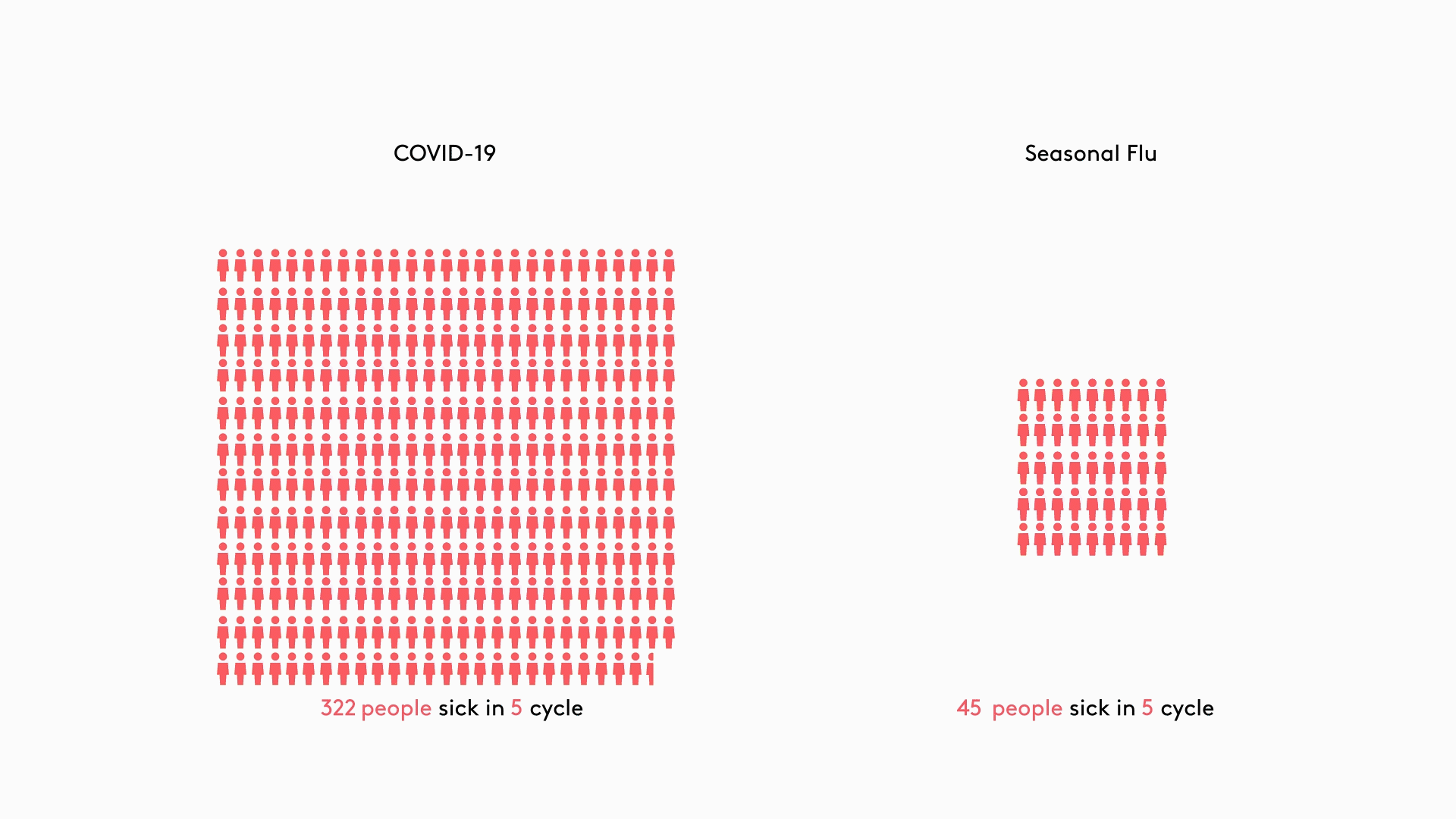
Вирус местами элиминировался, местами накапливался
Похоже, что пациент из Уханя, заболевший в ноябре, — далеко не «нулевой», и новый коронавирус «перепрыгнул» с животных на человека не в конце, а в середине или даже начале осени 2019 г. Так, до начала мая во Франции считалось, что отправной точкой для распространения вируса был департамент Уаза, где первые официальные случаи заражения датировали концом января 2020 г. Потом появилось сообщение о результатах ретроспективной оценки образцов пациентов, госпитализированных с пневмонией со 2 декабря 2019 г. в отделение неотложной терапии одной из больниц департамента Сена-Сен-Дени (регион Иль-де-Франс). «Самый ранний по времени положительный тест на COVID-19 был выявлен в пробе от 27 декабря», — пояснил заведующий отделением профессор Ив Коэн (Yves Cohen). Об этом больном известно, что «его жена была очень больна до него, что после заболел он и заразил своих детей», — отметил врач. В свою очередь, жена пациента с пневмонией, работающая в супермаркете, могла заразиться от людей из Азии в рыбном отделе или от покупателей, тем более что магазин находится поблизости от аэропорта «Шарль-де-Голль».
Однако расследование вспышки COVID-19 во Франции уходит еще глубже. «На востоке Франции есть несколько больниц, в том числе в Гарше, Ла-Пити-Сальпетриере и прочие, которые находятся в процессе продолжения сделанного нами», — пояснил И. Коэн в интервью радиостанции «BFM Paris» 3 мая. Одна из них, госпиталь Альберта Швейцера (Hôpital Albert Schweitzer) в Кольмаре, сообщила в пресс-релизе от 7 мая о первых случаях подозреваемого COVID-19, развившегося 16 ноября 2019 г. Ретроспективная оценка всех материалов компьютерной томографии органов грудной клетки, выполнявшихся в период с 1 ноября по 30 апреля, ведется в данной клинике под руководством заведующего отделением медицинской визуализации Михаэля Шмитта (Michel Schmitt).
Результаты исследования были проанализированы и нанесены на графики, что позволило сделать предварительные выводы:
- первые случаи подозреваемого COVID-19 в этой больнице отмечены 16 ноября;
- до конца февраля заболеваемость прогрессировала очень медленно;
- затем — быстро, с пиком 31.03.2020 г.
Рождественские ярмарки, семейные торжества — эти мероприятия способствовали распространению вируса в конце 2019 г. Затем, после собрания церкви евангелистов в Мюлузе в последнюю неделю февраля, ситуация критически обострилась.
«Несколько специалистов в области здравоохранения отметили этой зимой нетипичные нарушения состояния здоровья у взрослых и детей, первоначально расцененные как грипп: повышенная температура тела и кашель большей продолжительности, чем обычно (2–3 нед), потеря голоса (афония), отсутствие обоняния и вкуса, необычная длительная усталость, уменьшение массы тела», — отмечено в вышеупомянутом пресс-релизе.
Есть еще одна ниточка, связывающая азиатский эпицентр пандемии с остальным миром: VII Всемирные военные игры, проходившие в Ухани 14–29 октября. Есть много свидетельств о заболеваниях спортсменов, развившихся в непосредственной связи со временем проведения игр, скрупулезно собранные «France 24». Так, люксембургский пловец Жюльен Хенкс (Julien Henx) рассказал в эфире радиокомпании «RTL», что двое его товарищей по команде заболели во время соревнований. Сославшись на военного врача, о ряде подобных случаев сообщила также Элоди Кловель (Élodie Clouvel), чемпионка мира по пятиборью. Министерство обороны (Ministère des armées) дало малоинформативный комментарий.
Сведения о ранних вспышках COVID-19 помогают понять характерную последовательность событий: недооценка эпидемиологической опасности нескольких легких случаев — мероприятие со сверхраспространением — большая вспышка — несколько случаев с тяжелым течением = критическая ситуация местного значения. Показательный пример: ситуация на борту авианосца «Шарль-де-Голль» (Charles-De-Gaulle) — двухнедельный карантин после захода в порт г. Брест (Франция) — проигнорированные легкие случаи гриппоподобного заболевания — концерт на борту 30 марта сразу по окончании изоляции «для повышения морального духа» команды — 5 апреля COVID-19 диагностирован у высадившегося в Дании офицера, 7 апреля миссия корабля прервана — COVID-19 подтвержден у 1100 членов экипажа (⅔), о количестве госпитализированных не сообщают, но по состоянию на 11 мая один из моряков все еще находился в больнице.
Большая часть локальных вспышек COVID-19 затухает после минимального количества циклов передачи, еще часть «тлеет» в виде редких малозаметных эпизодов. Ситуация резко меняется при возникновении «событий со сверхраспространением». Если таковые случаются вблизи друг от друга во времени и пространстве, получается наложение «сверхразмерных вспышек» и возникает кризисная ситуация, подобная тем, что наблюдали в наиболее пострадавших регионах.
«ТТТ» — не панацея?
Исходя из вышеизложенного, становится понятно, что о чрезвычайной эпидемиологической опасности «сверхразмерных событий» эксперты должны были проинформировать общественность как можно раньше. Видимо, понимание этого было у властей Японии, Швеции, ограничившихся не самыми жесткими мерами по сдерживанию инфекции. Частичные ограничения + защита уязвимых групп (на родине Астрид Линдгрен с этим в значительной степени опоздали) + эпидемиологический мониторинг с особым упором на «слабые места» — такой «образ жизни» гарантирован Европе на ближайшие год-полтора. При этом повышенный риск крупных вспышек все равно сохраняется.
Тестирование, расследование и отслеживание (testing, tracking and tracing — TTT) — три главных элемента контроля за распространением COVID-19. На пути внедрения этой концепции уже возникают крупные разочарования. Самый недавний яркий пример — вспышка COVID-19 на крупнейшем мясоперерабатывающем предприятии Германии «Tönnies».
Оказывается, после ряда вспышек на заводах других фирм в Германии, Франции и Англии «мясной магнат» Клеменс Тённис (Clemens Tönnies) (имеющий 45% долю во владении гигантом мясной отрасли) внедрил на своих заводах широкое тестирование работников. Еще в апреле он заявлял о готовности проводить своими силами 180–200 тыс. анализов в месяц. Стратегия, похоже, работала, и «Tönnies» наблюдали у себя лишь редкие случаи COVID-19. Заявив еще тогда, что «теперь вся мясная промышленность находится под подозрением», как он мог выпустить ситуацию из-под контроля?
«Tönnies» как место научных изысканий
Как меняется вирулентность возбудителя в зависимости от температуры, влажности? Каким будет течение заболевания, не снизилась ли патогенность вируса? Наконец, какой будет серопревалентность среди инфицированных? Вообще в научную лабораторию сейчас превратился весь мир, и вирус SARS-CoV-2 как будто создан для того, чтобы надолго подчинить его себе. И правда: если бы инфекция имела более тяжелое течение, у нее не было бы такого потенциала «незаметного накопления» в популяции. Если бы он, подобно вирусу атипичной пневмонии (SARS), размножался преимущественно в нижних дыхательных путях с пиком вирусовыделения на 10-е сутки, не были бы такими заразными люди без серьезных симптомов. В отсутствие дыхательной недостаточности как довольно частого позднего симптома, многие случаи относили бы просто за счет обострения хронических заболеваний. Наконец, без «сверхраспространения» SARS-CoV-2 не был бы таким «непредсказуемым и диким».
Без этого феномена пандемии бы не было
Вспышки новых инфекционных заболеваний — MERS-CoV, SARS-CoV и в меньшей степени — лихорадки Эбола, случились «по вине» суперраспространителей (Wong G. et al., 2015). При этом значительная их часть произошла в лечебных учреждениях (Suwantarat N., Apisarnthanarak A., 2015). Футбольные матчи — опаснейшие «сверхразмерные» события в этой пандемии. Так, Италия и Испания долго будут помнить о «нулевой игре» — футбольном матче Лиги чемпионов между «Аталантой» (Бергамо) и «Валенсией» в присутствии 44 тыс. зрителей в Милане (Ломбардии). Мэр Бергамо Джорджио Гори (Giorgio Gori) назвал эту игру «биологической бомбой». Но, возможно то, что не получилось у «мясного магната», смогут осуществить футбольные менеджеры? Кстати, К. Тённис — председатель наблюдательного совета одной из команд Бундеслиги, предлагал футбольным чиновникам возможности своей лаборатории для тестирования игроков. Теперь, по сообщению СМИ, в немецком, а теперь и в итальянском профессиональном футболе в случае подтверждения COVID-19 у члена команды его коллеги смогут выйти на поле, но только после отрицательного результата теста, проведенного в тот же день.
А как «суперраспространение» проявило себя во время вспышек MERS-CoV (в Южной Корее в 2015 г.), SARS-CoV (в Китае в 2002–2003 гг.)?
80% случаев (135 из 166) вызваны тремя пациентами
Вспышка MERS-CoV в Южной Корее в 2015 г. началась с 68-летнего мужчины, посетившего незадолго до этого несколько стран Ближнего Востока, где в то время уже было несколько подтвержденных случаев MERS-CoV (Wong G. et al., 2015). Непосредственно до этого больного были прослежены 29 вторичных инфекций. Кроме того, два из этих вторичных случаев ответственны за 106 из 166 последующих инфекций, известных на тот момент (Cowling B.J. et al., 2015). Заражение происходило преимущественно в нозокомиальных условиях.
Таким образом, вспышка MERS-CoV в Южной Корее была вызвана в основном тремя инфицированными — «суперраспространителями», каждый из которых заразил непропорционально большое количество людей (см. рис. 2А). Данная вспышка MERS-CoV является второй по величине в истории и крупнейшей за пределами Ближнего Востока.
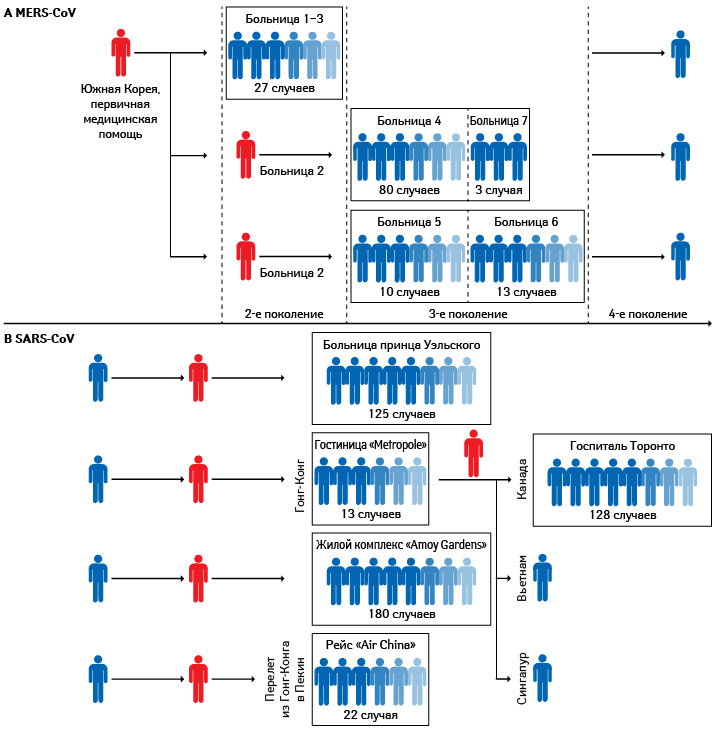
125 вторичных заражений от одного инфицированного
Ретроспективно во время вспышки SARS‑CoV в 2003 г. было также зарегистрировано несколько «сверхразмерных событий». «Нулевой» пациент эпидемии в Гонконге был связан как минимум со 125 вторичными случаями (Riley et al., 2003). Последующие «события суперраспределения» произошли в отеле «Metropole» (13 случаев) и жилом комплексе «Amoy Gardens» (более 180 случаев) в Гонконге и на борту рейса «Air China», направлявшегося из Гонконга в Пекин (22 случая) (Braden C.R. et al., 2013). Примечательно, что случаи из отеля «Metropole» были ответственны за распространение SARS‑CoV в Канаду, Вьетнам и Сингапур через путешествия (см. рис. 2В), а случай, импортированный в Канаду, привел к 128 заболеваниям SARS-CoV в больнице Торонто (Riley S. et al., 2003).
Естественно, не все вышеназванные случаи прослежены буквально до вызвавшего заражение человека, но налицо факты суперраспространения (Super-spreading) — непропорционально большого количества заражений вследствие контакта с одним из инфицированных.
10% инфицированных дают 80% заражений?
Спустя несколько месяцев после первоначальной вспышки сохраняется консенсус относительно того, что основное репродуктивное число (R0) инфекции COVID-19 равно 2–3, то есть столько на одного инфицированного в среднем приходится вторичных по отношению к нему случаев. Но в реальной жизни некоторые люди заражают многих, а другие вообще не распространяют болезнь. На самом деле последнее является нормой, пояснил на страницах журнала «Science» Джейми Ллойд-Смит (Lloyd-Smith) из Калифорнийского университета (University of California): «Естественная картина состоит в том, что наиболее распространенное значение R0 — ноль. Большинство людей не заражают».
Вот почему в дополнение к R0 ученые используют параметр, называемый коэффициентом дисперсии (k) — меру сгруппированности случаев вокруг источника. Чем ниже k, тем больше заражений исходит от ограниченного числа людей. В оригинальной статье «Nature» за 2005 г. Д. Ллойд-Смит и соавторы подсчитали, что при SARS значение k составило 0,16 (Lloyd-Smith J.O. et al., 2005). Почти ¾ зараженных тогда не передали вирус другим, в то время как 6% оказались «сверхраспространителями». Расчетный k для MERS, появившегося в 2012 г., составляет около 0,25, — отмечено в публикации «Science» (doi:10.1126/science.abc8931). Напротив, в пандемии гриппа 1918 г. (испанка) значение составляло около единицы, что указывает на то, что кластеры играли меньшую роль.
Оценки k для SARS-CoV-2 варьируют. В январе Жюльен Риу (Julien Riou) и Кристиан Альтхаус (Christian Althaus) в Университете Берна (University of Bern) смоделировали эпидемию в Китае для различных комбинаций R и k и сравнили результаты с реальными данными. Они пришли к выводу, что k для COVID-19 несколько выше, чем для SARS и MERS. «Это кажется правильным, — цитирует автор «Science» другого эксперта из Университета Гонконга (University of Hong Kong). — Я не думаю, что это похоже на SARS или MERS, где мы наблюдали очень большие кластеры сверхзаражений. Но мы, безусловно, видим много концентрированных вспышек, где небольшая доля людей «ответственна» за большую долю инфекций».
Более того, в опубликованном в виде препринта исследовании, проведенном Центром математического моделирования COVID-19 из Лондонской школы гигиены и тропической медицины (London School of Hygiene & Tropical Medicine) на основании данных об эволюции импортированных из Китая случаев в феврале 2019 г., k для COVID-19 оценен всего в 0,1. «Вероятно, около 10% случаев приводят к 80% заражений», — отметили авторы (Endo A. et al., 2020).
Если предвидеть кластеры…
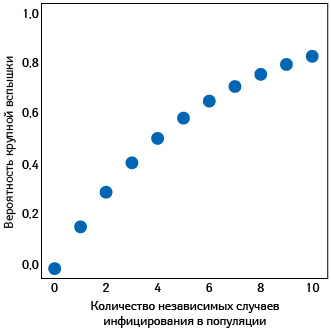
Низкий k при COVID-19 становится ключевым элементом, с помощью которого можно объяснить естественный процесс эволюции вспышек. Большая часть случаев загораются, как искорки, и гаснут. Только редкие из них приводят к появлению очагов заражения, некоторые из которых, сливаясь, дают пожары, подобно наблюдавшимся в Италии и Испании. Чтобы закрепиться в популяции, вирус SARS-CoV-2 должен быть занесен туда по крайней мере 4 раза, поясняют эксперты (рис. 3).
Почему коронавирусные инфекции гораздо больше других склонны к образованию кластеров, это «действительно интересный открытый научный вопрос», — подчеркнул Кристоф Фрейзер (Christophe Fraser) из Оксфордского университета (University of Oxford), который изучал распространение вируса Эбола и ВИЧ. Одним из факторов может быть способ их передачи. SARS-CoV-2, по-видимому, передается в основном через капли, но иногда он распространяется через аэрозоли, которые могут оставаться в воздухе, что позволяет одному человеку заразить многих. По словам К. Фрейзера, большинство опубликованных крупных кластеров передачи, по-видимому, подразумевают образование аэрозоля. Возможно, имеют значение еще и температура, и влажность, свидетельство чему — вспышки на мясокомбинатах.
Характеристики отдельных пациентов также играют роль. Некоторые люди выделяют гораздо больше вирусов и в течение более длительного периода, чем другие, возможно, из-за различий в их иммунной системе или из-за распределения вирусных рецепторов в их организме. Исследование здоровых людей, проведенное в 2019 г., показало, что некоторые из них выделяют гораздо больше частиц, чем другие, даже если устранить влияние громкости и особенностей произношения на разных языках (английском, испанском, китайском и арабском) (Asadi S. et al., 2019). Поведение людей также играет роль: интенсивная физическая работа, крик, пение повышают интенсивность образования аэрозолей. Наличие большого количества социальных контактов или отсутствие мытья рук повышает вероятность передачи вируса.
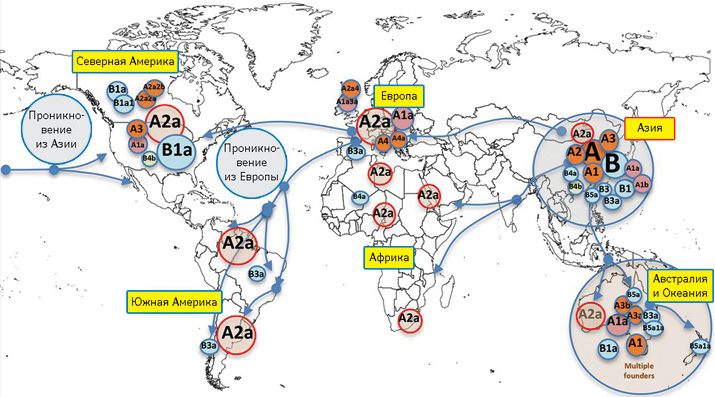
Исходя из того, что феномен «суперраспространения» играет ведущую роль в формировании крупных вспышек, распознавание связанных с этим рисков имеет неоценимое значение. Возможность «выключать» действительные и потенциальные кластеры из цепочек распространения инфекции позволит избежать масштабных «блокировок», поскольку всеобщий «карантин» — невероятно грубый инструмент, применяемый от безысходности, когда невозможно локализовать отдельные кластеры. Получение необходимых для этого данных в Европе — нерешенная до сих пор задача из-за проблем конфиденциальности. Секвенирование геномов вирусных изолятов — еще один «рабочий» метод отслеживания связей между вспышками (рис. 4).
Использованная литература
по материалам www.fondation-diaconat.fr; www.france24.com;
www.rtl.fr; www.lopinion.fr; www.lshtm.ac.uk

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим